-
 코로나바이러스 전염 메커니즘 규명
중증급성호흡기증후군(이하 SARS) 코로나바이러스와 같은 코로나 19(COVID-19)는 전 세계적 팬데믹으로 짧은 시간 안에 확산되었지만 왜 급격히 복제돼 빠르게 전염되는지 기전이 아직까지 규명되지 않았다. 우리 연구진이 코로나바이러스 핵심 효소 단백질(헬리케이스)의 복제과정이 급격히 촉진되어 전염되는 메커니즘을 밝혀내며 바이러스 백신 및 치료제 개발에 새로운 가능성을 제시했다.
우리 대학 생명과학과 이광록 교수 연구팀이 nsp13 단백질*은 두 가지 활성을 가지고 있어 시너지 효과를 내며, 이를 통해 SARS 코로나바이러스의 유전물질인 RNA 복제를 촉진한다는 기전을 규명했다고 17일 밝혔다.
*nsp13 단백질: SARS 코로나바이러스의 헬리케이스로, 바이러스가 증식하는 데 필수적인 유전자 복제와 전사 과정에 중요한 효소이다. 헬리케이스는 마치 지퍼를 열고 닫는 것처럼 DNA나 RNA의 꼬인 구조를 풀어주는데, 유전정보를 읽거나 복제할 때 유전물질을 먼저 풀려야 하므로 필수적이다. 쉽게 말해, 헬리케이스는 엉킨 실타래를 푸는 효소단백질이다.
여기 두 가지 활성에 해당되는 첫번째 헬리케이스 활성은 DNA 또는 RNA와 같은 이중 가닥 핵산을 단일 가닥으로 풀어주는 효소 기능이며, 복제나 전사 과정을 촉진시킨다. 두번째 RNA 샤페론 활성은 핵산 구조의 올바른 접힘(folding)과 풀림 기능을 돕는 단백질로, 잘못된 RNA를 교정하거나 안정성을 향상시켜 세포 내 RNA 대사과정을 돕는 역할을 한다.
코로나바이러스가 빠르게 전파하기 위해서는 바이러스의 유전물질을 빠르게 복제하고 구성성분인 단백질을 생산해서 이들을 조합하는 것이 필수적이다.
연구팀은 첫 번째 단계인 유전물질의 RNA 복제가 다른 바이러스에 비해 왜 빠르게 일어나는지 알려지지 않았으나, nsp13 단백질이 기존의 헬리케이스 활성과 이제까지 알려지지 않은 새로운 샤페론 활성으로 유전자 복제 과정을 빠르게 촉진한다는 것을 규명했다.
nsp13 단백질은 유전적으로 잘 보존되어 다양한 변이 코로나바이러스에 대응하는 백신이나 감염 치료의 중요 표적이지만, 정확한 작용 메커니즘에 대해서는 완전한 이해가 부족했다.
연구팀은 nsp13 헬리케이스가 ATP(아데노신 삼인산)*를 분해하여 나온 화학에너지를 이용하여 유전물질인 RNA의 꼬인 구조를 단일 가닥으로 풀어주고 부산물로 ADP(아데노신 이인산)*가 생성하게 된다. 이때 생성된 ADP가 nsp13와 재결합하게 되면 샤페론 기능을 활성화시켜 RNA 이차구조를 추가로 불안정화한다는 사실을 알아냈다.
*ATP(아데노신 삼인산)는 충전된 배터리처럼 에너지를 담고 있고 효소가 일을 할 때는 에너지를 공급해준다. ATP는 인산 3개를 가지고 있어 인산이 분해 될 때 에너지를 방출하고 인산 2개를 가진 ADP(아데노신 이인산)를 부산물로 생성한다.
결론적으로 헬리케이스 활성과 샤페론 활성이 시공간적으로 동시에 협력해 RNA 복제를 촉진하게 된다는 새로운 방식의 작용기전을 규명했다.
이광록 교수는 “이번 연구는 대표적 핵산-효소 단백질인 헬리케이스가 ADP를 통해 샤페론적 활성을 나타내는 새로운 발견이며, 이를 통해 헬리케이스의 기능 다양성에 대한 이해의 폭을 넓혀주고, SARS 코로나바이러스의 다양한 변이에 대응할 효과적 치료제 및 백신 개발의 실마리를 제공할 것으로 기대한다”라고 연구 결과의 의의를 밝혔다.
이 연구는 유정민 박사가 제 1저자로 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF: 16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 29일 게재됐다. (논문명 : A novel ADP-directed chaperone function facilitates the ATP-driven motor activity of SARS-CoV helicase) (doi: 10.1093/nar/gkaf034)
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구지원, 선도연구센터 지원사업, 글로벌 기초연구 지원사업과 합성생물학핵심기술개발사업의 지원을 받아 수행됐다.
코로나바이러스 전염 메커니즘 규명
중증급성호흡기증후군(이하 SARS) 코로나바이러스와 같은 코로나 19(COVID-19)는 전 세계적 팬데믹으로 짧은 시간 안에 확산되었지만 왜 급격히 복제돼 빠르게 전염되는지 기전이 아직까지 규명되지 않았다. 우리 연구진이 코로나바이러스 핵심 효소 단백질(헬리케이스)의 복제과정이 급격히 촉진되어 전염되는 메커니즘을 밝혀내며 바이러스 백신 및 치료제 개발에 새로운 가능성을 제시했다.
우리 대학 생명과학과 이광록 교수 연구팀이 nsp13 단백질*은 두 가지 활성을 가지고 있어 시너지 효과를 내며, 이를 통해 SARS 코로나바이러스의 유전물질인 RNA 복제를 촉진한다는 기전을 규명했다고 17일 밝혔다.
*nsp13 단백질: SARS 코로나바이러스의 헬리케이스로, 바이러스가 증식하는 데 필수적인 유전자 복제와 전사 과정에 중요한 효소이다. 헬리케이스는 마치 지퍼를 열고 닫는 것처럼 DNA나 RNA의 꼬인 구조를 풀어주는데, 유전정보를 읽거나 복제할 때 유전물질을 먼저 풀려야 하므로 필수적이다. 쉽게 말해, 헬리케이스는 엉킨 실타래를 푸는 효소단백질이다.
여기 두 가지 활성에 해당되는 첫번째 헬리케이스 활성은 DNA 또는 RNA와 같은 이중 가닥 핵산을 단일 가닥으로 풀어주는 효소 기능이며, 복제나 전사 과정을 촉진시킨다. 두번째 RNA 샤페론 활성은 핵산 구조의 올바른 접힘(folding)과 풀림 기능을 돕는 단백질로, 잘못된 RNA를 교정하거나 안정성을 향상시켜 세포 내 RNA 대사과정을 돕는 역할을 한다.
코로나바이러스가 빠르게 전파하기 위해서는 바이러스의 유전물질을 빠르게 복제하고 구성성분인 단백질을 생산해서 이들을 조합하는 것이 필수적이다.
연구팀은 첫 번째 단계인 유전물질의 RNA 복제가 다른 바이러스에 비해 왜 빠르게 일어나는지 알려지지 않았으나, nsp13 단백질이 기존의 헬리케이스 활성과 이제까지 알려지지 않은 새로운 샤페론 활성으로 유전자 복제 과정을 빠르게 촉진한다는 것을 규명했다.
nsp13 단백질은 유전적으로 잘 보존되어 다양한 변이 코로나바이러스에 대응하는 백신이나 감염 치료의 중요 표적이지만, 정확한 작용 메커니즘에 대해서는 완전한 이해가 부족했다.
연구팀은 nsp13 헬리케이스가 ATP(아데노신 삼인산)*를 분해하여 나온 화학에너지를 이용하여 유전물질인 RNA의 꼬인 구조를 단일 가닥으로 풀어주고 부산물로 ADP(아데노신 이인산)*가 생성하게 된다. 이때 생성된 ADP가 nsp13와 재결합하게 되면 샤페론 기능을 활성화시켜 RNA 이차구조를 추가로 불안정화한다는 사실을 알아냈다.
*ATP(아데노신 삼인산)는 충전된 배터리처럼 에너지를 담고 있고 효소가 일을 할 때는 에너지를 공급해준다. ATP는 인산 3개를 가지고 있어 인산이 분해 될 때 에너지를 방출하고 인산 2개를 가진 ADP(아데노신 이인산)를 부산물로 생성한다.
결론적으로 헬리케이스 활성과 샤페론 활성이 시공간적으로 동시에 협력해 RNA 복제를 촉진하게 된다는 새로운 방식의 작용기전을 규명했다.
이광록 교수는 “이번 연구는 대표적 핵산-효소 단백질인 헬리케이스가 ADP를 통해 샤페론적 활성을 나타내는 새로운 발견이며, 이를 통해 헬리케이스의 기능 다양성에 대한 이해의 폭을 넓혀주고, SARS 코로나바이러스의 다양한 변이에 대응할 효과적 치료제 및 백신 개발의 실마리를 제공할 것으로 기대한다”라고 연구 결과의 의의를 밝혔다.
이 연구는 유정민 박사가 제 1저자로 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF: 16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 29일 게재됐다. (논문명 : A novel ADP-directed chaperone function facilitates the ATP-driven motor activity of SARS-CoV helicase) (doi: 10.1093/nar/gkaf034)
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구지원, 선도연구센터 지원사업, 글로벌 기초연구 지원사업과 합성생물학핵심기술개발사업의 지원을 받아 수행됐다.
2025.02.17
조회수 3762
-
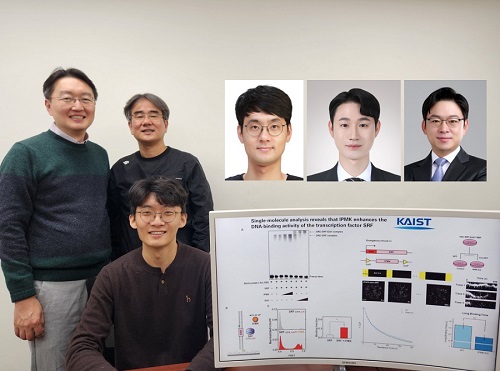 암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22
조회수 4571
-
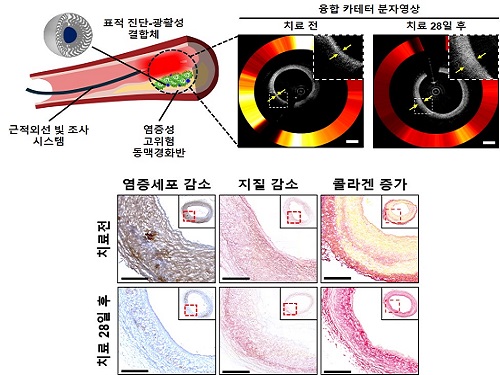 기계공학과 유홍기 교수 연구팀, 빛으로 동맥경화반 동시 진단 및 치료 기술 개발
관상동맥 내 고위험 동맥경화반은 파열과 협착을 유발하여 빠르게 혈관을 막을 수 있어 진단과 동시에 즉각적인 치료가 필요하다.
우리 대학 기계공학과 유홍기 교수 연구팀은 고려대학교구로병원 심혈관센터 김진원 교수팀, 중앙대학교 시스템생명공학과 박경순 교수팀과의 공동연구를 통해, 빛을 이용하여 동맥경화반 진단과 치료를 동시에 할 수 있는 새로운 원천 기술을 개발하였다.
이 기술은 유홍기 교수 연구팀이 개발한 광단층-분자영상 결합 카테터 기반 정밀 영상 시스템과 광치료 카테터를 이용해 빛을 조사하여 고위험 병변을 정확히 진단하고 치료하는 방법이다.
동맥경화반 내 대식세포의 특정 수용체를 표적하는 전달체와 광활성체를 결합한 테라노스틱 제제를 혈관에 투여한 후 혈관내 카테터를 이용해 위험 부위를 찾아내고 그 부위에 빛을 조사하였다. 그 결과, 고위험 동맥경화반을 실시간 정밀 영상으로 진단하였고 동시에 성공적으로 치료할 수 있었다.
치료 후 효과를 정밀 영상 시스템을 통해 생체 내에서 추적 검증했으며, 광활성에 의한 자가소화를 유도해 사멸 세포를 탐식 및 제거, 콜레스테롤 유출로 염증을 해소하고 콜라겐 조직 증가를 유도해 병변이 치료 및 안정화 됨을 밝혔다.
연구진은 “이번 연구를 통해 기존 방법의 한계였던 고위험 동맥경화반의 정밀 진단을 가능케 하였고, 동시에 광치료 시스템을 이용해 빛을 전달하여 고위험 동맥경화반을 치료하고 안정화하는 데 성공했다는 점에서 큰 의의가 있다.”라고 밝혔다. 또한 “기존 동맥경화반 치료법인 스텐트 치료가 가지는 이물질 잔존 위험을 극복할 수 있으며, 심혈관 진단 및 치료 분야에서 새로운 가능성을 제시했다.”고 했다. 연구진은 “이번 연구 결과를 바탕으로, 추후 임상 적용을 위한 시제품 개발을 적극적으로 추진할 계획”이라고 덧붙였다.
이번 연구 결과는 기계공학과 김연훈 박사과정생이 공동 제1저자로, 유홍기 교수가 공동교신저자로 참여하였으며, 국제학술지 Circulation Research (5-year IF: 20.3) 에 게재되었다.
한편 이번 연구는 한국연구재단이 주관하는 원천기술개발사업의 지원을 받아 수행됐다.
기계공학과 유홍기 교수 연구팀, 빛으로 동맥경화반 동시 진단 및 치료 기술 개발
관상동맥 내 고위험 동맥경화반은 파열과 협착을 유발하여 빠르게 혈관을 막을 수 있어 진단과 동시에 즉각적인 치료가 필요하다.
우리 대학 기계공학과 유홍기 교수 연구팀은 고려대학교구로병원 심혈관센터 김진원 교수팀, 중앙대학교 시스템생명공학과 박경순 교수팀과의 공동연구를 통해, 빛을 이용하여 동맥경화반 진단과 치료를 동시에 할 수 있는 새로운 원천 기술을 개발하였다.
이 기술은 유홍기 교수 연구팀이 개발한 광단층-분자영상 결합 카테터 기반 정밀 영상 시스템과 광치료 카테터를 이용해 빛을 조사하여 고위험 병변을 정확히 진단하고 치료하는 방법이다.
동맥경화반 내 대식세포의 특정 수용체를 표적하는 전달체와 광활성체를 결합한 테라노스틱 제제를 혈관에 투여한 후 혈관내 카테터를 이용해 위험 부위를 찾아내고 그 부위에 빛을 조사하였다. 그 결과, 고위험 동맥경화반을 실시간 정밀 영상으로 진단하였고 동시에 성공적으로 치료할 수 있었다.
치료 후 효과를 정밀 영상 시스템을 통해 생체 내에서 추적 검증했으며, 광활성에 의한 자가소화를 유도해 사멸 세포를 탐식 및 제거, 콜레스테롤 유출로 염증을 해소하고 콜라겐 조직 증가를 유도해 병변이 치료 및 안정화 됨을 밝혔다.
연구진은 “이번 연구를 통해 기존 방법의 한계였던 고위험 동맥경화반의 정밀 진단을 가능케 하였고, 동시에 광치료 시스템을 이용해 빛을 전달하여 고위험 동맥경화반을 치료하고 안정화하는 데 성공했다는 점에서 큰 의의가 있다.”라고 밝혔다. 또한 “기존 동맥경화반 치료법인 스텐트 치료가 가지는 이물질 잔존 위험을 극복할 수 있으며, 심혈관 진단 및 치료 분야에서 새로운 가능성을 제시했다.”고 했다. 연구진은 “이번 연구 결과를 바탕으로, 추후 임상 적용을 위한 시제품 개발을 적극적으로 추진할 계획”이라고 덧붙였다.
이번 연구 결과는 기계공학과 김연훈 박사과정생이 공동 제1저자로, 유홍기 교수가 공동교신저자로 참여하였으며, 국제학술지 Circulation Research (5-year IF: 20.3) 에 게재되었다.
한편 이번 연구는 한국연구재단이 주관하는 원천기술개발사업의 지원을 받아 수행됐다.
2024.08.23
조회수 5118
-
 바이러스와 세균의 진화를 규명하다
바이러스는 특정 세포 안에 침투했을 때만 증식의 생명력을 띠고 그 외에는 무생물 같으며, 사람 세포를 감염시키는 코로나19 바이러스, 세균을 잡아먹으며 증식하는 세균바이러스 등이 있다. 국내 연구진이 세균바이러스가 RNA 합성을 마무리 짓는 방식에 해체종결(1)만 있고 재생종결(2)은 없다는 사실을 밝히고 RNA 의약품 개발에 응용될 가능성을 높였다.
(1)해체종결: 합성 복합체가 중합효소, DNA, RNA로 해체
(2)재생종결: RNA만 분리되고 중합효소는 DNA에 남아 재생
우리 대학 생명과학과 강창원 명예교수(줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동연구팀이 세균의 리보핵산(RNA) 합성방식 두 가지 중 하나가 바이러스에는 없다는 것을 발견해, 세균이 바이러스로부터 진화하면서 획득한 방식을 처음 밝힌 연구 논문을 핵산 분야 최상급 국제학술지에 게재했다고 19일 밝혔다.
유전자 DNA의 유전정보에 따라 RNA를 합성하는 효소가 RNA 중합효소다. 이는 유전정보가 DNA에서 RNA로 옮겨 적히기에 전사(轉寫)라고 부르는 유전자 발현 첫 단계를 수행하며, RNA 백신 등 첨단 RNA 의약품을 개발 생산하는 데에 쓰인다. 연구팀은 세균바이러스의 RNA 중합효소를 연구해서 생물로 진화하기 이전 태초의 RNA 합성(전사) 방식을 밝힌 것이다.
유전자에 따라 다른 게 아니라 어느 유전자든 전사 마무리 방식에 두 가지가 있다는 것을 수년 전 세균에서 발견했었다. 그리고 세균보다 진화한 진핵생물 효모의 유전자 전사에서도 두 방식이 모두 쓰인다는 것이 지난달에 보고됐다. 사람도 진핵생물이어서, 세균과 효모뿐 아니라 사람까지 온갖 생물의 유전자 전사에 두 방식 모두 쓰일 개연성이 커졌다.
그런데 이번 연구에서 세균바이러스의 방식은 세균이나 효모와 사뭇 다르다는 것이 밝혀졌다. 바이러스의 경우 재생종결 없이 해체종결만 일어나는 것이다. 이를 토대로, 연구팀은 RNA 중합효소가 세균에서 바이러스와 달리 적응하면서 해체종결에 재생종결이 추가돼 두 방식이 공존하게 되었고, 최소한 효모로의 진화에서 그대로 보존됐다는 해석을 내놓았다.
이번 연구에서 거푸집 DNA와 전사물 RNA에 각기 다른 형광물질을 부착해 전사 복합체 하나하나의 형광을 실시간으로 측정하는 단일분자 형광기술 연구기법이 사용됐다. 전사 종결로 RNA가 방출될 때 DNA가 효소에 붙어있는지 떨어지는지를 낱낱이 구별할 수 있게 설계한 것이 특장점이다. 특히 형광물질이 전사 반응에 지장을 주지 않도록 하는 게 관건이었다.
송은호 박사후연구원과 한선 박사과정 대학원생이 공동 제1 저자로 참여한 논문(제목: Single-mode termination of phage transcriptions, disclosing bacterial adaptation for facilitated reinitiations)이 학술지 핵산연구(Nucleic Acids Research)에 7월 16일 게재됐다. 이로써 강창원 교수와 홍성철 교수는 2017년부터 총 8편의 논문을 공동으로 발표했다.
강창원 교수는 "이번 연구를 통해 수 초 동안의 분자 반응에서 유구한 진화과정을 밝혀냈고, 앞으로 더 광범위한 진화를 연구할 계획이다”라고 했다. 홍성철 교수는 "분자 하나하나를 관찰하여 복잡한 생물체의 진화를 파악했고, 이런 단일분자 연구기법을 차세대 RNA 의약품과 진단 시약의 개발에 응용하는 연구로 이어가고자 한다”라고 했다.
바이러스와 세균의 진화를 규명하다
바이러스는 특정 세포 안에 침투했을 때만 증식의 생명력을 띠고 그 외에는 무생물 같으며, 사람 세포를 감염시키는 코로나19 바이러스, 세균을 잡아먹으며 증식하는 세균바이러스 등이 있다. 국내 연구진이 세균바이러스가 RNA 합성을 마무리 짓는 방식에 해체종결(1)만 있고 재생종결(2)은 없다는 사실을 밝히고 RNA 의약품 개발에 응용될 가능성을 높였다.
(1)해체종결: 합성 복합체가 중합효소, DNA, RNA로 해체
(2)재생종결: RNA만 분리되고 중합효소는 DNA에 남아 재생
우리 대학 생명과학과 강창원 명예교수(줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동연구팀이 세균의 리보핵산(RNA) 합성방식 두 가지 중 하나가 바이러스에는 없다는 것을 발견해, 세균이 바이러스로부터 진화하면서 획득한 방식을 처음 밝힌 연구 논문을 핵산 분야 최상급 국제학술지에 게재했다고 19일 밝혔다.
유전자 DNA의 유전정보에 따라 RNA를 합성하는 효소가 RNA 중합효소다. 이는 유전정보가 DNA에서 RNA로 옮겨 적히기에 전사(轉寫)라고 부르는 유전자 발현 첫 단계를 수행하며, RNA 백신 등 첨단 RNA 의약품을 개발 생산하는 데에 쓰인다. 연구팀은 세균바이러스의 RNA 중합효소를 연구해서 생물로 진화하기 이전 태초의 RNA 합성(전사) 방식을 밝힌 것이다.
유전자에 따라 다른 게 아니라 어느 유전자든 전사 마무리 방식에 두 가지가 있다는 것을 수년 전 세균에서 발견했었다. 그리고 세균보다 진화한 진핵생물 효모의 유전자 전사에서도 두 방식이 모두 쓰인다는 것이 지난달에 보고됐다. 사람도 진핵생물이어서, 세균과 효모뿐 아니라 사람까지 온갖 생물의 유전자 전사에 두 방식 모두 쓰일 개연성이 커졌다.
그런데 이번 연구에서 세균바이러스의 방식은 세균이나 효모와 사뭇 다르다는 것이 밝혀졌다. 바이러스의 경우 재생종결 없이 해체종결만 일어나는 것이다. 이를 토대로, 연구팀은 RNA 중합효소가 세균에서 바이러스와 달리 적응하면서 해체종결에 재생종결이 추가돼 두 방식이 공존하게 되었고, 최소한 효모로의 진화에서 그대로 보존됐다는 해석을 내놓았다.
이번 연구에서 거푸집 DNA와 전사물 RNA에 각기 다른 형광물질을 부착해 전사 복합체 하나하나의 형광을 실시간으로 측정하는 단일분자 형광기술 연구기법이 사용됐다. 전사 종결로 RNA가 방출될 때 DNA가 효소에 붙어있는지 떨어지는지를 낱낱이 구별할 수 있게 설계한 것이 특장점이다. 특히 형광물질이 전사 반응에 지장을 주지 않도록 하는 게 관건이었다.
송은호 박사후연구원과 한선 박사과정 대학원생이 공동 제1 저자로 참여한 논문(제목: Single-mode termination of phage transcriptions, disclosing bacterial adaptation for facilitated reinitiations)이 학술지 핵산연구(Nucleic Acids Research)에 7월 16일 게재됐다. 이로써 강창원 교수와 홍성철 교수는 2017년부터 총 8편의 논문을 공동으로 발표했다.
강창원 교수는 "이번 연구를 통해 수 초 동안의 분자 반응에서 유구한 진화과정을 밝혀냈고, 앞으로 더 광범위한 진화를 연구할 계획이다”라고 했다. 홍성철 교수는 "분자 하나하나를 관찰하여 복잡한 생물체의 진화를 파악했고, 이런 단일분자 연구기법을 차세대 RNA 의약품과 진단 시약의 개발에 응용하는 연구로 이어가고자 한다”라고 했다.
2024.07.19
조회수 6423
-
 최진석 교수, 국제전기전자공학회 우수 젊은 연구자 상 수상
우리 대학 전기및전자공학부 최진석 교수가 무선 통신 분야에서의 업적으로 국제전기전자공학회(IEEE)의 통신 분야 아시아-태평양 우수 젊은 연구자 상(IEEE ComSoc Asia-Pacific Outstanding Young Researcher Award)을 수상했다고 22일 밝혔다.
최진석 교수는 꾸준한 연구와 혁신적인 아이디어로 통신 기술 발전에 중요한 역할을 해오고 있는 공로를 인정받았다. 해당 상은 매년 아시아-태평양 지역의 젊은 우수 연구자들에게 수여되는 상으로 올해 한국에서는 최진석 교수가 단독으로 수상했다. 그의 연구는 주로 저전력 통신 시스템 개발에 초점을 맞춰 새로운 무선 통신 기술과 솔루션의 개발을 통해 이 분야를 선도해 오고 있다.
특히, 최진석 교수는 무선 통신 분야에서의 창의적이고 도전적인 연구로 인해 꾸준한 평가를 받고 있다. 그의 주력 분야인 저전력 통신 시스템은 에너지 효율성을 극대화하면서도 안정적이고 고효율의 무선 통신을 실현하는 혁신적인 특징을 지니고 있다. 이를 통해 그가 개발한 시스템은 새로운 개념을 제시하며 세계적인 연구자들과 함께 무선 통신 기술의 발전을 선도하고 있다.
최진석 교수의 성과는 국내외의 우수 연구 그룹과의 긴밀한 협업, 다양한 학문 분야와의 융합, 그리고 산업계와의 적극적인 협력을 통해 이뤄지고 있다. 그는 무선 통신 분야에서의 현장 경험과 교육 활동을 통해 학문과 산업 간의 연계를 강조하며, 다양한 분야의 전문 지식을 융합해 새로운 연구 및 기술 개발에 도전하고 있다.
위 상을 받은 최진석 교수는 “앞으로의 통신 시스템은 에너지 효율성이 굉장히 중요한 이슈가 될 것으로 예상되는데, 최적화 이론과 정보이론을 기반으로 에너지 효율적인 통신 시스템을 개발하고자 했던 노력이 국제적으로 인정받아 매우 기쁘다ˮ며, “앞으로 이러한 기술을 실제 통신 시스템에 활용할 수 있도록 지속적인 노력을 하며 다양한 통신 어플리케이션에 적용하는 등 꾸준히 연구를 진행할 계획이다ˮ 라고 소감을 밝혔다.
시상식은 올해 12월 4일부터 8일까지 말레이시아 쿠알라룸푸르에서 열린 통신 분야 최우수 학회 중 하나인 세계 통신 학회(Globecom)에서 진행됐다.
최진석 교수, 국제전기전자공학회 우수 젊은 연구자 상 수상
우리 대학 전기및전자공학부 최진석 교수가 무선 통신 분야에서의 업적으로 국제전기전자공학회(IEEE)의 통신 분야 아시아-태평양 우수 젊은 연구자 상(IEEE ComSoc Asia-Pacific Outstanding Young Researcher Award)을 수상했다고 22일 밝혔다.
최진석 교수는 꾸준한 연구와 혁신적인 아이디어로 통신 기술 발전에 중요한 역할을 해오고 있는 공로를 인정받았다. 해당 상은 매년 아시아-태평양 지역의 젊은 우수 연구자들에게 수여되는 상으로 올해 한국에서는 최진석 교수가 단독으로 수상했다. 그의 연구는 주로 저전력 통신 시스템 개발에 초점을 맞춰 새로운 무선 통신 기술과 솔루션의 개발을 통해 이 분야를 선도해 오고 있다.
특히, 최진석 교수는 무선 통신 분야에서의 창의적이고 도전적인 연구로 인해 꾸준한 평가를 받고 있다. 그의 주력 분야인 저전력 통신 시스템은 에너지 효율성을 극대화하면서도 안정적이고 고효율의 무선 통신을 실현하는 혁신적인 특징을 지니고 있다. 이를 통해 그가 개발한 시스템은 새로운 개념을 제시하며 세계적인 연구자들과 함께 무선 통신 기술의 발전을 선도하고 있다.
최진석 교수의 성과는 국내외의 우수 연구 그룹과의 긴밀한 협업, 다양한 학문 분야와의 융합, 그리고 산업계와의 적극적인 협력을 통해 이뤄지고 있다. 그는 무선 통신 분야에서의 현장 경험과 교육 활동을 통해 학문과 산업 간의 연계를 강조하며, 다양한 분야의 전문 지식을 융합해 새로운 연구 및 기술 개발에 도전하고 있다.
위 상을 받은 최진석 교수는 “앞으로의 통신 시스템은 에너지 효율성이 굉장히 중요한 이슈가 될 것으로 예상되는데, 최적화 이론과 정보이론을 기반으로 에너지 효율적인 통신 시스템을 개발하고자 했던 노력이 국제적으로 인정받아 매우 기쁘다ˮ며, “앞으로 이러한 기술을 실제 통신 시스템에 활용할 수 있도록 지속적인 노력을 하며 다양한 통신 어플리케이션에 적용하는 등 꾸준히 연구를 진행할 계획이다ˮ 라고 소감을 밝혔다.
시상식은 올해 12월 4일부터 8일까지 말레이시아 쿠알라룸푸르에서 열린 통신 분야 최우수 학회 중 하나인 세계 통신 학회(Globecom)에서 진행됐다.
2023.12.22
조회수 6805
-
 혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14
조회수 13466
-
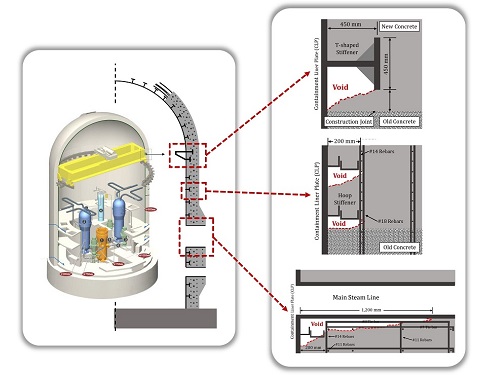 한빛원전의 시공 불량 문제를 해결하기 위한 시뮬레이션 개발
후쿠시마 사고 이후 원전 안전 및 관리에 대한 관심이 집중되고 있다. 한국에서는 2017년 6월경 한빛원전의 원자로 격납건물의 콘크리트 벽 속에서 대규모 공극이 발견되었다. 원자로 격납건물은 원전 사고 발생 시 방사능 유출을 막아주는 최후의 보루이기 때문에, 이러한 콘크리트 공극으로 인한 원전의 안전상 우려가 큰 상황이다.
국내 연구진들은 원자로 격납건물 시공시 콘크리트 다짐 및 채움 불량으로 인하여 격납로 내 콘크리트에 공극이 발생한 것으로 추정하고 있다. 원자로 격납건물은 일반 콘크리트 구조물과 달리 매우 높은 밀도의 철근 보강이 필요하기 때문에, 콘크리트 타설 시 진동 다짐기가 진입하지 못하는 구역이 존재할 가능성이 높아서 콘크리트 공동에 대한 위험성이 높다. 하지만 돔 형태의 벽체 내부를 감싼 6 mm 두께의 철판(콘크리트 라이너 플레이트, CLP)이 영구 거푸집으로 활용되기 때문에 내부 공동에 대한 육안 검사가 불가능하다는 점에서 공극 발생 여부의 발견에 대한 어려움이 있다.
우리 대학 건설및환경공학과 김재홍 교수 연구팀은 이러한 문제를 해결하기 위하여 콘크리트의 유동성과 다짐 불량으로 인해 발생하는 공동을 억제할 수 있는 시공 시뮬레이션 기법을 개발했다.
연구팀에서 제안한 콘크리트 유동 시뮬레이션 기법은 콘크리트의 레올로지와 진동다짐의 영향 반경을 고려하여 콘크리트 공동 발생 예상 부위를 예측하는 기술이다. 연구팀은 이번 연구를 통해 콘크리트 진동다짐의 영향 반경(감쇠계수)을 직접 측정하여 굳지 않은 콘크리트 내부의 진동 에너지 밀도 분포를 제시했다. 이어서, 진동 에너지에 따른 콘크리트의 Vibrorheology를 정량적으로 측정하여, 굳지 않은 콘크리트의 항복응력 감소를 정량적으로 모델링하여 시공 시뮬레이션을 가능하게 하였다.
새로 제안된 시공 시뮬레이션 기법은 기존 콘크리트 유동해석으로는 고려할 수 없었던 격납건물 내부 보강재의 형상과 크기, 콘크리트 레올로지, 그리고 진동다짐의 진폭과 진동수까지 고려하여 콘크리트의 채움성을 평가할 수 있게 되었다. 연구팀은 향후 보강 연구를 진행해 3D 프린팅 콘크리트의 레올로지 제어, 프리캐스트 콘크리트의 품질 관리 등에도 해당 기술을 활용할 계획이다.
이번 연구는 한국수력원자력(주)와 한국연구재단의 과학기술분야 기초연구사업의 지원으로 수행되었으며, 건설공학 분야에서 권위 있는 학술지인 ACI Materials Journal, Cement and Concrete Research 등에 출판되었다.
(논문명: (1) Quantitative evaluation of energy transfer of a concrete vibrator. (2) Flow simulation of fresh concrete accounting for vibrating compaction.)
한빛원전의 시공 불량 문제를 해결하기 위한 시뮬레이션 개발
후쿠시마 사고 이후 원전 안전 및 관리에 대한 관심이 집중되고 있다. 한국에서는 2017년 6월경 한빛원전의 원자로 격납건물의 콘크리트 벽 속에서 대규모 공극이 발견되었다. 원자로 격납건물은 원전 사고 발생 시 방사능 유출을 막아주는 최후의 보루이기 때문에, 이러한 콘크리트 공극으로 인한 원전의 안전상 우려가 큰 상황이다.
국내 연구진들은 원자로 격납건물 시공시 콘크리트 다짐 및 채움 불량으로 인하여 격납로 내 콘크리트에 공극이 발생한 것으로 추정하고 있다. 원자로 격납건물은 일반 콘크리트 구조물과 달리 매우 높은 밀도의 철근 보강이 필요하기 때문에, 콘크리트 타설 시 진동 다짐기가 진입하지 못하는 구역이 존재할 가능성이 높아서 콘크리트 공동에 대한 위험성이 높다. 하지만 돔 형태의 벽체 내부를 감싼 6 mm 두께의 철판(콘크리트 라이너 플레이트, CLP)이 영구 거푸집으로 활용되기 때문에 내부 공동에 대한 육안 검사가 불가능하다는 점에서 공극 발생 여부의 발견에 대한 어려움이 있다.
우리 대학 건설및환경공학과 김재홍 교수 연구팀은 이러한 문제를 해결하기 위하여 콘크리트의 유동성과 다짐 불량으로 인해 발생하는 공동을 억제할 수 있는 시공 시뮬레이션 기법을 개발했다.
연구팀에서 제안한 콘크리트 유동 시뮬레이션 기법은 콘크리트의 레올로지와 진동다짐의 영향 반경을 고려하여 콘크리트 공동 발생 예상 부위를 예측하는 기술이다. 연구팀은 이번 연구를 통해 콘크리트 진동다짐의 영향 반경(감쇠계수)을 직접 측정하여 굳지 않은 콘크리트 내부의 진동 에너지 밀도 분포를 제시했다. 이어서, 진동 에너지에 따른 콘크리트의 Vibrorheology를 정량적으로 측정하여, 굳지 않은 콘크리트의 항복응력 감소를 정량적으로 모델링하여 시공 시뮬레이션을 가능하게 하였다.
새로 제안된 시공 시뮬레이션 기법은 기존 콘크리트 유동해석으로는 고려할 수 없었던 격납건물 내부 보강재의 형상과 크기, 콘크리트 레올로지, 그리고 진동다짐의 진폭과 진동수까지 고려하여 콘크리트의 채움성을 평가할 수 있게 되었다. 연구팀은 향후 보강 연구를 진행해 3D 프린팅 콘크리트의 레올로지 제어, 프리캐스트 콘크리트의 품질 관리 등에도 해당 기술을 활용할 계획이다.
이번 연구는 한국수력원자력(주)와 한국연구재단의 과학기술분야 기초연구사업의 지원으로 수행되었으며, 건설공학 분야에서 권위 있는 학술지인 ACI Materials Journal, Cement and Concrete Research 등에 출판되었다.
(논문명: (1) Quantitative evaluation of energy transfer of a concrete vibrator. (2) Flow simulation of fresh concrete accounting for vibrating compaction.)
2023.10.24
조회수 7488
-
 저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
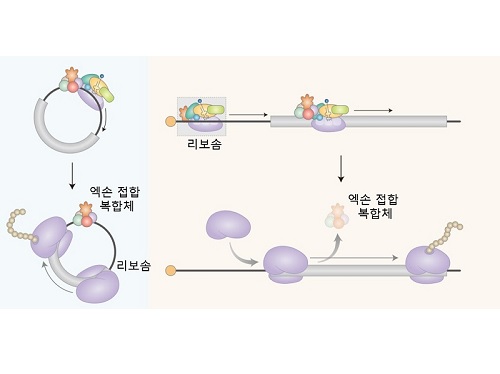
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
2023.10.24
조회수 7289
-
 호흡기부터 강력 차단하는 코로나19 백신 개발
코로나바이러스감염증-19는 3년 4개월 만에 비상사태가 해제됐으나, 잦은 돌연변이로 인해 발생한 변이들이 계속해서 보고되고 있어 재유행이 시작될 가능성은 여전히 남아 있다. 이 변이들은 백신 접종이나 감염으로 인해 숙주가 획득한 기존의 면역반응을 회피하는 방향으로 진화하고 있다. 현재 시판되는 근육 접종 백신으로는 바이러스의 확산을 억제할 수 있는 점막 면역은 충분히 일으키기 어렵다는 한계가 있으므로 장기간 지속되는 강력한 점막 면역을 유도할 수 있는 백신의 필요성은 여전하다.
우리 대학 의과학대학원 이흥규 교수 연구팀과 한국화학연구원(원장 이영국)은 아데노바이러스 벡터 플랫폼의 비강 접종 코로나19 백신을 개발하고 마우스 모델을 이용해 이 백신이 장기간 지속되는 강력한 점막 면역을 유도함을 규명했다고 29일 밝혔다.
점막 면역이란 면역 체계를 구성하는 요소 중에서도 호흡기, 소화기, 생식기관 등을 구성하는 체내 상피 조직인 점막에서 작용하는 면역을 말한다. 이는 체내와 체외의 접점이 되는 점막에 침입한 외부 인자를 인지하고 제거해 인체를 감염으로부터 보호하는 방어체계다. 점막이 병원체나 외부 항원이 침입하는 주요 경로라는 점에서 점막 면역은 전신적 면역반응에 비해 병원체의 침입에 빠르게 대응해 감염 및 확산을 막을 수 있다는 장점이 있다.
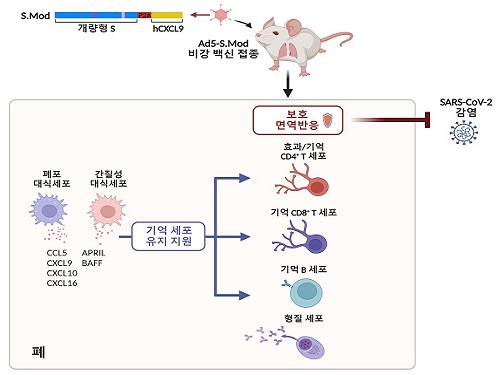
의과학대학원 연수연구원 정희은 박사가 주도하고 박사과정 구근본, 강병훈 연구원, 김현철 박사, 박장현 박사 및 한국화학연구원 김균도 박사가 참여한 이번 연구에서 연구팀은 아데노바이러스 벡터 플랫폼을 기반으로, 개량된 스파이크 단백질 항원 및 인간 유래 면역증강제(CXCL9)을 탑재한 비강 접종 코로나19 백신(Ad5-S.Mod)을 개발해 그 효능을 실험용 쥐를 이용해 검증했다. 연구팀은 인간 유래 면역증강제가 활성화된 T세포를 특정 위치로 이동하도록 유인한다는 점에 주목해, 이를 백신의 효능을 높이기 위한 면역증강제로 이용하였다.
연구팀은 1회 단일 비강 접종, 혹은 근육-비강 2회 접종하여 백신의 효능을 검증했다. 그 결과 비강 백신이 호흡기 점막의 항체 반응 및 기억 T세포 반응을 높은 수준으로 유도할 수 있음을 확인하였으며, 백신 투여군은 1회 단일 접종만으로도 신종 코로나바이러스 감염 시 100% 생존하였다. 또한 백신 접종으로 만들어진 면역반응은 최소 1년간은 유지된다는 것을 규명해 백신의 강력한 점막 면역반응 유도 능력을 입증했다.
또한, 연구팀은 단일세포 전사체 분석법을 이용해 백신을 접종한 실험용 쥐의 폐 대식세포가 기억 T세포 및 B세포를 유지를 돕는 인자들의 주 생산자이며, 폐 대식세포가 제거되면 기억 T세포 및 B세포가 폐 속에서 확연히 감소함을 확인해 이 세포들이 점막 백신 접종으로 만들어진 호흡기 기억 세포의 유지를 돕고 있음을 규명했다.
이번 연구는 인간 유래 면역증강제(CXCL9)로서 활용해 백신의 효능을 강화한 새로운 백신 설계 전략을 제시하고 있다는 점과, 폐 대식세포가 점막 백신에 의해 형성되는 기억 면역반응을 유지하는 데 중요한 역할을 한다는 사실을 새로이 규명하여 다양한 병원체에 대한 비강 백신 개발에 이용할 수 있는 새로운 타겟을 제시하고 있다는 점에서 그 의의가 있다.
의과학대학원 박사후연수연구원 정희은 박사가 제1 저자로 참여한 이번 연구는 바이러스 분야 국제 학술지 `앤티바이럴 리서치(Antiviral Research)' 온라인판으로 6월 14일에 게재됐다. (논문명: Intranasal delivery of an adenovirus-vector vaccine co-expressing a modified spike protein and a genetic adjuvant confers lasting mucosal immunity against SARS-CoV-2, 논문링크: https://doi.org/10.1016/j.antiviral.2023.105656)
한편 이번 연구는 KAIST 코로나 대응 과학기술 뉴딜사업, 2020 과기원공동연구 프로젝트, 한국연구재단 바이오의료기술개발사업, 창의·도전연구 기반지원 사업 및 한국화학연구원 감염병 예방 융합 플랫폼 개발 과제 및 GO! KRICT 사업의 지원을 받아 수행됐다.
호흡기부터 강력 차단하는 코로나19 백신 개발
코로나바이러스감염증-19는 3년 4개월 만에 비상사태가 해제됐으나, 잦은 돌연변이로 인해 발생한 변이들이 계속해서 보고되고 있어 재유행이 시작될 가능성은 여전히 남아 있다. 이 변이들은 백신 접종이나 감염으로 인해 숙주가 획득한 기존의 면역반응을 회피하는 방향으로 진화하고 있다. 현재 시판되는 근육 접종 백신으로는 바이러스의 확산을 억제할 수 있는 점막 면역은 충분히 일으키기 어렵다는 한계가 있으므로 장기간 지속되는 강력한 점막 면역을 유도할 수 있는 백신의 필요성은 여전하다.
우리 대학 의과학대학원 이흥규 교수 연구팀과 한국화학연구원(원장 이영국)은 아데노바이러스 벡터 플랫폼의 비강 접종 코로나19 백신을 개발하고 마우스 모델을 이용해 이 백신이 장기간 지속되는 강력한 점막 면역을 유도함을 규명했다고 29일 밝혔다.
점막 면역이란 면역 체계를 구성하는 요소 중에서도 호흡기, 소화기, 생식기관 등을 구성하는 체내 상피 조직인 점막에서 작용하는 면역을 말한다. 이는 체내와 체외의 접점이 되는 점막에 침입한 외부 인자를 인지하고 제거해 인체를 감염으로부터 보호하는 방어체계다. 점막이 병원체나 외부 항원이 침입하는 주요 경로라는 점에서 점막 면역은 전신적 면역반응에 비해 병원체의 침입에 빠르게 대응해 감염 및 확산을 막을 수 있다는 장점이 있다.
의과학대학원 연수연구원 정희은 박사가 주도하고 박사과정 구근본, 강병훈 연구원, 김현철 박사, 박장현 박사 및 한국화학연구원 김균도 박사가 참여한 이번 연구에서 연구팀은 아데노바이러스 벡터 플랫폼을 기반으로, 개량된 스파이크 단백질 항원 및 인간 유래 면역증강제(CXCL9)을 탑재한 비강 접종 코로나19 백신(Ad5-S.Mod)을 개발해 그 효능을 실험용 쥐를 이용해 검증했다. 연구팀은 인간 유래 면역증강제가 활성화된 T세포를 특정 위치로 이동하도록 유인한다는 점에 주목해, 이를 백신의 효능을 높이기 위한 면역증강제로 이용하였다.
연구팀은 1회 단일 비강 접종, 혹은 근육-비강 2회 접종하여 백신의 효능을 검증했다. 그 결과 비강 백신이 호흡기 점막의 항체 반응 및 기억 T세포 반응을 높은 수준으로 유도할 수 있음을 확인하였으며, 백신 투여군은 1회 단일 접종만으로도 신종 코로나바이러스 감염 시 100% 생존하였다. 또한 백신 접종으로 만들어진 면역반응은 최소 1년간은 유지된다는 것을 규명해 백신의 강력한 점막 면역반응 유도 능력을 입증했다.
또한, 연구팀은 단일세포 전사체 분석법을 이용해 백신을 접종한 실험용 쥐의 폐 대식세포가 기억 T세포 및 B세포를 유지를 돕는 인자들의 주 생산자이며, 폐 대식세포가 제거되면 기억 T세포 및 B세포가 폐 속에서 확연히 감소함을 확인해 이 세포들이 점막 백신 접종으로 만들어진 호흡기 기억 세포의 유지를 돕고 있음을 규명했다.
이번 연구는 인간 유래 면역증강제(CXCL9)로서 활용해 백신의 효능을 강화한 새로운 백신 설계 전략을 제시하고 있다는 점과, 폐 대식세포가 점막 백신에 의해 형성되는 기억 면역반응을 유지하는 데 중요한 역할을 한다는 사실을 새로이 규명하여 다양한 병원체에 대한 비강 백신 개발에 이용할 수 있는 새로운 타겟을 제시하고 있다는 점에서 그 의의가 있다.
의과학대학원 박사후연수연구원 정희은 박사가 제1 저자로 참여한 이번 연구는 바이러스 분야 국제 학술지 `앤티바이럴 리서치(Antiviral Research)' 온라인판으로 6월 14일에 게재됐다. (논문명: Intranasal delivery of an adenovirus-vector vaccine co-expressing a modified spike protein and a genetic adjuvant confers lasting mucosal immunity against SARS-CoV-2, 논문링크: https://doi.org/10.1016/j.antiviral.2023.105656)
한편 이번 연구는 KAIST 코로나 대응 과학기술 뉴딜사업, 2020 과기원공동연구 프로젝트, 한국연구재단 바이오의료기술개발사업, 창의·도전연구 기반지원 사업 및 한국화학연구원 감염병 예방 융합 플랫폼 개발 과제 및 GO! KRICT 사업의 지원을 받아 수행됐다.
2023.07.01
조회수 7109
-
 2023년 리서치데이 개최
'2023년 KAIST 리서치데이(Research Day)'가 16일 오전 대전 본원 학술문화관(E9) 5층 정근모 콘퍼런스홀에서 개최됐다.
리서치데이는 우수 연구자를 포상해 노고를 격려하고, 선정된 우수 연구 성과를 소개해 연구개발(R&D) 정보를 교류하는 자리다. 소통하는 연구문화를 조성해 연구자 간의 결집력을 높이고 융합연구를 활성화하기 위해 2016년부터 매년 개최하고 있다.
이날 행사에서는 김희탁 생명화학공학과 교수가 최고 연구상인 연구대상을 수상하고 ‘계면 공학을 통한 리튬금속전지 및 수계전지 고성능화’를 주제로 시상식 현장에서 기념 강연한다.
김 교수는 리튬이온전지의 에너지밀도 한계를 극복해 전기자동차의 항속거리를 2배 이상 증가시킬 수 있는 리튬금속전지 기술을 설명하고 더 나아가 전기화학, 소재 및 계면공학을 융복합해 에너지 저장과 변환 기술 분야의 난제 해결을 목표로 하는 연구 방향을 소개한다.
연구대상은 직전 5년 동안의 탁월한 연구개발 성과로 KAIST 발전에 크게 이바지한 교원에게 주어지는 상으로 연구의 우수성은 물론 연구계약액, 연구간접비 흡수 실적, 지식재산권 및 기술료 수입 등 종합적인 실적을 반영해 선정한다.
김 교수는 수소전지 등 산업 발전과 밀접하게 관련된 기술을 상용화하는 데 핵심적인 역할을 수행 중인 연구자로 2017년 한국공학한림원이 발표한 ‘2025년 대한민국 성장엔진이 될 미래 100대 기술과 차세대 주역’에 선정되기도 했다.
연구대상을 수상한 김 교수는 “지난 10년간 차세대 배터리, 연료전지 및 수전해 기술을 개발하며 관련 산업이 태동하고 성장하는 데 기여할 수 있어서 큰 보람이었다”라고 수상 소감을 밝혔다.
이어 김 교수는 “재능과 열정 있는 대학원생들과 함께 연구할 수 있는 큰 행운에 감사하는 마음으로 전기화학공학과 계면공학을 접목한 분야의 혁신을 이룰 수 있도록 정진하겠다”라고 덧붙였다.
이 밖에도 이필승(기계공학과)·명현(전기및전자공학부) 교수가 각각 연구상을, 배현민 교수(전기및전자공학부)가 이노베이션상 수상자로 선정됐다.
양용수(물리학과)·한상우(화학과)·유승화(기계공학과) 교수 3명은 한 팀으로 융합 연구상을 받는다. 국제공동연구상에는 조성호 교수(전산학부), 현우 KAIST 학술상은 김범준 교수(생명화학공학과), QAIST 창의도전연구상 수상자에는 박윤수 교수(화학과)가 선정됐다.
이들 수상자는 사전 촬영한 영상 강연을 통해 학생과 동료 연구자에게 연구 경험과 열정에 관한 이야기를 나눌 예정이다.
한편, KAIST의 2022년 대표 R&D 연구성과 10선도 소개된다. 자연과학 분야에서는 ▴준입자적 특성을 가지는 빛 소용돌이의 자발적 생성과 동역학적 제어(서민교 교수‧물리학과) ▴리드버그원자 양자컴퓨터 개발(안재욱 교수‧물리학과)이 선정됐다.
생명과학 분야에서는 ▴염증반응 없이 아밀로이드베타를 제거하는 새로운 치매 치료제 개발(김찬혁 교수, 정원석 교수‧생명과학과)이 이름을 올렸다.
▴사람처럼 느끼고 상처 치유가 가능한 로봇 피부 기술 개발(김정 교수‧기계공학과) ▴수면 조절을 위한 폐루프 초음파 자극 기술 개발(이현주 교수‧전기및전자공학부) ▴악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발(조광현 교수‧바이오및뇌공학과) ▴mRNA 암백신 핵심기술 개발(최정균 교수‧바이오및뇌공학과) ▴미생물 이용한 루테인 생산 기술 개발(이상엽 교수‧생명화학공학과) ▴신축성 인쇄 전자회로 기판 구현을 위한 액체 금속 입자 네트워크 개발(강지형 교수‧신소재공학과)은 공학 분야 우수 성과로 선정됐다.
▴지구 메타버스 기술을 이용한 지구온난화와 태풍 호우 빈도의 상관관계 증명(김형준 교수‧문술미래전략대학원)도 인문사회융합과학 분야의 우수 연구성과로 선정되어 동영상으로 시연·소개된다.
조병관 연구처장은 “올해는 코로나19 비상사태가 해제되어 3년 만에 다 함께 모여 얼굴을 마주 보고 축하할 수 있어 더욱 뜻깊은 자리인 만큼 리서치데이를 통해 다양하고 훌륭한 연구성과들이 널리 공유되고 창의적이고 혁신적인 연구 활동에 큰 영감을 얻는 계기가 되기를 바란다”라고 밝혔다.
2023년 리서치데이 개최
'2023년 KAIST 리서치데이(Research Day)'가 16일 오전 대전 본원 학술문화관(E9) 5층 정근모 콘퍼런스홀에서 개최됐다.
리서치데이는 우수 연구자를 포상해 노고를 격려하고, 선정된 우수 연구 성과를 소개해 연구개발(R&D) 정보를 교류하는 자리다. 소통하는 연구문화를 조성해 연구자 간의 결집력을 높이고 융합연구를 활성화하기 위해 2016년부터 매년 개최하고 있다.
이날 행사에서는 김희탁 생명화학공학과 교수가 최고 연구상인 연구대상을 수상하고 ‘계면 공학을 통한 리튬금속전지 및 수계전지 고성능화’를 주제로 시상식 현장에서 기념 강연한다.
김 교수는 리튬이온전지의 에너지밀도 한계를 극복해 전기자동차의 항속거리를 2배 이상 증가시킬 수 있는 리튬금속전지 기술을 설명하고 더 나아가 전기화학, 소재 및 계면공학을 융복합해 에너지 저장과 변환 기술 분야의 난제 해결을 목표로 하는 연구 방향을 소개한다.
연구대상은 직전 5년 동안의 탁월한 연구개발 성과로 KAIST 발전에 크게 이바지한 교원에게 주어지는 상으로 연구의 우수성은 물론 연구계약액, 연구간접비 흡수 실적, 지식재산권 및 기술료 수입 등 종합적인 실적을 반영해 선정한다.
김 교수는 수소전지 등 산업 발전과 밀접하게 관련된 기술을 상용화하는 데 핵심적인 역할을 수행 중인 연구자로 2017년 한국공학한림원이 발표한 ‘2025년 대한민국 성장엔진이 될 미래 100대 기술과 차세대 주역’에 선정되기도 했다.
연구대상을 수상한 김 교수는 “지난 10년간 차세대 배터리, 연료전지 및 수전해 기술을 개발하며 관련 산업이 태동하고 성장하는 데 기여할 수 있어서 큰 보람이었다”라고 수상 소감을 밝혔다.
이어 김 교수는 “재능과 열정 있는 대학원생들과 함께 연구할 수 있는 큰 행운에 감사하는 마음으로 전기화학공학과 계면공학을 접목한 분야의 혁신을 이룰 수 있도록 정진하겠다”라고 덧붙였다.
이 밖에도 이필승(기계공학과)·명현(전기및전자공학부) 교수가 각각 연구상을, 배현민 교수(전기및전자공학부)가 이노베이션상 수상자로 선정됐다.
양용수(물리학과)·한상우(화학과)·유승화(기계공학과) 교수 3명은 한 팀으로 융합 연구상을 받는다. 국제공동연구상에는 조성호 교수(전산학부), 현우 KAIST 학술상은 김범준 교수(생명화학공학과), QAIST 창의도전연구상 수상자에는 박윤수 교수(화학과)가 선정됐다.
이들 수상자는 사전 촬영한 영상 강연을 통해 학생과 동료 연구자에게 연구 경험과 열정에 관한 이야기를 나눌 예정이다.
한편, KAIST의 2022년 대표 R&D 연구성과 10선도 소개된다. 자연과학 분야에서는 ▴준입자적 특성을 가지는 빛 소용돌이의 자발적 생성과 동역학적 제어(서민교 교수‧물리학과) ▴리드버그원자 양자컴퓨터 개발(안재욱 교수‧물리학과)이 선정됐다.
생명과학 분야에서는 ▴염증반응 없이 아밀로이드베타를 제거하는 새로운 치매 치료제 개발(김찬혁 교수, 정원석 교수‧생명과학과)이 이름을 올렸다.
▴사람처럼 느끼고 상처 치유가 가능한 로봇 피부 기술 개발(김정 교수‧기계공학과) ▴수면 조절을 위한 폐루프 초음파 자극 기술 개발(이현주 교수‧전기및전자공학부) ▴악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발(조광현 교수‧바이오및뇌공학과) ▴mRNA 암백신 핵심기술 개발(최정균 교수‧바이오및뇌공학과) ▴미생물 이용한 루테인 생산 기술 개발(이상엽 교수‧생명화학공학과) ▴신축성 인쇄 전자회로 기판 구현을 위한 액체 금속 입자 네트워크 개발(강지형 교수‧신소재공학과)은 공학 분야 우수 성과로 선정됐다.
▴지구 메타버스 기술을 이용한 지구온난화와 태풍 호우 빈도의 상관관계 증명(김형준 교수‧문술미래전략대학원)도 인문사회융합과학 분야의 우수 연구성과로 선정되어 동영상으로 시연·소개된다.
조병관 연구처장은 “올해는 코로나19 비상사태가 해제되어 3년 만에 다 함께 모여 얼굴을 마주 보고 축하할 수 있어 더욱 뜻깊은 자리인 만큼 리서치데이를 통해 다양하고 훌륭한 연구성과들이 널리 공유되고 창의적이고 혁신적인 연구 활동에 큰 영감을 얻는 계기가 되기를 바란다”라고 밝혔다.
2023.05.16
조회수 7819
-
 강수 관측 오차범위 42.5% 줄인 알고리즘 개발
강수량의 정확한 파악은 지구의 물 순환을 이해하고 수자원과 재해 대응을 위해 중요하다. 강수량 추정을 위한 알고리즘에는 다양한 방법들이 제안되어 왔으며, 최근에는 기계학습을 이용한 방법들이 많이 제안되고 있다.
우리 대학 문술미래전략대학원(건설및환경공학과 및 녹색성장지속가능대학원 겸임) 김형준 교수와 도쿄대 등으로 구성된 국제 공동연구팀이 인공위성에 탑재된 마이크로파 라디오미터의 관측값을 이용해 지상 강수량을 추정하는 새로운 기계학습 방법을 제안했다고 25일 밝혔다. 연구팀은 기존의 방법과 비교해 전 강수량에 대해 오차(RMSE)를 최소 15.9%에서 최대 42.5%까지 줄이는 데 성공했다.
단순한 데이터 주도(data-driven)모델은 대량의 훈련 데이터가 필요하고 물리적인 일관성이 보장되지 않으며 결과의 원인 분석이 어렵다는 등의 문제가 있었다. 연구팀은 이번 연구에서 위성 강수량 추정에 대한 분야 지식을 명시적으로 포함함으로써 학습 모델 내의 상호 의존적인 지식 교환을 구현했다. 구체적으로, 멀티태스크 학습(multitask learning)이라는 심층 학습 기법을 사용해 강수 여부를 인식하는 분류 모델과 강수 강도를 추정하는 회귀 모델을 통합하고 동시에 학습시켰다.
이번 연구에서 제안한 기계학습 모델에는 이번에 포함된 메커니즘 외에도 다양한 물리적 메커니즘을 포함할 수 있다. 예를 들어, 비 또는 눈, 진눈깨비 등 강수 종류의 분류 및 상승 기류 또는 층상 구름 유형 등 강수를 일으키는 구름 유형의 분류를 포함함으로써 앞으로 추정의 정확도가 더욱 향상될 것으로 기대된다.
김형준 교수의 이번 연구 결과는 국제 학술지 ‘지구물리 연구 레터(Geophysical Research Letters)’에 지난 4월 16일 출판됐다. (논문명: Multi-Task Learning for Simultaneous Retrievals of Passive Microwave Precipitation Estimates and Rain/No-Rain Classification; doi:10.1029/2022GL102283)
한편 이번 연구는 한국연구재단 해외우수과학자유치사업(BP+)와 정보통신기획평가원 인공지능대학원지원(한국과학기술원)지원을 받아 수행됐다.
강수 관측 오차범위 42.5% 줄인 알고리즘 개발
강수량의 정확한 파악은 지구의 물 순환을 이해하고 수자원과 재해 대응을 위해 중요하다. 강수량 추정을 위한 알고리즘에는 다양한 방법들이 제안되어 왔으며, 최근에는 기계학습을 이용한 방법들이 많이 제안되고 있다.
우리 대학 문술미래전략대학원(건설및환경공학과 및 녹색성장지속가능대학원 겸임) 김형준 교수와 도쿄대 등으로 구성된 국제 공동연구팀이 인공위성에 탑재된 마이크로파 라디오미터의 관측값을 이용해 지상 강수량을 추정하는 새로운 기계학습 방법을 제안했다고 25일 밝혔다. 연구팀은 기존의 방법과 비교해 전 강수량에 대해 오차(RMSE)를 최소 15.9%에서 최대 42.5%까지 줄이는 데 성공했다.
단순한 데이터 주도(data-driven)모델은 대량의 훈련 데이터가 필요하고 물리적인 일관성이 보장되지 않으며 결과의 원인 분석이 어렵다는 등의 문제가 있었다. 연구팀은 이번 연구에서 위성 강수량 추정에 대한 분야 지식을 명시적으로 포함함으로써 학습 모델 내의 상호 의존적인 지식 교환을 구현했다. 구체적으로, 멀티태스크 학습(multitask learning)이라는 심층 학습 기법을 사용해 강수 여부를 인식하는 분류 모델과 강수 강도를 추정하는 회귀 모델을 통합하고 동시에 학습시켰다.
이번 연구에서 제안한 기계학습 모델에는 이번에 포함된 메커니즘 외에도 다양한 물리적 메커니즘을 포함할 수 있다. 예를 들어, 비 또는 눈, 진눈깨비 등 강수 종류의 분류 및 상승 기류 또는 층상 구름 유형 등 강수를 일으키는 구름 유형의 분류를 포함함으로써 앞으로 추정의 정확도가 더욱 향상될 것으로 기대된다.
김형준 교수의 이번 연구 결과는 국제 학술지 ‘지구물리 연구 레터(Geophysical Research Letters)’에 지난 4월 16일 출판됐다. (논문명: Multi-Task Learning for Simultaneous Retrievals of Passive Microwave Precipitation Estimates and Rain/No-Rain Classification; doi:10.1029/2022GL102283)
한편 이번 연구는 한국연구재단 해외우수과학자유치사업(BP+)와 정보통신기획평가원 인공지능대학원지원(한국과학기술원)지원을 받아 수행됐다.
2023.04.25
조회수 8607
-
 폐암 전이를 막고 치료 가능한 세포로 되돌리는 원천기술 개발
고령화에 따라 암의 발생이 늘어나면서 암은 인류의 건강수명을 위협하는 가장 치명적인 질환이 됐다. 특히 조기 발견을 놓쳐 여러 장기로 전이될 때 암의 치명률은 높아진다. 이러한 문제를 해결하기 위해 암세포의 전이 능력을 제거하거나 낮추려는 시도가 이어졌으나 오히려 중간상태의 불안정한 암세포 상태가 되면서 더욱 악성을 보이게 되어 암 치료의 난제로 남아 있었다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 폐암 세포의 성질을 변환시켜 암세포의 전이를 막고 약물에 대한 저항성을 제거할 수 있는 기술을 개발하는 데 성공했다고 30일 밝혔다.
조광현 교수 연구팀은 폐암 세포의 전이능력이 없는 상피(epithelial, 세포 방향성이 있어 유동성 없이 표면조직을 이루는 상태)세포에서 전이가 가능한 중간엽(mesenchymal, 방향성없이 개별적인 이동성을 가진 상태)세포로 변화되는 천이 과정(epithelial-to-mesenchymal transition, 이하 EMT)에서 나타나는 다양한 암세포 상태들을 나타낼 수 있는 세포의 분자 네트워크 수학모델을 만들었다. 컴퓨터 시뮬레이션 분석과 분자 세포실험을 통해 악성종양으로 증식하여 인접한 조직이나 세포로 침입하거나 약물에 내성을 가진 중간엽세포 상태에서 전이가 되지 않은 상피세포 상태로 다시 바뀔수 있도록 세포의 성질을 변환시켜주는 핵심 조절인자들을 발굴했다.
특히 이 과정에서 그동안 난제로 남아 있었던 중간과정의 불안정한 암세포 상태(EMT 하이브리드 세포 상태)를 피하는 동시에 항암 화학요법(chemotherapy) 치료가 잘 되는 상피세포 상태로 온전히 역전하는 데 성공했다.
우리 대학 김남희 박사과정, 황채영 박사, 김태영 연구원, 김현진 박사과정이 참여한 이번 연구 결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치(Cancer Research)' 1월 30일 字 온라인판 논문으로 출판됐다. (논문명: A cell fate reprogramming strategy reverses epithelial-to-mesenchymal transition of lung cancer cells while avoiding hybrid states)
암세포의 EMT 과정에서 불완전한 천이(변화과정)로 인해 발생하는 EMT 하이브리드 상태의 세포들은 상피세포와 중간엽세포의 특성을 모두 갖고 있으며, 높은 줄기세포능*을 획득해 약물저항성 및 전이 잠재성이 큰 것으로 알려져 있다. 불안정한 암세포 상태(EMT)는 매우 복잡하여 높은 전이 능력과 약물저항성을 가지는 EMT 하이브리드 세포 상태를 회피하면서 암세포를 전이 능력과 약물저항성이 제거된 상피세포 상태로 온전히 역전시키는 것은 매우 어려운 일이었다.
*줄기세포능: 줄기세포가 지속적 자가복제를 할 수 있도록 하는 세포내 신호전달체계
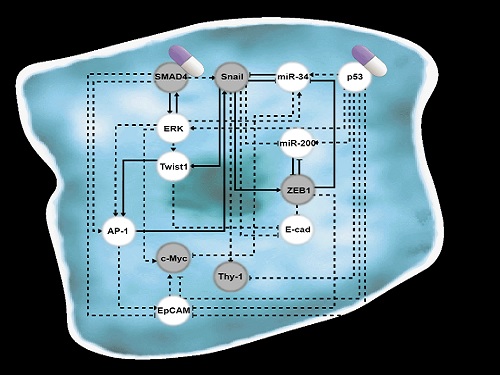
조광현 교수 연구팀은 복잡한 EMT를 지배하는 유전자 조절 네트워크의 수학모델을 정립한 후, 대규모 컴퓨터 시뮬레이션 분석 및 복잡계 네트워크 제어기술을 적용해 중간엽세포 상태인 폐암 세포를 EMT 하이브리드 세포 상태를 회피하면서 전이 능력이 상실된 상피세포 상태로 역전시킬 수 있는 세 개의 핵심 분자 타깃인 ‘p53 (암 억제 단백질)’, ‘SMAD4 (EMT를 조절하는 대표적 신호전달을 매개하는 중심물질로 SMAD 그룹에 포함된 단백질)’와 ‘ERK1/2 (세포의 성장 및 분화에 관여하는 조절인자)’를 발굴하고 이를 분자 세포실험을 통해 검증했다. 이러한 발견은 실제 인체 내 암 조직의 환경에서처럼 자극이 주어진 상황에서 중간엽세포 상태가 상피세포 상태로 역전될 수 있음을 증명해 그 의미가 크다.
암세포의 비정상적인 EMT는 암세포의 이동과 침윤, 화학요법 치료에 대한 반응성 변화, 강화된 줄기세포능, 암의 전이 등 다양한 악성 형질로 이어지게 된다. 특히 암세포의 전이 능력 획득은 암 환자의 예후를 결정짓는 매우 중요한 요소다. 이번에 개발된 폐암 세포의 EMT 역전 기술은 암세포를 리프로그래밍해 높은 가소성과 전이 능력을 제거하고 항암 화학치료의 반응성을 높이도록 하는 새로운 항암 치료 전략이다.
조광현 교수는 "높은 전이 능력과 약물저항성을 획득한 폐암 세포를 전이 능력이 제거되고 항암 화학요법치료에 민감한 상피세포 상태로 온전히 역전시키는 데 성공함으로써 암 환자의 예후를 증진할 수 있는 새로운 치료전략을 제시했다ˮ라고 말했다.
조광현 교수 연구팀은 암세포를 정상세포로 되돌리는 가역 치료원리를 최초로 제시한 뒤 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구 결과를 발표했고, 2022년 1월에는 가장 악성인 유방암세포를 호르몬 치료가 가능한 유방암세포로 리프로그래밍하는 연구에 성공한 바 있다. 이번 연구 결과는 전이 능력을 획득한 폐암 세포 상태를 전이 능력이 제거되고 약물 반응성이 증진된 세포 상태로 되돌리는 가역화 기술 개발의 세 번째 성과다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 등의 지원으로 수행됐다.
폐암 전이를 막고 치료 가능한 세포로 되돌리는 원천기술 개발
고령화에 따라 암의 발생이 늘어나면서 암은 인류의 건강수명을 위협하는 가장 치명적인 질환이 됐다. 특히 조기 발견을 놓쳐 여러 장기로 전이될 때 암의 치명률은 높아진다. 이러한 문제를 해결하기 위해 암세포의 전이 능력을 제거하거나 낮추려는 시도가 이어졌으나 오히려 중간상태의 불안정한 암세포 상태가 되면서 더욱 악성을 보이게 되어 암 치료의 난제로 남아 있었다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 폐암 세포의 성질을 변환시켜 암세포의 전이를 막고 약물에 대한 저항성을 제거할 수 있는 기술을 개발하는 데 성공했다고 30일 밝혔다.
조광현 교수 연구팀은 폐암 세포의 전이능력이 없는 상피(epithelial, 세포 방향성이 있어 유동성 없이 표면조직을 이루는 상태)세포에서 전이가 가능한 중간엽(mesenchymal, 방향성없이 개별적인 이동성을 가진 상태)세포로 변화되는 천이 과정(epithelial-to-mesenchymal transition, 이하 EMT)에서 나타나는 다양한 암세포 상태들을 나타낼 수 있는 세포의 분자 네트워크 수학모델을 만들었다. 컴퓨터 시뮬레이션 분석과 분자 세포실험을 통해 악성종양으로 증식하여 인접한 조직이나 세포로 침입하거나 약물에 내성을 가진 중간엽세포 상태에서 전이가 되지 않은 상피세포 상태로 다시 바뀔수 있도록 세포의 성질을 변환시켜주는 핵심 조절인자들을 발굴했다.
특히 이 과정에서 그동안 난제로 남아 있었던 중간과정의 불안정한 암세포 상태(EMT 하이브리드 세포 상태)를 피하는 동시에 항암 화학요법(chemotherapy) 치료가 잘 되는 상피세포 상태로 온전히 역전하는 데 성공했다.
우리 대학 김남희 박사과정, 황채영 박사, 김태영 연구원, 김현진 박사과정이 참여한 이번 연구 결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치(Cancer Research)' 1월 30일 字 온라인판 논문으로 출판됐다. (논문명: A cell fate reprogramming strategy reverses epithelial-to-mesenchymal transition of lung cancer cells while avoiding hybrid states)
암세포의 EMT 과정에서 불완전한 천이(변화과정)로 인해 발생하는 EMT 하이브리드 상태의 세포들은 상피세포와 중간엽세포의 특성을 모두 갖고 있으며, 높은 줄기세포능*을 획득해 약물저항성 및 전이 잠재성이 큰 것으로 알려져 있다. 불안정한 암세포 상태(EMT)는 매우 복잡하여 높은 전이 능력과 약물저항성을 가지는 EMT 하이브리드 세포 상태를 회피하면서 암세포를 전이 능력과 약물저항성이 제거된 상피세포 상태로 온전히 역전시키는 것은 매우 어려운 일이었다.
*줄기세포능: 줄기세포가 지속적 자가복제를 할 수 있도록 하는 세포내 신호전달체계
조광현 교수 연구팀은 복잡한 EMT를 지배하는 유전자 조절 네트워크의 수학모델을 정립한 후, 대규모 컴퓨터 시뮬레이션 분석 및 복잡계 네트워크 제어기술을 적용해 중간엽세포 상태인 폐암 세포를 EMT 하이브리드 세포 상태를 회피하면서 전이 능력이 상실된 상피세포 상태로 역전시킬 수 있는 세 개의 핵심 분자 타깃인 ‘p53 (암 억제 단백질)’, ‘SMAD4 (EMT를 조절하는 대표적 신호전달을 매개하는 중심물질로 SMAD 그룹에 포함된 단백질)’와 ‘ERK1/2 (세포의 성장 및 분화에 관여하는 조절인자)’를 발굴하고 이를 분자 세포실험을 통해 검증했다. 이러한 발견은 실제 인체 내 암 조직의 환경에서처럼 자극이 주어진 상황에서 중간엽세포 상태가 상피세포 상태로 역전될 수 있음을 증명해 그 의미가 크다.
암세포의 비정상적인 EMT는 암세포의 이동과 침윤, 화학요법 치료에 대한 반응성 변화, 강화된 줄기세포능, 암의 전이 등 다양한 악성 형질로 이어지게 된다. 특히 암세포의 전이 능력 획득은 암 환자의 예후를 결정짓는 매우 중요한 요소다. 이번에 개발된 폐암 세포의 EMT 역전 기술은 암세포를 리프로그래밍해 높은 가소성과 전이 능력을 제거하고 항암 화학치료의 반응성을 높이도록 하는 새로운 항암 치료 전략이다.
조광현 교수는 "높은 전이 능력과 약물저항성을 획득한 폐암 세포를 전이 능력이 제거되고 항암 화학요법치료에 민감한 상피세포 상태로 온전히 역전시키는 데 성공함으로써 암 환자의 예후를 증진할 수 있는 새로운 치료전략을 제시했다ˮ라고 말했다.
조광현 교수 연구팀은 암세포를 정상세포로 되돌리는 가역 치료원리를 최초로 제시한 뒤 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구 결과를 발표했고, 2022년 1월에는 가장 악성인 유방암세포를 호르몬 치료가 가능한 유방암세포로 리프로그래밍하는 연구에 성공한 바 있다. 이번 연구 결과는 전이 능력을 획득한 폐암 세포 상태를 전이 능력이 제거되고 약물 반응성이 증진된 세포 상태로 되돌리는 가역화 기술 개발의 세 번째 성과다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 등의 지원으로 수행됐다.
2023.01.30
조회수 11537
 코로나바이러스 전염 메커니즘 규명
중증급성호흡기증후군(이하 SARS) 코로나바이러스와 같은 코로나 19(COVID-19)는 전 세계적 팬데믹으로 짧은 시간 안에 확산되었지만 왜 급격히 복제돼 빠르게 전염되는지 기전이 아직까지 규명되지 않았다. 우리 연구진이 코로나바이러스 핵심 효소 단백질(헬리케이스)의 복제과정이 급격히 촉진되어 전염되는 메커니즘을 밝혀내며 바이러스 백신 및 치료제 개발에 새로운 가능성을 제시했다.
우리 대학 생명과학과 이광록 교수 연구팀이 nsp13 단백질*은 두 가지 활성을 가지고 있어 시너지 효과를 내며, 이를 통해 SARS 코로나바이러스의 유전물질인 RNA 복제를 촉진한다는 기전을 규명했다고 17일 밝혔다.
*nsp13 단백질: SARS 코로나바이러스의 헬리케이스로, 바이러스가 증식하는 데 필수적인 유전자 복제와 전사 과정에 중요한 효소이다. 헬리케이스는 마치 지퍼를 열고 닫는 것처럼 DNA나 RNA의 꼬인 구조를 풀어주는데, 유전정보를 읽거나 복제할 때 유전물질을 먼저 풀려야 하므로 필수적이다. 쉽게 말해, 헬리케이스는 엉킨 실타래를 푸는 효소단백질이다.
여기 두 가지 활성에 해당되는 첫번째 헬리케이스 활성은 DNA 또는 RNA와 같은 이중 가닥 핵산을 단일 가닥으로 풀어주는 효소 기능이며, 복제나 전사 과정을 촉진시킨다. 두번째 RNA 샤페론 활성은 핵산 구조의 올바른 접힘(folding)과 풀림 기능을 돕는 단백질로, 잘못된 RNA를 교정하거나 안정성을 향상시켜 세포 내 RNA 대사과정을 돕는 역할을 한다.
코로나바이러스가 빠르게 전파하기 위해서는 바이러스의 유전물질을 빠르게 복제하고 구성성분인 단백질을 생산해서 이들을 조합하는 것이 필수적이다.
연구팀은 첫 번째 단계인 유전물질의 RNA 복제가 다른 바이러스에 비해 왜 빠르게 일어나는지 알려지지 않았으나, nsp13 단백질이 기존의 헬리케이스 활성과 이제까지 알려지지 않은 새로운 샤페론 활성으로 유전자 복제 과정을 빠르게 촉진한다는 것을 규명했다.
nsp13 단백질은 유전적으로 잘 보존되어 다양한 변이 코로나바이러스에 대응하는 백신이나 감염 치료의 중요 표적이지만, 정확한 작용 메커니즘에 대해서는 완전한 이해가 부족했다.
연구팀은 nsp13 헬리케이스가 ATP(아데노신 삼인산)*를 분해하여 나온 화학에너지를 이용하여 유전물질인 RNA의 꼬인 구조를 단일 가닥으로 풀어주고 부산물로 ADP(아데노신 이인산)*가 생성하게 된다. 이때 생성된 ADP가 nsp13와 재결합하게 되면 샤페론 기능을 활성화시켜 RNA 이차구조를 추가로 불안정화한다는 사실을 알아냈다.
*ATP(아데노신 삼인산)는 충전된 배터리처럼 에너지를 담고 있고 효소가 일을 할 때는 에너지를 공급해준다. ATP는 인산 3개를 가지고 있어 인산이 분해 될 때 에너지를 방출하고 인산 2개를 가진 ADP(아데노신 이인산)를 부산물로 생성한다.
결론적으로 헬리케이스 활성과 샤페론 활성이 시공간적으로 동시에 협력해 RNA 복제를 촉진하게 된다는 새로운 방식의 작용기전을 규명했다.
이광록 교수는 “이번 연구는 대표적 핵산-효소 단백질인 헬리케이스가 ADP를 통해 샤페론적 활성을 나타내는 새로운 발견이며, 이를 통해 헬리케이스의 기능 다양성에 대한 이해의 폭을 넓혀주고, SARS 코로나바이러스의 다양한 변이에 대응할 효과적 치료제 및 백신 개발의 실마리를 제공할 것으로 기대한다”라고 연구 결과의 의의를 밝혔다.
이 연구는 유정민 박사가 제 1저자로 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF: 16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 29일 게재됐다. (논문명 : A novel ADP-directed chaperone function facilitates the ATP-driven motor activity of SARS-CoV helicase) (doi: 10.1093/nar/gkaf034)
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구지원, 선도연구센터 지원사업, 글로벌 기초연구 지원사업과 합성생물학핵심기술개발사업의 지원을 받아 수행됐다.
2025.02.17 조회수 3762
코로나바이러스 전염 메커니즘 규명
중증급성호흡기증후군(이하 SARS) 코로나바이러스와 같은 코로나 19(COVID-19)는 전 세계적 팬데믹으로 짧은 시간 안에 확산되었지만 왜 급격히 복제돼 빠르게 전염되는지 기전이 아직까지 규명되지 않았다. 우리 연구진이 코로나바이러스 핵심 효소 단백질(헬리케이스)의 복제과정이 급격히 촉진되어 전염되는 메커니즘을 밝혀내며 바이러스 백신 및 치료제 개발에 새로운 가능성을 제시했다.
우리 대학 생명과학과 이광록 교수 연구팀이 nsp13 단백질*은 두 가지 활성을 가지고 있어 시너지 효과를 내며, 이를 통해 SARS 코로나바이러스의 유전물질인 RNA 복제를 촉진한다는 기전을 규명했다고 17일 밝혔다.
*nsp13 단백질: SARS 코로나바이러스의 헬리케이스로, 바이러스가 증식하는 데 필수적인 유전자 복제와 전사 과정에 중요한 효소이다. 헬리케이스는 마치 지퍼를 열고 닫는 것처럼 DNA나 RNA의 꼬인 구조를 풀어주는데, 유전정보를 읽거나 복제할 때 유전물질을 먼저 풀려야 하므로 필수적이다. 쉽게 말해, 헬리케이스는 엉킨 실타래를 푸는 효소단백질이다.
여기 두 가지 활성에 해당되는 첫번째 헬리케이스 활성은 DNA 또는 RNA와 같은 이중 가닥 핵산을 단일 가닥으로 풀어주는 효소 기능이며, 복제나 전사 과정을 촉진시킨다. 두번째 RNA 샤페론 활성은 핵산 구조의 올바른 접힘(folding)과 풀림 기능을 돕는 단백질로, 잘못된 RNA를 교정하거나 안정성을 향상시켜 세포 내 RNA 대사과정을 돕는 역할을 한다.
코로나바이러스가 빠르게 전파하기 위해서는 바이러스의 유전물질을 빠르게 복제하고 구성성분인 단백질을 생산해서 이들을 조합하는 것이 필수적이다.
연구팀은 첫 번째 단계인 유전물질의 RNA 복제가 다른 바이러스에 비해 왜 빠르게 일어나는지 알려지지 않았으나, nsp13 단백질이 기존의 헬리케이스 활성과 이제까지 알려지지 않은 새로운 샤페론 활성으로 유전자 복제 과정을 빠르게 촉진한다는 것을 규명했다.
nsp13 단백질은 유전적으로 잘 보존되어 다양한 변이 코로나바이러스에 대응하는 백신이나 감염 치료의 중요 표적이지만, 정확한 작용 메커니즘에 대해서는 완전한 이해가 부족했다.
연구팀은 nsp13 헬리케이스가 ATP(아데노신 삼인산)*를 분해하여 나온 화학에너지를 이용하여 유전물질인 RNA의 꼬인 구조를 단일 가닥으로 풀어주고 부산물로 ADP(아데노신 이인산)*가 생성하게 된다. 이때 생성된 ADP가 nsp13와 재결합하게 되면 샤페론 기능을 활성화시켜 RNA 이차구조를 추가로 불안정화한다는 사실을 알아냈다.
*ATP(아데노신 삼인산)는 충전된 배터리처럼 에너지를 담고 있고 효소가 일을 할 때는 에너지를 공급해준다. ATP는 인산 3개를 가지고 있어 인산이 분해 될 때 에너지를 방출하고 인산 2개를 가진 ADP(아데노신 이인산)를 부산물로 생성한다.
결론적으로 헬리케이스 활성과 샤페론 활성이 시공간적으로 동시에 협력해 RNA 복제를 촉진하게 된다는 새로운 방식의 작용기전을 규명했다.
이광록 교수는 “이번 연구는 대표적 핵산-효소 단백질인 헬리케이스가 ADP를 통해 샤페론적 활성을 나타내는 새로운 발견이며, 이를 통해 헬리케이스의 기능 다양성에 대한 이해의 폭을 넓혀주고, SARS 코로나바이러스의 다양한 변이에 대응할 효과적 치료제 및 백신 개발의 실마리를 제공할 것으로 기대한다”라고 연구 결과의 의의를 밝혔다.
이 연구는 유정민 박사가 제 1저자로 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF: 16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 29일 게재됐다. (논문명 : A novel ADP-directed chaperone function facilitates the ATP-driven motor activity of SARS-CoV helicase) (doi: 10.1093/nar/gkaf034)
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구지원, 선도연구센터 지원사업, 글로벌 기초연구 지원사업과 합성생물학핵심기술개발사업의 지원을 받아 수행됐다.
2025.02.17 조회수 3762 암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22 조회수 4571
암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22 조회수 4571 기계공학과 유홍기 교수 연구팀, 빛으로 동맥경화반 동시 진단 및 치료 기술 개발
관상동맥 내 고위험 동맥경화반은 파열과 협착을 유발하여 빠르게 혈관을 막을 수 있어 진단과 동시에 즉각적인 치료가 필요하다.
우리 대학 기계공학과 유홍기 교수 연구팀은 고려대학교구로병원 심혈관센터 김진원 교수팀, 중앙대학교 시스템생명공학과 박경순 교수팀과의 공동연구를 통해, 빛을 이용하여 동맥경화반 진단과 치료를 동시에 할 수 있는 새로운 원천 기술을 개발하였다.
이 기술은 유홍기 교수 연구팀이 개발한 광단층-분자영상 결합 카테터 기반 정밀 영상 시스템과 광치료 카테터를 이용해 빛을 조사하여 고위험 병변을 정확히 진단하고 치료하는 방법이다.
동맥경화반 내 대식세포의 특정 수용체를 표적하는 전달체와 광활성체를 결합한 테라노스틱 제제를 혈관에 투여한 후 혈관내 카테터를 이용해 위험 부위를 찾아내고 그 부위에 빛을 조사하였다. 그 결과, 고위험 동맥경화반을 실시간 정밀 영상으로 진단하였고 동시에 성공적으로 치료할 수 있었다.
치료 후 효과를 정밀 영상 시스템을 통해 생체 내에서 추적 검증했으며, 광활성에 의한 자가소화를 유도해 사멸 세포를 탐식 및 제거, 콜레스테롤 유출로 염증을 해소하고 콜라겐 조직 증가를 유도해 병변이 치료 및 안정화 됨을 밝혔다.
연구진은 “이번 연구를 통해 기존 방법의 한계였던 고위험 동맥경화반의 정밀 진단을 가능케 하였고, 동시에 광치료 시스템을 이용해 빛을 전달하여 고위험 동맥경화반을 치료하고 안정화하는 데 성공했다는 점에서 큰 의의가 있다.”라고 밝혔다. 또한 “기존 동맥경화반 치료법인 스텐트 치료가 가지는 이물질 잔존 위험을 극복할 수 있으며, 심혈관 진단 및 치료 분야에서 새로운 가능성을 제시했다.”고 했다. 연구진은 “이번 연구 결과를 바탕으로, 추후 임상 적용을 위한 시제품 개발을 적극적으로 추진할 계획”이라고 덧붙였다.
이번 연구 결과는 기계공학과 김연훈 박사과정생이 공동 제1저자로, 유홍기 교수가 공동교신저자로 참여하였으며, 국제학술지 Circulation Research (5-year IF: 20.3) 에 게재되었다.
한편 이번 연구는 한국연구재단이 주관하는 원천기술개발사업의 지원을 받아 수행됐다.
2024.08.23 조회수 5118
기계공학과 유홍기 교수 연구팀, 빛으로 동맥경화반 동시 진단 및 치료 기술 개발
관상동맥 내 고위험 동맥경화반은 파열과 협착을 유발하여 빠르게 혈관을 막을 수 있어 진단과 동시에 즉각적인 치료가 필요하다.
우리 대학 기계공학과 유홍기 교수 연구팀은 고려대학교구로병원 심혈관센터 김진원 교수팀, 중앙대학교 시스템생명공학과 박경순 교수팀과의 공동연구를 통해, 빛을 이용하여 동맥경화반 진단과 치료를 동시에 할 수 있는 새로운 원천 기술을 개발하였다.
이 기술은 유홍기 교수 연구팀이 개발한 광단층-분자영상 결합 카테터 기반 정밀 영상 시스템과 광치료 카테터를 이용해 빛을 조사하여 고위험 병변을 정확히 진단하고 치료하는 방법이다.
동맥경화반 내 대식세포의 특정 수용체를 표적하는 전달체와 광활성체를 결합한 테라노스틱 제제를 혈관에 투여한 후 혈관내 카테터를 이용해 위험 부위를 찾아내고 그 부위에 빛을 조사하였다. 그 결과, 고위험 동맥경화반을 실시간 정밀 영상으로 진단하였고 동시에 성공적으로 치료할 수 있었다.
치료 후 효과를 정밀 영상 시스템을 통해 생체 내에서 추적 검증했으며, 광활성에 의한 자가소화를 유도해 사멸 세포를 탐식 및 제거, 콜레스테롤 유출로 염증을 해소하고 콜라겐 조직 증가를 유도해 병변이 치료 및 안정화 됨을 밝혔다.
연구진은 “이번 연구를 통해 기존 방법의 한계였던 고위험 동맥경화반의 정밀 진단을 가능케 하였고, 동시에 광치료 시스템을 이용해 빛을 전달하여 고위험 동맥경화반을 치료하고 안정화하는 데 성공했다는 점에서 큰 의의가 있다.”라고 밝혔다. 또한 “기존 동맥경화반 치료법인 스텐트 치료가 가지는 이물질 잔존 위험을 극복할 수 있으며, 심혈관 진단 및 치료 분야에서 새로운 가능성을 제시했다.”고 했다. 연구진은 “이번 연구 결과를 바탕으로, 추후 임상 적용을 위한 시제품 개발을 적극적으로 추진할 계획”이라고 덧붙였다.
이번 연구 결과는 기계공학과 김연훈 박사과정생이 공동 제1저자로, 유홍기 교수가 공동교신저자로 참여하였으며, 국제학술지 Circulation Research (5-year IF: 20.3) 에 게재되었다.
한편 이번 연구는 한국연구재단이 주관하는 원천기술개발사업의 지원을 받아 수행됐다.
2024.08.23 조회수 5118 바이러스와 세균의 진화를 규명하다
바이러스는 특정 세포 안에 침투했을 때만 증식의 생명력을 띠고 그 외에는 무생물 같으며, 사람 세포를 감염시키는 코로나19 바이러스, 세균을 잡아먹으며 증식하는 세균바이러스 등이 있다. 국내 연구진이 세균바이러스가 RNA 합성을 마무리 짓는 방식에 해체종결(1)만 있고 재생종결(2)은 없다는 사실을 밝히고 RNA 의약품 개발에 응용될 가능성을 높였다.
(1)해체종결: 합성 복합체가 중합효소, DNA, RNA로 해체
(2)재생종결: RNA만 분리되고 중합효소는 DNA에 남아 재생
우리 대학 생명과학과 강창원 명예교수(줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동연구팀이 세균의 리보핵산(RNA) 합성방식 두 가지 중 하나가 바이러스에는 없다는 것을 발견해, 세균이 바이러스로부터 진화하면서 획득한 방식을 처음 밝힌 연구 논문을 핵산 분야 최상급 국제학술지에 게재했다고 19일 밝혔다.
유전자 DNA의 유전정보에 따라 RNA를 합성하는 효소가 RNA 중합효소다. 이는 유전정보가 DNA에서 RNA로 옮겨 적히기에 전사(轉寫)라고 부르는 유전자 발현 첫 단계를 수행하며, RNA 백신 등 첨단 RNA 의약품을 개발 생산하는 데에 쓰인다. 연구팀은 세균바이러스의 RNA 중합효소를 연구해서 생물로 진화하기 이전 태초의 RNA 합성(전사) 방식을 밝힌 것이다.
유전자에 따라 다른 게 아니라 어느 유전자든 전사 마무리 방식에 두 가지가 있다는 것을 수년 전 세균에서 발견했었다. 그리고 세균보다 진화한 진핵생물 효모의 유전자 전사에서도 두 방식이 모두 쓰인다는 것이 지난달에 보고됐다. 사람도 진핵생물이어서, 세균과 효모뿐 아니라 사람까지 온갖 생물의 유전자 전사에 두 방식 모두 쓰일 개연성이 커졌다.
그런데 이번 연구에서 세균바이러스의 방식은 세균이나 효모와 사뭇 다르다는 것이 밝혀졌다. 바이러스의 경우 재생종결 없이 해체종결만 일어나는 것이다. 이를 토대로, 연구팀은 RNA 중합효소가 세균에서 바이러스와 달리 적응하면서 해체종결에 재생종결이 추가돼 두 방식이 공존하게 되었고, 최소한 효모로의 진화에서 그대로 보존됐다는 해석을 내놓았다.
이번 연구에서 거푸집 DNA와 전사물 RNA에 각기 다른 형광물질을 부착해 전사 복합체 하나하나의 형광을 실시간으로 측정하는 단일분자 형광기술 연구기법이 사용됐다. 전사 종결로 RNA가 방출될 때 DNA가 효소에 붙어있는지 떨어지는지를 낱낱이 구별할 수 있게 설계한 것이 특장점이다. 특히 형광물질이 전사 반응에 지장을 주지 않도록 하는 게 관건이었다.
송은호 박사후연구원과 한선 박사과정 대학원생이 공동 제1 저자로 참여한 논문(제목: Single-mode termination of phage transcriptions, disclosing bacterial adaptation for facilitated reinitiations)이 학술지 핵산연구(Nucleic Acids Research)에 7월 16일 게재됐다. 이로써 강창원 교수와 홍성철 교수는 2017년부터 총 8편의 논문을 공동으로 발표했다.
강창원 교수는 "이번 연구를 통해 수 초 동안의 분자 반응에서 유구한 진화과정을 밝혀냈고, 앞으로 더 광범위한 진화를 연구할 계획이다”라고 했다. 홍성철 교수는 "분자 하나하나를 관찰하여 복잡한 생물체의 진화를 파악했고, 이런 단일분자 연구기법을 차세대 RNA 의약품과 진단 시약의 개발에 응용하는 연구로 이어가고자 한다”라고 했다.
2024.07.19 조회수 6423
바이러스와 세균의 진화를 규명하다
바이러스는 특정 세포 안에 침투했을 때만 증식의 생명력을 띠고 그 외에는 무생물 같으며, 사람 세포를 감염시키는 코로나19 바이러스, 세균을 잡아먹으며 증식하는 세균바이러스 등이 있다. 국내 연구진이 세균바이러스가 RNA 합성을 마무리 짓는 방식에 해체종결(1)만 있고 재생종결(2)은 없다는 사실을 밝히고 RNA 의약품 개발에 응용될 가능성을 높였다.
(1)해체종결: 합성 복합체가 중합효소, DNA, RNA로 해체
(2)재생종결: RNA만 분리되고 중합효소는 DNA에 남아 재생
우리 대학 생명과학과 강창원 명예교수(줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동연구팀이 세균의 리보핵산(RNA) 합성방식 두 가지 중 하나가 바이러스에는 없다는 것을 발견해, 세균이 바이러스로부터 진화하면서 획득한 방식을 처음 밝힌 연구 논문을 핵산 분야 최상급 국제학술지에 게재했다고 19일 밝혔다.
유전자 DNA의 유전정보에 따라 RNA를 합성하는 효소가 RNA 중합효소다. 이는 유전정보가 DNA에서 RNA로 옮겨 적히기에 전사(轉寫)라고 부르는 유전자 발현 첫 단계를 수행하며, RNA 백신 등 첨단 RNA 의약품을 개발 생산하는 데에 쓰인다. 연구팀은 세균바이러스의 RNA 중합효소를 연구해서 생물로 진화하기 이전 태초의 RNA 합성(전사) 방식을 밝힌 것이다.
유전자에 따라 다른 게 아니라 어느 유전자든 전사 마무리 방식에 두 가지가 있다는 것을 수년 전 세균에서 발견했었다. 그리고 세균보다 진화한 진핵생물 효모의 유전자 전사에서도 두 방식이 모두 쓰인다는 것이 지난달에 보고됐다. 사람도 진핵생물이어서, 세균과 효모뿐 아니라 사람까지 온갖 생물의 유전자 전사에 두 방식 모두 쓰일 개연성이 커졌다.
그런데 이번 연구에서 세균바이러스의 방식은 세균이나 효모와 사뭇 다르다는 것이 밝혀졌다. 바이러스의 경우 재생종결 없이 해체종결만 일어나는 것이다. 이를 토대로, 연구팀은 RNA 중합효소가 세균에서 바이러스와 달리 적응하면서 해체종결에 재생종결이 추가돼 두 방식이 공존하게 되었고, 최소한 효모로의 진화에서 그대로 보존됐다는 해석을 내놓았다.
이번 연구에서 거푸집 DNA와 전사물 RNA에 각기 다른 형광물질을 부착해 전사 복합체 하나하나의 형광을 실시간으로 측정하는 단일분자 형광기술 연구기법이 사용됐다. 전사 종결로 RNA가 방출될 때 DNA가 효소에 붙어있는지 떨어지는지를 낱낱이 구별할 수 있게 설계한 것이 특장점이다. 특히 형광물질이 전사 반응에 지장을 주지 않도록 하는 게 관건이었다.
송은호 박사후연구원과 한선 박사과정 대학원생이 공동 제1 저자로 참여한 논문(제목: Single-mode termination of phage transcriptions, disclosing bacterial adaptation for facilitated reinitiations)이 학술지 핵산연구(Nucleic Acids Research)에 7월 16일 게재됐다. 이로써 강창원 교수와 홍성철 교수는 2017년부터 총 8편의 논문을 공동으로 발표했다.
강창원 교수는 "이번 연구를 통해 수 초 동안의 분자 반응에서 유구한 진화과정을 밝혀냈고, 앞으로 더 광범위한 진화를 연구할 계획이다”라고 했다. 홍성철 교수는 "분자 하나하나를 관찰하여 복잡한 생물체의 진화를 파악했고, 이런 단일분자 연구기법을 차세대 RNA 의약품과 진단 시약의 개발에 응용하는 연구로 이어가고자 한다”라고 했다.
2024.07.19 조회수 6423 최진석 교수, 국제전기전자공학회 우수 젊은 연구자 상 수상
우리 대학 전기및전자공학부 최진석 교수가 무선 통신 분야에서의 업적으로 국제전기전자공학회(IEEE)의 통신 분야 아시아-태평양 우수 젊은 연구자 상(IEEE ComSoc Asia-Pacific Outstanding Young Researcher Award)을 수상했다고 22일 밝혔다.
최진석 교수는 꾸준한 연구와 혁신적인 아이디어로 통신 기술 발전에 중요한 역할을 해오고 있는 공로를 인정받았다. 해당 상은 매년 아시아-태평양 지역의 젊은 우수 연구자들에게 수여되는 상으로 올해 한국에서는 최진석 교수가 단독으로 수상했다. 그의 연구는 주로 저전력 통신 시스템 개발에 초점을 맞춰 새로운 무선 통신 기술과 솔루션의 개발을 통해 이 분야를 선도해 오고 있다.
특히, 최진석 교수는 무선 통신 분야에서의 창의적이고 도전적인 연구로 인해 꾸준한 평가를 받고 있다. 그의 주력 분야인 저전력 통신 시스템은 에너지 효율성을 극대화하면서도 안정적이고 고효율의 무선 통신을 실현하는 혁신적인 특징을 지니고 있다. 이를 통해 그가 개발한 시스템은 새로운 개념을 제시하며 세계적인 연구자들과 함께 무선 통신 기술의 발전을 선도하고 있다.
최진석 교수의 성과는 국내외의 우수 연구 그룹과의 긴밀한 협업, 다양한 학문 분야와의 융합, 그리고 산업계와의 적극적인 협력을 통해 이뤄지고 있다. 그는 무선 통신 분야에서의 현장 경험과 교육 활동을 통해 학문과 산업 간의 연계를 강조하며, 다양한 분야의 전문 지식을 융합해 새로운 연구 및 기술 개발에 도전하고 있다.
위 상을 받은 최진석 교수는 “앞으로의 통신 시스템은 에너지 효율성이 굉장히 중요한 이슈가 될 것으로 예상되는데, 최적화 이론과 정보이론을 기반으로 에너지 효율적인 통신 시스템을 개발하고자 했던 노력이 국제적으로 인정받아 매우 기쁘다ˮ며, “앞으로 이러한 기술을 실제 통신 시스템에 활용할 수 있도록 지속적인 노력을 하며 다양한 통신 어플리케이션에 적용하는 등 꾸준히 연구를 진행할 계획이다ˮ 라고 소감을 밝혔다.
시상식은 올해 12월 4일부터 8일까지 말레이시아 쿠알라룸푸르에서 열린 통신 분야 최우수 학회 중 하나인 세계 통신 학회(Globecom)에서 진행됐다.
2023.12.22 조회수 6805
최진석 교수, 국제전기전자공학회 우수 젊은 연구자 상 수상
우리 대학 전기및전자공학부 최진석 교수가 무선 통신 분야에서의 업적으로 국제전기전자공학회(IEEE)의 통신 분야 아시아-태평양 우수 젊은 연구자 상(IEEE ComSoc Asia-Pacific Outstanding Young Researcher Award)을 수상했다고 22일 밝혔다.
최진석 교수는 꾸준한 연구와 혁신적인 아이디어로 통신 기술 발전에 중요한 역할을 해오고 있는 공로를 인정받았다. 해당 상은 매년 아시아-태평양 지역의 젊은 우수 연구자들에게 수여되는 상으로 올해 한국에서는 최진석 교수가 단독으로 수상했다. 그의 연구는 주로 저전력 통신 시스템 개발에 초점을 맞춰 새로운 무선 통신 기술과 솔루션의 개발을 통해 이 분야를 선도해 오고 있다.
특히, 최진석 교수는 무선 통신 분야에서의 창의적이고 도전적인 연구로 인해 꾸준한 평가를 받고 있다. 그의 주력 분야인 저전력 통신 시스템은 에너지 효율성을 극대화하면서도 안정적이고 고효율의 무선 통신을 실현하는 혁신적인 특징을 지니고 있다. 이를 통해 그가 개발한 시스템은 새로운 개념을 제시하며 세계적인 연구자들과 함께 무선 통신 기술의 발전을 선도하고 있다.
최진석 교수의 성과는 국내외의 우수 연구 그룹과의 긴밀한 협업, 다양한 학문 분야와의 융합, 그리고 산업계와의 적극적인 협력을 통해 이뤄지고 있다. 그는 무선 통신 분야에서의 현장 경험과 교육 활동을 통해 학문과 산업 간의 연계를 강조하며, 다양한 분야의 전문 지식을 융합해 새로운 연구 및 기술 개발에 도전하고 있다.
위 상을 받은 최진석 교수는 “앞으로의 통신 시스템은 에너지 효율성이 굉장히 중요한 이슈가 될 것으로 예상되는데, 최적화 이론과 정보이론을 기반으로 에너지 효율적인 통신 시스템을 개발하고자 했던 노력이 국제적으로 인정받아 매우 기쁘다ˮ며, “앞으로 이러한 기술을 실제 통신 시스템에 활용할 수 있도록 지속적인 노력을 하며 다양한 통신 어플리케이션에 적용하는 등 꾸준히 연구를 진행할 계획이다ˮ 라고 소감을 밝혔다.
시상식은 올해 12월 4일부터 8일까지 말레이시아 쿠알라룸푸르에서 열린 통신 분야 최우수 학회 중 하나인 세계 통신 학회(Globecom)에서 진행됐다.
2023.12.22 조회수 6805 혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14 조회수 13466
혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14 조회수 13466 한빛원전의 시공 불량 문제를 해결하기 위한 시뮬레이션 개발
후쿠시마 사고 이후 원전 안전 및 관리에 대한 관심이 집중되고 있다. 한국에서는 2017년 6월경 한빛원전의 원자로 격납건물의 콘크리트 벽 속에서 대규모 공극이 발견되었다. 원자로 격납건물은 원전 사고 발생 시 방사능 유출을 막아주는 최후의 보루이기 때문에, 이러한 콘크리트 공극으로 인한 원전의 안전상 우려가 큰 상황이다.
국내 연구진들은 원자로 격납건물 시공시 콘크리트 다짐 및 채움 불량으로 인하여 격납로 내 콘크리트에 공극이 발생한 것으로 추정하고 있다. 원자로 격납건물은 일반 콘크리트 구조물과 달리 매우 높은 밀도의 철근 보강이 필요하기 때문에, 콘크리트 타설 시 진동 다짐기가 진입하지 못하는 구역이 존재할 가능성이 높아서 콘크리트 공동에 대한 위험성이 높다. 하지만 돔 형태의 벽체 내부를 감싼 6 mm 두께의 철판(콘크리트 라이너 플레이트, CLP)이 영구 거푸집으로 활용되기 때문에 내부 공동에 대한 육안 검사가 불가능하다는 점에서 공극 발생 여부의 발견에 대한 어려움이 있다.
우리 대학 건설및환경공학과 김재홍 교수 연구팀은 이러한 문제를 해결하기 위하여 콘크리트의 유동성과 다짐 불량으로 인해 발생하는 공동을 억제할 수 있는 시공 시뮬레이션 기법을 개발했다.
연구팀에서 제안한 콘크리트 유동 시뮬레이션 기법은 콘크리트의 레올로지와 진동다짐의 영향 반경을 고려하여 콘크리트 공동 발생 예상 부위를 예측하는 기술이다. 연구팀은 이번 연구를 통해 콘크리트 진동다짐의 영향 반경(감쇠계수)을 직접 측정하여 굳지 않은 콘크리트 내부의 진동 에너지 밀도 분포를 제시했다. 이어서, 진동 에너지에 따른 콘크리트의 Vibrorheology를 정량적으로 측정하여, 굳지 않은 콘크리트의 항복응력 감소를 정량적으로 모델링하여 시공 시뮬레이션을 가능하게 하였다.
새로 제안된 시공 시뮬레이션 기법은 기존 콘크리트 유동해석으로는 고려할 수 없었던 격납건물 내부 보강재의 형상과 크기, 콘크리트 레올로지, 그리고 진동다짐의 진폭과 진동수까지 고려하여 콘크리트의 채움성을 평가할 수 있게 되었다. 연구팀은 향후 보강 연구를 진행해 3D 프린팅 콘크리트의 레올로지 제어, 프리캐스트 콘크리트의 품질 관리 등에도 해당 기술을 활용할 계획이다.
이번 연구는 한국수력원자력(주)와 한국연구재단의 과학기술분야 기초연구사업의 지원으로 수행되었으며, 건설공학 분야에서 권위 있는 학술지인 ACI Materials Journal, Cement and Concrete Research 등에 출판되었다.
(논문명: (1) Quantitative evaluation of energy transfer of a concrete vibrator. (2) Flow simulation of fresh concrete accounting for vibrating compaction.)
2023.10.24 조회수 7488
한빛원전의 시공 불량 문제를 해결하기 위한 시뮬레이션 개발
후쿠시마 사고 이후 원전 안전 및 관리에 대한 관심이 집중되고 있다. 한국에서는 2017년 6월경 한빛원전의 원자로 격납건물의 콘크리트 벽 속에서 대규모 공극이 발견되었다. 원자로 격납건물은 원전 사고 발생 시 방사능 유출을 막아주는 최후의 보루이기 때문에, 이러한 콘크리트 공극으로 인한 원전의 안전상 우려가 큰 상황이다.
국내 연구진들은 원자로 격납건물 시공시 콘크리트 다짐 및 채움 불량으로 인하여 격납로 내 콘크리트에 공극이 발생한 것으로 추정하고 있다. 원자로 격납건물은 일반 콘크리트 구조물과 달리 매우 높은 밀도의 철근 보강이 필요하기 때문에, 콘크리트 타설 시 진동 다짐기가 진입하지 못하는 구역이 존재할 가능성이 높아서 콘크리트 공동에 대한 위험성이 높다. 하지만 돔 형태의 벽체 내부를 감싼 6 mm 두께의 철판(콘크리트 라이너 플레이트, CLP)이 영구 거푸집으로 활용되기 때문에 내부 공동에 대한 육안 검사가 불가능하다는 점에서 공극 발생 여부의 발견에 대한 어려움이 있다.
우리 대학 건설및환경공학과 김재홍 교수 연구팀은 이러한 문제를 해결하기 위하여 콘크리트의 유동성과 다짐 불량으로 인해 발생하는 공동을 억제할 수 있는 시공 시뮬레이션 기법을 개발했다.
연구팀에서 제안한 콘크리트 유동 시뮬레이션 기법은 콘크리트의 레올로지와 진동다짐의 영향 반경을 고려하여 콘크리트 공동 발생 예상 부위를 예측하는 기술이다. 연구팀은 이번 연구를 통해 콘크리트 진동다짐의 영향 반경(감쇠계수)을 직접 측정하여 굳지 않은 콘크리트 내부의 진동 에너지 밀도 분포를 제시했다. 이어서, 진동 에너지에 따른 콘크리트의 Vibrorheology를 정량적으로 측정하여, 굳지 않은 콘크리트의 항복응력 감소를 정량적으로 모델링하여 시공 시뮬레이션을 가능하게 하였다.
새로 제안된 시공 시뮬레이션 기법은 기존 콘크리트 유동해석으로는 고려할 수 없었던 격납건물 내부 보강재의 형상과 크기, 콘크리트 레올로지, 그리고 진동다짐의 진폭과 진동수까지 고려하여 콘크리트의 채움성을 평가할 수 있게 되었다. 연구팀은 향후 보강 연구를 진행해 3D 프린팅 콘크리트의 레올로지 제어, 프리캐스트 콘크리트의 품질 관리 등에도 해당 기술을 활용할 계획이다.
이번 연구는 한국수력원자력(주)와 한국연구재단의 과학기술분야 기초연구사업의 지원으로 수행되었으며, 건설공학 분야에서 권위 있는 학술지인 ACI Materials Journal, Cement and Concrete Research 등에 출판되었다.
(논문명: (1) Quantitative evaluation of energy transfer of a concrete vibrator. (2) Flow simulation of fresh concrete accounting for vibrating compaction.)
2023.10.24 조회수 7488 저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
2023.10.24 조회수 7289
저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
2023.10.24 조회수 7289 호흡기부터 강력 차단하는 코로나19 백신 개발
코로나바이러스감염증-19는 3년 4개월 만에 비상사태가 해제됐으나, 잦은 돌연변이로 인해 발생한 변이들이 계속해서 보고되고 있어 재유행이 시작될 가능성은 여전히 남아 있다. 이 변이들은 백신 접종이나 감염으로 인해 숙주가 획득한 기존의 면역반응을 회피하는 방향으로 진화하고 있다. 현재 시판되는 근육 접종 백신으로는 바이러스의 확산을 억제할 수 있는 점막 면역은 충분히 일으키기 어렵다는 한계가 있으므로 장기간 지속되는 강력한 점막 면역을 유도할 수 있는 백신의 필요성은 여전하다.
우리 대학 의과학대학원 이흥규 교수 연구팀과 한국화학연구원(원장 이영국)은 아데노바이러스 벡터 플랫폼의 비강 접종 코로나19 백신을 개발하고 마우스 모델을 이용해 이 백신이 장기간 지속되는 강력한 점막 면역을 유도함을 규명했다고 29일 밝혔다.
점막 면역이란 면역 체계를 구성하는 요소 중에서도 호흡기, 소화기, 생식기관 등을 구성하는 체내 상피 조직인 점막에서 작용하는 면역을 말한다. 이는 체내와 체외의 접점이 되는 점막에 침입한 외부 인자를 인지하고 제거해 인체를 감염으로부터 보호하는 방어체계다. 점막이 병원체나 외부 항원이 침입하는 주요 경로라는 점에서 점막 면역은 전신적 면역반응에 비해 병원체의 침입에 빠르게 대응해 감염 및 확산을 막을 수 있다는 장점이 있다.
의과학대학원 연수연구원 정희은 박사가 주도하고 박사과정 구근본, 강병훈 연구원, 김현철 박사, 박장현 박사 및 한국화학연구원 김균도 박사가 참여한 이번 연구에서 연구팀은 아데노바이러스 벡터 플랫폼을 기반으로, 개량된 스파이크 단백질 항원 및 인간 유래 면역증강제(CXCL9)을 탑재한 비강 접종 코로나19 백신(Ad5-S.Mod)을 개발해 그 효능을 실험용 쥐를 이용해 검증했다. 연구팀은 인간 유래 면역증강제가 활성화된 T세포를 특정 위치로 이동하도록 유인한다는 점에 주목해, 이를 백신의 효능을 높이기 위한 면역증강제로 이용하였다.
연구팀은 1회 단일 비강 접종, 혹은 근육-비강 2회 접종하여 백신의 효능을 검증했다. 그 결과 비강 백신이 호흡기 점막의 항체 반응 및 기억 T세포 반응을 높은 수준으로 유도할 수 있음을 확인하였으며, 백신 투여군은 1회 단일 접종만으로도 신종 코로나바이러스 감염 시 100% 생존하였다. 또한 백신 접종으로 만들어진 면역반응은 최소 1년간은 유지된다는 것을 규명해 백신의 강력한 점막 면역반응 유도 능력을 입증했다.
또한, 연구팀은 단일세포 전사체 분석법을 이용해 백신을 접종한 실험용 쥐의 폐 대식세포가 기억 T세포 및 B세포를 유지를 돕는 인자들의 주 생산자이며, 폐 대식세포가 제거되면 기억 T세포 및 B세포가 폐 속에서 확연히 감소함을 확인해 이 세포들이 점막 백신 접종으로 만들어진 호흡기 기억 세포의 유지를 돕고 있음을 규명했다.
이번 연구는 인간 유래 면역증강제(CXCL9)로서 활용해 백신의 효능을 강화한 새로운 백신 설계 전략을 제시하고 있다는 점과, 폐 대식세포가 점막 백신에 의해 형성되는 기억 면역반응을 유지하는 데 중요한 역할을 한다는 사실을 새로이 규명하여 다양한 병원체에 대한 비강 백신 개발에 이용할 수 있는 새로운 타겟을 제시하고 있다는 점에서 그 의의가 있다.
의과학대학원 박사후연수연구원 정희은 박사가 제1 저자로 참여한 이번 연구는 바이러스 분야 국제 학술지 `앤티바이럴 리서치(Antiviral Research)' 온라인판으로 6월 14일에 게재됐다. (논문명: Intranasal delivery of an adenovirus-vector vaccine co-expressing a modified spike protein and a genetic adjuvant confers lasting mucosal immunity against SARS-CoV-2, 논문링크: https://doi.org/10.1016/j.antiviral.2023.105656)
한편 이번 연구는 KAIST 코로나 대응 과학기술 뉴딜사업, 2020 과기원공동연구 프로젝트, 한국연구재단 바이오의료기술개발사업, 창의·도전연구 기반지원 사업 및 한국화학연구원 감염병 예방 융합 플랫폼 개발 과제 및 GO! KRICT 사업의 지원을 받아 수행됐다.
2023.07.01 조회수 7109
호흡기부터 강력 차단하는 코로나19 백신 개발
코로나바이러스감염증-19는 3년 4개월 만에 비상사태가 해제됐으나, 잦은 돌연변이로 인해 발생한 변이들이 계속해서 보고되고 있어 재유행이 시작될 가능성은 여전히 남아 있다. 이 변이들은 백신 접종이나 감염으로 인해 숙주가 획득한 기존의 면역반응을 회피하는 방향으로 진화하고 있다. 현재 시판되는 근육 접종 백신으로는 바이러스의 확산을 억제할 수 있는 점막 면역은 충분히 일으키기 어렵다는 한계가 있으므로 장기간 지속되는 강력한 점막 면역을 유도할 수 있는 백신의 필요성은 여전하다.
우리 대학 의과학대학원 이흥규 교수 연구팀과 한국화학연구원(원장 이영국)은 아데노바이러스 벡터 플랫폼의 비강 접종 코로나19 백신을 개발하고 마우스 모델을 이용해 이 백신이 장기간 지속되는 강력한 점막 면역을 유도함을 규명했다고 29일 밝혔다.
점막 면역이란 면역 체계를 구성하는 요소 중에서도 호흡기, 소화기, 생식기관 등을 구성하는 체내 상피 조직인 점막에서 작용하는 면역을 말한다. 이는 체내와 체외의 접점이 되는 점막에 침입한 외부 인자를 인지하고 제거해 인체를 감염으로부터 보호하는 방어체계다. 점막이 병원체나 외부 항원이 침입하는 주요 경로라는 점에서 점막 면역은 전신적 면역반응에 비해 병원체의 침입에 빠르게 대응해 감염 및 확산을 막을 수 있다는 장점이 있다.
의과학대학원 연수연구원 정희은 박사가 주도하고 박사과정 구근본, 강병훈 연구원, 김현철 박사, 박장현 박사 및 한국화학연구원 김균도 박사가 참여한 이번 연구에서 연구팀은 아데노바이러스 벡터 플랫폼을 기반으로, 개량된 스파이크 단백질 항원 및 인간 유래 면역증강제(CXCL9)을 탑재한 비강 접종 코로나19 백신(Ad5-S.Mod)을 개발해 그 효능을 실험용 쥐를 이용해 검증했다. 연구팀은 인간 유래 면역증강제가 활성화된 T세포를 특정 위치로 이동하도록 유인한다는 점에 주목해, 이를 백신의 효능을 높이기 위한 면역증강제로 이용하였다.
연구팀은 1회 단일 비강 접종, 혹은 근육-비강 2회 접종하여 백신의 효능을 검증했다. 그 결과 비강 백신이 호흡기 점막의 항체 반응 및 기억 T세포 반응을 높은 수준으로 유도할 수 있음을 확인하였으며, 백신 투여군은 1회 단일 접종만으로도 신종 코로나바이러스 감염 시 100% 생존하였다. 또한 백신 접종으로 만들어진 면역반응은 최소 1년간은 유지된다는 것을 규명해 백신의 강력한 점막 면역반응 유도 능력을 입증했다.
또한, 연구팀은 단일세포 전사체 분석법을 이용해 백신을 접종한 실험용 쥐의 폐 대식세포가 기억 T세포 및 B세포를 유지를 돕는 인자들의 주 생산자이며, 폐 대식세포가 제거되면 기억 T세포 및 B세포가 폐 속에서 확연히 감소함을 확인해 이 세포들이 점막 백신 접종으로 만들어진 호흡기 기억 세포의 유지를 돕고 있음을 규명했다.
이번 연구는 인간 유래 면역증강제(CXCL9)로서 활용해 백신의 효능을 강화한 새로운 백신 설계 전략을 제시하고 있다는 점과, 폐 대식세포가 점막 백신에 의해 형성되는 기억 면역반응을 유지하는 데 중요한 역할을 한다는 사실을 새로이 규명하여 다양한 병원체에 대한 비강 백신 개발에 이용할 수 있는 새로운 타겟을 제시하고 있다는 점에서 그 의의가 있다.
의과학대학원 박사후연수연구원 정희은 박사가 제1 저자로 참여한 이번 연구는 바이러스 분야 국제 학술지 `앤티바이럴 리서치(Antiviral Research)' 온라인판으로 6월 14일에 게재됐다. (논문명: Intranasal delivery of an adenovirus-vector vaccine co-expressing a modified spike protein and a genetic adjuvant confers lasting mucosal immunity against SARS-CoV-2, 논문링크: https://doi.org/10.1016/j.antiviral.2023.105656)
한편 이번 연구는 KAIST 코로나 대응 과학기술 뉴딜사업, 2020 과기원공동연구 프로젝트, 한국연구재단 바이오의료기술개발사업, 창의·도전연구 기반지원 사업 및 한국화학연구원 감염병 예방 융합 플랫폼 개발 과제 및 GO! KRICT 사업의 지원을 받아 수행됐다.
2023.07.01 조회수 7109 2023년 리서치데이 개최
'2023년 KAIST 리서치데이(Research Day)'가 16일 오전 대전 본원 학술문화관(E9) 5층 정근모 콘퍼런스홀에서 개최됐다.
리서치데이는 우수 연구자를 포상해 노고를 격려하고, 선정된 우수 연구 성과를 소개해 연구개발(R&D) 정보를 교류하는 자리다. 소통하는 연구문화를 조성해 연구자 간의 결집력을 높이고 융합연구를 활성화하기 위해 2016년부터 매년 개최하고 있다.
이날 행사에서는 김희탁 생명화학공학과 교수가 최고 연구상인 연구대상을 수상하고 ‘계면 공학을 통한 리튬금속전지 및 수계전지 고성능화’를 주제로 시상식 현장에서 기념 강연한다.
김 교수는 리튬이온전지의 에너지밀도 한계를 극복해 전기자동차의 항속거리를 2배 이상 증가시킬 수 있는 리튬금속전지 기술을 설명하고 더 나아가 전기화학, 소재 및 계면공학을 융복합해 에너지 저장과 변환 기술 분야의 난제 해결을 목표로 하는 연구 방향을 소개한다.
연구대상은 직전 5년 동안의 탁월한 연구개발 성과로 KAIST 발전에 크게 이바지한 교원에게 주어지는 상으로 연구의 우수성은 물론 연구계약액, 연구간접비 흡수 실적, 지식재산권 및 기술료 수입 등 종합적인 실적을 반영해 선정한다.
김 교수는 수소전지 등 산업 발전과 밀접하게 관련된 기술을 상용화하는 데 핵심적인 역할을 수행 중인 연구자로 2017년 한국공학한림원이 발표한 ‘2025년 대한민국 성장엔진이 될 미래 100대 기술과 차세대 주역’에 선정되기도 했다.
연구대상을 수상한 김 교수는 “지난 10년간 차세대 배터리, 연료전지 및 수전해 기술을 개발하며 관련 산업이 태동하고 성장하는 데 기여할 수 있어서 큰 보람이었다”라고 수상 소감을 밝혔다.
이어 김 교수는 “재능과 열정 있는 대학원생들과 함께 연구할 수 있는 큰 행운에 감사하는 마음으로 전기화학공학과 계면공학을 접목한 분야의 혁신을 이룰 수 있도록 정진하겠다”라고 덧붙였다.
이 밖에도 이필승(기계공학과)·명현(전기및전자공학부) 교수가 각각 연구상을, 배현민 교수(전기및전자공학부)가 이노베이션상 수상자로 선정됐다.
양용수(물리학과)·한상우(화학과)·유승화(기계공학과) 교수 3명은 한 팀으로 융합 연구상을 받는다. 국제공동연구상에는 조성호 교수(전산학부), 현우 KAIST 학술상은 김범준 교수(생명화학공학과), QAIST 창의도전연구상 수상자에는 박윤수 교수(화학과)가 선정됐다.
이들 수상자는 사전 촬영한 영상 강연을 통해 학생과 동료 연구자에게 연구 경험과 열정에 관한 이야기를 나눌 예정이다.
한편, KAIST의 2022년 대표 R&D 연구성과 10선도 소개된다. 자연과학 분야에서는 ▴준입자적 특성을 가지는 빛 소용돌이의 자발적 생성과 동역학적 제어(서민교 교수‧물리학과) ▴리드버그원자 양자컴퓨터 개발(안재욱 교수‧물리학과)이 선정됐다.
생명과학 분야에서는 ▴염증반응 없이 아밀로이드베타를 제거하는 새로운 치매 치료제 개발(김찬혁 교수, 정원석 교수‧생명과학과)이 이름을 올렸다.
▴사람처럼 느끼고 상처 치유가 가능한 로봇 피부 기술 개발(김정 교수‧기계공학과) ▴수면 조절을 위한 폐루프 초음파 자극 기술 개발(이현주 교수‧전기및전자공학부) ▴악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발(조광현 교수‧바이오및뇌공학과) ▴mRNA 암백신 핵심기술 개발(최정균 교수‧바이오및뇌공학과) ▴미생물 이용한 루테인 생산 기술 개발(이상엽 교수‧생명화학공학과) ▴신축성 인쇄 전자회로 기판 구현을 위한 액체 금속 입자 네트워크 개발(강지형 교수‧신소재공학과)은 공학 분야 우수 성과로 선정됐다.
▴지구 메타버스 기술을 이용한 지구온난화와 태풍 호우 빈도의 상관관계 증명(김형준 교수‧문술미래전략대학원)도 인문사회융합과학 분야의 우수 연구성과로 선정되어 동영상으로 시연·소개된다.
조병관 연구처장은 “올해는 코로나19 비상사태가 해제되어 3년 만에 다 함께 모여 얼굴을 마주 보고 축하할 수 있어 더욱 뜻깊은 자리인 만큼 리서치데이를 통해 다양하고 훌륭한 연구성과들이 널리 공유되고 창의적이고 혁신적인 연구 활동에 큰 영감을 얻는 계기가 되기를 바란다”라고 밝혔다.
2023.05.16 조회수 7819
2023년 리서치데이 개최
'2023년 KAIST 리서치데이(Research Day)'가 16일 오전 대전 본원 학술문화관(E9) 5층 정근모 콘퍼런스홀에서 개최됐다.
리서치데이는 우수 연구자를 포상해 노고를 격려하고, 선정된 우수 연구 성과를 소개해 연구개발(R&D) 정보를 교류하는 자리다. 소통하는 연구문화를 조성해 연구자 간의 결집력을 높이고 융합연구를 활성화하기 위해 2016년부터 매년 개최하고 있다.
이날 행사에서는 김희탁 생명화학공학과 교수가 최고 연구상인 연구대상을 수상하고 ‘계면 공학을 통한 리튬금속전지 및 수계전지 고성능화’를 주제로 시상식 현장에서 기념 강연한다.
김 교수는 리튬이온전지의 에너지밀도 한계를 극복해 전기자동차의 항속거리를 2배 이상 증가시킬 수 있는 리튬금속전지 기술을 설명하고 더 나아가 전기화학, 소재 및 계면공학을 융복합해 에너지 저장과 변환 기술 분야의 난제 해결을 목표로 하는 연구 방향을 소개한다.
연구대상은 직전 5년 동안의 탁월한 연구개발 성과로 KAIST 발전에 크게 이바지한 교원에게 주어지는 상으로 연구의 우수성은 물론 연구계약액, 연구간접비 흡수 실적, 지식재산권 및 기술료 수입 등 종합적인 실적을 반영해 선정한다.
김 교수는 수소전지 등 산업 발전과 밀접하게 관련된 기술을 상용화하는 데 핵심적인 역할을 수행 중인 연구자로 2017년 한국공학한림원이 발표한 ‘2025년 대한민국 성장엔진이 될 미래 100대 기술과 차세대 주역’에 선정되기도 했다.
연구대상을 수상한 김 교수는 “지난 10년간 차세대 배터리, 연료전지 및 수전해 기술을 개발하며 관련 산업이 태동하고 성장하는 데 기여할 수 있어서 큰 보람이었다”라고 수상 소감을 밝혔다.
이어 김 교수는 “재능과 열정 있는 대학원생들과 함께 연구할 수 있는 큰 행운에 감사하는 마음으로 전기화학공학과 계면공학을 접목한 분야의 혁신을 이룰 수 있도록 정진하겠다”라고 덧붙였다.
이 밖에도 이필승(기계공학과)·명현(전기및전자공학부) 교수가 각각 연구상을, 배현민 교수(전기및전자공학부)가 이노베이션상 수상자로 선정됐다.
양용수(물리학과)·한상우(화학과)·유승화(기계공학과) 교수 3명은 한 팀으로 융합 연구상을 받는다. 국제공동연구상에는 조성호 교수(전산학부), 현우 KAIST 학술상은 김범준 교수(생명화학공학과), QAIST 창의도전연구상 수상자에는 박윤수 교수(화학과)가 선정됐다.
이들 수상자는 사전 촬영한 영상 강연을 통해 학생과 동료 연구자에게 연구 경험과 열정에 관한 이야기를 나눌 예정이다.
한편, KAIST의 2022년 대표 R&D 연구성과 10선도 소개된다. 자연과학 분야에서는 ▴준입자적 특성을 가지는 빛 소용돌이의 자발적 생성과 동역학적 제어(서민교 교수‧물리학과) ▴리드버그원자 양자컴퓨터 개발(안재욱 교수‧물리학과)이 선정됐다.
생명과학 분야에서는 ▴염증반응 없이 아밀로이드베타를 제거하는 새로운 치매 치료제 개발(김찬혁 교수, 정원석 교수‧생명과학과)이 이름을 올렸다.
▴사람처럼 느끼고 상처 치유가 가능한 로봇 피부 기술 개발(김정 교수‧기계공학과) ▴수면 조절을 위한 폐루프 초음파 자극 기술 개발(이현주 교수‧전기및전자공학부) ▴악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발(조광현 교수‧바이오및뇌공학과) ▴mRNA 암백신 핵심기술 개발(최정균 교수‧바이오및뇌공학과) ▴미생물 이용한 루테인 생산 기술 개발(이상엽 교수‧생명화학공학과) ▴신축성 인쇄 전자회로 기판 구현을 위한 액체 금속 입자 네트워크 개발(강지형 교수‧신소재공학과)은 공학 분야 우수 성과로 선정됐다.
▴지구 메타버스 기술을 이용한 지구온난화와 태풍 호우 빈도의 상관관계 증명(김형준 교수‧문술미래전략대학원)도 인문사회융합과학 분야의 우수 연구성과로 선정되어 동영상으로 시연·소개된다.
조병관 연구처장은 “올해는 코로나19 비상사태가 해제되어 3년 만에 다 함께 모여 얼굴을 마주 보고 축하할 수 있어 더욱 뜻깊은 자리인 만큼 리서치데이를 통해 다양하고 훌륭한 연구성과들이 널리 공유되고 창의적이고 혁신적인 연구 활동에 큰 영감을 얻는 계기가 되기를 바란다”라고 밝혔다.
2023.05.16 조회수 7819 강수 관측 오차범위 42.5% 줄인 알고리즘 개발
강수량의 정확한 파악은 지구의 물 순환을 이해하고 수자원과 재해 대응을 위해 중요하다. 강수량 추정을 위한 알고리즘에는 다양한 방법들이 제안되어 왔으며, 최근에는 기계학습을 이용한 방법들이 많이 제안되고 있다.
우리 대학 문술미래전략대학원(건설및환경공학과 및 녹색성장지속가능대학원 겸임) 김형준 교수와 도쿄대 등으로 구성된 국제 공동연구팀이 인공위성에 탑재된 마이크로파 라디오미터의 관측값을 이용해 지상 강수량을 추정하는 새로운 기계학습 방법을 제안했다고 25일 밝혔다. 연구팀은 기존의 방법과 비교해 전 강수량에 대해 오차(RMSE)를 최소 15.9%에서 최대 42.5%까지 줄이는 데 성공했다.
단순한 데이터 주도(data-driven)모델은 대량의 훈련 데이터가 필요하고 물리적인 일관성이 보장되지 않으며 결과의 원인 분석이 어렵다는 등의 문제가 있었다. 연구팀은 이번 연구에서 위성 강수량 추정에 대한 분야 지식을 명시적으로 포함함으로써 학습 모델 내의 상호 의존적인 지식 교환을 구현했다. 구체적으로, 멀티태스크 학습(multitask learning)이라는 심층 학습 기법을 사용해 강수 여부를 인식하는 분류 모델과 강수 강도를 추정하는 회귀 모델을 통합하고 동시에 학습시켰다.
이번 연구에서 제안한 기계학습 모델에는 이번에 포함된 메커니즘 외에도 다양한 물리적 메커니즘을 포함할 수 있다. 예를 들어, 비 또는 눈, 진눈깨비 등 강수 종류의 분류 및 상승 기류 또는 층상 구름 유형 등 강수를 일으키는 구름 유형의 분류를 포함함으로써 앞으로 추정의 정확도가 더욱 향상될 것으로 기대된다.
김형준 교수의 이번 연구 결과는 국제 학술지 ‘지구물리 연구 레터(Geophysical Research Letters)’에 지난 4월 16일 출판됐다. (논문명: Multi-Task Learning for Simultaneous Retrievals of Passive Microwave Precipitation Estimates and Rain/No-Rain Classification; doi:10.1029/2022GL102283)
한편 이번 연구는 한국연구재단 해외우수과학자유치사업(BP+)와 정보통신기획평가원 인공지능대학원지원(한국과학기술원)지원을 받아 수행됐다.
2023.04.25 조회수 8607
강수 관측 오차범위 42.5% 줄인 알고리즘 개발
강수량의 정확한 파악은 지구의 물 순환을 이해하고 수자원과 재해 대응을 위해 중요하다. 강수량 추정을 위한 알고리즘에는 다양한 방법들이 제안되어 왔으며, 최근에는 기계학습을 이용한 방법들이 많이 제안되고 있다.
우리 대학 문술미래전략대학원(건설및환경공학과 및 녹색성장지속가능대학원 겸임) 김형준 교수와 도쿄대 등으로 구성된 국제 공동연구팀이 인공위성에 탑재된 마이크로파 라디오미터의 관측값을 이용해 지상 강수량을 추정하는 새로운 기계학습 방법을 제안했다고 25일 밝혔다. 연구팀은 기존의 방법과 비교해 전 강수량에 대해 오차(RMSE)를 최소 15.9%에서 최대 42.5%까지 줄이는 데 성공했다.
단순한 데이터 주도(data-driven)모델은 대량의 훈련 데이터가 필요하고 물리적인 일관성이 보장되지 않으며 결과의 원인 분석이 어렵다는 등의 문제가 있었다. 연구팀은 이번 연구에서 위성 강수량 추정에 대한 분야 지식을 명시적으로 포함함으로써 학습 모델 내의 상호 의존적인 지식 교환을 구현했다. 구체적으로, 멀티태스크 학습(multitask learning)이라는 심층 학습 기법을 사용해 강수 여부를 인식하는 분류 모델과 강수 강도를 추정하는 회귀 모델을 통합하고 동시에 학습시켰다.
이번 연구에서 제안한 기계학습 모델에는 이번에 포함된 메커니즘 외에도 다양한 물리적 메커니즘을 포함할 수 있다. 예를 들어, 비 또는 눈, 진눈깨비 등 강수 종류의 분류 및 상승 기류 또는 층상 구름 유형 등 강수를 일으키는 구름 유형의 분류를 포함함으로써 앞으로 추정의 정확도가 더욱 향상될 것으로 기대된다.
김형준 교수의 이번 연구 결과는 국제 학술지 ‘지구물리 연구 레터(Geophysical Research Letters)’에 지난 4월 16일 출판됐다. (논문명: Multi-Task Learning for Simultaneous Retrievals of Passive Microwave Precipitation Estimates and Rain/No-Rain Classification; doi:10.1029/2022GL102283)
한편 이번 연구는 한국연구재단 해외우수과학자유치사업(BP+)와 정보통신기획평가원 인공지능대학원지원(한국과학기술원)지원을 받아 수행됐다.
2023.04.25 조회수 8607 폐암 전이를 막고 치료 가능한 세포로 되돌리는 원천기술 개발
고령화에 따라 암의 발생이 늘어나면서 암은 인류의 건강수명을 위협하는 가장 치명적인 질환이 됐다. 특히 조기 발견을 놓쳐 여러 장기로 전이될 때 암의 치명률은 높아진다. 이러한 문제를 해결하기 위해 암세포의 전이 능력을 제거하거나 낮추려는 시도가 이어졌으나 오히려 중간상태의 불안정한 암세포 상태가 되면서 더욱 악성을 보이게 되어 암 치료의 난제로 남아 있었다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 폐암 세포의 성질을 변환시켜 암세포의 전이를 막고 약물에 대한 저항성을 제거할 수 있는 기술을 개발하는 데 성공했다고 30일 밝혔다.
조광현 교수 연구팀은 폐암 세포의 전이능력이 없는 상피(epithelial, 세포 방향성이 있어 유동성 없이 표면조직을 이루는 상태)세포에서 전이가 가능한 중간엽(mesenchymal, 방향성없이 개별적인 이동성을 가진 상태)세포로 변화되는 천이 과정(epithelial-to-mesenchymal transition, 이하 EMT)에서 나타나는 다양한 암세포 상태들을 나타낼 수 있는 세포의 분자 네트워크 수학모델을 만들었다. 컴퓨터 시뮬레이션 분석과 분자 세포실험을 통해 악성종양으로 증식하여 인접한 조직이나 세포로 침입하거나 약물에 내성을 가진 중간엽세포 상태에서 전이가 되지 않은 상피세포 상태로 다시 바뀔수 있도록 세포의 성질을 변환시켜주는 핵심 조절인자들을 발굴했다.
특히 이 과정에서 그동안 난제로 남아 있었던 중간과정의 불안정한 암세포 상태(EMT 하이브리드 세포 상태)를 피하는 동시에 항암 화학요법(chemotherapy) 치료가 잘 되는 상피세포 상태로 온전히 역전하는 데 성공했다.
우리 대학 김남희 박사과정, 황채영 박사, 김태영 연구원, 김현진 박사과정이 참여한 이번 연구 결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치(Cancer Research)' 1월 30일 字 온라인판 논문으로 출판됐다. (논문명: A cell fate reprogramming strategy reverses epithelial-to-mesenchymal transition of lung cancer cells while avoiding hybrid states)
암세포의 EMT 과정에서 불완전한 천이(변화과정)로 인해 발생하는 EMT 하이브리드 상태의 세포들은 상피세포와 중간엽세포의 특성을 모두 갖고 있으며, 높은 줄기세포능*을 획득해 약물저항성 및 전이 잠재성이 큰 것으로 알려져 있다. 불안정한 암세포 상태(EMT)는 매우 복잡하여 높은 전이 능력과 약물저항성을 가지는 EMT 하이브리드 세포 상태를 회피하면서 암세포를 전이 능력과 약물저항성이 제거된 상피세포 상태로 온전히 역전시키는 것은 매우 어려운 일이었다.
*줄기세포능: 줄기세포가 지속적 자가복제를 할 수 있도록 하는 세포내 신호전달체계
조광현 교수 연구팀은 복잡한 EMT를 지배하는 유전자 조절 네트워크의 수학모델을 정립한 후, 대규모 컴퓨터 시뮬레이션 분석 및 복잡계 네트워크 제어기술을 적용해 중간엽세포 상태인 폐암 세포를 EMT 하이브리드 세포 상태를 회피하면서 전이 능력이 상실된 상피세포 상태로 역전시킬 수 있는 세 개의 핵심 분자 타깃인 ‘p53 (암 억제 단백질)’, ‘SMAD4 (EMT를 조절하는 대표적 신호전달을 매개하는 중심물질로 SMAD 그룹에 포함된 단백질)’와 ‘ERK1/2 (세포의 성장 및 분화에 관여하는 조절인자)’를 발굴하고 이를 분자 세포실험을 통해 검증했다. 이러한 발견은 실제 인체 내 암 조직의 환경에서처럼 자극이 주어진 상황에서 중간엽세포 상태가 상피세포 상태로 역전될 수 있음을 증명해 그 의미가 크다.
암세포의 비정상적인 EMT는 암세포의 이동과 침윤, 화학요법 치료에 대한 반응성 변화, 강화된 줄기세포능, 암의 전이 등 다양한 악성 형질로 이어지게 된다. 특히 암세포의 전이 능력 획득은 암 환자의 예후를 결정짓는 매우 중요한 요소다. 이번에 개발된 폐암 세포의 EMT 역전 기술은 암세포를 리프로그래밍해 높은 가소성과 전이 능력을 제거하고 항암 화학치료의 반응성을 높이도록 하는 새로운 항암 치료 전략이다.
조광현 교수는 "높은 전이 능력과 약물저항성을 획득한 폐암 세포를 전이 능력이 제거되고 항암 화학요법치료에 민감한 상피세포 상태로 온전히 역전시키는 데 성공함으로써 암 환자의 예후를 증진할 수 있는 새로운 치료전략을 제시했다ˮ라고 말했다.
조광현 교수 연구팀은 암세포를 정상세포로 되돌리는 가역 치료원리를 최초로 제시한 뒤 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구 결과를 발표했고, 2022년 1월에는 가장 악성인 유방암세포를 호르몬 치료가 가능한 유방암세포로 리프로그래밍하는 연구에 성공한 바 있다. 이번 연구 결과는 전이 능력을 획득한 폐암 세포 상태를 전이 능력이 제거되고 약물 반응성이 증진된 세포 상태로 되돌리는 가역화 기술 개발의 세 번째 성과다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 등의 지원으로 수행됐다.
2023.01.30 조회수 11537
폐암 전이를 막고 치료 가능한 세포로 되돌리는 원천기술 개발
고령화에 따라 암의 발생이 늘어나면서 암은 인류의 건강수명을 위협하는 가장 치명적인 질환이 됐다. 특히 조기 발견을 놓쳐 여러 장기로 전이될 때 암의 치명률은 높아진다. 이러한 문제를 해결하기 위해 암세포의 전이 능력을 제거하거나 낮추려는 시도가 이어졌으나 오히려 중간상태의 불안정한 암세포 상태가 되면서 더욱 악성을 보이게 되어 암 치료의 난제로 남아 있었다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 폐암 세포의 성질을 변환시켜 암세포의 전이를 막고 약물에 대한 저항성을 제거할 수 있는 기술을 개발하는 데 성공했다고 30일 밝혔다.
조광현 교수 연구팀은 폐암 세포의 전이능력이 없는 상피(epithelial, 세포 방향성이 있어 유동성 없이 표면조직을 이루는 상태)세포에서 전이가 가능한 중간엽(mesenchymal, 방향성없이 개별적인 이동성을 가진 상태)세포로 변화되는 천이 과정(epithelial-to-mesenchymal transition, 이하 EMT)에서 나타나는 다양한 암세포 상태들을 나타낼 수 있는 세포의 분자 네트워크 수학모델을 만들었다. 컴퓨터 시뮬레이션 분석과 분자 세포실험을 통해 악성종양으로 증식하여 인접한 조직이나 세포로 침입하거나 약물에 내성을 가진 중간엽세포 상태에서 전이가 되지 않은 상피세포 상태로 다시 바뀔수 있도록 세포의 성질을 변환시켜주는 핵심 조절인자들을 발굴했다.
특히 이 과정에서 그동안 난제로 남아 있었던 중간과정의 불안정한 암세포 상태(EMT 하이브리드 세포 상태)를 피하는 동시에 항암 화학요법(chemotherapy) 치료가 잘 되는 상피세포 상태로 온전히 역전하는 데 성공했다.
우리 대학 김남희 박사과정, 황채영 박사, 김태영 연구원, 김현진 박사과정이 참여한 이번 연구 결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치(Cancer Research)' 1월 30일 字 온라인판 논문으로 출판됐다. (논문명: A cell fate reprogramming strategy reverses epithelial-to-mesenchymal transition of lung cancer cells while avoiding hybrid states)
암세포의 EMT 과정에서 불완전한 천이(변화과정)로 인해 발생하는 EMT 하이브리드 상태의 세포들은 상피세포와 중간엽세포의 특성을 모두 갖고 있으며, 높은 줄기세포능*을 획득해 약물저항성 및 전이 잠재성이 큰 것으로 알려져 있다. 불안정한 암세포 상태(EMT)는 매우 복잡하여 높은 전이 능력과 약물저항성을 가지는 EMT 하이브리드 세포 상태를 회피하면서 암세포를 전이 능력과 약물저항성이 제거된 상피세포 상태로 온전히 역전시키는 것은 매우 어려운 일이었다.
*줄기세포능: 줄기세포가 지속적 자가복제를 할 수 있도록 하는 세포내 신호전달체계
조광현 교수 연구팀은 복잡한 EMT를 지배하는 유전자 조절 네트워크의 수학모델을 정립한 후, 대규모 컴퓨터 시뮬레이션 분석 및 복잡계 네트워크 제어기술을 적용해 중간엽세포 상태인 폐암 세포를 EMT 하이브리드 세포 상태를 회피하면서 전이 능력이 상실된 상피세포 상태로 역전시킬 수 있는 세 개의 핵심 분자 타깃인 ‘p53 (암 억제 단백질)’, ‘SMAD4 (EMT를 조절하는 대표적 신호전달을 매개하는 중심물질로 SMAD 그룹에 포함된 단백질)’와 ‘ERK1/2 (세포의 성장 및 분화에 관여하는 조절인자)’를 발굴하고 이를 분자 세포실험을 통해 검증했다. 이러한 발견은 실제 인체 내 암 조직의 환경에서처럼 자극이 주어진 상황에서 중간엽세포 상태가 상피세포 상태로 역전될 수 있음을 증명해 그 의미가 크다.
암세포의 비정상적인 EMT는 암세포의 이동과 침윤, 화학요법 치료에 대한 반응성 변화, 강화된 줄기세포능, 암의 전이 등 다양한 악성 형질로 이어지게 된다. 특히 암세포의 전이 능력 획득은 암 환자의 예후를 결정짓는 매우 중요한 요소다. 이번에 개발된 폐암 세포의 EMT 역전 기술은 암세포를 리프로그래밍해 높은 가소성과 전이 능력을 제거하고 항암 화학치료의 반응성을 높이도록 하는 새로운 항암 치료 전략이다.
조광현 교수는 "높은 전이 능력과 약물저항성을 획득한 폐암 세포를 전이 능력이 제거되고 항암 화학요법치료에 민감한 상피세포 상태로 온전히 역전시키는 데 성공함으로써 암 환자의 예후를 증진할 수 있는 새로운 치료전략을 제시했다ˮ라고 말했다.
조광현 교수 연구팀은 암세포를 정상세포로 되돌리는 가역 치료원리를 최초로 제시한 뒤 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구 결과를 발표했고, 2022년 1월에는 가장 악성인 유방암세포를 호르몬 치료가 가능한 유방암세포로 리프로그래밍하는 연구에 성공한 바 있다. 이번 연구 결과는 전이 능력을 획득한 폐암 세포 상태를 전이 능력이 제거되고 약물 반응성이 증진된 세포 상태로 되돌리는 가역화 기술 개발의 세 번째 성과다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 등의 지원으로 수행됐다.
2023.01.30 조회수 11537