-
 AI 기반 효소 발굴하여 새로운 미생물 설계 가능
효소는 세포 내에서 일어나는 생화학적 반응을 촉매하는 단백질로, 세포의 대사 과정에서 핵심적인 역할을 수행한다. 이에 따라 새로운 효소의 기능을 규명하는 것은 미생물 세포공장 구축에서 핵심적인 과제다.
KAIST 연구진이 인공지능(AI)을 활용해 자연에 존재하지 않는 새로운 효소를 설계함으로써, 미생물 세포공장 구축을 가속화하고 신약·바이오 연료 등 차세대 바이오산업의 개발 가능성을 크게 높였다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 AI를 활용한 효소 기능 예측 기술의 발전 과정과 최신 동향을 정리하고, AI가 새로운 효소를 찾고 설계하는데 어떤 역할을 해왔는지 분석하여 ‘인공지능을 이용한 효소 기능 분류’를 발표했다.
이상엽 특훈교수 연구팀은 이번 연구에서 머신러닝(Machine learning)과 딥러닝(Deep learning)을 활용한 효소 기능 예측 기술의 발전 과정을 체계적으로 정리·분석하여 제공했다.
초기의 서열 유사성 기반 예측 기법에서부터 합성곱 신경망, 순환 신경망, 그래프 신경망, 그리고 트랜스포머(Transformer) 기반 대규모 언어 모델까지 다양한 AI 기법이 효소 기능 예측 연구에 접목된 사례를 다루며, 이들 기술이 단백질 서열에서 의미 있는 정보를 어떻게 추출하고, 예측 성능을 극대화하는지를 분석했다.
특히, 딥러닝 기술을 활용한 효소 기능 예측은 단순한 서열 유사성 분석을 넘어, 구조적·진화적 정보 등 아미노산 서열에 내재된 효소의 촉매 기능과 관련된 중요한 특성을 자동으로 추출함으로써 보다 정밀한 예측이 가능하다는 점이 강조됐다.
이는 기존의 생명정보학적 접근법과 비교해 인공지능 모델이 가지는 차별성과 장점을 부각하는 중요한 부분이다.
또한, 생성형 인공지능 모델의 발전에 기반하여, 기존 효소 기능 예측을 넘어 자연계에 존재하지 않는 새로운 기능을 가진 효소를 생성하는 기술이 미래 연구 방향이 될 것으로 제시했다. 이러한 AI 기반 효소 예측 및 설계 기술의 지속적인 발전은 향후 바이오 산업과 생명공학 연구의 방향성에 큰 변화를 가져올 것으로 전망했다.
공동 제 1저자인 생명화학공학과 김하림 박사과정생은 “AI 기반 효소 기능 예측 및 효소 설계는 대사공학, 합성 생물학 및 헬스케어 등 다양한 분야에서 매우 중요”하다고 말했다.
이상엽 특훈교수는“AI 활용 효소 기능 예측은 다양한 생물학적 문제 해결에 효과적으로 적용될 수 있는 가능성을 보여주며 바이오 분야 전반의 연구를 가속화하는 데 크게 기여할 것.”이라고 밝혔다.
해당 논문은 셀(Cell) 誌가 발행하는 생명공학 분야 권위 저널인 `생명공학 동향(Trends in Biotechnology)'에 3월 28일자 게재됐다.
※ 논문명 : Enzyme Functional Classification Using Artificial Intelligence doi.org/10.1016/j.tibtech.2025.03.003
※ 저자 정보 : 김하림(한국과학기술원, 공동 제1 저자), 지홍근(한국과학기술원, 공동 제1 저자), 김기배(한국과학기술원, 제3 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유 대체 친환경 화학기술 개발 사업의‘바이오 제조 산업 선도를 위한 첨단 합성 생물학 원천기술 개발’, 그리고 과기정통부와 보건복지부가 지원하는 ‘딥러닝 기반 합성 생물학을 이용한 혁신구조 항생제 개발’ 과제의 지원을 받아 수행됐다.
AI 기반 효소 발굴하여 새로운 미생물 설계 가능
효소는 세포 내에서 일어나는 생화학적 반응을 촉매하는 단백질로, 세포의 대사 과정에서 핵심적인 역할을 수행한다. 이에 따라 새로운 효소의 기능을 규명하는 것은 미생물 세포공장 구축에서 핵심적인 과제다.
KAIST 연구진이 인공지능(AI)을 활용해 자연에 존재하지 않는 새로운 효소를 설계함으로써, 미생물 세포공장 구축을 가속화하고 신약·바이오 연료 등 차세대 바이오산업의 개발 가능성을 크게 높였다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 AI를 활용한 효소 기능 예측 기술의 발전 과정과 최신 동향을 정리하고, AI가 새로운 효소를 찾고 설계하는데 어떤 역할을 해왔는지 분석하여 ‘인공지능을 이용한 효소 기능 분류’를 발표했다.
이상엽 특훈교수 연구팀은 이번 연구에서 머신러닝(Machine learning)과 딥러닝(Deep learning)을 활용한 효소 기능 예측 기술의 발전 과정을 체계적으로 정리·분석하여 제공했다.
초기의 서열 유사성 기반 예측 기법에서부터 합성곱 신경망, 순환 신경망, 그래프 신경망, 그리고 트랜스포머(Transformer) 기반 대규모 언어 모델까지 다양한 AI 기법이 효소 기능 예측 연구에 접목된 사례를 다루며, 이들 기술이 단백질 서열에서 의미 있는 정보를 어떻게 추출하고, 예측 성능을 극대화하는지를 분석했다.
특히, 딥러닝 기술을 활용한 효소 기능 예측은 단순한 서열 유사성 분석을 넘어, 구조적·진화적 정보 등 아미노산 서열에 내재된 효소의 촉매 기능과 관련된 중요한 특성을 자동으로 추출함으로써 보다 정밀한 예측이 가능하다는 점이 강조됐다.
이는 기존의 생명정보학적 접근법과 비교해 인공지능 모델이 가지는 차별성과 장점을 부각하는 중요한 부분이다.
또한, 생성형 인공지능 모델의 발전에 기반하여, 기존 효소 기능 예측을 넘어 자연계에 존재하지 않는 새로운 기능을 가진 효소를 생성하는 기술이 미래 연구 방향이 될 것으로 제시했다. 이러한 AI 기반 효소 예측 및 설계 기술의 지속적인 발전은 향후 바이오 산업과 생명공학 연구의 방향성에 큰 변화를 가져올 것으로 전망했다.
공동 제 1저자인 생명화학공학과 김하림 박사과정생은 “AI 기반 효소 기능 예측 및 효소 설계는 대사공학, 합성 생물학 및 헬스케어 등 다양한 분야에서 매우 중요”하다고 말했다.
이상엽 특훈교수는“AI 활용 효소 기능 예측은 다양한 생물학적 문제 해결에 효과적으로 적용될 수 있는 가능성을 보여주며 바이오 분야 전반의 연구를 가속화하는 데 크게 기여할 것.”이라고 밝혔다.
해당 논문은 셀(Cell) 誌가 발행하는 생명공학 분야 권위 저널인 `생명공학 동향(Trends in Biotechnology)'에 3월 28일자 게재됐다.
※ 논문명 : Enzyme Functional Classification Using Artificial Intelligence doi.org/10.1016/j.tibtech.2025.03.003
※ 저자 정보 : 김하림(한국과학기술원, 공동 제1 저자), 지홍근(한국과학기술원, 공동 제1 저자), 김기배(한국과학기술원, 제3 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유 대체 친환경 화학기술 개발 사업의‘바이오 제조 산업 선도를 위한 첨단 합성 생물학 원천기술 개발’, 그리고 과기정통부와 보건복지부가 지원하는 ‘딥러닝 기반 합성 생물학을 이용한 혁신구조 항생제 개발’ 과제의 지원을 받아 수행됐다.
2025.04.17
조회수 4512
-
 암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22
조회수 4448
-
 숨겨진 효소 쏙쏙 찾아내는 인공지능 개발
대장균은 가장 많이 연구된 생명체 중 하나에 해당되지만 아직 대장균을 구성한 단백질 30%의 기능에 대해 명확하게 밝혀지지 않았다. 이에 대해 인공지능을 활용하여 아직 명확하게 밝혀진 바 없던 단백질에서 464종의 효소를 발견하였으며, 이 중 3종의 단백질의 예측된 기능을 시험관 내 효소 분석 방법을 통해 검증하는데 성공하였다.
우리 대학 생명화학공학과 이상엽 특훈교수와 캘리포니아대학교 샌디에이고(UCSD) 생명공학과 버나드 펄슨(Bernhard Palsson) 교수 공동연구팀이 단백질 서열을 활용, 해당 단백질의 효소 기능을 예측할 수 있는 인공지능, `딥 EC 트랜스포머(DeepECtransformer)'를 개발해 빠르고 정확하게 효소 기능을 파악할 수 있는 예측 시스템을 구축했다고 24일 밝혔다.
효소는 생물학적 반응을 촉매하는 단백질로서, 생명체 내 존재하는 다양한 화학 반응과 이에 따라 결정되는 생명체의 대사 특성을 파악하기 위해서는 각 효소의 기능을 이해하는 것이 필수적이다. EC 번호(효소 고유 번호, Enzyme Commission number)는 국제생화학 및 분자 생물학연맹 (International Union of Biochemistry and Molecular Biology, IUBMB)가 고안한 효소 기능 분류 체계로서, 다양한 유기체의 대사 특성을 이해하기 위해선 게놈 서열에서 존재하는 효소의 종류와 EC 번호를 빠르게 분석할 수 있는 기술 개발이 필요하다.
단백질의 기능 및 효소 기능 예측을 위해 인공지능을 활용하는 다양한 예측 시스템 또한 보고됐지만, 인공지능의 추론 과정을 직접 확인할 수 없는 블랙박스(black box)의 특징을 가졌거나, 효소 서열 내 아미노산 잔기(최소 단위) 수준으로 해석하지 못하는 문제가 있었다.
공동연구팀은 심층학습 기법과 단백질 상동성 분석 모듈을 활용해 주어진 단백질 서열의 효소 기능을 예측하는 인공지능 딥 EC 트랜스포머(DeepECtransformer)를 개발했다. 연구팀은 이번 연구에서 더 다양한 효소 기능을 정확하게 예측할 수 있도록 단백질 서열 전체 문맥에서 효소 기능에 중요한 정보를 추출하였고, 이를 통해 효소의 EC 번호를 정확하게 예측할 수 있었다. 개발된 인공지능은 총 5,360종류의 EC 번호를 예측할 수 있었다.
공동연구팀은 나아가 딥 EC 트랜스포머의 인공신경망 내 정보 흐름을 분석하여 인공지능이 추론 과정에서 효소 기능에 중요한 활성 부위나 보조 인자 결합 부위 정보를 활용하고 있음을 밝혀냈다. 이처럼 인공지능의 블랙박스를 해석함으로써 인공지능이 학습 과정에서 스스로 효소 기능에 중요한 특징을 파악하고 있음을 연구팀은 확인했다.
이번 논문의 제1 저자인 우리 대학 김기배 박사과정생은 “이번에 개발한 예측 시스템을 활용해 아직 밝혀진 적 없던 효소의 기능을 새롭게 예측하고 실험으로 검증할 수 있었다”고 말했다. 그는 또한 “딥 EC 트랜스포머를 활용해 생명체 내 밝혀지지 않았던 효소를 파악함으로써 유용 화합물을 생합성하기 위해 필요한 효소나 플라스틱을 생분해하기 위해 필요한 효소 등 다양한 대사 과정을 새롭게 밝혀낼 수 있을 것”이라고 덧붙였다.
또한 이상엽 특훈교수는 “효소 기능을 빠르고 정확하게 예측하는 딥 EC 트랜스포머는 기능 유전체학의 핵심 기술로서 시스템 수준에서 전체 효소들의 기능들을 분석할 수 있게 한다”며 “이를 활용해 모든 효소 정보를 포함한 대사 네트워크를 기반으로 친환경 미생물 공장 개발을 수행할 수 있을 것”이라고 밝혔다.
생명화학공학과 김기배 박사과정이 참여한 이번 논문은 국제 학술지 네이처(Nature) 誌가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 동료 심사를 거쳐 11월 14일 字 게재됐다.
※ 논문명 : 트랜스포머 레이어와 딥러닝을 사용하여 효소 인코딩 유전자의 기능적 주석 달기 (Functional annotation of enzyme-encoding genes using deep learning with transformer layers)
※ 저자 정보 : 김기배 (한국과학기술원, 제1 저자), 김지연 (한국과학기술원, 제2 저자), 이종언 (한국과학기술원, 제3 저자), Charles J. Norsigian (UCSD, 제4 저자), Bernhard O. Palsson (UCSD, 제5 저자) 및 이상엽(한국과학기술원, 교신저자) 포함 총 6 명
한편, 이번 연구는 과기정통부가 지원하는 ‘석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
숨겨진 효소 쏙쏙 찾아내는 인공지능 개발
대장균은 가장 많이 연구된 생명체 중 하나에 해당되지만 아직 대장균을 구성한 단백질 30%의 기능에 대해 명확하게 밝혀지지 않았다. 이에 대해 인공지능을 활용하여 아직 명확하게 밝혀진 바 없던 단백질에서 464종의 효소를 발견하였으며, 이 중 3종의 단백질의 예측된 기능을 시험관 내 효소 분석 방법을 통해 검증하는데 성공하였다.
우리 대학 생명화학공학과 이상엽 특훈교수와 캘리포니아대학교 샌디에이고(UCSD) 생명공학과 버나드 펄슨(Bernhard Palsson) 교수 공동연구팀이 단백질 서열을 활용, 해당 단백질의 효소 기능을 예측할 수 있는 인공지능, `딥 EC 트랜스포머(DeepECtransformer)'를 개발해 빠르고 정확하게 효소 기능을 파악할 수 있는 예측 시스템을 구축했다고 24일 밝혔다.
효소는 생물학적 반응을 촉매하는 단백질로서, 생명체 내 존재하는 다양한 화학 반응과 이에 따라 결정되는 생명체의 대사 특성을 파악하기 위해서는 각 효소의 기능을 이해하는 것이 필수적이다. EC 번호(효소 고유 번호, Enzyme Commission number)는 국제생화학 및 분자 생물학연맹 (International Union of Biochemistry and Molecular Biology, IUBMB)가 고안한 효소 기능 분류 체계로서, 다양한 유기체의 대사 특성을 이해하기 위해선 게놈 서열에서 존재하는 효소의 종류와 EC 번호를 빠르게 분석할 수 있는 기술 개발이 필요하다.
단백질의 기능 및 효소 기능 예측을 위해 인공지능을 활용하는 다양한 예측 시스템 또한 보고됐지만, 인공지능의 추론 과정을 직접 확인할 수 없는 블랙박스(black box)의 특징을 가졌거나, 효소 서열 내 아미노산 잔기(최소 단위) 수준으로 해석하지 못하는 문제가 있었다.
공동연구팀은 심층학습 기법과 단백질 상동성 분석 모듈을 활용해 주어진 단백질 서열의 효소 기능을 예측하는 인공지능 딥 EC 트랜스포머(DeepECtransformer)를 개발했다. 연구팀은 이번 연구에서 더 다양한 효소 기능을 정확하게 예측할 수 있도록 단백질 서열 전체 문맥에서 효소 기능에 중요한 정보를 추출하였고, 이를 통해 효소의 EC 번호를 정확하게 예측할 수 있었다. 개발된 인공지능은 총 5,360종류의 EC 번호를 예측할 수 있었다.
공동연구팀은 나아가 딥 EC 트랜스포머의 인공신경망 내 정보 흐름을 분석하여 인공지능이 추론 과정에서 효소 기능에 중요한 활성 부위나 보조 인자 결합 부위 정보를 활용하고 있음을 밝혀냈다. 이처럼 인공지능의 블랙박스를 해석함으로써 인공지능이 학습 과정에서 스스로 효소 기능에 중요한 특징을 파악하고 있음을 연구팀은 확인했다.
이번 논문의 제1 저자인 우리 대학 김기배 박사과정생은 “이번에 개발한 예측 시스템을 활용해 아직 밝혀진 적 없던 효소의 기능을 새롭게 예측하고 실험으로 검증할 수 있었다”고 말했다. 그는 또한 “딥 EC 트랜스포머를 활용해 생명체 내 밝혀지지 않았던 효소를 파악함으로써 유용 화합물을 생합성하기 위해 필요한 효소나 플라스틱을 생분해하기 위해 필요한 효소 등 다양한 대사 과정을 새롭게 밝혀낼 수 있을 것”이라고 덧붙였다.
또한 이상엽 특훈교수는 “효소 기능을 빠르고 정확하게 예측하는 딥 EC 트랜스포머는 기능 유전체학의 핵심 기술로서 시스템 수준에서 전체 효소들의 기능들을 분석할 수 있게 한다”며 “이를 활용해 모든 효소 정보를 포함한 대사 네트워크를 기반으로 친환경 미생물 공장 개발을 수행할 수 있을 것”이라고 밝혔다.
생명화학공학과 김기배 박사과정이 참여한 이번 논문은 국제 학술지 네이처(Nature) 誌가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 동료 심사를 거쳐 11월 14일 字 게재됐다.
※ 논문명 : 트랜스포머 레이어와 딥러닝을 사용하여 효소 인코딩 유전자의 기능적 주석 달기 (Functional annotation of enzyme-encoding genes using deep learning with transformer layers)
※ 저자 정보 : 김기배 (한국과학기술원, 제1 저자), 김지연 (한국과학기술원, 제2 저자), 이종언 (한국과학기술원, 제3 저자), Charles J. Norsigian (UCSD, 제4 저자), Bernhard O. Palsson (UCSD, 제5 저자) 및 이상엽(한국과학기술원, 교신저자) 포함 총 6 명
한편, 이번 연구는 과기정통부가 지원하는 ‘석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
2023.11.24
조회수 8725
-
 김학성 명예교수, 2023 효소공학상 수상
우리 대학 생명과학과 김학성 명예교수가 2023년 효소 공학상(Enzyme Engineering Award) 수상자로 선정됐다고 24일 밝혔다. 본 상은 효소공학(Enzyme Engineering) 분야 최고 권위 국제학회 상으로 2년마다 개최되는 국제 효소공학 학회(Enzyme Engineering Conference)에서 수여된다. 시상식은 오는 10월 1일부터 6일까지 싱가포르에서 개최되는 제27차 학회에서 수상 강연과 함께 진행된다.
효소(Enzyme)는 반응 특이성과 효율이 매우 높은 단백질의 일종으로 생체 내에서 생명 현상을 유지하는 데 가장 중요한 역할을 수행하는데, 예를 들면 유전자 복제, 신호전달, 대사, 단백질 합성 등 다양한 과정에 필수적으로 작용한다. 산업적으로 효소는 의약품 및 정밀/범용 화학제품 생산에 사용되고 있으며 최근에는 환경오염과 지구 온난화를 해결하고자 효소 기반 공정 개발 연구가 전 세계적으로 진행되고 있다.
그러나, 자연계에 존재하는 수많은 종류의 효소는 생체 내 반응에 적합하도록 진화되었기 때문에 이를 실제 산업적으로 사용하는 데 많은 제약이 있다. 이를 해결하고자 생명공학, 화학기업, 대학과 연구소에서 응용 목적에 맞는 효소 개발에 집중하고 있다.
김학성 교수는 지난 30여 년 동안 구조 기반 설계, 방향적 진화 및 컴퓨터 기반 설계를 통해 목적에 맞는 기능을 갖는 효소를 효율적으로 창출할 수 있는 기반 기술을 성공적으로 개발했다. 김 교수팀이 개발한 기반 기술은 산업용 효소, 단백질 신약, 합성 생물학, 바이오 화학, 생유기 합성 분야에서 광범위하게 활용될 수 있는 원천 기반 기술이다.
김 교수는 일련의 연구를 세계 최고 학술지인 ‘사이언스(Science)’를 비롯한 ‘네이쳐 케미컬 바이올로지(Nature Chemical Biology)’, ‘네이쳐 커뮤니케이션즈(Nature Communications)’, ‘앙게반테 케미(Angewandte Chemi.)’, ‘어드밴스드 사이언스(Advanced Science)’ 등의 저명 학술지에 발표하였고 60편의 특허를 등록하는 등 국제적으로 괄목할 업적을 이뤘다. 또한, 효소를 이용한 정밀화학 및 의약품 생산 기술을 산업체에 기술 이전 하여 관련 산업 발전에 크게 기여했다.
김학성 교수는 이러한 공로를 인정받아 관련분야의 최고 권위 국제 학회상인 ‘효소 공학상(Enzyme Engineering Award)’ 수상자로 선정됐다.
상을 수상한 김학성 교수는 “연구실 실적이 국제적으로 인정받아 권위 있는 상을 받게 되어 매우 영광이고, 연구실 졸업생들과 재정적 지원을 해주신 기관에 감사를 드린다. 앞으로 다양한 분야에서 효소의 산업적 응용을 확대시키는데 노력을 할 것이다”라고 수상 소감을 밝혔다.
김학성 명예교수, 2023 효소공학상 수상
우리 대학 생명과학과 김학성 명예교수가 2023년 효소 공학상(Enzyme Engineering Award) 수상자로 선정됐다고 24일 밝혔다. 본 상은 효소공학(Enzyme Engineering) 분야 최고 권위 국제학회 상으로 2년마다 개최되는 국제 효소공학 학회(Enzyme Engineering Conference)에서 수여된다. 시상식은 오는 10월 1일부터 6일까지 싱가포르에서 개최되는 제27차 학회에서 수상 강연과 함께 진행된다.
효소(Enzyme)는 반응 특이성과 효율이 매우 높은 단백질의 일종으로 생체 내에서 생명 현상을 유지하는 데 가장 중요한 역할을 수행하는데, 예를 들면 유전자 복제, 신호전달, 대사, 단백질 합성 등 다양한 과정에 필수적으로 작용한다. 산업적으로 효소는 의약품 및 정밀/범용 화학제품 생산에 사용되고 있으며 최근에는 환경오염과 지구 온난화를 해결하고자 효소 기반 공정 개발 연구가 전 세계적으로 진행되고 있다.
그러나, 자연계에 존재하는 수많은 종류의 효소는 생체 내 반응에 적합하도록 진화되었기 때문에 이를 실제 산업적으로 사용하는 데 많은 제약이 있다. 이를 해결하고자 생명공학, 화학기업, 대학과 연구소에서 응용 목적에 맞는 효소 개발에 집중하고 있다.
김학성 교수는 지난 30여 년 동안 구조 기반 설계, 방향적 진화 및 컴퓨터 기반 설계를 통해 목적에 맞는 기능을 갖는 효소를 효율적으로 창출할 수 있는 기반 기술을 성공적으로 개발했다. 김 교수팀이 개발한 기반 기술은 산업용 효소, 단백질 신약, 합성 생물학, 바이오 화학, 생유기 합성 분야에서 광범위하게 활용될 수 있는 원천 기반 기술이다.
김 교수는 일련의 연구를 세계 최고 학술지인 ‘사이언스(Science)’를 비롯한 ‘네이쳐 케미컬 바이올로지(Nature Chemical Biology)’, ‘네이쳐 커뮤니케이션즈(Nature Communications)’, ‘앙게반테 케미(Angewandte Chemi.)’, ‘어드밴스드 사이언스(Advanced Science)’ 등의 저명 학술지에 발표하였고 60편의 특허를 등록하는 등 국제적으로 괄목할 업적을 이뤘다. 또한, 효소를 이용한 정밀화학 및 의약품 생산 기술을 산업체에 기술 이전 하여 관련 산업 발전에 크게 기여했다.
김학성 교수는 이러한 공로를 인정받아 관련분야의 최고 권위 국제 학회상인 ‘효소 공학상(Enzyme Engineering Award)’ 수상자로 선정됐다.
상을 수상한 김학성 교수는 “연구실 실적이 국제적으로 인정받아 권위 있는 상을 받게 되어 매우 영광이고, 연구실 졸업생들과 재정적 지원을 해주신 기관에 감사를 드린다. 앞으로 다양한 분야에서 효소의 산업적 응용을 확대시키는데 노력을 할 것이다”라고 수상 소감을 밝혔다.
2023.08.24
조회수 5757
-
 RNA 합성에서 ‘기다림의 미학’ 규명
DNA에서 RNA를 생성하는 과정을 마무리 짓는 전사종결인자가 단백질 로(이하 Rho)이다. 일반 단백질이 작용물질에 미리 붙어 있으면 반응이 빨리 된다는 통념과 다르게 RNA 중합효소에 붙어 기다리는 Rho는 중합효소가 오래 멈출수록 종결 효율이 높아진다는 유의미한 결과가 발표되었다. 이번 연구 결과를 통해 자연에서 기다림의 미학이 증명된 것이다.
우리 대학 생명과학과 강창원 명예교수(KAIST 줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동 연구팀이 우리 대학 화학과 강진영 교수, 우리 대학 생명과학과 서연수 교수 연구팀과 협업 연구를 통해 RNA 합성 종결인자의 동역학적 특성을 발견했으며 그런 특성이 유전자 발현 조절에 미치는 생물학적 기능을 규명했다고 27일 밝혔다.
공동 연구팀은 세균의 전사 종결에 단백질 Rho가 관여하는 분자기작에 관해 작년에 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 발표한 바에 따르면, Rho가 중합효소에 미리 결합해 RNA의 특수부위를 기다린 후 중합효소‧DNA‧RNA의 전사 복합체를 해체하는 방식과 Rho가 RNA에 먼저 결합해 중합효소를 쫓아간 후 복합체를 해체하는 방식, 쫓아간 후 RNA만 방출하고 중합효소가 DNA에 남는 방식 등 세 갈래로 나뉘어 진행된다. (아래 그림 참조)
그런데 흥미롭게도 세 갈래 진행하는 속도가 기존 통념과는 다른 새로운 사실을 발견했다. 기존에는 Rho가 RNA에 붙어 중합효소를 쫓아가서 끝내는 방식과 비교하면 Rho가 중합효소에 미리 붙어 기다렸다가 끝내는 방식이 쫓아가는 시간이 들지 않기 때문에 더 빠를 것으로 인식되어 왔다. 하지만 공동 연구팀의 연구 결과는 기다려서 끝내는 방식이 오히려 더 느렸다. 그런데 느린 기다림 방식은 중합효소의 멈춤 시간이 길수록 종결 효율이 높고 상황에 따라 달라질 수 있는 반면에 쫓아가는 빠른 방식은 종결 효율이 중합효소 멈춘 시간과 상관이 없으며 상황에 따라 변화의 여지도 없다는 사실을 새롭게 밝혔다.
RNA가 방출되는 전사 종결이 일어나려면 RNA의 연장 합성이 일단 멈춰야 한다. 종결이 더디게 일어나려면 멈춤이 오래 유지되어야 하므로 전사 멈춤 시간과 전사 종결 효율의 상관관계를 이번 공동 연구에서 분석했다. 연구 결과, 기다려서 전사의 세 갈래 끝내기 방식이 진행하는 속도가 제각각 다를 뿐 아니라 그 조절 양상도 다르다는 것을 처음으로 규명한 것이다.
생물물리학 분야 첨단 기술인 단일분자 실험을 수행한 서울대 물리천문학부 송은호 박사과정 대학원생이 제1 저자로 참여한 이번 논문(제목: Transcriptional pause extension benefits the stand-by rather than catch-up Rho-dependent termination)은 저명 국제학술지 핵산연구(Nucleic Acids Research, 최근 영향지수 = 19.160)에 지난 2월 10일 자 게재됐다. KAIST 팔린다 무나싱하 박사, KAIST 황승하 박사과정 대학원생도 참여해 저자가 총 7명이다.
송은호 제1 저자는 "기존 통념과 상반된 결과를 처음 발견했을 때 당황스러웠지만 데이터를 꾸준히 쌓아가고 적절한 통계 모델을 통해서 그 결과를 검증해냈을 때 뿌듯했고, 또 이 발견의 생물학적 역할을 규명했을 때 더욱 기뻤다ˮ며 "항생제 개발 등에 중요한 단서를 줄 것이다ˮ라고 연구의 의의를 설명했다.
이번 공동 연구에는 단일분자 형광 기술을 구사하는 물리학자, 유전자 발현을 탐구하는 생명과학자, 중합체 구조를 분석하는 화학자가 두루 참여했다. 다양한 분야의 전공자가 꾸준히 협업하는 다학제 기초과학 연구의 우수 사례이며, 이번 연구는 한국연구재단 중견연구자지원사업, KAIST 고위험‧고성과 연구사업의 지원을 받았고, 논문게재비는 KAIST에서 지원했다.
RNA 합성에서 ‘기다림의 미학’ 규명
DNA에서 RNA를 생성하는 과정을 마무리 짓는 전사종결인자가 단백질 로(이하 Rho)이다. 일반 단백질이 작용물질에 미리 붙어 있으면 반응이 빨리 된다는 통념과 다르게 RNA 중합효소에 붙어 기다리는 Rho는 중합효소가 오래 멈출수록 종결 효율이 높아진다는 유의미한 결과가 발표되었다. 이번 연구 결과를 통해 자연에서 기다림의 미학이 증명된 것이다.
우리 대학 생명과학과 강창원 명예교수(KAIST 줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동 연구팀이 우리 대학 화학과 강진영 교수, 우리 대학 생명과학과 서연수 교수 연구팀과 협업 연구를 통해 RNA 합성 종결인자의 동역학적 특성을 발견했으며 그런 특성이 유전자 발현 조절에 미치는 생물학적 기능을 규명했다고 27일 밝혔다.
공동 연구팀은 세균의 전사 종결에 단백질 Rho가 관여하는 분자기작에 관해 작년에 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 발표한 바에 따르면, Rho가 중합효소에 미리 결합해 RNA의 특수부위를 기다린 후 중합효소‧DNA‧RNA의 전사 복합체를 해체하는 방식과 Rho가 RNA에 먼저 결합해 중합효소를 쫓아간 후 복합체를 해체하는 방식, 쫓아간 후 RNA만 방출하고 중합효소가 DNA에 남는 방식 등 세 갈래로 나뉘어 진행된다. (아래 그림 참조)
그런데 흥미롭게도 세 갈래 진행하는 속도가 기존 통념과는 다른 새로운 사실을 발견했다. 기존에는 Rho가 RNA에 붙어 중합효소를 쫓아가서 끝내는 방식과 비교하면 Rho가 중합효소에 미리 붙어 기다렸다가 끝내는 방식이 쫓아가는 시간이 들지 않기 때문에 더 빠를 것으로 인식되어 왔다. 하지만 공동 연구팀의 연구 결과는 기다려서 끝내는 방식이 오히려 더 느렸다. 그런데 느린 기다림 방식은 중합효소의 멈춤 시간이 길수록 종결 효율이 높고 상황에 따라 달라질 수 있는 반면에 쫓아가는 빠른 방식은 종결 효율이 중합효소 멈춘 시간과 상관이 없으며 상황에 따라 변화의 여지도 없다는 사실을 새롭게 밝혔다.
RNA가 방출되는 전사 종결이 일어나려면 RNA의 연장 합성이 일단 멈춰야 한다. 종결이 더디게 일어나려면 멈춤이 오래 유지되어야 하므로 전사 멈춤 시간과 전사 종결 효율의 상관관계를 이번 공동 연구에서 분석했다. 연구 결과, 기다려서 전사의 세 갈래 끝내기 방식이 진행하는 속도가 제각각 다를 뿐 아니라 그 조절 양상도 다르다는 것을 처음으로 규명한 것이다.
생물물리학 분야 첨단 기술인 단일분자 실험을 수행한 서울대 물리천문학부 송은호 박사과정 대학원생이 제1 저자로 참여한 이번 논문(제목: Transcriptional pause extension benefits the stand-by rather than catch-up Rho-dependent termination)은 저명 국제학술지 핵산연구(Nucleic Acids Research, 최근 영향지수 = 19.160)에 지난 2월 10일 자 게재됐다. KAIST 팔린다 무나싱하 박사, KAIST 황승하 박사과정 대학원생도 참여해 저자가 총 7명이다.
송은호 제1 저자는 "기존 통념과 상반된 결과를 처음 발견했을 때 당황스러웠지만 데이터를 꾸준히 쌓아가고 적절한 통계 모델을 통해서 그 결과를 검증해냈을 때 뿌듯했고, 또 이 발견의 생물학적 역할을 규명했을 때 더욱 기뻤다ˮ며 "항생제 개발 등에 중요한 단서를 줄 것이다ˮ라고 연구의 의의를 설명했다.
이번 공동 연구에는 단일분자 형광 기술을 구사하는 물리학자, 유전자 발현을 탐구하는 생명과학자, 중합체 구조를 분석하는 화학자가 두루 참여했다. 다양한 분야의 전공자가 꾸준히 협업하는 다학제 기초과학 연구의 우수 사례이며, 이번 연구는 한국연구재단 중견연구자지원사업, KAIST 고위험‧고성과 연구사업의 지원을 받았고, 논문게재비는 KAIST에서 지원했다.
2023.02.27
조회수 8703
-
 RNA를 통한 유전자 전사 조절 원리 규명
세포가 어떤 유전자를 얼마나 발현하느냐에 따라 그 세포의 모양, 기능, 수명 등이 결정되므로 유전정보를 처음으로 발현하는 RNA 합성효소의 활성은 세포 내에서 매우 중요하게, 또 정교하게 조절된다. 그러나 이러한 유전자 전사(transcription) 조절의 중요성에도 불구하고 RNA 합성효소가 이러한 단백질과 RNA들에 의해서 어떻게 조절되는지 분자적인 수준에서는 잘 알려져 있지 않았다.
☞ 유전자 전사: DNA의 유전정보가 RNA에 옮겨지는 과정을 말한다. 유전정보의 복사물인 RNA는 단백질 합성에 사용된다.
우리 대학 화학과 강진영 교수 연구팀이 RNA를 통한 RNA 합성효소의 조절 메커니즘을 알아내고자 RNA 합성효소와 RNA 합성효소를 조절하는 바이러스 유래 RNA인 *HK022 putRNA의 결합 구조를 초저온 전자현미경(cryo-EM)으로 규명하여 유전자 전사조절의 기초 원리를 규명했다고 7일 밝혔다.
*HK022 putRNA: HK022 박테리오파지(박테리아를 감염시키는 바이러스)의 RNA로 다른 단백질의 도움 없이 해당 RNA를 만든 RNA 중합효소와 결합해 RNA 합성이 계속 되도록 RNA 중합효소를 조절
화학과 황승하 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 지난 8월 15일 출판되었다. (논문명: Structural basis of transcriptional regulation by a nascent RNA element, HK022 putRNA).
HK022 putRNA는 RNA 합성효소와 결합해서 RNA 합성이 멈추지 않고 계속 되도록 도와주는 역할을 한다. 이러한 기능을 이해하기 위해서 본 연구팀은 putRNA와 RNA 합성효소의 결합 복합체(put-associated RNA polymerase elongation complex, putEC)의 세 가지 구조를 초저온 전자현미경으로 규명하였다.
이 연구에서는 활성을 가진 putRNA를 제작하기 위해 장애물 단백질을 RNA 합성에 활용하는 방법을 고안하였으며, 초저온 전자현미경 촬영 결과 예상하지 못했던 세 종류의 복합체 – putRNA가 잘 접혀서 RNA 합성효소와 결합하고 있는 putEC, put RNA가 접히지 않은 put-없는 EC, 잘 접힌 putRNA와 시그마 단백질이 함께 RNA 합성효소와 결합하고 있는 시그마* 결합-putEC – 를 발견할 수 있었다. (그림 1)
*시그마: RNA 합성효소가 유전자 RNA 합성을 처음 시작할 때 필요한 단백질로 RNA 합성이 어느 정도 안정화되면 RNA 합성효소에서 떨어진다.
연구팀은 이들 복합체의 구조를 통해 putRNA가 이전 연구에서 예측된 대로 RNA 합성효소와 안정적으로 결합하고 있지만 예측과 달리 예상보다 더 많은 염기쌍(base pair)을 사용해 RNA 이중나선(double helix) 뿐 아니라 삼중나선(triple helix)을 형성하는 것을 확인하였다. 또한, putRNA가 RNA 합성효소와 결합하면 RNA 합성효소가 RNA 합성을 잠시 멈출 때 가지는 구조의 변화를 방해해서 RNA 합성을 지속하도록 한다는 가설을 제시할 수 있었다.
한편, 시그마 단백질(σ70)은 RNA 합성효소가 전사를 시작할 때 필요한 전사 개시인자로, RNA 합성이 안정되면 RNA 합성효소에서 떨어졌다가 특정 DNA 서열(–10-유사 서열)이 있으면 전사 과정 중이라도 다시 RNA 중합효소와 결합해 RNA 합성을 일시적으로 멈추는 것으로 알려져 있다. 이번 연구에서는 예상치 못하게 관찰된 시그마 결합-putEC 구조를 통해 시그마가 RNA 합성효소와 결합하여 RNA 합성이 잠깐 멈추면 putRNA가 더 잘 접힌다는 것을 알 수 있었다.
이 연구의 교신저자인 강진영 교수는 "RNA 합성효소는 세포 내에 저장된 유전 정보를 처음으로 꺼내어 생명활동에 활용하는, 세포 내에서 제일 중요한 단백질 중 하나이다. 그러나 RNA 합성효소의 큰 크기와 다양한 구조 변화 때문에 이전에 주로 활용하던 X-ray 결정학 방식으로는 그 구조를 관찰하기가 어려웠다. 최근 초저온 전자현미경의 발달로 이제야 조금씩 RNA 합성효소의 작동 원리가 알려지고 있는 상황이다. 이번 연구는 이전에 잘 알려지지 않았던, RNA를 통한 전사 조절의 기초적인 원리를 설명한 것으로, RNA를 통한 RNA 합성효소 조절의 다양한 전략을 밝혀줄 시작점이며, 더 나아가 유전자 발현을 조작할 수 있는 RNA의 개발을 도울 수 있는 정보를 제공할 것이라 기대한다.ˮ고 밝혔다.
한편 이번 연구는 한국연구재단의 이공분야기초연구사업(우수신진연구)과 원천기술개발사업의 지원을 받아 수행됐다.
RNA를 통한 유전자 전사 조절 원리 규명
세포가 어떤 유전자를 얼마나 발현하느냐에 따라 그 세포의 모양, 기능, 수명 등이 결정되므로 유전정보를 처음으로 발현하는 RNA 합성효소의 활성은 세포 내에서 매우 중요하게, 또 정교하게 조절된다. 그러나 이러한 유전자 전사(transcription) 조절의 중요성에도 불구하고 RNA 합성효소가 이러한 단백질과 RNA들에 의해서 어떻게 조절되는지 분자적인 수준에서는 잘 알려져 있지 않았다.
☞ 유전자 전사: DNA의 유전정보가 RNA에 옮겨지는 과정을 말한다. 유전정보의 복사물인 RNA는 단백질 합성에 사용된다.
우리 대학 화학과 강진영 교수 연구팀이 RNA를 통한 RNA 합성효소의 조절 메커니즘을 알아내고자 RNA 합성효소와 RNA 합성효소를 조절하는 바이러스 유래 RNA인 *HK022 putRNA의 결합 구조를 초저온 전자현미경(cryo-EM)으로 규명하여 유전자 전사조절의 기초 원리를 규명했다고 7일 밝혔다.
*HK022 putRNA: HK022 박테리오파지(박테리아를 감염시키는 바이러스)의 RNA로 다른 단백질의 도움 없이 해당 RNA를 만든 RNA 중합효소와 결합해 RNA 합성이 계속 되도록 RNA 중합효소를 조절
화학과 황승하 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 지난 8월 15일 출판되었다. (논문명: Structural basis of transcriptional regulation by a nascent RNA element, HK022 putRNA).
HK022 putRNA는 RNA 합성효소와 결합해서 RNA 합성이 멈추지 않고 계속 되도록 도와주는 역할을 한다. 이러한 기능을 이해하기 위해서 본 연구팀은 putRNA와 RNA 합성효소의 결합 복합체(put-associated RNA polymerase elongation complex, putEC)의 세 가지 구조를 초저온 전자현미경으로 규명하였다.
이 연구에서는 활성을 가진 putRNA를 제작하기 위해 장애물 단백질을 RNA 합성에 활용하는 방법을 고안하였으며, 초저온 전자현미경 촬영 결과 예상하지 못했던 세 종류의 복합체 – putRNA가 잘 접혀서 RNA 합성효소와 결합하고 있는 putEC, put RNA가 접히지 않은 put-없는 EC, 잘 접힌 putRNA와 시그마 단백질이 함께 RNA 합성효소와 결합하고 있는 시그마* 결합-putEC – 를 발견할 수 있었다. (그림 1)
*시그마: RNA 합성효소가 유전자 RNA 합성을 처음 시작할 때 필요한 단백질로 RNA 합성이 어느 정도 안정화되면 RNA 합성효소에서 떨어진다.
연구팀은 이들 복합체의 구조를 통해 putRNA가 이전 연구에서 예측된 대로 RNA 합성효소와 안정적으로 결합하고 있지만 예측과 달리 예상보다 더 많은 염기쌍(base pair)을 사용해 RNA 이중나선(double helix) 뿐 아니라 삼중나선(triple helix)을 형성하는 것을 확인하였다. 또한, putRNA가 RNA 합성효소와 결합하면 RNA 합성효소가 RNA 합성을 잠시 멈출 때 가지는 구조의 변화를 방해해서 RNA 합성을 지속하도록 한다는 가설을 제시할 수 있었다.
한편, 시그마 단백질(σ70)은 RNA 합성효소가 전사를 시작할 때 필요한 전사 개시인자로, RNA 합성이 안정되면 RNA 합성효소에서 떨어졌다가 특정 DNA 서열(–10-유사 서열)이 있으면 전사 과정 중이라도 다시 RNA 중합효소와 결합해 RNA 합성을 일시적으로 멈추는 것으로 알려져 있다. 이번 연구에서는 예상치 못하게 관찰된 시그마 결합-putEC 구조를 통해 시그마가 RNA 합성효소와 결합하여 RNA 합성이 잠깐 멈추면 putRNA가 더 잘 접힌다는 것을 알 수 있었다.
이 연구의 교신저자인 강진영 교수는 "RNA 합성효소는 세포 내에 저장된 유전 정보를 처음으로 꺼내어 생명활동에 활용하는, 세포 내에서 제일 중요한 단백질 중 하나이다. 그러나 RNA 합성효소의 큰 크기와 다양한 구조 변화 때문에 이전에 주로 활용하던 X-ray 결정학 방식으로는 그 구조를 관찰하기가 어려웠다. 최근 초저온 전자현미경의 발달로 이제야 조금씩 RNA 합성효소의 작동 원리가 알려지고 있는 상황이다. 이번 연구는 이전에 잘 알려지지 않았던, RNA를 통한 전사 조절의 기초적인 원리를 설명한 것으로, RNA를 통한 RNA 합성효소 조절의 다양한 전략을 밝혀줄 시작점이며, 더 나아가 유전자 발현을 조작할 수 있는 RNA의 개발을 도울 수 있는 정보를 제공할 것이라 기대한다.ˮ고 밝혔다.
한편 이번 연구는 한국연구재단의 이공분야기초연구사업(우수신진연구)과 원천기술개발사업의 지원을 받아 수행됐다.
2022.09.07
조회수 13053
-
 유전자 가위를 이용한 RNA 분해효소 검출 신기술 개발
우리 대학 생명화학공학과 박현규 교수 연구팀이 *크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 *부수적 절단 활성을 활용해 RNA 분해효소를 민감하게 검출해내는 신기술을 개발했다고 14일 밝혔다.
☞ 크리스퍼 카스 시스템 (유전자 가위 기술)
- 크리스퍼 카스 시스템은 박테리아가 바이러스 감염으로부터 자신을 보호하기 위해 진화시킨 적응 면역 시스템이다. 이는 외래 유전자의 정보를 담고있는 가이드RNA와 직접 핵산을 절단하는 카스 단백질로 이루어져 있다. 2020년 제니퍼 다우드나 교수의 연구팀이 크리스퍼 카스9 유전자 가위 시스템을 개발한 공로로 노벨화학상을 수상해 널리 알려졌으며, 높은 표적 특이성과 빠른 역학 덕분에 최근에는 유전체 편집을 넘어 생체물질 검출 및 분자진단 분야에 광범위하게 적용되고 있다.
☞ 부수적 절단 활성
- 카스9 이외에도 Cas12, Cas13 등의 다양한 카스 단백질이 발굴되고 활용되고 있다. 카스12a는 표적 DNA 서열을 인식해 이를 절단하며, 이에 더해 주변의 비표적 단일 가닥 DNA를 무작위하게 절단하는 부수적 절단 활성을 가지고 있다. 이러한 성질은 분자진단 분야에서 활발하게 사용되고 있다.
우리 대학 생명화학공학과 김한솔 박사가 제1 저자로 참여한 이번 연구는 영국왕립화학회가 발행하는 국제 학술지 `케미컬 커뮤니케이션스 (Chemical Communications)'에 2022년도 16호 표지(Back cover) 논문으로 지난달 24일 선정됐다. (논문명: CRISPR/Cas12a collateral cleavage activity for an ultrasensitive assay of RNase H)
RNA 분해효소의 일종인 `리보핵산가수분해효소 H'는 후천성면역결핍증(에이즈)을 일으키는 바이러스인 인간 면역결핍 바이러스(HIV-1) 및 B형 간염 바이러스를 포함한 역전사 바이러스의 역전사효소에서 필수적인 영역으로, 역전사 바이러스의 증식에 관여한다. 따라서 리보핵산가수분해효소 H는 항바이러스제 개발의 중요한 표적으로 알려져 있다. 일반적으로 리보핵산가수분해효소 H의 활성을 검출하기 위해서는 전기영동 또는 고성능 액체크로마토그래피 등의 방식을 사용하고 있지만, 이와 같은 기술들은 낮은 특이도와 민감도, 복잡한 검출 과정, 긴 검출 시간 등의 단점이 있다.
연구팀은 이러한 현행 기술의 한계를 극복하기 위해, 크리스퍼 카스12a (CRISPR-Cas12a) 시스템을 활용해 검출의 민감도를 크게 향상하고 리보핵산가수분해효소 H를 현재 보고된 기술 중 가장 높은 민감도로(검출한계: 0.24 U/L) 1시간 이내에 검출하는 데 성공했다.
연구팀은 리보핵산가수분해효소 H의 기질로 짧은 DNA/RNA 키메라 복합체를 이용해 리보핵산가수분해효소 H의 활성 하에 활성제 DNA (Activator DNA, AD)가 방출되도록 설계했다. Cas12a/crRNA 복합체가 방출된 활성제 DNA를 인식할 시 Cas12a의 부수적 절단 활성을 가동해 주변의 리포터 DNA를 절단해 형광 신호가 발생하도록 설계함으로써, 표적 유전자 돌연변이를 고감도로 매우 정확하게 검출했다. 연구팀은 이 기술을 통해서 암세포의 리보핵산가수분해효소 H 활성도 성공적으로 검출할 수 있었다.
특히 리보핵산가수분해효소 H가 인간 면역결핍 바이러스 증식에 관여한다는 점을 고려할 때, 이번 연구 성과는 에이즈 치료제 개발에 기여할 수 있을 것으로도 기대된다.
박현규 교수는 “이번 기술은 크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 부수적 절단 활성을 활용해 리보핵산가수분해효소 H를 고도로 민감하게 검출함으로써, 항바이러스제의 표적 발굴에 활용될 수 있다”라고 연구의 의의를 설명했다.
한편 이번 연구는 경찰청의 치안과학기술연구개발사업 및 한국연구재단의 중견연구자지원사업과 바이오·의료기술개발사업의 일환으로 수행됐다.
유전자 가위를 이용한 RNA 분해효소 검출 신기술 개발
우리 대학 생명화학공학과 박현규 교수 연구팀이 *크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 *부수적 절단 활성을 활용해 RNA 분해효소를 민감하게 검출해내는 신기술을 개발했다고 14일 밝혔다.
☞ 크리스퍼 카스 시스템 (유전자 가위 기술)
- 크리스퍼 카스 시스템은 박테리아가 바이러스 감염으로부터 자신을 보호하기 위해 진화시킨 적응 면역 시스템이다. 이는 외래 유전자의 정보를 담고있는 가이드RNA와 직접 핵산을 절단하는 카스 단백질로 이루어져 있다. 2020년 제니퍼 다우드나 교수의 연구팀이 크리스퍼 카스9 유전자 가위 시스템을 개발한 공로로 노벨화학상을 수상해 널리 알려졌으며, 높은 표적 특이성과 빠른 역학 덕분에 최근에는 유전체 편집을 넘어 생체물질 검출 및 분자진단 분야에 광범위하게 적용되고 있다.
☞ 부수적 절단 활성
- 카스9 이외에도 Cas12, Cas13 등의 다양한 카스 단백질이 발굴되고 활용되고 있다. 카스12a는 표적 DNA 서열을 인식해 이를 절단하며, 이에 더해 주변의 비표적 단일 가닥 DNA를 무작위하게 절단하는 부수적 절단 활성을 가지고 있다. 이러한 성질은 분자진단 분야에서 활발하게 사용되고 있다.
우리 대학 생명화학공학과 김한솔 박사가 제1 저자로 참여한 이번 연구는 영국왕립화학회가 발행하는 국제 학술지 `케미컬 커뮤니케이션스 (Chemical Communications)'에 2022년도 16호 표지(Back cover) 논문으로 지난달 24일 선정됐다. (논문명: CRISPR/Cas12a collateral cleavage activity for an ultrasensitive assay of RNase H)
RNA 분해효소의 일종인 `리보핵산가수분해효소 H'는 후천성면역결핍증(에이즈)을 일으키는 바이러스인 인간 면역결핍 바이러스(HIV-1) 및 B형 간염 바이러스를 포함한 역전사 바이러스의 역전사효소에서 필수적인 영역으로, 역전사 바이러스의 증식에 관여한다. 따라서 리보핵산가수분해효소 H는 항바이러스제 개발의 중요한 표적으로 알려져 있다. 일반적으로 리보핵산가수분해효소 H의 활성을 검출하기 위해서는 전기영동 또는 고성능 액체크로마토그래피 등의 방식을 사용하고 있지만, 이와 같은 기술들은 낮은 특이도와 민감도, 복잡한 검출 과정, 긴 검출 시간 등의 단점이 있다.
연구팀은 이러한 현행 기술의 한계를 극복하기 위해, 크리스퍼 카스12a (CRISPR-Cas12a) 시스템을 활용해 검출의 민감도를 크게 향상하고 리보핵산가수분해효소 H를 현재 보고된 기술 중 가장 높은 민감도로(검출한계: 0.24 U/L) 1시간 이내에 검출하는 데 성공했다.
연구팀은 리보핵산가수분해효소 H의 기질로 짧은 DNA/RNA 키메라 복합체를 이용해 리보핵산가수분해효소 H의 활성 하에 활성제 DNA (Activator DNA, AD)가 방출되도록 설계했다. Cas12a/crRNA 복합체가 방출된 활성제 DNA를 인식할 시 Cas12a의 부수적 절단 활성을 가동해 주변의 리포터 DNA를 절단해 형광 신호가 발생하도록 설계함으로써, 표적 유전자 돌연변이를 고감도로 매우 정확하게 검출했다. 연구팀은 이 기술을 통해서 암세포의 리보핵산가수분해효소 H 활성도 성공적으로 검출할 수 있었다.
특히 리보핵산가수분해효소 H가 인간 면역결핍 바이러스 증식에 관여한다는 점을 고려할 때, 이번 연구 성과는 에이즈 치료제 개발에 기여할 수 있을 것으로도 기대된다.
박현규 교수는 “이번 기술은 크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 부수적 절단 활성을 활용해 리보핵산가수분해효소 H를 고도로 민감하게 검출함으로써, 항바이러스제의 표적 발굴에 활용될 수 있다”라고 연구의 의의를 설명했다.
한편 이번 연구는 경찰청의 치안과학기술연구개발사업 및 한국연구재단의 중견연구자지원사업과 바이오·의료기술개발사업의 일환으로 수행됐다.
2022.03.14
조회수 13269
-
 6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
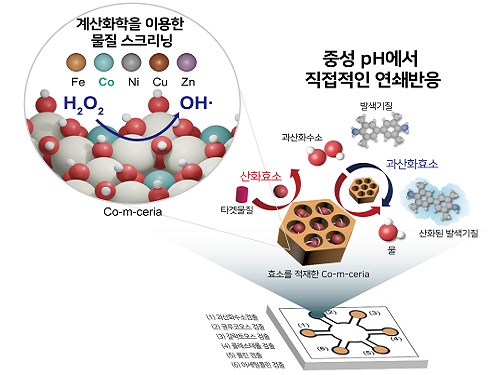
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07
조회수 12718
-
 자연계 효소 원리를 이용한 신개념 산업용 촉매 개발
우리 대학 생명화학공학과 최민기 교수 연구팀이 자연계 효소와 같이 원하는 반응물만 선택적으로 전환할 수 있는 신개념의 고성능 산업 촉매를 개발했다고 9일 밝혔다.
촉매는 기초 유분 생산에서부터 다양한 화학 제품 제조까지 대부분의 석유화학 공정에서 사용되는 물질로 공정의 경제성과 친환경성을 높이기 위해서 원하는 생성물만 만들어지는 높은 선택성을 갖는 촉매 개발이 필수적이다.
지구상에 존재하는 촉매 중 가장 높은 선택성을 보이는 촉매는 효소다. 효소는 천연 고분자인 단백질이 반응이 일어나는 활성점을 3차원적으로 둘러싸고 있는 구조를 갖는데, 단백질의 구조 및 활성점과의 상호작용에 따라 특정 반응물만 선택적으로 접근할 수 있도록 조절해 높은 선택성을 갖는다. 연구팀은 이번 연구에서 효소의 단백질과 유사한 고분자를 이용해 금속 활성점과의 상호작용을 조절한 새로운 개념의 촉매 설계 방법을 제시했다.
고분자는 일정 단위체의 반복적인 화학 결합을 통해 만들어지는 높은 분자량의 거대분자이며 합성에 사용한 단위체에 따라 고분자의 작용기를 쉽게 조절할 수 있다. 연구팀은 금속과 상호작용을 할 수 있는 작용기를 포함한 고분자를 합성하고 팔라듐 금속 입자를 포함한 촉매를 만들었다. 금속과 강하게 상호작용을 하는 고분자는 효소와 같이 금속 주위를 고분자가 3차원적으로 둘러싸는 형태를 보이는 한편 약하게 상호작용하는 고분자는 금속을 둘러싸지 못하고 금속 표면이 노출된 형태가 됐다.
연구팀은 이렇게 합성된 촉매를 이용해 석유화학의 에틸렌 생산 공정에서 매우 중요한 아세틸렌 부분 수소화 반응에 적용했다. 에틸렌은 플라스틱, 비닐, 접착제 등 다양한 제품을 만드는 데 이용하는 기본 핵심 원료이며 현재 우리나라에서는 주로 나프타를 분해하여 생산한다.
나프타분해시설에서 생산되는 에틸렌에는 불순물인 미량의 아세틸렌이 함께 포함돼 있는데, 이 아세틸렌이 화학 제품을 만드는 데 사용되는 촉매에 치명적으로 작용하기 때문에 수소화 반응을 통해 제거해 주는 공정이 필수적이다. 이 공정에서 핵심은 99% 이상의 에틸렌은 소모하지 않으면서 1% 미만의 아세틸렌만 선택적으로 제거하는 것이다.
연구진이 개발한 신규 촉매를 이 공정에 적용한 결과, 강하게 상호작용해 3차원 구조를 형성한 촉매는 고분자가 아세틸렌에만 접근해 높은 선택도를 보였다. 하지만 약한 상호작용으로 인해 고분자가 금속 표면을 덮지 못한 촉매에서는 아세틸렌과 에틸렌에 모두 접근해 낮은 선택도를 보였다.
또한 강하게 상호작용을 하는 고분자일수록 비활성화를 일으키는 탄소 침적물인 코크의 생성을 차단하고 금속 입자의 뭉침 현상을 억제해 장기간 반응에서도 높은 활성과 선택도를 유지했다.
연구를 주도한 최민기 교수는 "자연계 효소의 원리를 모방해 고분자와 금속 사이의 상호작용을 조절하고 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 가지는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념이다ˮ라며, "향후 높은 선택도가 필요한 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것이다ˮ라고 말했다.
우리 대학 생명화학공학과 현경림 박사과정 학생이 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `앙게반테 케미(Angewandte chemi)'에 지난 5월 17일 字 온라인판에 게재됐다. (논문명: Tailoring a Dynamic Metal-Polymer Interaction to Improve Catalyst Selectivity and Longevity in Hydrogenation),
한편 이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원을 받아 수행됐다.
자연계 효소 원리를 이용한 신개념 산업용 촉매 개발
우리 대학 생명화학공학과 최민기 교수 연구팀이 자연계 효소와 같이 원하는 반응물만 선택적으로 전환할 수 있는 신개념의 고성능 산업 촉매를 개발했다고 9일 밝혔다.
촉매는 기초 유분 생산에서부터 다양한 화학 제품 제조까지 대부분의 석유화학 공정에서 사용되는 물질로 공정의 경제성과 친환경성을 높이기 위해서 원하는 생성물만 만들어지는 높은 선택성을 갖는 촉매 개발이 필수적이다.
지구상에 존재하는 촉매 중 가장 높은 선택성을 보이는 촉매는 효소다. 효소는 천연 고분자인 단백질이 반응이 일어나는 활성점을 3차원적으로 둘러싸고 있는 구조를 갖는데, 단백질의 구조 및 활성점과의 상호작용에 따라 특정 반응물만 선택적으로 접근할 수 있도록 조절해 높은 선택성을 갖는다. 연구팀은 이번 연구에서 효소의 단백질과 유사한 고분자를 이용해 금속 활성점과의 상호작용을 조절한 새로운 개념의 촉매 설계 방법을 제시했다.
고분자는 일정 단위체의 반복적인 화학 결합을 통해 만들어지는 높은 분자량의 거대분자이며 합성에 사용한 단위체에 따라 고분자의 작용기를 쉽게 조절할 수 있다. 연구팀은 금속과 상호작용을 할 수 있는 작용기를 포함한 고분자를 합성하고 팔라듐 금속 입자를 포함한 촉매를 만들었다. 금속과 강하게 상호작용을 하는 고분자는 효소와 같이 금속 주위를 고분자가 3차원적으로 둘러싸는 형태를 보이는 한편 약하게 상호작용하는 고분자는 금속을 둘러싸지 못하고 금속 표면이 노출된 형태가 됐다.
연구팀은 이렇게 합성된 촉매를 이용해 석유화학의 에틸렌 생산 공정에서 매우 중요한 아세틸렌 부분 수소화 반응에 적용했다. 에틸렌은 플라스틱, 비닐, 접착제 등 다양한 제품을 만드는 데 이용하는 기본 핵심 원료이며 현재 우리나라에서는 주로 나프타를 분해하여 생산한다.
나프타분해시설에서 생산되는 에틸렌에는 불순물인 미량의 아세틸렌이 함께 포함돼 있는데, 이 아세틸렌이 화학 제품을 만드는 데 사용되는 촉매에 치명적으로 작용하기 때문에 수소화 반응을 통해 제거해 주는 공정이 필수적이다. 이 공정에서 핵심은 99% 이상의 에틸렌은 소모하지 않으면서 1% 미만의 아세틸렌만 선택적으로 제거하는 것이다.
연구진이 개발한 신규 촉매를 이 공정에 적용한 결과, 강하게 상호작용해 3차원 구조를 형성한 촉매는 고분자가 아세틸렌에만 접근해 높은 선택도를 보였다. 하지만 약한 상호작용으로 인해 고분자가 금속 표면을 덮지 못한 촉매에서는 아세틸렌과 에틸렌에 모두 접근해 낮은 선택도를 보였다.
또한 강하게 상호작용을 하는 고분자일수록 비활성화를 일으키는 탄소 침적물인 코크의 생성을 차단하고 금속 입자의 뭉침 현상을 억제해 장기간 반응에서도 높은 활성과 선택도를 유지했다.
연구를 주도한 최민기 교수는 "자연계 효소의 원리를 모방해 고분자와 금속 사이의 상호작용을 조절하고 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 가지는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념이다ˮ라며, "향후 높은 선택도가 필요한 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것이다ˮ라고 말했다.
우리 대학 생명화학공학과 현경림 박사과정 학생이 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `앙게반테 케미(Angewandte chemi)'에 지난 5월 17일 字 온라인판에 게재됐다. (논문명: Tailoring a Dynamic Metal-Polymer Interaction to Improve Catalyst Selectivity and Longevity in Hydrogenation),
한편 이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원을 받아 수행됐다.
2021.06.09
조회수 74561
-
 현장 진단형 초고속 실시간 유전자 분석기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 *나노 플라즈모닉 구조를 통해 빠른 열 순환 및 실시간 정량 분석이 가능한 초고속 실시간 중합효소연쇄반응(PCR) 기술을 개발했다고 7일 밝혔다.
☞ 나노 플라즈모닉 구조(Nanostructures for Plasmonic): 빛의 파장보다 작은 크기의 금속나노구조이며, 빛이 표면에 조사될 때 금속 표면과 유전체의 경계에서 빛과 전자가 상호작용을 한다. 주로 바이오 물질의 검출이나 분자진단에 많이 응용된다.
최근 코로나19를 포함한 전염성이 높은 바이러스의 확산을 방지하기 위해 신속하고 정확하게 바이러스를 검출하는 기술이 절실하게 필요하다. 역전사 중합효소연쇄반응(RT-PCR)은 가장 표준화된 코로나19 진단법으로 바이러스 내부의 유전물질인 RNA를 상보적 DNA로 역전사한 후 타겟 DNA를 증폭해 형광 프로브로 검출하는 방법이다. 그러나 기존 RT-PCR은 높은 민감도와 정확도를 갖추지만, 검출 시간이 길고 고가의 대형장비를 갖춘 장소로 검체를 운송한 후 진단하는 등 실시간 현장 대응의 한계가 존재한다.
연구팀이 개발한 `실시간 나노 플라즈모닉 PCR'은 백색 발광다이오드(LED)의 높은 광 흡수율을 갖는 나노 플라즈모닉 기판에 진공 설계된 미세 유체칩을 결합해 소량의 검체를 신속하게 증폭하고 정량적으로 분석해 바이러스를 단시간 내에 정확하게 검출할 수 있다. 이러한 특징을 이용해 공공장소 등 환자 발생 장소에서 병원성 바이러스의 확산 및 해외유입을 차단할 수 있을 것으로 기대된다.
나노 플라즈모닉 기판은 유리 나노기둥 위 금 나노섬 구조로 가시광선 전 영역에서 높은 광 흡수율을 가지므로 백색 LED의 빛을 열에너지로 치환해 빠르게 열을 발생시키고 내보낼 수 있다. 또한 광열 발생장치의 수직적인 온도 구배로 인한 증폭 효율 저하를 해결하기 위해 연구팀은 진공 설계된 미세 유체칩을 결합했다.
이는 샘플 한 방울을 칩에 넣으면 진공이 액체를 마이크로 챔버로 잡아당겨 자동으로 3분 이내에 주입되고, PCR 과정 동안에 발생하는 미세 기포는 공기 투과성 벽을 통해 제거돼 PCR 효율을 높이는 원리다.
연구팀은 SARS-CoV-2 플라스미드 DNA를 사용해 해당 기술을 검증했고, 40싸이클(95도-60도)을 5분 이내에 수행해 타겟 바이러스를 91%의 증폭 효율과 함께 정량적으로 검출했다. 이는 기존 실시간 PCR 시스템의 긴 소요 시간(약 1시간)에 비해 매우 빠르고, 높은 증폭 효율을 보이므로 신속한 현장 진단에 적용되기 적합할 것으로 보인다.
정기훈 교수는 "실질적으로 현장에서 사용 가능한 초고속 분자진단법을 개발했다ˮ며 "이 실시간 나노 플라즈모닉 PCR 기술은 현장에서 분자진단을 위한 차세대 유전자 증폭 플랫폼을 제공할 것이며 바이러스 확산 방지에 기여할 수 있을 것으로 예상한다ˮ라고 말했다.
우리 대학 바이오및뇌공학과 강병훈 박사과정이 주도한 이번 연구 결과는 국제 학술지 `에이씨에스 나노 (ACS Nano)'에 지난 5월 19일 字로 게재됐다. (논문명: Ultrafast and Real-time Nanoplasmonic On-Chip Polymerase Chain Reaction for Rapid and Quantitative Molecular Diagnostics)
한편 이번 연구는 KAIST 코로나19대응 과학기술뉴딜사업단과 한국연구재단 개인연구지원사업, 바이오기술개발사업으로 수행됐다.
현장 진단형 초고속 실시간 유전자 분석기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 *나노 플라즈모닉 구조를 통해 빠른 열 순환 및 실시간 정량 분석이 가능한 초고속 실시간 중합효소연쇄반응(PCR) 기술을 개발했다고 7일 밝혔다.
☞ 나노 플라즈모닉 구조(Nanostructures for Plasmonic): 빛의 파장보다 작은 크기의 금속나노구조이며, 빛이 표면에 조사될 때 금속 표면과 유전체의 경계에서 빛과 전자가 상호작용을 한다. 주로 바이오 물질의 검출이나 분자진단에 많이 응용된다.
최근 코로나19를 포함한 전염성이 높은 바이러스의 확산을 방지하기 위해 신속하고 정확하게 바이러스를 검출하는 기술이 절실하게 필요하다. 역전사 중합효소연쇄반응(RT-PCR)은 가장 표준화된 코로나19 진단법으로 바이러스 내부의 유전물질인 RNA를 상보적 DNA로 역전사한 후 타겟 DNA를 증폭해 형광 프로브로 검출하는 방법이다. 그러나 기존 RT-PCR은 높은 민감도와 정확도를 갖추지만, 검출 시간이 길고 고가의 대형장비를 갖춘 장소로 검체를 운송한 후 진단하는 등 실시간 현장 대응의 한계가 존재한다.
연구팀이 개발한 `실시간 나노 플라즈모닉 PCR'은 백색 발광다이오드(LED)의 높은 광 흡수율을 갖는 나노 플라즈모닉 기판에 진공 설계된 미세 유체칩을 결합해 소량의 검체를 신속하게 증폭하고 정량적으로 분석해 바이러스를 단시간 내에 정확하게 검출할 수 있다. 이러한 특징을 이용해 공공장소 등 환자 발생 장소에서 병원성 바이러스의 확산 및 해외유입을 차단할 수 있을 것으로 기대된다.
나노 플라즈모닉 기판은 유리 나노기둥 위 금 나노섬 구조로 가시광선 전 영역에서 높은 광 흡수율을 가지므로 백색 LED의 빛을 열에너지로 치환해 빠르게 열을 발생시키고 내보낼 수 있다. 또한 광열 발생장치의 수직적인 온도 구배로 인한 증폭 효율 저하를 해결하기 위해 연구팀은 진공 설계된 미세 유체칩을 결합했다.
이는 샘플 한 방울을 칩에 넣으면 진공이 액체를 마이크로 챔버로 잡아당겨 자동으로 3분 이내에 주입되고, PCR 과정 동안에 발생하는 미세 기포는 공기 투과성 벽을 통해 제거돼 PCR 효율을 높이는 원리다.
연구팀은 SARS-CoV-2 플라스미드 DNA를 사용해 해당 기술을 검증했고, 40싸이클(95도-60도)을 5분 이내에 수행해 타겟 바이러스를 91%의 증폭 효율과 함께 정량적으로 검출했다. 이는 기존 실시간 PCR 시스템의 긴 소요 시간(약 1시간)에 비해 매우 빠르고, 높은 증폭 효율을 보이므로 신속한 현장 진단에 적용되기 적합할 것으로 보인다.
정기훈 교수는 "실질적으로 현장에서 사용 가능한 초고속 분자진단법을 개발했다ˮ며 "이 실시간 나노 플라즈모닉 PCR 기술은 현장에서 분자진단을 위한 차세대 유전자 증폭 플랫폼을 제공할 것이며 바이러스 확산 방지에 기여할 수 있을 것으로 예상한다ˮ라고 말했다.
우리 대학 바이오및뇌공학과 강병훈 박사과정이 주도한 이번 연구 결과는 국제 학술지 `에이씨에스 나노 (ACS Nano)'에 지난 5월 19일 字로 게재됐다. (논문명: Ultrafast and Real-time Nanoplasmonic On-Chip Polymerase Chain Reaction for Rapid and Quantitative Molecular Diagnostics)
한편 이번 연구는 KAIST 코로나19대응 과학기술뉴딜사업단과 한국연구재단 개인연구지원사업, 바이오기술개발사업으로 수행됐다.
2021.06.07
조회수 47104
-
 알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28
조회수 26924
-
 자연계 효소처럼 작동하는 신개념 산업용 촉매 개발
우리 대학 연구진이 생체 내 단백질 *촉매인 *효소를 모방해 공급자 또는 개발자가 원하는 화학반응만 선택적으로 유도하되 안정성도 갖춘 기존에 없는 새로운 개념의 산업용 촉매 개발에 성공했다.
☞ 촉매(catalyst): 자신은 변하지 않으면서 물질 간의 화학반응이 잘 일어나도록 돕는 물질. 표면에 흡착된 반응물을 생성물로 빠르게 전환해주는 역할을 한다.
☞ 효소(enzyme): 생체 내의 화학반응을 매개하는 단백질 촉매. 반응물을 전환할 수 있는 금속 촉매 활성점(active site)이 부드러운 유기 고분자인 단백질로 둘러싸인 형태를 지니고 있는데, 단백질의 구조에 따라 오직 원하는 반응물만이 활성점에 접근해 생성물로 전환될 수 있다.
생명화학공학과 최민기, 화학과 김형준 교수 공동연구팀은 실생활에 흔히 쓰이는 플라스틱, 비닐 등의 재료인 화학 원료를 만들 때, 자연계 효소와 동일한 원리로 반응물을 선택적으로 전환할 수 있는 고성능 산업용 촉매를 개발하는 데 성공했다.
한정된 자원을 효율적으로 이용하기 위해서는 다양한 화학반응 경로 중 목표하는 반응물을 원하는 생성물로 선택적으로 전환해줄 수 있는 촉매를 디자인하는 것이 매우 중요하다. 지구상에 존재하는 촉매 중 가장 효율이 좋은 촉매는 자연계 및 우리 몸 등에 존재하는 '효소'다.
이와 달리 석유화학 산업에서 이용되는 촉매들은 알루미나·실리카·제올라이트와 같이 딱딱한 무기물 표면 위에 금속을 퍼뜨려 노출한 구조로 구성돼 있다. 이런 형태의 촉매에서는 금속 표면에 모든 반응물이 흡착되기 쉬워 특정 반응물만을 선택적으로 생성물로 전환하기에는 한계가 있다. 그 럼에도 불구하고 대부분 산업용 촉매 설계에서 무기 소재를 사용하는 이유는 이들이 열화학적 안정성이 뛰어나 다양한 반응 조건에서도 촉매가 안정적으로 작용하기 때문이다.
최민기·김형준 교수 공동연구팀은 이번 연구를 통해 단백질과 같이 부드럽고 유동성이 있으면서도 매우 높은 열화학적 안정성을 지닌 `폴리페닐렌설파이드(polyphenylene sulfide, PPS)'라는 엔지니어링 플라스틱 물질을 이용해서 고분자 막이 금속촉매 활성점을 감싼 형태의 신개념 촉매를 세계 최초로 개발했다. PPS는 내열성과 내화학성이 매우 뛰어나 자동차나 항공우주 산업 등에서 많이 사용되는 상용 고분자다.
연구팀은 이 새로운 촉매를 이용해 석유화학의 에틸렌 생산 공정 중 매우 중요한 아세틸렌 수소화 반응에 적용하는 데 성공했다. 우리나라 석유화학 산업의 원료는 90% 이상이 *나프타인데, 나프타분해시설(Naphtha Cracking Center, NCC)에서 이를 분해해 에틸렌 및 기타 기초유분들을 생산하고 있다. 특히 에틸렌은 주변에 흔한 플라스틱, 비닐, 접착제, 페인트까지 일상에서 사용하는 다양한 제품을 만드는데 이용하는 기본 핵심 화학 원료다.
☞ 나프타(naphtha): 원유를 증류할 때, 35~220℃의 끓는점 범위에서 유출되는 탄화수소의 혼합체이다. 중질 가솔린이라고도 부른다.
나프타를 분해할 때 생산되는 에틸렌에는 미량의 아세틸렌이 불순물로 함께 포함돼 있다. 아세틸렌은 추후 에틸렌을 이용해 화학제품을 만드는 데 매우 치명적이므로 미량의 아세틸렌을 수소화 반응으로 제거해 주는 공정을 반드시 거쳐야 한다. 그런데 이 공정은 99% 이상 에틸렌은 건들지 않으면서도, 1% 미만의 아세틸렌만 선택적으로 전환해야 하는 난제가 존재해왔다.
공동연구팀은 새로 개발한 촉매를 이 공정에 적용한 결과 1% 미만의 아세틸렌은 금속 입자를 둘러싸고 있는 고분자막을 투과해 쉽게 전환되는 대신 99% 이상의 에틸렌은 고분자막에 가로막혀 촉매 반응이 진행되지 않아서 기존 팔라듐(Pd) 촉매와 비교할 때 선택도는 2 배 이상, 안정성은 10배 이상 증진된 놀라운 결과를 얻었다.
우리 대학 생명화학공학과 이송현, 화학과 신승재 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스(Science Advances)' 7월 8일 字 온라인판에 게재됐다(논문명: Dynamic Metal-Polymer Interaction for the Design of Chemoselective and Long-Lived Hydrogenation Catalysts).
최민기 교수는 "자연계의 효소를 모방해 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 갖는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념"이라면서 "향후 높은 선택도가 있어야 하는 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것"이라고 전망했다.
이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원으로 이뤄졌다.
자연계 효소처럼 작동하는 신개념 산업용 촉매 개발
우리 대학 연구진이 생체 내 단백질 *촉매인 *효소를 모방해 공급자 또는 개발자가 원하는 화학반응만 선택적으로 유도하되 안정성도 갖춘 기존에 없는 새로운 개념의 산업용 촉매 개발에 성공했다.
☞ 촉매(catalyst): 자신은 변하지 않으면서 물질 간의 화학반응이 잘 일어나도록 돕는 물질. 표면에 흡착된 반응물을 생성물로 빠르게 전환해주는 역할을 한다.
☞ 효소(enzyme): 생체 내의 화학반응을 매개하는 단백질 촉매. 반응물을 전환할 수 있는 금속 촉매 활성점(active site)이 부드러운 유기 고분자인 단백질로 둘러싸인 형태를 지니고 있는데, 단백질의 구조에 따라 오직 원하는 반응물만이 활성점에 접근해 생성물로 전환될 수 있다.
생명화학공학과 최민기, 화학과 김형준 교수 공동연구팀은 실생활에 흔히 쓰이는 플라스틱, 비닐 등의 재료인 화학 원료를 만들 때, 자연계 효소와 동일한 원리로 반응물을 선택적으로 전환할 수 있는 고성능 산업용 촉매를 개발하는 데 성공했다.
한정된 자원을 효율적으로 이용하기 위해서는 다양한 화학반응 경로 중 목표하는 반응물을 원하는 생성물로 선택적으로 전환해줄 수 있는 촉매를 디자인하는 것이 매우 중요하다. 지구상에 존재하는 촉매 중 가장 효율이 좋은 촉매는 자연계 및 우리 몸 등에 존재하는 '효소'다.
이와 달리 석유화학 산업에서 이용되는 촉매들은 알루미나·실리카·제올라이트와 같이 딱딱한 무기물 표면 위에 금속을 퍼뜨려 노출한 구조로 구성돼 있다. 이런 형태의 촉매에서는 금속 표면에 모든 반응물이 흡착되기 쉬워 특정 반응물만을 선택적으로 생성물로 전환하기에는 한계가 있다. 그 럼에도 불구하고 대부분 산업용 촉매 설계에서 무기 소재를 사용하는 이유는 이들이 열화학적 안정성이 뛰어나 다양한 반응 조건에서도 촉매가 안정적으로 작용하기 때문이다.
최민기·김형준 교수 공동연구팀은 이번 연구를 통해 단백질과 같이 부드럽고 유동성이 있으면서도 매우 높은 열화학적 안정성을 지닌 `폴리페닐렌설파이드(polyphenylene sulfide, PPS)'라는 엔지니어링 플라스틱 물질을 이용해서 고분자 막이 금속촉매 활성점을 감싼 형태의 신개념 촉매를 세계 최초로 개발했다. PPS는 내열성과 내화학성이 매우 뛰어나 자동차나 항공우주 산업 등에서 많이 사용되는 상용 고분자다.
연구팀은 이 새로운 촉매를 이용해 석유화학의 에틸렌 생산 공정 중 매우 중요한 아세틸렌 수소화 반응에 적용하는 데 성공했다. 우리나라 석유화학 산업의 원료는 90% 이상이 *나프타인데, 나프타분해시설(Naphtha Cracking Center, NCC)에서 이를 분해해 에틸렌 및 기타 기초유분들을 생산하고 있다. 특히 에틸렌은 주변에 흔한 플라스틱, 비닐, 접착제, 페인트까지 일상에서 사용하는 다양한 제품을 만드는데 이용하는 기본 핵심 화학 원료다.
☞ 나프타(naphtha): 원유를 증류할 때, 35~220℃의 끓는점 범위에서 유출되는 탄화수소의 혼합체이다. 중질 가솔린이라고도 부른다.
나프타를 분해할 때 생산되는 에틸렌에는 미량의 아세틸렌이 불순물로 함께 포함돼 있다. 아세틸렌은 추후 에틸렌을 이용해 화학제품을 만드는 데 매우 치명적이므로 미량의 아세틸렌을 수소화 반응으로 제거해 주는 공정을 반드시 거쳐야 한다. 그런데 이 공정은 99% 이상 에틸렌은 건들지 않으면서도, 1% 미만의 아세틸렌만 선택적으로 전환해야 하는 난제가 존재해왔다.
공동연구팀은 새로 개발한 촉매를 이 공정에 적용한 결과 1% 미만의 아세틸렌은 금속 입자를 둘러싸고 있는 고분자막을 투과해 쉽게 전환되는 대신 99% 이상의 에틸렌은 고분자막에 가로막혀 촉매 반응이 진행되지 않아서 기존 팔라듐(Pd) 촉매와 비교할 때 선택도는 2 배 이상, 안정성은 10배 이상 증진된 놀라운 결과를 얻었다.
우리 대학 생명화학공학과 이송현, 화학과 신승재 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스(Science Advances)' 7월 8일 字 온라인판에 게재됐다(논문명: Dynamic Metal-Polymer Interaction for the Design of Chemoselective and Long-Lived Hydrogenation Catalysts).
최민기 교수는 "자연계의 효소를 모방해 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 갖는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념"이라면서 "향후 높은 선택도가 있어야 하는 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것"이라고 전망했다.
이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원으로 이뤄졌다.
2020.07.31
조회수 43351
 AI 기반 효소 발굴하여 새로운 미생물 설계 가능
효소는 세포 내에서 일어나는 생화학적 반응을 촉매하는 단백질로, 세포의 대사 과정에서 핵심적인 역할을 수행한다. 이에 따라 새로운 효소의 기능을 규명하는 것은 미생물 세포공장 구축에서 핵심적인 과제다.
KAIST 연구진이 인공지능(AI)을 활용해 자연에 존재하지 않는 새로운 효소를 설계함으로써, 미생물 세포공장 구축을 가속화하고 신약·바이오 연료 등 차세대 바이오산업의 개발 가능성을 크게 높였다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 AI를 활용한 효소 기능 예측 기술의 발전 과정과 최신 동향을 정리하고, AI가 새로운 효소를 찾고 설계하는데 어떤 역할을 해왔는지 분석하여 ‘인공지능을 이용한 효소 기능 분류’를 발표했다.
이상엽 특훈교수 연구팀은 이번 연구에서 머신러닝(Machine learning)과 딥러닝(Deep learning)을 활용한 효소 기능 예측 기술의 발전 과정을 체계적으로 정리·분석하여 제공했다.
초기의 서열 유사성 기반 예측 기법에서부터 합성곱 신경망, 순환 신경망, 그래프 신경망, 그리고 트랜스포머(Transformer) 기반 대규모 언어 모델까지 다양한 AI 기법이 효소 기능 예측 연구에 접목된 사례를 다루며, 이들 기술이 단백질 서열에서 의미 있는 정보를 어떻게 추출하고, 예측 성능을 극대화하는지를 분석했다.
특히, 딥러닝 기술을 활용한 효소 기능 예측은 단순한 서열 유사성 분석을 넘어, 구조적·진화적 정보 등 아미노산 서열에 내재된 효소의 촉매 기능과 관련된 중요한 특성을 자동으로 추출함으로써 보다 정밀한 예측이 가능하다는 점이 강조됐다.
이는 기존의 생명정보학적 접근법과 비교해 인공지능 모델이 가지는 차별성과 장점을 부각하는 중요한 부분이다.
또한, 생성형 인공지능 모델의 발전에 기반하여, 기존 효소 기능 예측을 넘어 자연계에 존재하지 않는 새로운 기능을 가진 효소를 생성하는 기술이 미래 연구 방향이 될 것으로 제시했다. 이러한 AI 기반 효소 예측 및 설계 기술의 지속적인 발전은 향후 바이오 산업과 생명공학 연구의 방향성에 큰 변화를 가져올 것으로 전망했다.
공동 제 1저자인 생명화학공학과 김하림 박사과정생은 “AI 기반 효소 기능 예측 및 효소 설계는 대사공학, 합성 생물학 및 헬스케어 등 다양한 분야에서 매우 중요”하다고 말했다.
이상엽 특훈교수는“AI 활용 효소 기능 예측은 다양한 생물학적 문제 해결에 효과적으로 적용될 수 있는 가능성을 보여주며 바이오 분야 전반의 연구를 가속화하는 데 크게 기여할 것.”이라고 밝혔다.
해당 논문은 셀(Cell) 誌가 발행하는 생명공학 분야 권위 저널인 `생명공학 동향(Trends in Biotechnology)'에 3월 28일자 게재됐다.
※ 논문명 : Enzyme Functional Classification Using Artificial Intelligence doi.org/10.1016/j.tibtech.2025.03.003
※ 저자 정보 : 김하림(한국과학기술원, 공동 제1 저자), 지홍근(한국과학기술원, 공동 제1 저자), 김기배(한국과학기술원, 제3 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유 대체 친환경 화학기술 개발 사업의‘바이오 제조 산업 선도를 위한 첨단 합성 생물학 원천기술 개발’, 그리고 과기정통부와 보건복지부가 지원하는 ‘딥러닝 기반 합성 생물학을 이용한 혁신구조 항생제 개발’ 과제의 지원을 받아 수행됐다.
2025.04.17 조회수 4512
AI 기반 효소 발굴하여 새로운 미생물 설계 가능
효소는 세포 내에서 일어나는 생화학적 반응을 촉매하는 단백질로, 세포의 대사 과정에서 핵심적인 역할을 수행한다. 이에 따라 새로운 효소의 기능을 규명하는 것은 미생물 세포공장 구축에서 핵심적인 과제다.
KAIST 연구진이 인공지능(AI)을 활용해 자연에 존재하지 않는 새로운 효소를 설계함으로써, 미생물 세포공장 구축을 가속화하고 신약·바이오 연료 등 차세대 바이오산업의 개발 가능성을 크게 높였다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 AI를 활용한 효소 기능 예측 기술의 발전 과정과 최신 동향을 정리하고, AI가 새로운 효소를 찾고 설계하는데 어떤 역할을 해왔는지 분석하여 ‘인공지능을 이용한 효소 기능 분류’를 발표했다.
이상엽 특훈교수 연구팀은 이번 연구에서 머신러닝(Machine learning)과 딥러닝(Deep learning)을 활용한 효소 기능 예측 기술의 발전 과정을 체계적으로 정리·분석하여 제공했다.
초기의 서열 유사성 기반 예측 기법에서부터 합성곱 신경망, 순환 신경망, 그래프 신경망, 그리고 트랜스포머(Transformer) 기반 대규모 언어 모델까지 다양한 AI 기법이 효소 기능 예측 연구에 접목된 사례를 다루며, 이들 기술이 단백질 서열에서 의미 있는 정보를 어떻게 추출하고, 예측 성능을 극대화하는지를 분석했다.
특히, 딥러닝 기술을 활용한 효소 기능 예측은 단순한 서열 유사성 분석을 넘어, 구조적·진화적 정보 등 아미노산 서열에 내재된 효소의 촉매 기능과 관련된 중요한 특성을 자동으로 추출함으로써 보다 정밀한 예측이 가능하다는 점이 강조됐다.
이는 기존의 생명정보학적 접근법과 비교해 인공지능 모델이 가지는 차별성과 장점을 부각하는 중요한 부분이다.
또한, 생성형 인공지능 모델의 발전에 기반하여, 기존 효소 기능 예측을 넘어 자연계에 존재하지 않는 새로운 기능을 가진 효소를 생성하는 기술이 미래 연구 방향이 될 것으로 제시했다. 이러한 AI 기반 효소 예측 및 설계 기술의 지속적인 발전은 향후 바이오 산업과 생명공학 연구의 방향성에 큰 변화를 가져올 것으로 전망했다.
공동 제 1저자인 생명화학공학과 김하림 박사과정생은 “AI 기반 효소 기능 예측 및 효소 설계는 대사공학, 합성 생물학 및 헬스케어 등 다양한 분야에서 매우 중요”하다고 말했다.
이상엽 특훈교수는“AI 활용 효소 기능 예측은 다양한 생물학적 문제 해결에 효과적으로 적용될 수 있는 가능성을 보여주며 바이오 분야 전반의 연구를 가속화하는 데 크게 기여할 것.”이라고 밝혔다.
해당 논문은 셀(Cell) 誌가 발행하는 생명공학 분야 권위 저널인 `생명공학 동향(Trends in Biotechnology)'에 3월 28일자 게재됐다.
※ 논문명 : Enzyme Functional Classification Using Artificial Intelligence doi.org/10.1016/j.tibtech.2025.03.003
※ 저자 정보 : 김하림(한국과학기술원, 공동 제1 저자), 지홍근(한국과학기술원, 공동 제1 저자), 김기배(한국과학기술원, 제3 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유 대체 친환경 화학기술 개발 사업의‘바이오 제조 산업 선도를 위한 첨단 합성 생물학 원천기술 개발’, 그리고 과기정통부와 보건복지부가 지원하는 ‘딥러닝 기반 합성 생물학을 이용한 혁신구조 항생제 개발’ 과제의 지원을 받아 수행됐다.
2025.04.17 조회수 4512 암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22 조회수 4448
암 발생 현상 등 유전자 발현 조절 원리 규명
다양한 암 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포의 활성화 과정 등을 근본적으로 일으키는 유전자 발현 조절 단백질의 핵심 유전자 발현 네트워크를 발견했다. 우리 연구진은 이 발견을 기초로 하여 혁신적인 치료 기술 개발에 활용 가능성을 높였다.
우리 대학 생명과학과 김세윤 교수, 이광록 교수, 조원기 교수 공동연구팀이 동물 세포의 유전자 발현을 조절하는 핵심적인 원리를 규명했다고 22일 밝혔다.
이노시톨 대사 효소에 의해 만들어지는 이노시톨 인산 대사체는 진핵 세포의 신호전달 시스템에 필요한 다양한 이차 신호전달물질로 작용하며 암, 비만, 당뇨, 신경계 질환들에 폭넓게 관여한다.
연구팀은 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자로 작용함을 규명했다.
포도당과 유사한 영양소로 알려진 이노시톨의 대사 반응에 핵심적으로 작용하는 효소인 IPMK 단백질(inositol polyphosphate multikinase)은 유전자 발현을 직접적으로 조절하는 기능을 가지고 있다. 특히 IPMK 효소는 동물 세포의 대표적인 전사 인자(transcription factor)인 혈청 반응 인자(serum response factor, 이하 SRF)에 의한 유전자 전사 과정에 중요하다고 보고된 바 있으나 작용하는 기전에 대하여 알려진 바는 없었다.
SRF 전사 인자는 최소 200~300여 개의 유전자 발현을 직접적으로 조절하는 단백질로서, 동물 세포의 성장과 증식, 세포 사멸, 세포의 이동성 등을 조절하며 심장과 같은 장기 발생에 필수적이다.
연구팀은 IPMK 단백질이 SRF 전사 인자와 직접적으로 결합한다는 사실을 발견하고 이를 통해 SRF 전사 인자의 3차원적 단백질 구조를 변화시킨다는 것을 밝혔다.
연구팀은 IPMK 효소에 의하여 활성화된 SRF 전사 인자를 통해 다양한 유전자들의 전사 과정이 촉진된다는 것을 밝혔다. 즉, IPMK 단백질은 SRF 전사 인자의 단백질 활성을 높이는 데 반드시 필요한 조절 스위치와 같은 역할을 수행하는 것임을 연구팀은 규명했다.
연구팀은 IPMK 효소와 SRF 전사 인자 사이의 직접적인 결합에 문제가 발생할 경우, SRF 전사 인자의 기능과 활성이 낮아져 유전자 발현에 심각한 장애가 발생한다는 점을 최종적으로 검증하였다.
특히 SRF 전사 인자가 가지고 있는 비정형 영역(Intrinsically disordered region, IDR)이 중요한 조절 부위라는 점을 밝힘으로써 비정형 단백질의 생물학적 중요성을 제시했다. 보통 단백질은 접힘을 통해 고유의 구조를 나타내지만 비정형 영역을 포함하게 되는 경우에는 특정한 단백질 구조가 관찰되지 않는다. 학계에서는 이러한 비정형 영역을 가지고 있는 단백질들을 비정형 단백질이라고 구분하고 어떠한 기능을 수행하는지 주목하고 있다.
김세윤 교수는 “이번 연구는 이노시톨 대사 시스템의 핵심 효소인 IPMK 단백질이 동물 세포의 핵심 유전자 발현 네트워크의 중요한 전사 활성화 인자이며 이를 증명하는 핵심 메커니즘을 제시한 중요한 발견”이라며, “SRF 전사 인자로부터 파생되는 다양한 암의 발생과 암전이 현상, 줄기세포로부터의 조직 분화 및 발생, 신경 세포 활성화 과정 등을 근본적으로 이해함으로써 혁신적인 치료 기술 개발 등에 폭넓게 활용되기를 바란다”라는 기대를 전했다.
이 연구는 세계적 국제학술지 ‘핵산 연구 (Nucleic Acids Research)’ (IF=16.7, 생화학 및 분자생물학 분야 상위 1.8%) 온라인판에 1월 7일 게재됐다. (논문명 : Single-molecule analysis reveals that IPMK enhances the DNA-binding activity of the transcription factor SRF) (doi: 10.1093/nar/gkae1281)
한편 이번 연구는 한국연구재단의 중견연구사업, 선도연구센터 지원사업, 글로벌 기초연구실 지원사업과 서경배과학재단, 삼성미래기술육성사업의 지원을 받아 수행됐다.
2025.01.22 조회수 4448 숨겨진 효소 쏙쏙 찾아내는 인공지능 개발
대장균은 가장 많이 연구된 생명체 중 하나에 해당되지만 아직 대장균을 구성한 단백질 30%의 기능에 대해 명확하게 밝혀지지 않았다. 이에 대해 인공지능을 활용하여 아직 명확하게 밝혀진 바 없던 단백질에서 464종의 효소를 발견하였으며, 이 중 3종의 단백질의 예측된 기능을 시험관 내 효소 분석 방법을 통해 검증하는데 성공하였다.
우리 대학 생명화학공학과 이상엽 특훈교수와 캘리포니아대학교 샌디에이고(UCSD) 생명공학과 버나드 펄슨(Bernhard Palsson) 교수 공동연구팀이 단백질 서열을 활용, 해당 단백질의 효소 기능을 예측할 수 있는 인공지능, `딥 EC 트랜스포머(DeepECtransformer)'를 개발해 빠르고 정확하게 효소 기능을 파악할 수 있는 예측 시스템을 구축했다고 24일 밝혔다.
효소는 생물학적 반응을 촉매하는 단백질로서, 생명체 내 존재하는 다양한 화학 반응과 이에 따라 결정되는 생명체의 대사 특성을 파악하기 위해서는 각 효소의 기능을 이해하는 것이 필수적이다. EC 번호(효소 고유 번호, Enzyme Commission number)는 국제생화학 및 분자 생물학연맹 (International Union of Biochemistry and Molecular Biology, IUBMB)가 고안한 효소 기능 분류 체계로서, 다양한 유기체의 대사 특성을 이해하기 위해선 게놈 서열에서 존재하는 효소의 종류와 EC 번호를 빠르게 분석할 수 있는 기술 개발이 필요하다.
단백질의 기능 및 효소 기능 예측을 위해 인공지능을 활용하는 다양한 예측 시스템 또한 보고됐지만, 인공지능의 추론 과정을 직접 확인할 수 없는 블랙박스(black box)의 특징을 가졌거나, 효소 서열 내 아미노산 잔기(최소 단위) 수준으로 해석하지 못하는 문제가 있었다.
공동연구팀은 심층학습 기법과 단백질 상동성 분석 모듈을 활용해 주어진 단백질 서열의 효소 기능을 예측하는 인공지능 딥 EC 트랜스포머(DeepECtransformer)를 개발했다. 연구팀은 이번 연구에서 더 다양한 효소 기능을 정확하게 예측할 수 있도록 단백질 서열 전체 문맥에서 효소 기능에 중요한 정보를 추출하였고, 이를 통해 효소의 EC 번호를 정확하게 예측할 수 있었다. 개발된 인공지능은 총 5,360종류의 EC 번호를 예측할 수 있었다.
공동연구팀은 나아가 딥 EC 트랜스포머의 인공신경망 내 정보 흐름을 분석하여 인공지능이 추론 과정에서 효소 기능에 중요한 활성 부위나 보조 인자 결합 부위 정보를 활용하고 있음을 밝혀냈다. 이처럼 인공지능의 블랙박스를 해석함으로써 인공지능이 학습 과정에서 스스로 효소 기능에 중요한 특징을 파악하고 있음을 연구팀은 확인했다.
이번 논문의 제1 저자인 우리 대학 김기배 박사과정생은 “이번에 개발한 예측 시스템을 활용해 아직 밝혀진 적 없던 효소의 기능을 새롭게 예측하고 실험으로 검증할 수 있었다”고 말했다. 그는 또한 “딥 EC 트랜스포머를 활용해 생명체 내 밝혀지지 않았던 효소를 파악함으로써 유용 화합물을 생합성하기 위해 필요한 효소나 플라스틱을 생분해하기 위해 필요한 효소 등 다양한 대사 과정을 새롭게 밝혀낼 수 있을 것”이라고 덧붙였다.
또한 이상엽 특훈교수는 “효소 기능을 빠르고 정확하게 예측하는 딥 EC 트랜스포머는 기능 유전체학의 핵심 기술로서 시스템 수준에서 전체 효소들의 기능들을 분석할 수 있게 한다”며 “이를 활용해 모든 효소 정보를 포함한 대사 네트워크를 기반으로 친환경 미생물 공장 개발을 수행할 수 있을 것”이라고 밝혔다.
생명화학공학과 김기배 박사과정이 참여한 이번 논문은 국제 학술지 네이처(Nature) 誌가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 동료 심사를 거쳐 11월 14일 字 게재됐다.
※ 논문명 : 트랜스포머 레이어와 딥러닝을 사용하여 효소 인코딩 유전자의 기능적 주석 달기 (Functional annotation of enzyme-encoding genes using deep learning with transformer layers)
※ 저자 정보 : 김기배 (한국과학기술원, 제1 저자), 김지연 (한국과학기술원, 제2 저자), 이종언 (한국과학기술원, 제3 저자), Charles J. Norsigian (UCSD, 제4 저자), Bernhard O. Palsson (UCSD, 제5 저자) 및 이상엽(한국과학기술원, 교신저자) 포함 총 6 명
한편, 이번 연구는 과기정통부가 지원하는 ‘석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
2023.11.24 조회수 8725
숨겨진 효소 쏙쏙 찾아내는 인공지능 개발
대장균은 가장 많이 연구된 생명체 중 하나에 해당되지만 아직 대장균을 구성한 단백질 30%의 기능에 대해 명확하게 밝혀지지 않았다. 이에 대해 인공지능을 활용하여 아직 명확하게 밝혀진 바 없던 단백질에서 464종의 효소를 발견하였으며, 이 중 3종의 단백질의 예측된 기능을 시험관 내 효소 분석 방법을 통해 검증하는데 성공하였다.
우리 대학 생명화학공학과 이상엽 특훈교수와 캘리포니아대학교 샌디에이고(UCSD) 생명공학과 버나드 펄슨(Bernhard Palsson) 교수 공동연구팀이 단백질 서열을 활용, 해당 단백질의 효소 기능을 예측할 수 있는 인공지능, `딥 EC 트랜스포머(DeepECtransformer)'를 개발해 빠르고 정확하게 효소 기능을 파악할 수 있는 예측 시스템을 구축했다고 24일 밝혔다.
효소는 생물학적 반응을 촉매하는 단백질로서, 생명체 내 존재하는 다양한 화학 반응과 이에 따라 결정되는 생명체의 대사 특성을 파악하기 위해서는 각 효소의 기능을 이해하는 것이 필수적이다. EC 번호(효소 고유 번호, Enzyme Commission number)는 국제생화학 및 분자 생물학연맹 (International Union of Biochemistry and Molecular Biology, IUBMB)가 고안한 효소 기능 분류 체계로서, 다양한 유기체의 대사 특성을 이해하기 위해선 게놈 서열에서 존재하는 효소의 종류와 EC 번호를 빠르게 분석할 수 있는 기술 개발이 필요하다.
단백질의 기능 및 효소 기능 예측을 위해 인공지능을 활용하는 다양한 예측 시스템 또한 보고됐지만, 인공지능의 추론 과정을 직접 확인할 수 없는 블랙박스(black box)의 특징을 가졌거나, 효소 서열 내 아미노산 잔기(최소 단위) 수준으로 해석하지 못하는 문제가 있었다.
공동연구팀은 심층학습 기법과 단백질 상동성 분석 모듈을 활용해 주어진 단백질 서열의 효소 기능을 예측하는 인공지능 딥 EC 트랜스포머(DeepECtransformer)를 개발했다. 연구팀은 이번 연구에서 더 다양한 효소 기능을 정확하게 예측할 수 있도록 단백질 서열 전체 문맥에서 효소 기능에 중요한 정보를 추출하였고, 이를 통해 효소의 EC 번호를 정확하게 예측할 수 있었다. 개발된 인공지능은 총 5,360종류의 EC 번호를 예측할 수 있었다.
공동연구팀은 나아가 딥 EC 트랜스포머의 인공신경망 내 정보 흐름을 분석하여 인공지능이 추론 과정에서 효소 기능에 중요한 활성 부위나 보조 인자 결합 부위 정보를 활용하고 있음을 밝혀냈다. 이처럼 인공지능의 블랙박스를 해석함으로써 인공지능이 학습 과정에서 스스로 효소 기능에 중요한 특징을 파악하고 있음을 연구팀은 확인했다.
이번 논문의 제1 저자인 우리 대학 김기배 박사과정생은 “이번에 개발한 예측 시스템을 활용해 아직 밝혀진 적 없던 효소의 기능을 새롭게 예측하고 실험으로 검증할 수 있었다”고 말했다. 그는 또한 “딥 EC 트랜스포머를 활용해 생명체 내 밝혀지지 않았던 효소를 파악함으로써 유용 화합물을 생합성하기 위해 필요한 효소나 플라스틱을 생분해하기 위해 필요한 효소 등 다양한 대사 과정을 새롭게 밝혀낼 수 있을 것”이라고 덧붙였다.
또한 이상엽 특훈교수는 “효소 기능을 빠르고 정확하게 예측하는 딥 EC 트랜스포머는 기능 유전체학의 핵심 기술로서 시스템 수준에서 전체 효소들의 기능들을 분석할 수 있게 한다”며 “이를 활용해 모든 효소 정보를 포함한 대사 네트워크를 기반으로 친환경 미생물 공장 개발을 수행할 수 있을 것”이라고 밝혔다.
생명화학공학과 김기배 박사과정이 참여한 이번 논문은 국제 학술지 네이처(Nature) 誌가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 동료 심사를 거쳐 11월 14일 字 게재됐다.
※ 논문명 : 트랜스포머 레이어와 딥러닝을 사용하여 효소 인코딩 유전자의 기능적 주석 달기 (Functional annotation of enzyme-encoding genes using deep learning with transformer layers)
※ 저자 정보 : 김기배 (한국과학기술원, 제1 저자), 김지연 (한국과학기술원, 제2 저자), 이종언 (한국과학기술원, 제3 저자), Charles J. Norsigian (UCSD, 제4 저자), Bernhard O. Palsson (UCSD, 제5 저자) 및 이상엽(한국과학기술원, 교신저자) 포함 총 6 명
한편, 이번 연구는 과기정통부가 지원하는 ‘석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
2023.11.24 조회수 8725 김학성 명예교수, 2023 효소공학상 수상
우리 대학 생명과학과 김학성 명예교수가 2023년 효소 공학상(Enzyme Engineering Award) 수상자로 선정됐다고 24일 밝혔다. 본 상은 효소공학(Enzyme Engineering) 분야 최고 권위 국제학회 상으로 2년마다 개최되는 국제 효소공학 학회(Enzyme Engineering Conference)에서 수여된다. 시상식은 오는 10월 1일부터 6일까지 싱가포르에서 개최되는 제27차 학회에서 수상 강연과 함께 진행된다.
효소(Enzyme)는 반응 특이성과 효율이 매우 높은 단백질의 일종으로 생체 내에서 생명 현상을 유지하는 데 가장 중요한 역할을 수행하는데, 예를 들면 유전자 복제, 신호전달, 대사, 단백질 합성 등 다양한 과정에 필수적으로 작용한다. 산업적으로 효소는 의약품 및 정밀/범용 화학제품 생산에 사용되고 있으며 최근에는 환경오염과 지구 온난화를 해결하고자 효소 기반 공정 개발 연구가 전 세계적으로 진행되고 있다.
그러나, 자연계에 존재하는 수많은 종류의 효소는 생체 내 반응에 적합하도록 진화되었기 때문에 이를 실제 산업적으로 사용하는 데 많은 제약이 있다. 이를 해결하고자 생명공학, 화학기업, 대학과 연구소에서 응용 목적에 맞는 효소 개발에 집중하고 있다.
김학성 교수는 지난 30여 년 동안 구조 기반 설계, 방향적 진화 및 컴퓨터 기반 설계를 통해 목적에 맞는 기능을 갖는 효소를 효율적으로 창출할 수 있는 기반 기술을 성공적으로 개발했다. 김 교수팀이 개발한 기반 기술은 산업용 효소, 단백질 신약, 합성 생물학, 바이오 화학, 생유기 합성 분야에서 광범위하게 활용될 수 있는 원천 기반 기술이다.
김 교수는 일련의 연구를 세계 최고 학술지인 ‘사이언스(Science)’를 비롯한 ‘네이쳐 케미컬 바이올로지(Nature Chemical Biology)’, ‘네이쳐 커뮤니케이션즈(Nature Communications)’, ‘앙게반테 케미(Angewandte Chemi.)’, ‘어드밴스드 사이언스(Advanced Science)’ 등의 저명 학술지에 발표하였고 60편의 특허를 등록하는 등 국제적으로 괄목할 업적을 이뤘다. 또한, 효소를 이용한 정밀화학 및 의약품 생산 기술을 산업체에 기술 이전 하여 관련 산업 발전에 크게 기여했다.
김학성 교수는 이러한 공로를 인정받아 관련분야의 최고 권위 국제 학회상인 ‘효소 공학상(Enzyme Engineering Award)’ 수상자로 선정됐다.
상을 수상한 김학성 교수는 “연구실 실적이 국제적으로 인정받아 권위 있는 상을 받게 되어 매우 영광이고, 연구실 졸업생들과 재정적 지원을 해주신 기관에 감사를 드린다. 앞으로 다양한 분야에서 효소의 산업적 응용을 확대시키는데 노력을 할 것이다”라고 수상 소감을 밝혔다.
2023.08.24 조회수 5757
김학성 명예교수, 2023 효소공학상 수상
우리 대학 생명과학과 김학성 명예교수가 2023년 효소 공학상(Enzyme Engineering Award) 수상자로 선정됐다고 24일 밝혔다. 본 상은 효소공학(Enzyme Engineering) 분야 최고 권위 국제학회 상으로 2년마다 개최되는 국제 효소공학 학회(Enzyme Engineering Conference)에서 수여된다. 시상식은 오는 10월 1일부터 6일까지 싱가포르에서 개최되는 제27차 학회에서 수상 강연과 함께 진행된다.
효소(Enzyme)는 반응 특이성과 효율이 매우 높은 단백질의 일종으로 생체 내에서 생명 현상을 유지하는 데 가장 중요한 역할을 수행하는데, 예를 들면 유전자 복제, 신호전달, 대사, 단백질 합성 등 다양한 과정에 필수적으로 작용한다. 산업적으로 효소는 의약품 및 정밀/범용 화학제품 생산에 사용되고 있으며 최근에는 환경오염과 지구 온난화를 해결하고자 효소 기반 공정 개발 연구가 전 세계적으로 진행되고 있다.
그러나, 자연계에 존재하는 수많은 종류의 효소는 생체 내 반응에 적합하도록 진화되었기 때문에 이를 실제 산업적으로 사용하는 데 많은 제약이 있다. 이를 해결하고자 생명공학, 화학기업, 대학과 연구소에서 응용 목적에 맞는 효소 개발에 집중하고 있다.
김학성 교수는 지난 30여 년 동안 구조 기반 설계, 방향적 진화 및 컴퓨터 기반 설계를 통해 목적에 맞는 기능을 갖는 효소를 효율적으로 창출할 수 있는 기반 기술을 성공적으로 개발했다. 김 교수팀이 개발한 기반 기술은 산업용 효소, 단백질 신약, 합성 생물학, 바이오 화학, 생유기 합성 분야에서 광범위하게 활용될 수 있는 원천 기반 기술이다.
김 교수는 일련의 연구를 세계 최고 학술지인 ‘사이언스(Science)’를 비롯한 ‘네이쳐 케미컬 바이올로지(Nature Chemical Biology)’, ‘네이쳐 커뮤니케이션즈(Nature Communications)’, ‘앙게반테 케미(Angewandte Chemi.)’, ‘어드밴스드 사이언스(Advanced Science)’ 등의 저명 학술지에 발표하였고 60편의 특허를 등록하는 등 국제적으로 괄목할 업적을 이뤘다. 또한, 효소를 이용한 정밀화학 및 의약품 생산 기술을 산업체에 기술 이전 하여 관련 산업 발전에 크게 기여했다.
김학성 교수는 이러한 공로를 인정받아 관련분야의 최고 권위 국제 학회상인 ‘효소 공학상(Enzyme Engineering Award)’ 수상자로 선정됐다.
상을 수상한 김학성 교수는 “연구실 실적이 국제적으로 인정받아 권위 있는 상을 받게 되어 매우 영광이고, 연구실 졸업생들과 재정적 지원을 해주신 기관에 감사를 드린다. 앞으로 다양한 분야에서 효소의 산업적 응용을 확대시키는데 노력을 할 것이다”라고 수상 소감을 밝혔다.
2023.08.24 조회수 5757 RNA 합성에서 ‘기다림의 미학’ 규명
DNA에서 RNA를 생성하는 과정을 마무리 짓는 전사종결인자가 단백질 로(이하 Rho)이다. 일반 단백질이 작용물질에 미리 붙어 있으면 반응이 빨리 된다는 통념과 다르게 RNA 중합효소에 붙어 기다리는 Rho는 중합효소가 오래 멈출수록 종결 효율이 높아진다는 유의미한 결과가 발표되었다. 이번 연구 결과를 통해 자연에서 기다림의 미학이 증명된 것이다.
우리 대학 생명과학과 강창원 명예교수(KAIST 줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동 연구팀이 우리 대학 화학과 강진영 교수, 우리 대학 생명과학과 서연수 교수 연구팀과 협업 연구를 통해 RNA 합성 종결인자의 동역학적 특성을 발견했으며 그런 특성이 유전자 발현 조절에 미치는 생물학적 기능을 규명했다고 27일 밝혔다.
공동 연구팀은 세균의 전사 종결에 단백질 Rho가 관여하는 분자기작에 관해 작년에 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 발표한 바에 따르면, Rho가 중합효소에 미리 결합해 RNA의 특수부위를 기다린 후 중합효소‧DNA‧RNA의 전사 복합체를 해체하는 방식과 Rho가 RNA에 먼저 결합해 중합효소를 쫓아간 후 복합체를 해체하는 방식, 쫓아간 후 RNA만 방출하고 중합효소가 DNA에 남는 방식 등 세 갈래로 나뉘어 진행된다. (아래 그림 참조)
그런데 흥미롭게도 세 갈래 진행하는 속도가 기존 통념과는 다른 새로운 사실을 발견했다. 기존에는 Rho가 RNA에 붙어 중합효소를 쫓아가서 끝내는 방식과 비교하면 Rho가 중합효소에 미리 붙어 기다렸다가 끝내는 방식이 쫓아가는 시간이 들지 않기 때문에 더 빠를 것으로 인식되어 왔다. 하지만 공동 연구팀의 연구 결과는 기다려서 끝내는 방식이 오히려 더 느렸다. 그런데 느린 기다림 방식은 중합효소의 멈춤 시간이 길수록 종결 효율이 높고 상황에 따라 달라질 수 있는 반면에 쫓아가는 빠른 방식은 종결 효율이 중합효소 멈춘 시간과 상관이 없으며 상황에 따라 변화의 여지도 없다는 사실을 새롭게 밝혔다.
RNA가 방출되는 전사 종결이 일어나려면 RNA의 연장 합성이 일단 멈춰야 한다. 종결이 더디게 일어나려면 멈춤이 오래 유지되어야 하므로 전사 멈춤 시간과 전사 종결 효율의 상관관계를 이번 공동 연구에서 분석했다. 연구 결과, 기다려서 전사의 세 갈래 끝내기 방식이 진행하는 속도가 제각각 다를 뿐 아니라 그 조절 양상도 다르다는 것을 처음으로 규명한 것이다.
생물물리학 분야 첨단 기술인 단일분자 실험을 수행한 서울대 물리천문학부 송은호 박사과정 대학원생이 제1 저자로 참여한 이번 논문(제목: Transcriptional pause extension benefits the stand-by rather than catch-up Rho-dependent termination)은 저명 국제학술지 핵산연구(Nucleic Acids Research, 최근 영향지수 = 19.160)에 지난 2월 10일 자 게재됐다. KAIST 팔린다 무나싱하 박사, KAIST 황승하 박사과정 대학원생도 참여해 저자가 총 7명이다.
송은호 제1 저자는 "기존 통념과 상반된 결과를 처음 발견했을 때 당황스러웠지만 데이터를 꾸준히 쌓아가고 적절한 통계 모델을 통해서 그 결과를 검증해냈을 때 뿌듯했고, 또 이 발견의 생물학적 역할을 규명했을 때 더욱 기뻤다ˮ며 "항생제 개발 등에 중요한 단서를 줄 것이다ˮ라고 연구의 의의를 설명했다.
이번 공동 연구에는 단일분자 형광 기술을 구사하는 물리학자, 유전자 발현을 탐구하는 생명과학자, 중합체 구조를 분석하는 화학자가 두루 참여했다. 다양한 분야의 전공자가 꾸준히 협업하는 다학제 기초과학 연구의 우수 사례이며, 이번 연구는 한국연구재단 중견연구자지원사업, KAIST 고위험‧고성과 연구사업의 지원을 받았고, 논문게재비는 KAIST에서 지원했다.
2023.02.27 조회수 8703
RNA 합성에서 ‘기다림의 미학’ 규명
DNA에서 RNA를 생성하는 과정을 마무리 짓는 전사종결인자가 단백질 로(이하 Rho)이다. 일반 단백질이 작용물질에 미리 붙어 있으면 반응이 빨리 된다는 통념과 다르게 RNA 중합효소에 붙어 기다리는 Rho는 중합효소가 오래 멈출수록 종결 효율이 높아진다는 유의미한 결과가 발표되었다. 이번 연구 결과를 통해 자연에서 기다림의 미학이 증명된 것이다.
우리 대학 생명과학과 강창원 명예교수(KAIST 줄기세포연구센터 고문)와 서울대학교 물리천문학부 홍성철 교수의 공동 연구팀이 우리 대학 화학과 강진영 교수, 우리 대학 생명과학과 서연수 교수 연구팀과 협업 연구를 통해 RNA 합성 종결인자의 동역학적 특성을 발견했으며 그런 특성이 유전자 발현 조절에 미치는 생물학적 기능을 규명했다고 27일 밝혔다.
공동 연구팀은 세균의 전사 종결에 단백질 Rho가 관여하는 분자기작에 관해 작년에 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 발표한 바에 따르면, Rho가 중합효소에 미리 결합해 RNA의 특수부위를 기다린 후 중합효소‧DNA‧RNA의 전사 복합체를 해체하는 방식과 Rho가 RNA에 먼저 결합해 중합효소를 쫓아간 후 복합체를 해체하는 방식, 쫓아간 후 RNA만 방출하고 중합효소가 DNA에 남는 방식 등 세 갈래로 나뉘어 진행된다. (아래 그림 참조)
그런데 흥미롭게도 세 갈래 진행하는 속도가 기존 통념과는 다른 새로운 사실을 발견했다. 기존에는 Rho가 RNA에 붙어 중합효소를 쫓아가서 끝내는 방식과 비교하면 Rho가 중합효소에 미리 붙어 기다렸다가 끝내는 방식이 쫓아가는 시간이 들지 않기 때문에 더 빠를 것으로 인식되어 왔다. 하지만 공동 연구팀의 연구 결과는 기다려서 끝내는 방식이 오히려 더 느렸다. 그런데 느린 기다림 방식은 중합효소의 멈춤 시간이 길수록 종결 효율이 높고 상황에 따라 달라질 수 있는 반면에 쫓아가는 빠른 방식은 종결 효율이 중합효소 멈춘 시간과 상관이 없으며 상황에 따라 변화의 여지도 없다는 사실을 새롭게 밝혔다.
RNA가 방출되는 전사 종결이 일어나려면 RNA의 연장 합성이 일단 멈춰야 한다. 종결이 더디게 일어나려면 멈춤이 오래 유지되어야 하므로 전사 멈춤 시간과 전사 종결 효율의 상관관계를 이번 공동 연구에서 분석했다. 연구 결과, 기다려서 전사의 세 갈래 끝내기 방식이 진행하는 속도가 제각각 다를 뿐 아니라 그 조절 양상도 다르다는 것을 처음으로 규명한 것이다.
생물물리학 분야 첨단 기술인 단일분자 실험을 수행한 서울대 물리천문학부 송은호 박사과정 대학원생이 제1 저자로 참여한 이번 논문(제목: Transcriptional pause extension benefits the stand-by rather than catch-up Rho-dependent termination)은 저명 국제학술지 핵산연구(Nucleic Acids Research, 최근 영향지수 = 19.160)에 지난 2월 10일 자 게재됐다. KAIST 팔린다 무나싱하 박사, KAIST 황승하 박사과정 대학원생도 참여해 저자가 총 7명이다.
송은호 제1 저자는 "기존 통념과 상반된 결과를 처음 발견했을 때 당황스러웠지만 데이터를 꾸준히 쌓아가고 적절한 통계 모델을 통해서 그 결과를 검증해냈을 때 뿌듯했고, 또 이 발견의 생물학적 역할을 규명했을 때 더욱 기뻤다ˮ며 "항생제 개발 등에 중요한 단서를 줄 것이다ˮ라고 연구의 의의를 설명했다.
이번 공동 연구에는 단일분자 형광 기술을 구사하는 물리학자, 유전자 발현을 탐구하는 생명과학자, 중합체 구조를 분석하는 화학자가 두루 참여했다. 다양한 분야의 전공자가 꾸준히 협업하는 다학제 기초과학 연구의 우수 사례이며, 이번 연구는 한국연구재단 중견연구자지원사업, KAIST 고위험‧고성과 연구사업의 지원을 받았고, 논문게재비는 KAIST에서 지원했다.
2023.02.27 조회수 8703 RNA를 통한 유전자 전사 조절 원리 규명
세포가 어떤 유전자를 얼마나 발현하느냐에 따라 그 세포의 모양, 기능, 수명 등이 결정되므로 유전정보를 처음으로 발현하는 RNA 합성효소의 활성은 세포 내에서 매우 중요하게, 또 정교하게 조절된다. 그러나 이러한 유전자 전사(transcription) 조절의 중요성에도 불구하고 RNA 합성효소가 이러한 단백질과 RNA들에 의해서 어떻게 조절되는지 분자적인 수준에서는 잘 알려져 있지 않았다.
☞ 유전자 전사: DNA의 유전정보가 RNA에 옮겨지는 과정을 말한다. 유전정보의 복사물인 RNA는 단백질 합성에 사용된다.
우리 대학 화학과 강진영 교수 연구팀이 RNA를 통한 RNA 합성효소의 조절 메커니즘을 알아내고자 RNA 합성효소와 RNA 합성효소를 조절하는 바이러스 유래 RNA인 *HK022 putRNA의 결합 구조를 초저온 전자현미경(cryo-EM)으로 규명하여 유전자 전사조절의 기초 원리를 규명했다고 7일 밝혔다.
*HK022 putRNA: HK022 박테리오파지(박테리아를 감염시키는 바이러스)의 RNA로 다른 단백질의 도움 없이 해당 RNA를 만든 RNA 중합효소와 결합해 RNA 합성이 계속 되도록 RNA 중합효소를 조절
화학과 황승하 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 지난 8월 15일 출판되었다. (논문명: Structural basis of transcriptional regulation by a nascent RNA element, HK022 putRNA).
HK022 putRNA는 RNA 합성효소와 결합해서 RNA 합성이 멈추지 않고 계속 되도록 도와주는 역할을 한다. 이러한 기능을 이해하기 위해서 본 연구팀은 putRNA와 RNA 합성효소의 결합 복합체(put-associated RNA polymerase elongation complex, putEC)의 세 가지 구조를 초저온 전자현미경으로 규명하였다.
이 연구에서는 활성을 가진 putRNA를 제작하기 위해 장애물 단백질을 RNA 합성에 활용하는 방법을 고안하였으며, 초저온 전자현미경 촬영 결과 예상하지 못했던 세 종류의 복합체 – putRNA가 잘 접혀서 RNA 합성효소와 결합하고 있는 putEC, put RNA가 접히지 않은 put-없는 EC, 잘 접힌 putRNA와 시그마 단백질이 함께 RNA 합성효소와 결합하고 있는 시그마* 결합-putEC – 를 발견할 수 있었다. (그림 1)
*시그마: RNA 합성효소가 유전자 RNA 합성을 처음 시작할 때 필요한 단백질로 RNA 합성이 어느 정도 안정화되면 RNA 합성효소에서 떨어진다.
연구팀은 이들 복합체의 구조를 통해 putRNA가 이전 연구에서 예측된 대로 RNA 합성효소와 안정적으로 결합하고 있지만 예측과 달리 예상보다 더 많은 염기쌍(base pair)을 사용해 RNA 이중나선(double helix) 뿐 아니라 삼중나선(triple helix)을 형성하는 것을 확인하였다. 또한, putRNA가 RNA 합성효소와 결합하면 RNA 합성효소가 RNA 합성을 잠시 멈출 때 가지는 구조의 변화를 방해해서 RNA 합성을 지속하도록 한다는 가설을 제시할 수 있었다.
한편, 시그마 단백질(σ70)은 RNA 합성효소가 전사를 시작할 때 필요한 전사 개시인자로, RNA 합성이 안정되면 RNA 합성효소에서 떨어졌다가 특정 DNA 서열(–10-유사 서열)이 있으면 전사 과정 중이라도 다시 RNA 중합효소와 결합해 RNA 합성을 일시적으로 멈추는 것으로 알려져 있다. 이번 연구에서는 예상치 못하게 관찰된 시그마 결합-putEC 구조를 통해 시그마가 RNA 합성효소와 결합하여 RNA 합성이 잠깐 멈추면 putRNA가 더 잘 접힌다는 것을 알 수 있었다.
이 연구의 교신저자인 강진영 교수는 "RNA 합성효소는 세포 내에 저장된 유전 정보를 처음으로 꺼내어 생명활동에 활용하는, 세포 내에서 제일 중요한 단백질 중 하나이다. 그러나 RNA 합성효소의 큰 크기와 다양한 구조 변화 때문에 이전에 주로 활용하던 X-ray 결정학 방식으로는 그 구조를 관찰하기가 어려웠다. 최근 초저온 전자현미경의 발달로 이제야 조금씩 RNA 합성효소의 작동 원리가 알려지고 있는 상황이다. 이번 연구는 이전에 잘 알려지지 않았던, RNA를 통한 전사 조절의 기초적인 원리를 설명한 것으로, RNA를 통한 RNA 합성효소 조절의 다양한 전략을 밝혀줄 시작점이며, 더 나아가 유전자 발현을 조작할 수 있는 RNA의 개발을 도울 수 있는 정보를 제공할 것이라 기대한다.ˮ고 밝혔다.
한편 이번 연구는 한국연구재단의 이공분야기초연구사업(우수신진연구)과 원천기술개발사업의 지원을 받아 수행됐다.
2022.09.07 조회수 13053
RNA를 통한 유전자 전사 조절 원리 규명
세포가 어떤 유전자를 얼마나 발현하느냐에 따라 그 세포의 모양, 기능, 수명 등이 결정되므로 유전정보를 처음으로 발현하는 RNA 합성효소의 활성은 세포 내에서 매우 중요하게, 또 정교하게 조절된다. 그러나 이러한 유전자 전사(transcription) 조절의 중요성에도 불구하고 RNA 합성효소가 이러한 단백질과 RNA들에 의해서 어떻게 조절되는지 분자적인 수준에서는 잘 알려져 있지 않았다.
☞ 유전자 전사: DNA의 유전정보가 RNA에 옮겨지는 과정을 말한다. 유전정보의 복사물인 RNA는 단백질 합성에 사용된다.
우리 대학 화학과 강진영 교수 연구팀이 RNA를 통한 RNA 합성효소의 조절 메커니즘을 알아내고자 RNA 합성효소와 RNA 합성효소를 조절하는 바이러스 유래 RNA인 *HK022 putRNA의 결합 구조를 초저온 전자현미경(cryo-EM)으로 규명하여 유전자 전사조절의 기초 원리를 규명했다고 7일 밝혔다.
*HK022 putRNA: HK022 박테리오파지(박테리아를 감염시키는 바이러스)의 RNA로 다른 단백질의 도움 없이 해당 RNA를 만든 RNA 중합효소와 결합해 RNA 합성이 계속 되도록 RNA 중합효소를 조절
화학과 황승하 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 지난 8월 15일 출판되었다. (논문명: Structural basis of transcriptional regulation by a nascent RNA element, HK022 putRNA).
HK022 putRNA는 RNA 합성효소와 결합해서 RNA 합성이 멈추지 않고 계속 되도록 도와주는 역할을 한다. 이러한 기능을 이해하기 위해서 본 연구팀은 putRNA와 RNA 합성효소의 결합 복합체(put-associated RNA polymerase elongation complex, putEC)의 세 가지 구조를 초저온 전자현미경으로 규명하였다.
이 연구에서는 활성을 가진 putRNA를 제작하기 위해 장애물 단백질을 RNA 합성에 활용하는 방법을 고안하였으며, 초저온 전자현미경 촬영 결과 예상하지 못했던 세 종류의 복합체 – putRNA가 잘 접혀서 RNA 합성효소와 결합하고 있는 putEC, put RNA가 접히지 않은 put-없는 EC, 잘 접힌 putRNA와 시그마 단백질이 함께 RNA 합성효소와 결합하고 있는 시그마* 결합-putEC – 를 발견할 수 있었다. (그림 1)
*시그마: RNA 합성효소가 유전자 RNA 합성을 처음 시작할 때 필요한 단백질로 RNA 합성이 어느 정도 안정화되면 RNA 합성효소에서 떨어진다.
연구팀은 이들 복합체의 구조를 통해 putRNA가 이전 연구에서 예측된 대로 RNA 합성효소와 안정적으로 결합하고 있지만 예측과 달리 예상보다 더 많은 염기쌍(base pair)을 사용해 RNA 이중나선(double helix) 뿐 아니라 삼중나선(triple helix)을 형성하는 것을 확인하였다. 또한, putRNA가 RNA 합성효소와 결합하면 RNA 합성효소가 RNA 합성을 잠시 멈출 때 가지는 구조의 변화를 방해해서 RNA 합성을 지속하도록 한다는 가설을 제시할 수 있었다.
한편, 시그마 단백질(σ70)은 RNA 합성효소가 전사를 시작할 때 필요한 전사 개시인자로, RNA 합성이 안정되면 RNA 합성효소에서 떨어졌다가 특정 DNA 서열(–10-유사 서열)이 있으면 전사 과정 중이라도 다시 RNA 중합효소와 결합해 RNA 합성을 일시적으로 멈추는 것으로 알려져 있다. 이번 연구에서는 예상치 못하게 관찰된 시그마 결합-putEC 구조를 통해 시그마가 RNA 합성효소와 결합하여 RNA 합성이 잠깐 멈추면 putRNA가 더 잘 접힌다는 것을 알 수 있었다.
이 연구의 교신저자인 강진영 교수는 "RNA 합성효소는 세포 내에 저장된 유전 정보를 처음으로 꺼내어 생명활동에 활용하는, 세포 내에서 제일 중요한 단백질 중 하나이다. 그러나 RNA 합성효소의 큰 크기와 다양한 구조 변화 때문에 이전에 주로 활용하던 X-ray 결정학 방식으로는 그 구조를 관찰하기가 어려웠다. 최근 초저온 전자현미경의 발달로 이제야 조금씩 RNA 합성효소의 작동 원리가 알려지고 있는 상황이다. 이번 연구는 이전에 잘 알려지지 않았던, RNA를 통한 전사 조절의 기초적인 원리를 설명한 것으로, RNA를 통한 RNA 합성효소 조절의 다양한 전략을 밝혀줄 시작점이며, 더 나아가 유전자 발현을 조작할 수 있는 RNA의 개발을 도울 수 있는 정보를 제공할 것이라 기대한다.ˮ고 밝혔다.
한편 이번 연구는 한국연구재단의 이공분야기초연구사업(우수신진연구)과 원천기술개발사업의 지원을 받아 수행됐다.
2022.09.07 조회수 13053 유전자 가위를 이용한 RNA 분해효소 검출 신기술 개발
우리 대학 생명화학공학과 박현규 교수 연구팀이 *크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 *부수적 절단 활성을 활용해 RNA 분해효소를 민감하게 검출해내는 신기술을 개발했다고 14일 밝혔다.
☞ 크리스퍼 카스 시스템 (유전자 가위 기술)
- 크리스퍼 카스 시스템은 박테리아가 바이러스 감염으로부터 자신을 보호하기 위해 진화시킨 적응 면역 시스템이다. 이는 외래 유전자의 정보를 담고있는 가이드RNA와 직접 핵산을 절단하는 카스 단백질로 이루어져 있다. 2020년 제니퍼 다우드나 교수의 연구팀이 크리스퍼 카스9 유전자 가위 시스템을 개발한 공로로 노벨화학상을 수상해 널리 알려졌으며, 높은 표적 특이성과 빠른 역학 덕분에 최근에는 유전체 편집을 넘어 생체물질 검출 및 분자진단 분야에 광범위하게 적용되고 있다.
☞ 부수적 절단 활성
- 카스9 이외에도 Cas12, Cas13 등의 다양한 카스 단백질이 발굴되고 활용되고 있다. 카스12a는 표적 DNA 서열을 인식해 이를 절단하며, 이에 더해 주변의 비표적 단일 가닥 DNA를 무작위하게 절단하는 부수적 절단 활성을 가지고 있다. 이러한 성질은 분자진단 분야에서 활발하게 사용되고 있다.
우리 대학 생명화학공학과 김한솔 박사가 제1 저자로 참여한 이번 연구는 영국왕립화학회가 발행하는 국제 학술지 `케미컬 커뮤니케이션스 (Chemical Communications)'에 2022년도 16호 표지(Back cover) 논문으로 지난달 24일 선정됐다. (논문명: CRISPR/Cas12a collateral cleavage activity for an ultrasensitive assay of RNase H)
RNA 분해효소의 일종인 `리보핵산가수분해효소 H'는 후천성면역결핍증(에이즈)을 일으키는 바이러스인 인간 면역결핍 바이러스(HIV-1) 및 B형 간염 바이러스를 포함한 역전사 바이러스의 역전사효소에서 필수적인 영역으로, 역전사 바이러스의 증식에 관여한다. 따라서 리보핵산가수분해효소 H는 항바이러스제 개발의 중요한 표적으로 알려져 있다. 일반적으로 리보핵산가수분해효소 H의 활성을 검출하기 위해서는 전기영동 또는 고성능 액체크로마토그래피 등의 방식을 사용하고 있지만, 이와 같은 기술들은 낮은 특이도와 민감도, 복잡한 검출 과정, 긴 검출 시간 등의 단점이 있다.
연구팀은 이러한 현행 기술의 한계를 극복하기 위해, 크리스퍼 카스12a (CRISPR-Cas12a) 시스템을 활용해 검출의 민감도를 크게 향상하고 리보핵산가수분해효소 H를 현재 보고된 기술 중 가장 높은 민감도로(검출한계: 0.24 U/L) 1시간 이내에 검출하는 데 성공했다.
연구팀은 리보핵산가수분해효소 H의 기질로 짧은 DNA/RNA 키메라 복합체를 이용해 리보핵산가수분해효소 H의 활성 하에 활성제 DNA (Activator DNA, AD)가 방출되도록 설계했다. Cas12a/crRNA 복합체가 방출된 활성제 DNA를 인식할 시 Cas12a의 부수적 절단 활성을 가동해 주변의 리포터 DNA를 절단해 형광 신호가 발생하도록 설계함으로써, 표적 유전자 돌연변이를 고감도로 매우 정확하게 검출했다. 연구팀은 이 기술을 통해서 암세포의 리보핵산가수분해효소 H 활성도 성공적으로 검출할 수 있었다.
특히 리보핵산가수분해효소 H가 인간 면역결핍 바이러스 증식에 관여한다는 점을 고려할 때, 이번 연구 성과는 에이즈 치료제 개발에 기여할 수 있을 것으로도 기대된다.
박현규 교수는 “이번 기술은 크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 부수적 절단 활성을 활용해 리보핵산가수분해효소 H를 고도로 민감하게 검출함으로써, 항바이러스제의 표적 발굴에 활용될 수 있다”라고 연구의 의의를 설명했다.
한편 이번 연구는 경찰청의 치안과학기술연구개발사업 및 한국연구재단의 중견연구자지원사업과 바이오·의료기술개발사업의 일환으로 수행됐다.
2022.03.14 조회수 13269
유전자 가위를 이용한 RNA 분해효소 검출 신기술 개발
우리 대학 생명화학공학과 박현규 교수 연구팀이 *크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 *부수적 절단 활성을 활용해 RNA 분해효소를 민감하게 검출해내는 신기술을 개발했다고 14일 밝혔다.
☞ 크리스퍼 카스 시스템 (유전자 가위 기술)
- 크리스퍼 카스 시스템은 박테리아가 바이러스 감염으로부터 자신을 보호하기 위해 진화시킨 적응 면역 시스템이다. 이는 외래 유전자의 정보를 담고있는 가이드RNA와 직접 핵산을 절단하는 카스 단백질로 이루어져 있다. 2020년 제니퍼 다우드나 교수의 연구팀이 크리스퍼 카스9 유전자 가위 시스템을 개발한 공로로 노벨화학상을 수상해 널리 알려졌으며, 높은 표적 특이성과 빠른 역학 덕분에 최근에는 유전체 편집을 넘어 생체물질 검출 및 분자진단 분야에 광범위하게 적용되고 있다.
☞ 부수적 절단 활성
- 카스9 이외에도 Cas12, Cas13 등의 다양한 카스 단백질이 발굴되고 활용되고 있다. 카스12a는 표적 DNA 서열을 인식해 이를 절단하며, 이에 더해 주변의 비표적 단일 가닥 DNA를 무작위하게 절단하는 부수적 절단 활성을 가지고 있다. 이러한 성질은 분자진단 분야에서 활발하게 사용되고 있다.
우리 대학 생명화학공학과 김한솔 박사가 제1 저자로 참여한 이번 연구는 영국왕립화학회가 발행하는 국제 학술지 `케미컬 커뮤니케이션스 (Chemical Communications)'에 2022년도 16호 표지(Back cover) 논문으로 지난달 24일 선정됐다. (논문명: CRISPR/Cas12a collateral cleavage activity for an ultrasensitive assay of RNase H)
RNA 분해효소의 일종인 `리보핵산가수분해효소 H'는 후천성면역결핍증(에이즈)을 일으키는 바이러스인 인간 면역결핍 바이러스(HIV-1) 및 B형 간염 바이러스를 포함한 역전사 바이러스의 역전사효소에서 필수적인 영역으로, 역전사 바이러스의 증식에 관여한다. 따라서 리보핵산가수분해효소 H는 항바이러스제 개발의 중요한 표적으로 알려져 있다. 일반적으로 리보핵산가수분해효소 H의 활성을 검출하기 위해서는 전기영동 또는 고성능 액체크로마토그래피 등의 방식을 사용하고 있지만, 이와 같은 기술들은 낮은 특이도와 민감도, 복잡한 검출 과정, 긴 검출 시간 등의 단점이 있다.
연구팀은 이러한 현행 기술의 한계를 극복하기 위해, 크리스퍼 카스12a (CRISPR-Cas12a) 시스템을 활용해 검출의 민감도를 크게 향상하고 리보핵산가수분해효소 H를 현재 보고된 기술 중 가장 높은 민감도로(검출한계: 0.24 U/L) 1시간 이내에 검출하는 데 성공했다.
연구팀은 리보핵산가수분해효소 H의 기질로 짧은 DNA/RNA 키메라 복합체를 이용해 리보핵산가수분해효소 H의 활성 하에 활성제 DNA (Activator DNA, AD)가 방출되도록 설계했다. Cas12a/crRNA 복합체가 방출된 활성제 DNA를 인식할 시 Cas12a의 부수적 절단 활성을 가동해 주변의 리포터 DNA를 절단해 형광 신호가 발생하도록 설계함으로써, 표적 유전자 돌연변이를 고감도로 매우 정확하게 검출했다. 연구팀은 이 기술을 통해서 암세포의 리보핵산가수분해효소 H 활성도 성공적으로 검출할 수 있었다.
특히 리보핵산가수분해효소 H가 인간 면역결핍 바이러스 증식에 관여한다는 점을 고려할 때, 이번 연구 성과는 에이즈 치료제 개발에 기여할 수 있을 것으로도 기대된다.
박현규 교수는 “이번 기술은 크리스퍼 카스12a (CRISPR-Cas12a) 시스템의 부수적 절단 활성을 활용해 리보핵산가수분해효소 H를 고도로 민감하게 검출함으로써, 항바이러스제의 표적 발굴에 활용될 수 있다”라고 연구의 의의를 설명했다.
한편 이번 연구는 경찰청의 치안과학기술연구개발사업 및 한국연구재단의 중견연구자지원사업과 바이오·의료기술개발사업의 일환으로 수행됐다.
2022.03.14 조회수 13269 6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07 조회수 12718
6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07 조회수 12718 자연계 효소 원리를 이용한 신개념 산업용 촉매 개발
우리 대학 생명화학공학과 최민기 교수 연구팀이 자연계 효소와 같이 원하는 반응물만 선택적으로 전환할 수 있는 신개념의 고성능 산업 촉매를 개발했다고 9일 밝혔다.
촉매는 기초 유분 생산에서부터 다양한 화학 제품 제조까지 대부분의 석유화학 공정에서 사용되는 물질로 공정의 경제성과 친환경성을 높이기 위해서 원하는 생성물만 만들어지는 높은 선택성을 갖는 촉매 개발이 필수적이다.
지구상에 존재하는 촉매 중 가장 높은 선택성을 보이는 촉매는 효소다. 효소는 천연 고분자인 단백질이 반응이 일어나는 활성점을 3차원적으로 둘러싸고 있는 구조를 갖는데, 단백질의 구조 및 활성점과의 상호작용에 따라 특정 반응물만 선택적으로 접근할 수 있도록 조절해 높은 선택성을 갖는다. 연구팀은 이번 연구에서 효소의 단백질과 유사한 고분자를 이용해 금속 활성점과의 상호작용을 조절한 새로운 개념의 촉매 설계 방법을 제시했다.
고분자는 일정 단위체의 반복적인 화학 결합을 통해 만들어지는 높은 분자량의 거대분자이며 합성에 사용한 단위체에 따라 고분자의 작용기를 쉽게 조절할 수 있다. 연구팀은 금속과 상호작용을 할 수 있는 작용기를 포함한 고분자를 합성하고 팔라듐 금속 입자를 포함한 촉매를 만들었다. 금속과 강하게 상호작용을 하는 고분자는 효소와 같이 금속 주위를 고분자가 3차원적으로 둘러싸는 형태를 보이는 한편 약하게 상호작용하는 고분자는 금속을 둘러싸지 못하고 금속 표면이 노출된 형태가 됐다.
연구팀은 이렇게 합성된 촉매를 이용해 석유화학의 에틸렌 생산 공정에서 매우 중요한 아세틸렌 부분 수소화 반응에 적용했다. 에틸렌은 플라스틱, 비닐, 접착제 등 다양한 제품을 만드는 데 이용하는 기본 핵심 원료이며 현재 우리나라에서는 주로 나프타를 분해하여 생산한다.
나프타분해시설에서 생산되는 에틸렌에는 불순물인 미량의 아세틸렌이 함께 포함돼 있는데, 이 아세틸렌이 화학 제품을 만드는 데 사용되는 촉매에 치명적으로 작용하기 때문에 수소화 반응을 통해 제거해 주는 공정이 필수적이다. 이 공정에서 핵심은 99% 이상의 에틸렌은 소모하지 않으면서 1% 미만의 아세틸렌만 선택적으로 제거하는 것이다.
연구진이 개발한 신규 촉매를 이 공정에 적용한 결과, 강하게 상호작용해 3차원 구조를 형성한 촉매는 고분자가 아세틸렌에만 접근해 높은 선택도를 보였다. 하지만 약한 상호작용으로 인해 고분자가 금속 표면을 덮지 못한 촉매에서는 아세틸렌과 에틸렌에 모두 접근해 낮은 선택도를 보였다.
또한 강하게 상호작용을 하는 고분자일수록 비활성화를 일으키는 탄소 침적물인 코크의 생성을 차단하고 금속 입자의 뭉침 현상을 억제해 장기간 반응에서도 높은 활성과 선택도를 유지했다.
연구를 주도한 최민기 교수는 "자연계 효소의 원리를 모방해 고분자와 금속 사이의 상호작용을 조절하고 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 가지는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념이다ˮ라며, "향후 높은 선택도가 필요한 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것이다ˮ라고 말했다.
우리 대학 생명화학공학과 현경림 박사과정 학생이 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `앙게반테 케미(Angewandte chemi)'에 지난 5월 17일 字 온라인판에 게재됐다. (논문명: Tailoring a Dynamic Metal-Polymer Interaction to Improve Catalyst Selectivity and Longevity in Hydrogenation),
한편 이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원을 받아 수행됐다.
2021.06.09 조회수 74561
자연계 효소 원리를 이용한 신개념 산업용 촉매 개발
우리 대학 생명화학공학과 최민기 교수 연구팀이 자연계 효소와 같이 원하는 반응물만 선택적으로 전환할 수 있는 신개념의 고성능 산업 촉매를 개발했다고 9일 밝혔다.
촉매는 기초 유분 생산에서부터 다양한 화학 제품 제조까지 대부분의 석유화학 공정에서 사용되는 물질로 공정의 경제성과 친환경성을 높이기 위해서 원하는 생성물만 만들어지는 높은 선택성을 갖는 촉매 개발이 필수적이다.
지구상에 존재하는 촉매 중 가장 높은 선택성을 보이는 촉매는 효소다. 효소는 천연 고분자인 단백질이 반응이 일어나는 활성점을 3차원적으로 둘러싸고 있는 구조를 갖는데, 단백질의 구조 및 활성점과의 상호작용에 따라 특정 반응물만 선택적으로 접근할 수 있도록 조절해 높은 선택성을 갖는다. 연구팀은 이번 연구에서 효소의 단백질과 유사한 고분자를 이용해 금속 활성점과의 상호작용을 조절한 새로운 개념의 촉매 설계 방법을 제시했다.
고분자는 일정 단위체의 반복적인 화학 결합을 통해 만들어지는 높은 분자량의 거대분자이며 합성에 사용한 단위체에 따라 고분자의 작용기를 쉽게 조절할 수 있다. 연구팀은 금속과 상호작용을 할 수 있는 작용기를 포함한 고분자를 합성하고 팔라듐 금속 입자를 포함한 촉매를 만들었다. 금속과 강하게 상호작용을 하는 고분자는 효소와 같이 금속 주위를 고분자가 3차원적으로 둘러싸는 형태를 보이는 한편 약하게 상호작용하는 고분자는 금속을 둘러싸지 못하고 금속 표면이 노출된 형태가 됐다.
연구팀은 이렇게 합성된 촉매를 이용해 석유화학의 에틸렌 생산 공정에서 매우 중요한 아세틸렌 부분 수소화 반응에 적용했다. 에틸렌은 플라스틱, 비닐, 접착제 등 다양한 제품을 만드는 데 이용하는 기본 핵심 원료이며 현재 우리나라에서는 주로 나프타를 분해하여 생산한다.
나프타분해시설에서 생산되는 에틸렌에는 불순물인 미량의 아세틸렌이 함께 포함돼 있는데, 이 아세틸렌이 화학 제품을 만드는 데 사용되는 촉매에 치명적으로 작용하기 때문에 수소화 반응을 통해 제거해 주는 공정이 필수적이다. 이 공정에서 핵심은 99% 이상의 에틸렌은 소모하지 않으면서 1% 미만의 아세틸렌만 선택적으로 제거하는 것이다.
연구진이 개발한 신규 촉매를 이 공정에 적용한 결과, 강하게 상호작용해 3차원 구조를 형성한 촉매는 고분자가 아세틸렌에만 접근해 높은 선택도를 보였다. 하지만 약한 상호작용으로 인해 고분자가 금속 표면을 덮지 못한 촉매에서는 아세틸렌과 에틸렌에 모두 접근해 낮은 선택도를 보였다.
또한 강하게 상호작용을 하는 고분자일수록 비활성화를 일으키는 탄소 침적물인 코크의 생성을 차단하고 금속 입자의 뭉침 현상을 억제해 장기간 반응에서도 높은 활성과 선택도를 유지했다.
연구를 주도한 최민기 교수는 "자연계 효소의 원리를 모방해 고분자와 금속 사이의 상호작용을 조절하고 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 가지는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념이다ˮ라며, "향후 높은 선택도가 필요한 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것이다ˮ라고 말했다.
우리 대학 생명화학공학과 현경림 박사과정 학생이 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `앙게반테 케미(Angewandte chemi)'에 지난 5월 17일 字 온라인판에 게재됐다. (논문명: Tailoring a Dynamic Metal-Polymer Interaction to Improve Catalyst Selectivity and Longevity in Hydrogenation),
한편 이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원을 받아 수행됐다.
2021.06.09 조회수 74561 현장 진단형 초고속 실시간 유전자 분석기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 *나노 플라즈모닉 구조를 통해 빠른 열 순환 및 실시간 정량 분석이 가능한 초고속 실시간 중합효소연쇄반응(PCR) 기술을 개발했다고 7일 밝혔다.
☞ 나노 플라즈모닉 구조(Nanostructures for Plasmonic): 빛의 파장보다 작은 크기의 금속나노구조이며, 빛이 표면에 조사될 때 금속 표면과 유전체의 경계에서 빛과 전자가 상호작용을 한다. 주로 바이오 물질의 검출이나 분자진단에 많이 응용된다.
최근 코로나19를 포함한 전염성이 높은 바이러스의 확산을 방지하기 위해 신속하고 정확하게 바이러스를 검출하는 기술이 절실하게 필요하다. 역전사 중합효소연쇄반응(RT-PCR)은 가장 표준화된 코로나19 진단법으로 바이러스 내부의 유전물질인 RNA를 상보적 DNA로 역전사한 후 타겟 DNA를 증폭해 형광 프로브로 검출하는 방법이다. 그러나 기존 RT-PCR은 높은 민감도와 정확도를 갖추지만, 검출 시간이 길고 고가의 대형장비를 갖춘 장소로 검체를 운송한 후 진단하는 등 실시간 현장 대응의 한계가 존재한다.
연구팀이 개발한 `실시간 나노 플라즈모닉 PCR'은 백색 발광다이오드(LED)의 높은 광 흡수율을 갖는 나노 플라즈모닉 기판에 진공 설계된 미세 유체칩을 결합해 소량의 검체를 신속하게 증폭하고 정량적으로 분석해 바이러스를 단시간 내에 정확하게 검출할 수 있다. 이러한 특징을 이용해 공공장소 등 환자 발생 장소에서 병원성 바이러스의 확산 및 해외유입을 차단할 수 있을 것으로 기대된다.
나노 플라즈모닉 기판은 유리 나노기둥 위 금 나노섬 구조로 가시광선 전 영역에서 높은 광 흡수율을 가지므로 백색 LED의 빛을 열에너지로 치환해 빠르게 열을 발생시키고 내보낼 수 있다. 또한 광열 발생장치의 수직적인 온도 구배로 인한 증폭 효율 저하를 해결하기 위해 연구팀은 진공 설계된 미세 유체칩을 결합했다.
이는 샘플 한 방울을 칩에 넣으면 진공이 액체를 마이크로 챔버로 잡아당겨 자동으로 3분 이내에 주입되고, PCR 과정 동안에 발생하는 미세 기포는 공기 투과성 벽을 통해 제거돼 PCR 효율을 높이는 원리다.
연구팀은 SARS-CoV-2 플라스미드 DNA를 사용해 해당 기술을 검증했고, 40싸이클(95도-60도)을 5분 이내에 수행해 타겟 바이러스를 91%의 증폭 효율과 함께 정량적으로 검출했다. 이는 기존 실시간 PCR 시스템의 긴 소요 시간(약 1시간)에 비해 매우 빠르고, 높은 증폭 효율을 보이므로 신속한 현장 진단에 적용되기 적합할 것으로 보인다.
정기훈 교수는 "실질적으로 현장에서 사용 가능한 초고속 분자진단법을 개발했다ˮ며 "이 실시간 나노 플라즈모닉 PCR 기술은 현장에서 분자진단을 위한 차세대 유전자 증폭 플랫폼을 제공할 것이며 바이러스 확산 방지에 기여할 수 있을 것으로 예상한다ˮ라고 말했다.
우리 대학 바이오및뇌공학과 강병훈 박사과정이 주도한 이번 연구 결과는 국제 학술지 `에이씨에스 나노 (ACS Nano)'에 지난 5월 19일 字로 게재됐다. (논문명: Ultrafast and Real-time Nanoplasmonic On-Chip Polymerase Chain Reaction for Rapid and Quantitative Molecular Diagnostics)
한편 이번 연구는 KAIST 코로나19대응 과학기술뉴딜사업단과 한국연구재단 개인연구지원사업, 바이오기술개발사업으로 수행됐다.
2021.06.07 조회수 47104
현장 진단형 초고속 실시간 유전자 분석기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 *나노 플라즈모닉 구조를 통해 빠른 열 순환 및 실시간 정량 분석이 가능한 초고속 실시간 중합효소연쇄반응(PCR) 기술을 개발했다고 7일 밝혔다.
☞ 나노 플라즈모닉 구조(Nanostructures for Plasmonic): 빛의 파장보다 작은 크기의 금속나노구조이며, 빛이 표면에 조사될 때 금속 표면과 유전체의 경계에서 빛과 전자가 상호작용을 한다. 주로 바이오 물질의 검출이나 분자진단에 많이 응용된다.
최근 코로나19를 포함한 전염성이 높은 바이러스의 확산을 방지하기 위해 신속하고 정확하게 바이러스를 검출하는 기술이 절실하게 필요하다. 역전사 중합효소연쇄반응(RT-PCR)은 가장 표준화된 코로나19 진단법으로 바이러스 내부의 유전물질인 RNA를 상보적 DNA로 역전사한 후 타겟 DNA를 증폭해 형광 프로브로 검출하는 방법이다. 그러나 기존 RT-PCR은 높은 민감도와 정확도를 갖추지만, 검출 시간이 길고 고가의 대형장비를 갖춘 장소로 검체를 운송한 후 진단하는 등 실시간 현장 대응의 한계가 존재한다.
연구팀이 개발한 `실시간 나노 플라즈모닉 PCR'은 백색 발광다이오드(LED)의 높은 광 흡수율을 갖는 나노 플라즈모닉 기판에 진공 설계된 미세 유체칩을 결합해 소량의 검체를 신속하게 증폭하고 정량적으로 분석해 바이러스를 단시간 내에 정확하게 검출할 수 있다. 이러한 특징을 이용해 공공장소 등 환자 발생 장소에서 병원성 바이러스의 확산 및 해외유입을 차단할 수 있을 것으로 기대된다.
나노 플라즈모닉 기판은 유리 나노기둥 위 금 나노섬 구조로 가시광선 전 영역에서 높은 광 흡수율을 가지므로 백색 LED의 빛을 열에너지로 치환해 빠르게 열을 발생시키고 내보낼 수 있다. 또한 광열 발생장치의 수직적인 온도 구배로 인한 증폭 효율 저하를 해결하기 위해 연구팀은 진공 설계된 미세 유체칩을 결합했다.
이는 샘플 한 방울을 칩에 넣으면 진공이 액체를 마이크로 챔버로 잡아당겨 자동으로 3분 이내에 주입되고, PCR 과정 동안에 발생하는 미세 기포는 공기 투과성 벽을 통해 제거돼 PCR 효율을 높이는 원리다.
연구팀은 SARS-CoV-2 플라스미드 DNA를 사용해 해당 기술을 검증했고, 40싸이클(95도-60도)을 5분 이내에 수행해 타겟 바이러스를 91%의 증폭 효율과 함께 정량적으로 검출했다. 이는 기존 실시간 PCR 시스템의 긴 소요 시간(약 1시간)에 비해 매우 빠르고, 높은 증폭 효율을 보이므로 신속한 현장 진단에 적용되기 적합할 것으로 보인다.
정기훈 교수는 "실질적으로 현장에서 사용 가능한 초고속 분자진단법을 개발했다ˮ며 "이 실시간 나노 플라즈모닉 PCR 기술은 현장에서 분자진단을 위한 차세대 유전자 증폭 플랫폼을 제공할 것이며 바이러스 확산 방지에 기여할 수 있을 것으로 예상한다ˮ라고 말했다.
우리 대학 바이오및뇌공학과 강병훈 박사과정이 주도한 이번 연구 결과는 국제 학술지 `에이씨에스 나노 (ACS Nano)'에 지난 5월 19일 字로 게재됐다. (논문명: Ultrafast and Real-time Nanoplasmonic On-Chip Polymerase Chain Reaction for Rapid and Quantitative Molecular Diagnostics)
한편 이번 연구는 KAIST 코로나19대응 과학기술뉴딜사업단과 한국연구재단 개인연구지원사업, 바이오기술개발사업으로 수행됐다.
2021.06.07 조회수 47104 알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 26924
알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 26924 자연계 효소처럼 작동하는 신개념 산업용 촉매 개발
우리 대학 연구진이 생체 내 단백질 *촉매인 *효소를 모방해 공급자 또는 개발자가 원하는 화학반응만 선택적으로 유도하되 안정성도 갖춘 기존에 없는 새로운 개념의 산업용 촉매 개발에 성공했다.
☞ 촉매(catalyst): 자신은 변하지 않으면서 물질 간의 화학반응이 잘 일어나도록 돕는 물질. 표면에 흡착된 반응물을 생성물로 빠르게 전환해주는 역할을 한다.
☞ 효소(enzyme): 생체 내의 화학반응을 매개하는 단백질 촉매. 반응물을 전환할 수 있는 금속 촉매 활성점(active site)이 부드러운 유기 고분자인 단백질로 둘러싸인 형태를 지니고 있는데, 단백질의 구조에 따라 오직 원하는 반응물만이 활성점에 접근해 생성물로 전환될 수 있다.
생명화학공학과 최민기, 화학과 김형준 교수 공동연구팀은 실생활에 흔히 쓰이는 플라스틱, 비닐 등의 재료인 화학 원료를 만들 때, 자연계 효소와 동일한 원리로 반응물을 선택적으로 전환할 수 있는 고성능 산업용 촉매를 개발하는 데 성공했다.
한정된 자원을 효율적으로 이용하기 위해서는 다양한 화학반응 경로 중 목표하는 반응물을 원하는 생성물로 선택적으로 전환해줄 수 있는 촉매를 디자인하는 것이 매우 중요하다. 지구상에 존재하는 촉매 중 가장 효율이 좋은 촉매는 자연계 및 우리 몸 등에 존재하는 '효소'다.
이와 달리 석유화학 산업에서 이용되는 촉매들은 알루미나·실리카·제올라이트와 같이 딱딱한 무기물 표면 위에 금속을 퍼뜨려 노출한 구조로 구성돼 있다. 이런 형태의 촉매에서는 금속 표면에 모든 반응물이 흡착되기 쉬워 특정 반응물만을 선택적으로 생성물로 전환하기에는 한계가 있다. 그 럼에도 불구하고 대부분 산업용 촉매 설계에서 무기 소재를 사용하는 이유는 이들이 열화학적 안정성이 뛰어나 다양한 반응 조건에서도 촉매가 안정적으로 작용하기 때문이다.
최민기·김형준 교수 공동연구팀은 이번 연구를 통해 단백질과 같이 부드럽고 유동성이 있으면서도 매우 높은 열화학적 안정성을 지닌 `폴리페닐렌설파이드(polyphenylene sulfide, PPS)'라는 엔지니어링 플라스틱 물질을 이용해서 고분자 막이 금속촉매 활성점을 감싼 형태의 신개념 촉매를 세계 최초로 개발했다. PPS는 내열성과 내화학성이 매우 뛰어나 자동차나 항공우주 산업 등에서 많이 사용되는 상용 고분자다.
연구팀은 이 새로운 촉매를 이용해 석유화학의 에틸렌 생산 공정 중 매우 중요한 아세틸렌 수소화 반응에 적용하는 데 성공했다. 우리나라 석유화학 산업의 원료는 90% 이상이 *나프타인데, 나프타분해시설(Naphtha Cracking Center, NCC)에서 이를 분해해 에틸렌 및 기타 기초유분들을 생산하고 있다. 특히 에틸렌은 주변에 흔한 플라스틱, 비닐, 접착제, 페인트까지 일상에서 사용하는 다양한 제품을 만드는데 이용하는 기본 핵심 화학 원료다.
☞ 나프타(naphtha): 원유를 증류할 때, 35~220℃의 끓는점 범위에서 유출되는 탄화수소의 혼합체이다. 중질 가솔린이라고도 부른다.
나프타를 분해할 때 생산되는 에틸렌에는 미량의 아세틸렌이 불순물로 함께 포함돼 있다. 아세틸렌은 추후 에틸렌을 이용해 화학제품을 만드는 데 매우 치명적이므로 미량의 아세틸렌을 수소화 반응으로 제거해 주는 공정을 반드시 거쳐야 한다. 그런데 이 공정은 99% 이상 에틸렌은 건들지 않으면서도, 1% 미만의 아세틸렌만 선택적으로 전환해야 하는 난제가 존재해왔다.
공동연구팀은 새로 개발한 촉매를 이 공정에 적용한 결과 1% 미만의 아세틸렌은 금속 입자를 둘러싸고 있는 고분자막을 투과해 쉽게 전환되는 대신 99% 이상의 에틸렌은 고분자막에 가로막혀 촉매 반응이 진행되지 않아서 기존 팔라듐(Pd) 촉매와 비교할 때 선택도는 2 배 이상, 안정성은 10배 이상 증진된 놀라운 결과를 얻었다.
우리 대학 생명화학공학과 이송현, 화학과 신승재 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스(Science Advances)' 7월 8일 字 온라인판에 게재됐다(논문명: Dynamic Metal-Polymer Interaction for the Design of Chemoselective and Long-Lived Hydrogenation Catalysts).
최민기 교수는 "자연계의 효소를 모방해 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 갖는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념"이라면서 "향후 높은 선택도가 있어야 하는 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것"이라고 전망했다.
이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원으로 이뤄졌다.
2020.07.31 조회수 43351
자연계 효소처럼 작동하는 신개념 산업용 촉매 개발
우리 대학 연구진이 생체 내 단백질 *촉매인 *효소를 모방해 공급자 또는 개발자가 원하는 화학반응만 선택적으로 유도하되 안정성도 갖춘 기존에 없는 새로운 개념의 산업용 촉매 개발에 성공했다.
☞ 촉매(catalyst): 자신은 변하지 않으면서 물질 간의 화학반응이 잘 일어나도록 돕는 물질. 표면에 흡착된 반응물을 생성물로 빠르게 전환해주는 역할을 한다.
☞ 효소(enzyme): 생체 내의 화학반응을 매개하는 단백질 촉매. 반응물을 전환할 수 있는 금속 촉매 활성점(active site)이 부드러운 유기 고분자인 단백질로 둘러싸인 형태를 지니고 있는데, 단백질의 구조에 따라 오직 원하는 반응물만이 활성점에 접근해 생성물로 전환될 수 있다.
생명화학공학과 최민기, 화학과 김형준 교수 공동연구팀은 실생활에 흔히 쓰이는 플라스틱, 비닐 등의 재료인 화학 원료를 만들 때, 자연계 효소와 동일한 원리로 반응물을 선택적으로 전환할 수 있는 고성능 산업용 촉매를 개발하는 데 성공했다.
한정된 자원을 효율적으로 이용하기 위해서는 다양한 화학반응 경로 중 목표하는 반응물을 원하는 생성물로 선택적으로 전환해줄 수 있는 촉매를 디자인하는 것이 매우 중요하다. 지구상에 존재하는 촉매 중 가장 효율이 좋은 촉매는 자연계 및 우리 몸 등에 존재하는 '효소'다.
이와 달리 석유화학 산업에서 이용되는 촉매들은 알루미나·실리카·제올라이트와 같이 딱딱한 무기물 표면 위에 금속을 퍼뜨려 노출한 구조로 구성돼 있다. 이런 형태의 촉매에서는 금속 표면에 모든 반응물이 흡착되기 쉬워 특정 반응물만을 선택적으로 생성물로 전환하기에는 한계가 있다. 그 럼에도 불구하고 대부분 산업용 촉매 설계에서 무기 소재를 사용하는 이유는 이들이 열화학적 안정성이 뛰어나 다양한 반응 조건에서도 촉매가 안정적으로 작용하기 때문이다.
최민기·김형준 교수 공동연구팀은 이번 연구를 통해 단백질과 같이 부드럽고 유동성이 있으면서도 매우 높은 열화학적 안정성을 지닌 `폴리페닐렌설파이드(polyphenylene sulfide, PPS)'라는 엔지니어링 플라스틱 물질을 이용해서 고분자 막이 금속촉매 활성점을 감싼 형태의 신개념 촉매를 세계 최초로 개발했다. PPS는 내열성과 내화학성이 매우 뛰어나 자동차나 항공우주 산업 등에서 많이 사용되는 상용 고분자다.
연구팀은 이 새로운 촉매를 이용해 석유화학의 에틸렌 생산 공정 중 매우 중요한 아세틸렌 수소화 반응에 적용하는 데 성공했다. 우리나라 석유화학 산업의 원료는 90% 이상이 *나프타인데, 나프타분해시설(Naphtha Cracking Center, NCC)에서 이를 분해해 에틸렌 및 기타 기초유분들을 생산하고 있다. 특히 에틸렌은 주변에 흔한 플라스틱, 비닐, 접착제, 페인트까지 일상에서 사용하는 다양한 제품을 만드는데 이용하는 기본 핵심 화학 원료다.
☞ 나프타(naphtha): 원유를 증류할 때, 35~220℃의 끓는점 범위에서 유출되는 탄화수소의 혼합체이다. 중질 가솔린이라고도 부른다.
나프타를 분해할 때 생산되는 에틸렌에는 미량의 아세틸렌이 불순물로 함께 포함돼 있다. 아세틸렌은 추후 에틸렌을 이용해 화학제품을 만드는 데 매우 치명적이므로 미량의 아세틸렌을 수소화 반응으로 제거해 주는 공정을 반드시 거쳐야 한다. 그런데 이 공정은 99% 이상 에틸렌은 건들지 않으면서도, 1% 미만의 아세틸렌만 선택적으로 전환해야 하는 난제가 존재해왔다.
공동연구팀은 새로 개발한 촉매를 이 공정에 적용한 결과 1% 미만의 아세틸렌은 금속 입자를 둘러싸고 있는 고분자막을 투과해 쉽게 전환되는 대신 99% 이상의 에틸렌은 고분자막에 가로막혀 촉매 반응이 진행되지 않아서 기존 팔라듐(Pd) 촉매와 비교할 때 선택도는 2 배 이상, 안정성은 10배 이상 증진된 놀라운 결과를 얻었다.
우리 대학 생명화학공학과 이송현, 화학과 신승재 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스(Science Advances)' 7월 8일 字 온라인판에 게재됐다(논문명: Dynamic Metal-Polymer Interaction for the Design of Chemoselective and Long-Lived Hydrogenation Catalysts).
최민기 교수는 "자연계의 효소를 모방해 원하는 반응물만 선택적으로 전환할 수 있으면서도 매우 우수한 안정성을 갖는 촉매 설계 방법은 세계적으로 보고된 바가 없던 새로운 개념"이라면서 "향후 높은 선택도가 있어야 하는 다양한 화학반응에 폭넓게 응용 및 적용될 수 있을 것"이라고 전망했다.
이번 연구는 한국연구재단 중견연구자 지원사업과 LG화학의 지원으로 이뤄졌다.
2020.07.31 조회수 43351