%EC%9C%A0%EC%A0%84%EC%B2%B4
-
 강유전체 활용 차세대 반도체 메모리 혁신
강유전체는 메모리 소자에서 전하를 잘 저장하기 때문에 "전기를 기억하는 소재"와 같다는 특성으로 차세대 반도체 기술 개발에 있어 핵심 소재로 부각되고 있다. 우리 연구진이 이러한 강유전체 소재를 활용해 현재 메모리 반도체 산업의 양대 산맥인 디램(DRAM)과 낸드 플래시(NAND Flash) 메모리의 한계를 극복한 고성능, 고집적 차세대 메모리 소자를 개발하는데 성공했다.
우리 대학 전상훈 교수 연구팀이 하프니아 강유전체 소재*를 활용한 차세대 메모리 및 스토리지 메모리 기술을 개발했다고 6일 밝혔다.
*하프니아 강유전체 소재: 비휘발성 절연막으로, CMOS 공정 호환성, 동작 속도, 내구성 등의 우수한 물리적 특성을 바탕으로 차세대 반도체의 핵심 소재로 활발하게 연구되고 있는 물질
디램 메모리는 우리가 스마트폰, 컴퓨터, USB 등에서 사용하는 데이터를 저장하는 휘발성 메모리다. 휘발성 특성으로 인해, 외부 전력이 끊어지면 저장된 데이터가 손실되지만, 공정 단가가 낮고 집적도가 높아 메인 메모리로 활용돼 왔다. 하지만 디램 메모리 기술은 소자의 크기가 작아질수록 디램 소자가 정보를 저장하는 저장 커패시터의 용량도 작아지게 되고, 더 이상 메모리 동작을 수행하기 어렵다.
연구팀은 저장 커패시터는 정보를 저장하는 디램 기술의 한계를 극복하고자 이러한 저장 커패시터가 물리적으로 작은 면적에서도 높은 저장 용량을 달성할 수 있도록 개선하는 데에 집중했다. 이를 위해 하프니아 강유전체 기반 극박막의 고유전율 물질을 개발했다. 연구 결과 현재까지 보고된 디램 커패시터 중, 가장 낮은 2.4 Å (머리카락 굵기의 약 10만분의 1)의 SiO2(실리콘 산화물) 유효 두께와 같이 얇은 층에 저장하는 것을 달성했다.
또한 연구팀은 디램 메모리 기술을 잠재적으로 대체할 수 있는 후보군으로 주목받고 있는 강유전체 메모리 FRAM 메모리도 개발하였다. 현 DRAM 수준의 1V 이하의 낮은 전압에서도 비 휘발성 정보 저장과 삭제가 확실히 이루어지는 기술은 에너지 효율성을 크게 향상시켜 차세대 메모리에 필수적이다.
디램 메모리 기술에 이어 연구팀은 낸드 플래시 메모리의 한계를 극복할 하프니아 강유전체 기반의 차세대 메모리 기술을 개발했다. 낸드 플래시 메모리는 우리가 스마트폰, 컴퓨터, USB 등에서 사용하는 데이터를 저장하는 비휘발성 메모리이다. 현재, 낸드플래시 메모리의 저장 용량을 늘리기 위해 여러 층을 쌓아 올리는 방식으로 발전해 왔지만, 물리적인 한계로 인해 500층, 1000층 이상으로 쌓기가 어려운 상황이다.
이에 연구팀은 강유전체라는 새로운 소재를 낸드 플래시에 적용하는 방식을 연구한 결과, 소재 계면에 TiO2 층이라는 얇은 층을 추가함으로써 1000단 이상의 수직 적층 3차원이며 외부 환경의 간섭에도 데이터를 안정적으로 유지하도록 설계했다.
마지막으로 기존의 낸드 플래시 기술에서 산화물 채널 기반의 메모리 소자는 데이터를 완전히 지울 수 없는 한계가 있어 새로운 구조의 고성능 산화물 채널 기반 낸드 플래시 소자를 개발하는 데 성공했다. 이 소자는 더 많은 데이터를 저장할 수 있고 데이터를 10년 이상 안정적으로 보존할 수 있는 특징을 가진다.
전상훈 교수는 “이번 연구 결과들은 스케일링 이슈로 인해 답보상태에 있는 메모리 반도체 기술 개발에 돌파구가 되는 기술이 될 것으로 판단되며, 향후 다양한 인공지능 컴퓨팅 및 엣지 컴퓨팅 기술 상용화에 기여할 수 있을 것”이라고 설명했다.
벤카테스왈루 가담(Venkateswarlu Gaddam) 연구 교수, 김기욱 박사 과정, 조홍래 박사 과정, 황정현 박사 과정, 이상호 박사 과정, 최효준 석사 과정, 강현준 석사 과정이 공동 제1 저자로 참여했고 이러한 연구 성과를 국제적으로 인정받아 반도체 산업계 최고 수준의(Top-tier) 컨퍼런스에 2024년 5편의 논문을 발표했다. (2024 VLSI 2편, 2024 IEDM 3편)
- In-depth analysis of the Hafnia ferroelectrics as a key enabler for low voltage & QLC 3D VNAND beyond 1K layers: Experimental demonstration and modeling VLSI 24 DOI: 10.1109/VLSITechnologyandCir46783.2024
- Low-Damage Processed and High-Pressure Annealed High-k Hafnium Zirconium Oxide Capacitors near Morphotropic Phase Boundary with Record-Low EOT of 2.4 Å & high-k of 70 for DRAM … VLSI 24 DOI: 10.1109/VLSITechnologyandCir46783.2024
- Unveiling the Origin of Disturbance in FeFET and the Potential of Multifunctional TiO2 as a Breakthrough for Disturb-free 3D NAND Cell: Experimental and Modeling https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=4
- Oxide Channel Ferroelectric NAND Device with Source- tied Covering Metal Structure: Wide Memory Window (14.3 V), Reliable Retention (> 10 years) and Disturbance Immunity (△Vth ≤ 0.1 V) for QLC Operation
https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=47
- Design Methodology for Low-Voltage Operational (≤1 V) FRAM Cell Capacitors and Approaches for Overcoming Disturb Issues in 1T-nC Arrays: Experimental & Modeling:
https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=54
참고로, IEEE VLSI와 IEEE IEDM 학회는 삼성전자, SK 하이닉스, 마이크론, 인텔 등 굴지의 반도체 업계와 세계적인 석학들이 최신 기술 개발을 공유하고 미래 기술의 지향점을 논의하는 학회로 반도체 올림픽이라고 불린다.
한편, 이 연구는 삼성전자, 한양대학교와 협업을 통해서 수행되었으며, 한국산업기술평가원 (KEIT) 민관공동투자 반도체 고급인력양성사업, 과학기술정보통신부 혁신연구센터(IRC) 지원 사업, 삼성전자(Samsung Electronics)의 지원을 받아 진행됐다.
2025.01.06 조회수 6157
강유전체 활용 차세대 반도체 메모리 혁신
강유전체는 메모리 소자에서 전하를 잘 저장하기 때문에 "전기를 기억하는 소재"와 같다는 특성으로 차세대 반도체 기술 개발에 있어 핵심 소재로 부각되고 있다. 우리 연구진이 이러한 강유전체 소재를 활용해 현재 메모리 반도체 산업의 양대 산맥인 디램(DRAM)과 낸드 플래시(NAND Flash) 메모리의 한계를 극복한 고성능, 고집적 차세대 메모리 소자를 개발하는데 성공했다.
우리 대학 전상훈 교수 연구팀이 하프니아 강유전체 소재*를 활용한 차세대 메모리 및 스토리지 메모리 기술을 개발했다고 6일 밝혔다.
*하프니아 강유전체 소재: 비휘발성 절연막으로, CMOS 공정 호환성, 동작 속도, 내구성 등의 우수한 물리적 특성을 바탕으로 차세대 반도체의 핵심 소재로 활발하게 연구되고 있는 물질
디램 메모리는 우리가 스마트폰, 컴퓨터, USB 등에서 사용하는 데이터를 저장하는 휘발성 메모리다. 휘발성 특성으로 인해, 외부 전력이 끊어지면 저장된 데이터가 손실되지만, 공정 단가가 낮고 집적도가 높아 메인 메모리로 활용돼 왔다. 하지만 디램 메모리 기술은 소자의 크기가 작아질수록 디램 소자가 정보를 저장하는 저장 커패시터의 용량도 작아지게 되고, 더 이상 메모리 동작을 수행하기 어렵다.
연구팀은 저장 커패시터는 정보를 저장하는 디램 기술의 한계를 극복하고자 이러한 저장 커패시터가 물리적으로 작은 면적에서도 높은 저장 용량을 달성할 수 있도록 개선하는 데에 집중했다. 이를 위해 하프니아 강유전체 기반 극박막의 고유전율 물질을 개발했다. 연구 결과 현재까지 보고된 디램 커패시터 중, 가장 낮은 2.4 Å (머리카락 굵기의 약 10만분의 1)의 SiO2(실리콘 산화물) 유효 두께와 같이 얇은 층에 저장하는 것을 달성했다.
또한 연구팀은 디램 메모리 기술을 잠재적으로 대체할 수 있는 후보군으로 주목받고 있는 강유전체 메모리 FRAM 메모리도 개발하였다. 현 DRAM 수준의 1V 이하의 낮은 전압에서도 비 휘발성 정보 저장과 삭제가 확실히 이루어지는 기술은 에너지 효율성을 크게 향상시켜 차세대 메모리에 필수적이다.
디램 메모리 기술에 이어 연구팀은 낸드 플래시 메모리의 한계를 극복할 하프니아 강유전체 기반의 차세대 메모리 기술을 개발했다. 낸드 플래시 메모리는 우리가 스마트폰, 컴퓨터, USB 등에서 사용하는 데이터를 저장하는 비휘발성 메모리이다. 현재, 낸드플래시 메모리의 저장 용량을 늘리기 위해 여러 층을 쌓아 올리는 방식으로 발전해 왔지만, 물리적인 한계로 인해 500층, 1000층 이상으로 쌓기가 어려운 상황이다.
이에 연구팀은 강유전체라는 새로운 소재를 낸드 플래시에 적용하는 방식을 연구한 결과, 소재 계면에 TiO2 층이라는 얇은 층을 추가함으로써 1000단 이상의 수직 적층 3차원이며 외부 환경의 간섭에도 데이터를 안정적으로 유지하도록 설계했다.
마지막으로 기존의 낸드 플래시 기술에서 산화물 채널 기반의 메모리 소자는 데이터를 완전히 지울 수 없는 한계가 있어 새로운 구조의 고성능 산화물 채널 기반 낸드 플래시 소자를 개발하는 데 성공했다. 이 소자는 더 많은 데이터를 저장할 수 있고 데이터를 10년 이상 안정적으로 보존할 수 있는 특징을 가진다.
전상훈 교수는 “이번 연구 결과들은 스케일링 이슈로 인해 답보상태에 있는 메모리 반도체 기술 개발에 돌파구가 되는 기술이 될 것으로 판단되며, 향후 다양한 인공지능 컴퓨팅 및 엣지 컴퓨팅 기술 상용화에 기여할 수 있을 것”이라고 설명했다.
벤카테스왈루 가담(Venkateswarlu Gaddam) 연구 교수, 김기욱 박사 과정, 조홍래 박사 과정, 황정현 박사 과정, 이상호 박사 과정, 최효준 석사 과정, 강현준 석사 과정이 공동 제1 저자로 참여했고 이러한 연구 성과를 국제적으로 인정받아 반도체 산업계 최고 수준의(Top-tier) 컨퍼런스에 2024년 5편의 논문을 발표했다. (2024 VLSI 2편, 2024 IEDM 3편)
- In-depth analysis of the Hafnia ferroelectrics as a key enabler for low voltage & QLC 3D VNAND beyond 1K layers: Experimental demonstration and modeling VLSI 24 DOI: 10.1109/VLSITechnologyandCir46783.2024
- Low-Damage Processed and High-Pressure Annealed High-k Hafnium Zirconium Oxide Capacitors near Morphotropic Phase Boundary with Record-Low EOT of 2.4 Å & high-k of 70 for DRAM … VLSI 24 DOI: 10.1109/VLSITechnologyandCir46783.2024
- Unveiling the Origin of Disturbance in FeFET and the Potential of Multifunctional TiO2 as a Breakthrough for Disturb-free 3D NAND Cell: Experimental and Modeling https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=4
- Oxide Channel Ferroelectric NAND Device with Source- tied Covering Metal Structure: Wide Memory Window (14.3 V), Reliable Retention (> 10 years) and Disturbance Immunity (△Vth ≤ 0.1 V) for QLC Operation
https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=47
- Design Methodology for Low-Voltage Operational (≤1 V) FRAM Cell Capacitors and Approaches for Overcoming Disturb Issues in 1T-nC Arrays: Experimental & Modeling:
https://iedm24.mapyourshow.com/8_0/sessions/session-details.cfm?scheduleid=54
참고로, IEEE VLSI와 IEEE IEDM 학회는 삼성전자, SK 하이닉스, 마이크론, 인텔 등 굴지의 반도체 업계와 세계적인 석학들이 최신 기술 개발을 공유하고 미래 기술의 지향점을 논의하는 학회로 반도체 올림픽이라고 불린다.
한편, 이 연구는 삼성전자, 한양대학교와 협업을 통해서 수행되었으며, 한국산업기술평가원 (KEIT) 민관공동투자 반도체 고급인력양성사업, 과학기술정보통신부 혁신연구센터(IRC) 지원 사업, 삼성전자(Samsung Electronics)의 지원을 받아 진행됐다.
2025.01.06 조회수 6157 -
 미토콘드리아 DNA 돌연변이를 밝혀내다
우리 몸의 세포는 평생 동안 DNA 돌연변이를 지속적으로 축적하며, 이는 세포 간의 유전적 다양성(모자이시즘) 및 세포 노화를 초래한다. 한국 연구진이 세포소기관 미토콘드리아 DNA의 인체 내 모자이시즘 현상을 최초로 규명했다.
우리 대학 의과학대학원 주영석 교수 연구팀 안지송 박사과정이 미토콘드리아 DNA 돌연변이 연구를 주도해 국제 과학학술지 ‘네이처 지네틱스(Nature Genetics)’ 7월 22일 字 온라인판에 게재했다고 24일 밝혔다. (논문명: Mitochondrial DNA mosaicism in normal human somatic cells).
이번 연구에는 서울대학교 의과대학, 연세대학교 의과대학, 고려대학교 의과대학, 국립암센터, 그리고 KAIST 교원창업기업 이노크라스의 연구자들도 참여했다.
미토콘드리아는 세포 에너지 대사 및 사멸에 관여하는 세포소기관으로, 세포핵과 독립적으로 자체 DNA를 가지고 있으며 돌연변이도 발생할 수 있다. 하지만 이러한 돌연변이를 정밀하게 찾아내는 데 필수적인 단일세포 전장유전체(whole-genome sequencing) 기술의 한계로 그동안 미토콘드리아 DNA 돌연변이 및 모자이시즘에 대한 연구는 미흡했다.
연구팀은 31명의 정상 대장 상피 조직, 섬유아세포, 혈액에서 확보한 총 2,096개 단일세포의 전장 유전체 서열을 생명정보학 기법으로 분석해 세계 최대 규모의 연구를 수행했다. 세포 사이에서는 평균적으로 3개의 유의미한 미토콘드리아 DNA 차이가 존재했으며, 대부분은 노화 과정에서 생성됐으나 약 6%의 차이는 모계로부터 이형상태(헤테로플라스미; heteroplasmy)로 전달됨이 확인됐다.
또한, 암 발생 과정에서 돌연변이 수가 유의미하게 증가했으며, 이들 변이 중 일부는 미토콘드리아 RNA 불안정성에 기여한다는 사실도 확인했다. 관찰된 데이터를 바탕으로 연구팀은 인간의 배아 발생단계부터 노화 및 발암 과정에서의 미토콘드리아 발생 및 진화 과정을 이해할 수 있는 모델을 구축했다.
이번 연구는 사람의 정상 세포에서 발생하는 미토콘드리아 DNA 돌연변이의 형성 메커니즘을 체계적으로 밝혀내, 향후 미토콘드리아 DNA가 노화와 질병 발생에 미치는 영향을 이해하는 데 중요한 초석을 제공할 수 있을 것으로 기대된다.
의과학대학원 주영석 교수는 “전장유전체 빅데이터를 체계적으로 활용함으로써 미지의 영역이었던 생명과학 현상을 규명할 수 있다”며, “암 발생 과정뿐만 아니라 인간의 배아 발생과정 및 노화과정에서 나타나는 미토콘드리아 DNA의 변화를 체계적으로 이해할 수 있는 방법을 처음으로 수립했다” 라고 연구의 중요성을 설명했다.
한편 이번 연구는 한국연구재단 리더연구, 선도연구센터 및 서경배과학재단 신진과학자 연구지원 사업의 지원을 받아 수행됐다.
2024.07.24 조회수 7437
미토콘드리아 DNA 돌연변이를 밝혀내다
우리 몸의 세포는 평생 동안 DNA 돌연변이를 지속적으로 축적하며, 이는 세포 간의 유전적 다양성(모자이시즘) 및 세포 노화를 초래한다. 한국 연구진이 세포소기관 미토콘드리아 DNA의 인체 내 모자이시즘 현상을 최초로 규명했다.
우리 대학 의과학대학원 주영석 교수 연구팀 안지송 박사과정이 미토콘드리아 DNA 돌연변이 연구를 주도해 국제 과학학술지 ‘네이처 지네틱스(Nature Genetics)’ 7월 22일 字 온라인판에 게재했다고 24일 밝혔다. (논문명: Mitochondrial DNA mosaicism in normal human somatic cells).
이번 연구에는 서울대학교 의과대학, 연세대학교 의과대학, 고려대학교 의과대학, 국립암센터, 그리고 KAIST 교원창업기업 이노크라스의 연구자들도 참여했다.
미토콘드리아는 세포 에너지 대사 및 사멸에 관여하는 세포소기관으로, 세포핵과 독립적으로 자체 DNA를 가지고 있으며 돌연변이도 발생할 수 있다. 하지만 이러한 돌연변이를 정밀하게 찾아내는 데 필수적인 단일세포 전장유전체(whole-genome sequencing) 기술의 한계로 그동안 미토콘드리아 DNA 돌연변이 및 모자이시즘에 대한 연구는 미흡했다.
연구팀은 31명의 정상 대장 상피 조직, 섬유아세포, 혈액에서 확보한 총 2,096개 단일세포의 전장 유전체 서열을 생명정보학 기법으로 분석해 세계 최대 규모의 연구를 수행했다. 세포 사이에서는 평균적으로 3개의 유의미한 미토콘드리아 DNA 차이가 존재했으며, 대부분은 노화 과정에서 생성됐으나 약 6%의 차이는 모계로부터 이형상태(헤테로플라스미; heteroplasmy)로 전달됨이 확인됐다.
또한, 암 발생 과정에서 돌연변이 수가 유의미하게 증가했으며, 이들 변이 중 일부는 미토콘드리아 RNA 불안정성에 기여한다는 사실도 확인했다. 관찰된 데이터를 바탕으로 연구팀은 인간의 배아 발생단계부터 노화 및 발암 과정에서의 미토콘드리아 발생 및 진화 과정을 이해할 수 있는 모델을 구축했다.
이번 연구는 사람의 정상 세포에서 발생하는 미토콘드리아 DNA 돌연변이의 형성 메커니즘을 체계적으로 밝혀내, 향후 미토콘드리아 DNA가 노화와 질병 발생에 미치는 영향을 이해하는 데 중요한 초석을 제공할 수 있을 것으로 기대된다.
의과학대학원 주영석 교수는 “전장유전체 빅데이터를 체계적으로 활용함으로써 미지의 영역이었던 생명과학 현상을 규명할 수 있다”며, “암 발생 과정뿐만 아니라 인간의 배아 발생과정 및 노화과정에서 나타나는 미토콘드리아 DNA의 변화를 체계적으로 이해할 수 있는 방법을 처음으로 수립했다” 라고 연구의 중요성을 설명했다.
한편 이번 연구는 한국연구재단 리더연구, 선도연구센터 및 서경배과학재단 신진과학자 연구지원 사업의 지원을 받아 수행됐다.
2024.07.24 조회수 7437 -
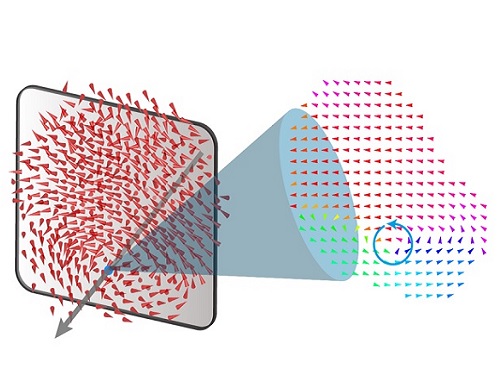 강유전체 ‘3차원 소용돌이’ 20년 난제 풀어
약 20년 전 아주 작은 나노 크기 0차원 강유전체 내부에 특이한 형태의 분극 분포가 발생할 수 있음이 로랑 벨라이쉬(Laurent Bellaiche) 교수(現 미국 아칸소대 물리학과 교수) 연구진에 의해 이론적으로 예측됐다. 해당 소용돌이 분포를 적절히 제어하면 기존에 비해 10,000배 이상 높은 용량의 초고밀도 메모리 소자로 응용이 가능할 것이라는 가능성이 제시돼 학계의 이목을 끌었으나, 3차원 분극 분포 측정의 어려움으로 인해 실험적인 규명이 되지 못하고 있었다.
우리 대학 물리학과 양용수 교수 연구팀이 포항공과대학교, 서울대학교, 한국기초과학지원연구원과의 공동연구 및 미국 로런스 버클리 국립연구소, 아칸소대학교 연구진과의 국제협력 연구를 통해 나노강유전체 내부의 3차원 소용돌이 형태 분극 분포를 최초로 실험적으로 규명하였다고 30일 밝혔다.
영구자석과 같이 외부의 자기장이 없어도 자화 상태를 스스로 유지할 수 있는 물질들을 강자성체(ferromagnet)라 하고, 강유전체(ferroelectric)는 외부의 전기장 없어도 분극상태를 유지할 수 있는 물질로서 강자성체의 전기(electric) 버전이라고 생각하면 된다. 강자성체(자석)의 경우 나노 크기로 너무 작게 만들면 일정 이하 크기에서는 자석으로서의 성질을 잃어버린다는 것이 잘 알려져 있는 반면, 강유전체를 모든 방향에서 아주 작게 나노 크기로 만들면(즉 0차원 구조를 만들면) 어떤 현상이 발생하는지는 오랜 기간 논란거리였다.
인체 내부 장기들을 3차원적으로 보기 위해 병원에서 CT 촬영을 하는 것과 동일한 방식으로, 양용수 교수 연구팀은 전자현미경을 이용해 다양한 각도에서 투과전자현미경 이미지를 획득하고, 이를 고급화된 재구성 알고리즘을 통해 3차원으로 재구성하는 방식으로 원자 분해능 전자토모그래피 기술을 개발 및 응용하였다.
이를 통해 연구팀은 강유전체인 바륨-티타늄 산화물(BaTiO3) 나노입자 내부 원자들의 위치를 3차원적으로 완전히 측정하고, 내부의 3차원적 분극 분포 또한 단일 원자 단위로 규명했다. 분극 분포 분석 결과, 20년 전에 이론적으로 예측됐던 대로 강유전체 내부에 소용돌이를 비롯한 다양한 위상학적 분극 분포가 발생하고, 강유전체의 크기에 따라 내부 소용돌이의 개수 또한 제어할 수 있다는 사실을 연구팀은 최초로 실험적으로 밝힐 수 있었다.
연구팀은 이 결과를 바탕으로 20년 전 해당 소용돌이 분극 이론을 최초 제시했던 벨라이쉬(Bellaiche) 교수와 국제공동연구를 수행했고, 실험에서 얻은 소용돌이 분포 결과가 이론적인 계산으로도 잘 설명됨을 추가적으로 증명했다.
연구를 주도한 양용수 교수는 "이번 결과는 기판의 유/무나 주변 환경에 무관하게 강유전체 크기와 형태를 적절히 조절하는 것만으로도 나노 크기에서 강유전성 소용돌이를 제어할 수 있음을 시사하였다. 아울러, 이러한 분극 분포 소용돌이의 개수 및 회전 방향을 조절함으로써 기존보다 약 10,000배 이상 많은 양의 정보를 같은 크기의 소자에 저장할 수 있는 차세대 고밀도 메모리 소자 기술로 발전시킬 수 있을 것으로 기대한다” 라고 말했다.
물리학과 정채화 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)' 에 지난 5월 8일 字 게재됐다. (논문명 : Revealing the Three-Dimensional Arrangement of Polar Topology in Nanoparticles).
한편 이번 연구는 한국연구재단 개인기초연구지원사업 및 KAIST 특이점교수사업의 지원을 받아 수행됐다.
2024.05.30 조회수 7422
강유전체 ‘3차원 소용돌이’ 20년 난제 풀어
약 20년 전 아주 작은 나노 크기 0차원 강유전체 내부에 특이한 형태의 분극 분포가 발생할 수 있음이 로랑 벨라이쉬(Laurent Bellaiche) 교수(現 미국 아칸소대 물리학과 교수) 연구진에 의해 이론적으로 예측됐다. 해당 소용돌이 분포를 적절히 제어하면 기존에 비해 10,000배 이상 높은 용량의 초고밀도 메모리 소자로 응용이 가능할 것이라는 가능성이 제시돼 학계의 이목을 끌었으나, 3차원 분극 분포 측정의 어려움으로 인해 실험적인 규명이 되지 못하고 있었다.
우리 대학 물리학과 양용수 교수 연구팀이 포항공과대학교, 서울대학교, 한국기초과학지원연구원과의 공동연구 및 미국 로런스 버클리 국립연구소, 아칸소대학교 연구진과의 국제협력 연구를 통해 나노강유전체 내부의 3차원 소용돌이 형태 분극 분포를 최초로 실험적으로 규명하였다고 30일 밝혔다.
영구자석과 같이 외부의 자기장이 없어도 자화 상태를 스스로 유지할 수 있는 물질들을 강자성체(ferromagnet)라 하고, 강유전체(ferroelectric)는 외부의 전기장 없어도 분극상태를 유지할 수 있는 물질로서 강자성체의 전기(electric) 버전이라고 생각하면 된다. 강자성체(자석)의 경우 나노 크기로 너무 작게 만들면 일정 이하 크기에서는 자석으로서의 성질을 잃어버린다는 것이 잘 알려져 있는 반면, 강유전체를 모든 방향에서 아주 작게 나노 크기로 만들면(즉 0차원 구조를 만들면) 어떤 현상이 발생하는지는 오랜 기간 논란거리였다.
인체 내부 장기들을 3차원적으로 보기 위해 병원에서 CT 촬영을 하는 것과 동일한 방식으로, 양용수 교수 연구팀은 전자현미경을 이용해 다양한 각도에서 투과전자현미경 이미지를 획득하고, 이를 고급화된 재구성 알고리즘을 통해 3차원으로 재구성하는 방식으로 원자 분해능 전자토모그래피 기술을 개발 및 응용하였다.
이를 통해 연구팀은 강유전체인 바륨-티타늄 산화물(BaTiO3) 나노입자 내부 원자들의 위치를 3차원적으로 완전히 측정하고, 내부의 3차원적 분극 분포 또한 단일 원자 단위로 규명했다. 분극 분포 분석 결과, 20년 전에 이론적으로 예측됐던 대로 강유전체 내부에 소용돌이를 비롯한 다양한 위상학적 분극 분포가 발생하고, 강유전체의 크기에 따라 내부 소용돌이의 개수 또한 제어할 수 있다는 사실을 연구팀은 최초로 실험적으로 밝힐 수 있었다.
연구팀은 이 결과를 바탕으로 20년 전 해당 소용돌이 분극 이론을 최초 제시했던 벨라이쉬(Bellaiche) 교수와 국제공동연구를 수행했고, 실험에서 얻은 소용돌이 분포 결과가 이론적인 계산으로도 잘 설명됨을 추가적으로 증명했다.
연구를 주도한 양용수 교수는 "이번 결과는 기판의 유/무나 주변 환경에 무관하게 강유전체 크기와 형태를 적절히 조절하는 것만으로도 나노 크기에서 강유전성 소용돌이를 제어할 수 있음을 시사하였다. 아울러, 이러한 분극 분포 소용돌이의 개수 및 회전 방향을 조절함으로써 기존보다 약 10,000배 이상 많은 양의 정보를 같은 크기의 소자에 저장할 수 있는 차세대 고밀도 메모리 소자 기술로 발전시킬 수 있을 것으로 기대한다” 라고 말했다.
물리학과 정채화 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)' 에 지난 5월 8일 字 게재됐다. (논문명 : Revealing the Three-Dimensional Arrangement of Polar Topology in Nanoparticles).
한편 이번 연구는 한국연구재단 개인기초연구지원사업 및 KAIST 특이점교수사업의 지원을 받아 수행됐다.
2024.05.30 조회수 7422 -
 제30회 삼성휴먼테크논문대상에서 물리학과 정채화 학생 은상 수상
제30회 삼성휴먼테크논문대상에서 우리 대학 물리학과 정채화 학생(지도교수 : 물리학과 양용수 교수)이 기초과학분야 은상을 수상했다.
삼성휴먼테크논문대상은 과학기술 분야의 주역이 될 젊고 우수한 과학자를 발굴하기 위해 1994년부터 시행 중이며 과학기술정보통신부와 중앙일보가 공동 후원하고 있다. 이번 제30회 대회에는 총 1189편의 논문이 접수되었으며, 797명에 달하는 전문가들이 심사를 진행하였다.
정채화 학생은 2000년대 초반 이론적으로만 예측되었으나 20년 이상 풀리지 않았던 난제인 0차원 강유전체에서의 위상학적 분극 정렬을 세계 최초로 실험적으로 규명하였다. 영구자석과 같이 외부의 자기장이 없어도 자화 상태를 스스로 유지할 수 있는 물질들을 강자성체(ferromagnet)라 하고, 강유전체(ferroelectric)는 외부의 전기장 없어도 분극상태를 유지할 수 있는 물질로서 강자성체의 전기(electric) 버전이라고 생각하면 된다. 강자성체(자석)의 경우 나노크기로 너무 작게 만들면 일정 이하 크기에서는 자석으로서의 성질을 잃어버린다는 것이 잘 알려져 있는데, 강유전체를 모든 방향에서 아주 작게 나노크기로 만들면(즉 0차원 구조를 만들면) 어떤 현상이 발생하는지는 오랜 기간 학계의 논란거리였다.
정채화 학생은 원자 분해능 전자토모그래피(Atomic Electron Tomography) 실험을 통해 나노크기 0차원 강유전체 내부에서는 소용돌이와 같은 형태의 위상학적 분극분포가 발생하고, 강유전체의 크기에 따라 내부 소용돌이의 개수가 달라진다는 사실을 최초로 실험적으로 규명하였다.
정채화 학생의 연구결과를 응용하여 이러한 분극분포 소용돌이의 회전 방향을 조절함으로써 기존보다 약 1,000배 이상 많은 양의 정보를 같은 크기의 소자에 저장할 수 있는 차세대 고밀도 소자기술로 발전시킬 수 있을 것으로 기대된다.
2024.04.04 조회수 5699
제30회 삼성휴먼테크논문대상에서 물리학과 정채화 학생 은상 수상
제30회 삼성휴먼테크논문대상에서 우리 대학 물리학과 정채화 학생(지도교수 : 물리학과 양용수 교수)이 기초과학분야 은상을 수상했다.
삼성휴먼테크논문대상은 과학기술 분야의 주역이 될 젊고 우수한 과학자를 발굴하기 위해 1994년부터 시행 중이며 과학기술정보통신부와 중앙일보가 공동 후원하고 있다. 이번 제30회 대회에는 총 1189편의 논문이 접수되었으며, 797명에 달하는 전문가들이 심사를 진행하였다.
정채화 학생은 2000년대 초반 이론적으로만 예측되었으나 20년 이상 풀리지 않았던 난제인 0차원 강유전체에서의 위상학적 분극 정렬을 세계 최초로 실험적으로 규명하였다. 영구자석과 같이 외부의 자기장이 없어도 자화 상태를 스스로 유지할 수 있는 물질들을 강자성체(ferromagnet)라 하고, 강유전체(ferroelectric)는 외부의 전기장 없어도 분극상태를 유지할 수 있는 물질로서 강자성체의 전기(electric) 버전이라고 생각하면 된다. 강자성체(자석)의 경우 나노크기로 너무 작게 만들면 일정 이하 크기에서는 자석으로서의 성질을 잃어버린다는 것이 잘 알려져 있는데, 강유전체를 모든 방향에서 아주 작게 나노크기로 만들면(즉 0차원 구조를 만들면) 어떤 현상이 발생하는지는 오랜 기간 학계의 논란거리였다.
정채화 학생은 원자 분해능 전자토모그래피(Atomic Electron Tomography) 실험을 통해 나노크기 0차원 강유전체 내부에서는 소용돌이와 같은 형태의 위상학적 분극분포가 발생하고, 강유전체의 크기에 따라 내부 소용돌이의 개수가 달라진다는 사실을 최초로 실험적으로 규명하였다.
정채화 학생의 연구결과를 응용하여 이러한 분극분포 소용돌이의 회전 방향을 조절함으로써 기존보다 약 1,000배 이상 많은 양의 정보를 같은 크기의 소자에 저장할 수 있는 차세대 고밀도 소자기술로 발전시킬 수 있을 것으로 기대된다.
2024.04.04 조회수 5699 -
 화학물질 없이 식각하는 반도체 기술 최초 개발
차세대 반도체 메모리의 소재로 주목을 받고 있는 강유전체는 차세대 메모리 소자 혹은 작은 물리적 변화를 감지하는 센서로 활용되는 등 그 중요성이 커지고 있다. 이에 반도체의 핵심 소자가 되는 강유전체를 화학물질없이 식각할 수 있는 연구를 성공해 화제다.
우리 대학 신소재공학과 홍승범 교수가 제네바 대학교와 국제공동연구를 통해 강유전체 표면의 비대칭 마멸* 현상을 세계 최초로 관찰 및 규명했고, 이를 활용해 혁신적인 나노 패터닝 기술**을 개발했다고 26일 밝혔다.
*마멸: 물체 표면의 재료가 점진적으로 손실 또는 제거되는 현상
**나노 패터닝 기술: 나노스케일로 소재의 표면에 정밀한 패턴을 생성하여 다양한 첨단 기술 분야에서 제품 성능을 향상시키는데 사용되는 기술
연구팀은 강유전체 소재의 표면 특성에 관한 연구에 집중했다. 이들은 원자간력 현미경(Atomic Force Microscopy)을 활용해 다양한 강유전체의 트라이볼로지(Tribology, 마찰 및 마모) 현상을 관찰했고, 강유전체의 전기적인 분극* 방향에 따라 마찰되거나 마모되는 특성이 다르다는 것을 세계 최초로 발견했다. (그림 1) 아울러, 이러한 분극 방향에 따라 달라지는 트라이볼로지의 원인으로 변전 효과(Flexoelectric effect)*에 주목했다.
*전기적 분극(electric dipole): 자석의 북극과 남극처럼 전기적으로 양극과 음극이 있는 것을 의미함
*변전 효과: 물질이 휘어졌을 때 분극이 발생하는 현상이지만, 거시 규모에서 물질을 구부렸을 때 유도되는 분극의 크기가 매우 작아 그동안 큰 주목을 받지 못했다. 그러나 2010년대 들어서 물질이 나노스케일로 미세화될 경우, 매우 큰 변전 효과가 발생할 수 있다는 연구 결과가 나오면서 많은 연구자의 주목을 받기 시작했다.
연구진은 강유전체의 트라이볼로지 특성이 나노 단위에서 강한 응력이 가해질 때 발생하는 변전 효과로 인해 강유전체 내부의 분극 방향에 따른 상호작용으로 트라이볼로지 특성이 바뀌게 된다는 것을 발견했다. 또한 이러한 새로운 강유전체 트라이볼로지 현상을 소재의 나노 패터닝에 응용했다.
이러한 패터닝 방식은 기존의 반도체 패터닝 방식과는 다르게 화학 물질 및 고비용의 리소그래피 장비가 필요하지 않고, 기존 공정 대비 매우 빠르게 나노 구조를 제작할 수 있는 장점이 있다.
이번 연구의 제1 저자인 신소재공학과 졸업생 조성우 박사는 “이번 연구는 세계 최초로 강유전체 비대칭 트라이볼로지를 관찰하고 규명한 데 의의가 있고, 이러한 분극에 민감한 트라이볼로지 비대칭성이 다양한 화학적 구성 및 결정 구조를 가진 강유전체에서 널리 적용될 수 있어 많은 후속 연구를 기대할 수 있다”고 밝혔다.
공동교신저자로 본 연구를 공동 지도한 제네바 대학교 파루치(Paruch) 교수는 “변전 효과를 통해 강유전체의 도메인이 분극 방향에 따라 서로 다른 표면 특성을 나타내는 것을 활용함으로써, 다양하고 유용한 기술들을 개발할 수 있을 것이다”며 이번 연구가 앞으로 뻗어나갈 분야에 대한 강한 자신감을 피력했다.
연구를 이끈 홍승범 교수는 “이번 연구에서 개발된 패터닝 기술은 기존 반도체 공정에서 쓰이는 패터닝 공정과 달리 화학 물질을 사용하지 않고, 매우 낮은 비용으로 대면적 나노 구조를 만들 수 있어 산업적으로 활용될 수 있는 잠재력을 가지고 있다”고 전망했다.
한편, 이번 연구는 한국연구재단(2020R1A2C2012078, NRF-2022K1A4A7A04095892, RS-2023-00247245), KAIST 글로벌특이점 사업의 지원 및 스위스, 스페인 연구진과의 국제공동연구를 통해 수행됐으며, 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 1월 9일 자 출판됐다. (논문 제목: Switchable tribology of ferroelectrics)
2024.03.26 조회수 9283
화학물질 없이 식각하는 반도체 기술 최초 개발
차세대 반도체 메모리의 소재로 주목을 받고 있는 강유전체는 차세대 메모리 소자 혹은 작은 물리적 변화를 감지하는 센서로 활용되는 등 그 중요성이 커지고 있다. 이에 반도체의 핵심 소자가 되는 강유전체를 화학물질없이 식각할 수 있는 연구를 성공해 화제다.
우리 대학 신소재공학과 홍승범 교수가 제네바 대학교와 국제공동연구를 통해 강유전체 표면의 비대칭 마멸* 현상을 세계 최초로 관찰 및 규명했고, 이를 활용해 혁신적인 나노 패터닝 기술**을 개발했다고 26일 밝혔다.
*마멸: 물체 표면의 재료가 점진적으로 손실 또는 제거되는 현상
**나노 패터닝 기술: 나노스케일로 소재의 표면에 정밀한 패턴을 생성하여 다양한 첨단 기술 분야에서 제품 성능을 향상시키는데 사용되는 기술
연구팀은 강유전체 소재의 표면 특성에 관한 연구에 집중했다. 이들은 원자간력 현미경(Atomic Force Microscopy)을 활용해 다양한 강유전체의 트라이볼로지(Tribology, 마찰 및 마모) 현상을 관찰했고, 강유전체의 전기적인 분극* 방향에 따라 마찰되거나 마모되는 특성이 다르다는 것을 세계 최초로 발견했다. (그림 1) 아울러, 이러한 분극 방향에 따라 달라지는 트라이볼로지의 원인으로 변전 효과(Flexoelectric effect)*에 주목했다.
*전기적 분극(electric dipole): 자석의 북극과 남극처럼 전기적으로 양극과 음극이 있는 것을 의미함
*변전 효과: 물질이 휘어졌을 때 분극이 발생하는 현상이지만, 거시 규모에서 물질을 구부렸을 때 유도되는 분극의 크기가 매우 작아 그동안 큰 주목을 받지 못했다. 그러나 2010년대 들어서 물질이 나노스케일로 미세화될 경우, 매우 큰 변전 효과가 발생할 수 있다는 연구 결과가 나오면서 많은 연구자의 주목을 받기 시작했다.
연구진은 강유전체의 트라이볼로지 특성이 나노 단위에서 강한 응력이 가해질 때 발생하는 변전 효과로 인해 강유전체 내부의 분극 방향에 따른 상호작용으로 트라이볼로지 특성이 바뀌게 된다는 것을 발견했다. 또한 이러한 새로운 강유전체 트라이볼로지 현상을 소재의 나노 패터닝에 응용했다.
이러한 패터닝 방식은 기존의 반도체 패터닝 방식과는 다르게 화학 물질 및 고비용의 리소그래피 장비가 필요하지 않고, 기존 공정 대비 매우 빠르게 나노 구조를 제작할 수 있는 장점이 있다.
이번 연구의 제1 저자인 신소재공학과 졸업생 조성우 박사는 “이번 연구는 세계 최초로 강유전체 비대칭 트라이볼로지를 관찰하고 규명한 데 의의가 있고, 이러한 분극에 민감한 트라이볼로지 비대칭성이 다양한 화학적 구성 및 결정 구조를 가진 강유전체에서 널리 적용될 수 있어 많은 후속 연구를 기대할 수 있다”고 밝혔다.
공동교신저자로 본 연구를 공동 지도한 제네바 대학교 파루치(Paruch) 교수는 “변전 효과를 통해 강유전체의 도메인이 분극 방향에 따라 서로 다른 표면 특성을 나타내는 것을 활용함으로써, 다양하고 유용한 기술들을 개발할 수 있을 것이다”며 이번 연구가 앞으로 뻗어나갈 분야에 대한 강한 자신감을 피력했다.
연구를 이끈 홍승범 교수는 “이번 연구에서 개발된 패터닝 기술은 기존 반도체 공정에서 쓰이는 패터닝 공정과 달리 화학 물질을 사용하지 않고, 매우 낮은 비용으로 대면적 나노 구조를 만들 수 있어 산업적으로 활용될 수 있는 잠재력을 가지고 있다”고 전망했다.
한편, 이번 연구는 한국연구재단(2020R1A2C2012078, NRF-2022K1A4A7A04095892, RS-2023-00247245), KAIST 글로벌특이점 사업의 지원 및 스위스, 스페인 연구진과의 국제공동연구를 통해 수행됐으며, 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 1월 9일 자 출판됐다. (논문 제목: Switchable tribology of ferroelectrics)
2024.03.26 조회수 9283 -
 방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
2024.02.15 조회수 7450
방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
2024.02.15 조회수 7450 -
 정크 DNA가 노화와 발암에 관여한다
인간 유전체 중 일반적인 단백질 생성 유전자는 전체 염기서열의 1% 정도에 불과하며 나머지 99%의 유전체 영역은 그 기능이 뚜렷하게 알려지지 않아 ‘쓸모없는 DNA’라는 뜻으로 ‘정크 DNA’라고 불리고 있다. 정크 DNA 가운데 약 1/6을 차지하는 L1 점핑 유전자는 활성화될 경우 세포의 유전정보를 파괴하거나 교란하는 역할을 할 수 있어 사람의 진화 과정에서 불활성화(화석화) 됐다고 알려져 있었다. 하지만 이번 연구에서 L1 점핑 유전자가 활성화되며, 노화와 발암 과정에 연관이 있음을 처음 확인하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 서울대학교병원 외과 김민정 교수, 고려대학교 의과대학 권현우 교수팀과의 공동연구로 ‘L1 점핑 유전자’의 활성화에 의한 사람 대장 상피 세포의 유전체 파괴 현상을 규명했다고 15일 밝혔다.
의과학대학원 남창현 박사과정과 육정환 박사(現 서울대병원 내과 임상조교수)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 5월 10일 字 온라인판(영국 현지시간)에 게재됐다 (논문명 : Widespread somatic L1 retrotransposition in normal colorectal epithelium). 이번 연구에는 한국과학기술정보연구원 (KISTI), 서울대학교병원 내과, 연세대학교 의과대학, 서울시립대학교, 및 KAIST 교원창업기업 지놈인사이트(Genome Insight)의 연구자들도 참여했다.
우리 몸에서 L1 점핑 유전자의 활성화는 유전체 서열의 ‘파괴적 혁신’을 일으킬 수 있기 때문에 인간 종의 진화 과정을 촉진하였다고 알려져 있으나, 사람 개개인의 입장에서는 L1 점핑 유전자의 활성화가 세포 유전체의 파괴 및 암 등 질병 발생을 촉진하여 생존에 불리하기 때문에 현생 인류에서 대다수의 L1 점핑 유전자는 불활성화(화석화)된 것으로 여겨졌다.
이번 연구는 이러한 일반적인 믿음과는 달리 L1 점핑 유전자의 일부는 아직도 특정 조직에서 활성화될 수 있고, 노화 과정에서 이들이 유전체 돌연변이를 빈번하게 생성하고 있음을 명확하게 규명하여, 세포의 노화 및 암 발생 과정을 이해하는 새로운 관점을 제시한 것으로 평가된다.
연구팀은 28명의 개인의 피부(섬유아세포), 혈액 및 대장 상피 조직에서 확보한 총 899개 단일세포의 전장 유전체(whole-genome sequencing) 서열을 생명정보학 기법으로 분석했다. L1 점핑 유전자에 의한 돌연변이의 빈도는 세포 종류에 따라 큰 차이를 보였으며 노화된 대장 상피세포에서 주로 발견됐다. 연구팀은 L1 점핑 유전자의 활성화에 의한 대장 상피세포의 유전체 돌연변이가 태어나기 전 배아 발생단계에서부터 평생에 걸쳐서 지속적으로 일어나고 있음을 확인했다. 연구에 따르면 40세가 된 개인의 대장 상피 세포들은 평균적으로 1개 이상의 L1 점핑 유전자에 의한 돌연변이를 갖게 된다.
연구팀은 L1 점핑 유전자 활성화 기전을 추적하기 위해 DNA 뿐만 아니라 후성 유전체 (DNA 메틸레이션) 서열을 함께 확인하였다. L1 점핑 유전자가 활성화된 세포에서는 후성 유전체의 불안정성이 발견되어 후성 유전체의 변화가 L1 점핑 유전자의 활성을 조절하는 스위치임을 확인하였다. 연구팀은 세포들의 배아발생과정을 추적하여, 이러한 후성 유전체 불안정성의 대다수가 초기 배아 발생과정에 형성되었음을 제시하였다.
이번 연구는 향후 더 많은 조직에서 L1 점핑유전자 활성화에 의한 노화 및 발암 과정을 확인하고 이의 활성화를 억제하여 인체 노화 및 질환 발생을 제어하는 기술개발에 이바지할 수 있을 것으로 연구팀은 기대했다.
의과학대학원 주영석 교수는 "전장유전체 및 생명정보학의 광범위한 적용을 통해 그동안 규명하기 어려웠던 L1 점핑 유전자에 의한 생명현상을 확인한 대표적인 연구ˮ라며 “이번 연구는 DNA 돌연변이가 암이나 질환을 갖고 있는 세포의 전유물이 아니며, 인간의 정상 세포의 노화과정에서 세포 자체의 불안정성에 의해 끊임없이 돌연변이가 생성되고 있음을 보여준다”라고 말했다.
서울대학교병원 외과 김민정 교수는 "임상현장에서 체계적으로 확보한 사람 유래 조직이 실제 인간에서 일어나는 질병 과정을 발견하는 데 큰 역할을 할 수 있음을 보여주는 사례ˮ라며 "향후 임상 및 기초의학의 밀접한 공동연구가 필요하다ˮ라고 말했다.
고려대학교 의과대학 핵의학과 권현우 교수는 “그동안 연구팀에서 고도화한 단일세포 유전체 기술이 큰 결실을 맺게 되어 기쁘다”라며 “앞으로 지속적으로 단일세포 유전체 기술을 선도할 수 있도록 매진할 것”이라고 말했다.
한편 이번 연구는 한국연구재단 리더연구, 한국연구재단 생애첫연구, 한국보건산업진흥원 융합형 의사과학자 양성 지원 사업, 서경배과학재단 신진과학자 연구지원 프로그램의 지원을 받아 수행됐다.
2023.05.15 조회수 9600
정크 DNA가 노화와 발암에 관여한다
인간 유전체 중 일반적인 단백질 생성 유전자는 전체 염기서열의 1% 정도에 불과하며 나머지 99%의 유전체 영역은 그 기능이 뚜렷하게 알려지지 않아 ‘쓸모없는 DNA’라는 뜻으로 ‘정크 DNA’라고 불리고 있다. 정크 DNA 가운데 약 1/6을 차지하는 L1 점핑 유전자는 활성화될 경우 세포의 유전정보를 파괴하거나 교란하는 역할을 할 수 있어 사람의 진화 과정에서 불활성화(화석화) 됐다고 알려져 있었다. 하지만 이번 연구에서 L1 점핑 유전자가 활성화되며, 노화와 발암 과정에 연관이 있음을 처음 확인하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 서울대학교병원 외과 김민정 교수, 고려대학교 의과대학 권현우 교수팀과의 공동연구로 ‘L1 점핑 유전자’의 활성화에 의한 사람 대장 상피 세포의 유전체 파괴 현상을 규명했다고 15일 밝혔다.
의과학대학원 남창현 박사과정과 육정환 박사(現 서울대병원 내과 임상조교수)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 5월 10일 字 온라인판(영국 현지시간)에 게재됐다 (논문명 : Widespread somatic L1 retrotransposition in normal colorectal epithelium). 이번 연구에는 한국과학기술정보연구원 (KISTI), 서울대학교병원 내과, 연세대학교 의과대학, 서울시립대학교, 및 KAIST 교원창업기업 지놈인사이트(Genome Insight)의 연구자들도 참여했다.
우리 몸에서 L1 점핑 유전자의 활성화는 유전체 서열의 ‘파괴적 혁신’을 일으킬 수 있기 때문에 인간 종의 진화 과정을 촉진하였다고 알려져 있으나, 사람 개개인의 입장에서는 L1 점핑 유전자의 활성화가 세포 유전체의 파괴 및 암 등 질병 발생을 촉진하여 생존에 불리하기 때문에 현생 인류에서 대다수의 L1 점핑 유전자는 불활성화(화석화)된 것으로 여겨졌다.
이번 연구는 이러한 일반적인 믿음과는 달리 L1 점핑 유전자의 일부는 아직도 특정 조직에서 활성화될 수 있고, 노화 과정에서 이들이 유전체 돌연변이를 빈번하게 생성하고 있음을 명확하게 규명하여, 세포의 노화 및 암 발생 과정을 이해하는 새로운 관점을 제시한 것으로 평가된다.
연구팀은 28명의 개인의 피부(섬유아세포), 혈액 및 대장 상피 조직에서 확보한 총 899개 단일세포의 전장 유전체(whole-genome sequencing) 서열을 생명정보학 기법으로 분석했다. L1 점핑 유전자에 의한 돌연변이의 빈도는 세포 종류에 따라 큰 차이를 보였으며 노화된 대장 상피세포에서 주로 발견됐다. 연구팀은 L1 점핑 유전자의 활성화에 의한 대장 상피세포의 유전체 돌연변이가 태어나기 전 배아 발생단계에서부터 평생에 걸쳐서 지속적으로 일어나고 있음을 확인했다. 연구에 따르면 40세가 된 개인의 대장 상피 세포들은 평균적으로 1개 이상의 L1 점핑 유전자에 의한 돌연변이를 갖게 된다.
연구팀은 L1 점핑 유전자 활성화 기전을 추적하기 위해 DNA 뿐만 아니라 후성 유전체 (DNA 메틸레이션) 서열을 함께 확인하였다. L1 점핑 유전자가 활성화된 세포에서는 후성 유전체의 불안정성이 발견되어 후성 유전체의 변화가 L1 점핑 유전자의 활성을 조절하는 스위치임을 확인하였다. 연구팀은 세포들의 배아발생과정을 추적하여, 이러한 후성 유전체 불안정성의 대다수가 초기 배아 발생과정에 형성되었음을 제시하였다.
이번 연구는 향후 더 많은 조직에서 L1 점핑유전자 활성화에 의한 노화 및 발암 과정을 확인하고 이의 활성화를 억제하여 인체 노화 및 질환 발생을 제어하는 기술개발에 이바지할 수 있을 것으로 연구팀은 기대했다.
의과학대학원 주영석 교수는 "전장유전체 및 생명정보학의 광범위한 적용을 통해 그동안 규명하기 어려웠던 L1 점핑 유전자에 의한 생명현상을 확인한 대표적인 연구ˮ라며 “이번 연구는 DNA 돌연변이가 암이나 질환을 갖고 있는 세포의 전유물이 아니며, 인간의 정상 세포의 노화과정에서 세포 자체의 불안정성에 의해 끊임없이 돌연변이가 생성되고 있음을 보여준다”라고 말했다.
서울대학교병원 외과 김민정 교수는 "임상현장에서 체계적으로 확보한 사람 유래 조직이 실제 인간에서 일어나는 질병 과정을 발견하는 데 큰 역할을 할 수 있음을 보여주는 사례ˮ라며 "향후 임상 및 기초의학의 밀접한 공동연구가 필요하다ˮ라고 말했다.
고려대학교 의과대학 핵의학과 권현우 교수는 “그동안 연구팀에서 고도화한 단일세포 유전체 기술이 큰 결실을 맺게 되어 기쁘다”라며 “앞으로 지속적으로 단일세포 유전체 기술을 선도할 수 있도록 매진할 것”이라고 말했다.
한편 이번 연구는 한국연구재단 리더연구, 한국연구재단 생애첫연구, 한국보건산업진흥원 융합형 의사과학자 양성 지원 사업, 서경배과학재단 신진과학자 연구지원 프로그램의 지원을 받아 수행됐다.
2023.05.15 조회수 9600 -
 파킨슨병 발병 3차원 게놈 지도 최초 제시
파킨슨병은 60세 이상 인구의 1.2% 이상 발병하는 흔한 퇴행성 뇌 질환으로 급격한 인구 고령화에 따라 전 세계적으로 발병률이 증가하고 있어, 2040년 약 1,420만 명의 환자가 발병할 것으로 예측되고 있다. 현재 파킨슨병의 다양한 발병 원인이 명확하게 규명되지 않은 상황에서, 비정상적으로 발생하는 후성 유전학적 특징들이 파킨슨병 발병에 관여하는 것을 최초로 확인되어 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 미국 국립보건원(National Institute of Health, NIH) 산하 국립노화연구소(National Institute on Aging, NIA) 엘리에자 매슬리아(Eliezer Masliah) 교수와의 공동연구를 통해 전 세계 최초로 파킨슨병 발병 뇌 조직의 단일세포 3차원 후성유전체 지도를 작성하고, 이를 토대로 656개의 파킨슨병 연관 신규 유전자들을 제시했다고 8일 밝혔다.
이번 연구에서 연구팀은 최신 개발된 단일세포 유전체 기술과 3차원 후성 유전체 기술을 접목하여 신경세포 뿐 아니라 뇌 환경 유지에 주요한 역할을 하는 것으로 알려진 신경교세포 (희소돌기아교세포, 미세아교세포 등)의 후성유전적 변화들이 3차원 게놈 구조를 통해 파킨슨병 발병에 관여하는 것을 밝혔다. 이러한 비정상적인 후성유전학적 특징들은 파킨슨병의 원인 또는 진행에 관여하는 유전자 발현 조절에 핵심적인 역할을 하기 때문에, 본 연구 결과는 차후 진단과 치료 연구에 중요한 단서를 제공하게 될 것이라고 연구팀은 전했다.
이번 연구를 수행한 생명과학과 이정운 박사는 단일세포 수준에서 환자 뇌조직을 분석한 결과 기존의 신경세포에 국한된 연구에서 한발 나아가, 신경교세포 또한 파킨슨병에 중요한 역할을 할 수 있다는 단서를 제시하였다는 점에서 중요한 발견이라고 밝혔다.
이번 연구 결과는 국제 학술지, ‘사이언스 어드벤시스(Science Advances, IF=14.14)'에 4월 14일 게재됐다. (논문명 : Characterization of altered molecular mechanisms in Parkinson’s disease through cell type-resolved multi-omics analyses)
교신 저자인 정인경 교수는 "이번 연구 결과는 퇴행성 뇌 질환의 표적 발굴에 있어 3차원 후성유전체 지도 작성의 중요성을 보였기에 차후 다양한 복합유전질환 규명에도 중요하게 활용될 것이다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 보건복지부, 과학기술정보통신부의 지원을 받아 수행됐다.
2023.05.08 조회수 7517
파킨슨병 발병 3차원 게놈 지도 최초 제시
파킨슨병은 60세 이상 인구의 1.2% 이상 발병하는 흔한 퇴행성 뇌 질환으로 급격한 인구 고령화에 따라 전 세계적으로 발병률이 증가하고 있어, 2040년 약 1,420만 명의 환자가 발병할 것으로 예측되고 있다. 현재 파킨슨병의 다양한 발병 원인이 명확하게 규명되지 않은 상황에서, 비정상적으로 발생하는 후성 유전학적 특징들이 파킨슨병 발병에 관여하는 것을 최초로 확인되어 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 미국 국립보건원(National Institute of Health, NIH) 산하 국립노화연구소(National Institute on Aging, NIA) 엘리에자 매슬리아(Eliezer Masliah) 교수와의 공동연구를 통해 전 세계 최초로 파킨슨병 발병 뇌 조직의 단일세포 3차원 후성유전체 지도를 작성하고, 이를 토대로 656개의 파킨슨병 연관 신규 유전자들을 제시했다고 8일 밝혔다.
이번 연구에서 연구팀은 최신 개발된 단일세포 유전체 기술과 3차원 후성 유전체 기술을 접목하여 신경세포 뿐 아니라 뇌 환경 유지에 주요한 역할을 하는 것으로 알려진 신경교세포 (희소돌기아교세포, 미세아교세포 등)의 후성유전적 변화들이 3차원 게놈 구조를 통해 파킨슨병 발병에 관여하는 것을 밝혔다. 이러한 비정상적인 후성유전학적 특징들은 파킨슨병의 원인 또는 진행에 관여하는 유전자 발현 조절에 핵심적인 역할을 하기 때문에, 본 연구 결과는 차후 진단과 치료 연구에 중요한 단서를 제공하게 될 것이라고 연구팀은 전했다.
이번 연구를 수행한 생명과학과 이정운 박사는 단일세포 수준에서 환자 뇌조직을 분석한 결과 기존의 신경세포에 국한된 연구에서 한발 나아가, 신경교세포 또한 파킨슨병에 중요한 역할을 할 수 있다는 단서를 제시하였다는 점에서 중요한 발견이라고 밝혔다.
이번 연구 결과는 국제 학술지, ‘사이언스 어드벤시스(Science Advances, IF=14.14)'에 4월 14일 게재됐다. (논문명 : Characterization of altered molecular mechanisms in Parkinson’s disease through cell type-resolved multi-omics analyses)
교신 저자인 정인경 교수는 "이번 연구 결과는 퇴행성 뇌 질환의 표적 발굴에 있어 3차원 후성유전체 지도 작성의 중요성을 보였기에 차후 다양한 복합유전질환 규명에도 중요하게 활용될 것이다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 보건복지부, 과학기술정보통신부의 지원을 받아 수행됐다.
2023.05.08 조회수 7517 -
 획기적 음의 정전용량 플래시 메모리 최초 개발
우리 대학 전기및전자공학부 전상훈 교수 연구팀이 `음의 정전용량 효과(Negative Capacitance Effect, 이하 NC 효과)*'를 활용해 기존 플래시 메모리의 물리적 성능 한계를 뛰어넘는 음의 정전용량 플래시 메모리 (NC-Flash Memory)를 세계 최초로 개발했다고 18일 밝혔다.
*음의 정전용량 효과: 음의 정전용량 현상은 인가되는 전압이 증가하면 전하량이 감소함을 의미한다. 음의 정전용량 특성을 가지는 유전체 사용시, 트랜지스터에 인가되는 전압을 내부적으로 증폭하여 상대적으로 낮은 동작전압을 사용할 수 있어, 파워소모를 줄일 수 있다.
전기및전자공학부 김태호 박사과정과 김기욱 박사과정이 공동 제1 저자로 수행한 이번 연구는 저명 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2022년 12월호에 출판됐다. (논문명 : The Opportunity of Negative Capacitance Behavior in Flash Memory for High-Density and Energy-Efficient In-Memory Computing Applications) 이 국제학술지는 독일 와일리 출판사(Wiley-VCH)에서 발행하는 피어리뷰 과학 저널이다. (Impact Factor : 19.924)
현대 전자 소자에서 축전기(Capacitor)는 매우 중요한 구성 요소의 하나로, 전자 소자가 소형화되고 수직 방향으로 적층 되면서 축전기에 저장되는 전하량(Charge, Q)이 감소하는 문제가 생기므로 높은 정전용량(Capacitance, C)을 가진 유전체 물질이 필수적으로 요구되고 있다. 여기에 일반적인 축전기와 다르게 정전용량이 음의 값을 갖는(Negative Capacitance) 축전기를 활용한다면 다층의 축전기의 전체 정전용량을 오히려 더 증가시킬 수 있고, 차세대 소자에 적합한 높은 정전용량 소자 개발 난제를 해결할 수 있을 것이라는 가설이 제안되었다.
최근 메모리 공급업체들은 데이터의 폭발적 증가와 더 높은 용량의 솔리드 스테이트 드라이브(SSD) 및 더 빠른 액세스 시간에 대한 요구로 인해 기술 경쟁을 치열하게 하고 있다. 스토리지의 핵심 기술인 3D 낸드 플래시는 지속적으로 더 높은 층을 적층할 수 있는 기술을 요구하고 있고, 2028년에는 1,000단 이상의 메모리 적층이 필요할 것으로 예상되고 있다.
한편, 강유전체* 물질에서 보이는 `음의 정전용량 효과(NC 효과)'은 전자 소자에 인가된 외부 전압을 내부적으로 증폭해 전력 소모를 줄이는 특성이 있어, 전자 소자의 물리적 성능 한계를 극복할 수 있다는 가능성이 제시됐다. 최근 페로브스카이트 강유전체에서 NC 효과를 실험적으로 관찰했으나, 페로브스카이트 강유전체의 소형화 한계 및 CMOS 공정과의 부적합성으로 인해 NC 효과를 활용한 전자 소자의 구현에 대해 상당한 회의론을 불러일으켰다.
*강유전체: 전기적으로는 절연체이지만 자연상태에서 외부 전기장이 없어도 전기 편극을 지닐 수 있는 특이한 물리적 성질을 가진 물질
전상훈 교수 연구팀은 기존 플래시 메모리의 물리적 성능 한계를 극복하고 동작전압을 낮추기 위해, 반도체 공정에 사용되는 하프늄옥사이드(HfO2) 강유전체 박막의 NC 효과를 안정화해 저전압 구동이 가능한 강유전체 소재의 NC-플래시 메모리를 세계 최초로 개발했다. 개발된 NC-플래시 메모리는 기존 플래시 메모리 대비 전력 소모가 10,000배 이상 낮은 저전력 고성능 특성을 달성했다.
연구팀은 그뿐만 아니라 기존 컴퓨팅 구조인 폰노이만 아키텍처를 대체하여 새롭게 지향하는 인메모리 컴퓨팅을 NC-플래시 메모리를 기반으로 구현해 세계 최고 수준의 에너지 효율 또한 달성했다.
이번 연구 결과는 빠른 스토리지를 필요로 하는 최신 컴퓨팅과 네트워킹의 요구를 충족하는 차세대 낸드 플래시 메모리 개발에 있어 핵심 역할을 할 것이다.
한편, 이번 연구는 연세대학교와 협업을 통해서 이루어졌고, 한국 연구재단 지능형 반도체 기술개발사업의 지원을 받아 수행됐다.
2023.01.18 조회수 9915
획기적 음의 정전용량 플래시 메모리 최초 개발
우리 대학 전기및전자공학부 전상훈 교수 연구팀이 `음의 정전용량 효과(Negative Capacitance Effect, 이하 NC 효과)*'를 활용해 기존 플래시 메모리의 물리적 성능 한계를 뛰어넘는 음의 정전용량 플래시 메모리 (NC-Flash Memory)를 세계 최초로 개발했다고 18일 밝혔다.
*음의 정전용량 효과: 음의 정전용량 현상은 인가되는 전압이 증가하면 전하량이 감소함을 의미한다. 음의 정전용량 특성을 가지는 유전체 사용시, 트랜지스터에 인가되는 전압을 내부적으로 증폭하여 상대적으로 낮은 동작전압을 사용할 수 있어, 파워소모를 줄일 수 있다.
전기및전자공학부 김태호 박사과정과 김기욱 박사과정이 공동 제1 저자로 수행한 이번 연구는 저명 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2022년 12월호에 출판됐다. (논문명 : The Opportunity of Negative Capacitance Behavior in Flash Memory for High-Density and Energy-Efficient In-Memory Computing Applications) 이 국제학술지는 독일 와일리 출판사(Wiley-VCH)에서 발행하는 피어리뷰 과학 저널이다. (Impact Factor : 19.924)
현대 전자 소자에서 축전기(Capacitor)는 매우 중요한 구성 요소의 하나로, 전자 소자가 소형화되고 수직 방향으로 적층 되면서 축전기에 저장되는 전하량(Charge, Q)이 감소하는 문제가 생기므로 높은 정전용량(Capacitance, C)을 가진 유전체 물질이 필수적으로 요구되고 있다. 여기에 일반적인 축전기와 다르게 정전용량이 음의 값을 갖는(Negative Capacitance) 축전기를 활용한다면 다층의 축전기의 전체 정전용량을 오히려 더 증가시킬 수 있고, 차세대 소자에 적합한 높은 정전용량 소자 개발 난제를 해결할 수 있을 것이라는 가설이 제안되었다.
최근 메모리 공급업체들은 데이터의 폭발적 증가와 더 높은 용량의 솔리드 스테이트 드라이브(SSD) 및 더 빠른 액세스 시간에 대한 요구로 인해 기술 경쟁을 치열하게 하고 있다. 스토리지의 핵심 기술인 3D 낸드 플래시는 지속적으로 더 높은 층을 적층할 수 있는 기술을 요구하고 있고, 2028년에는 1,000단 이상의 메모리 적층이 필요할 것으로 예상되고 있다.
한편, 강유전체* 물질에서 보이는 `음의 정전용량 효과(NC 효과)'은 전자 소자에 인가된 외부 전압을 내부적으로 증폭해 전력 소모를 줄이는 특성이 있어, 전자 소자의 물리적 성능 한계를 극복할 수 있다는 가능성이 제시됐다. 최근 페로브스카이트 강유전체에서 NC 효과를 실험적으로 관찰했으나, 페로브스카이트 강유전체의 소형화 한계 및 CMOS 공정과의 부적합성으로 인해 NC 효과를 활용한 전자 소자의 구현에 대해 상당한 회의론을 불러일으켰다.
*강유전체: 전기적으로는 절연체이지만 자연상태에서 외부 전기장이 없어도 전기 편극을 지닐 수 있는 특이한 물리적 성질을 가진 물질
전상훈 교수 연구팀은 기존 플래시 메모리의 물리적 성능 한계를 극복하고 동작전압을 낮추기 위해, 반도체 공정에 사용되는 하프늄옥사이드(HfO2) 강유전체 박막의 NC 효과를 안정화해 저전압 구동이 가능한 강유전체 소재의 NC-플래시 메모리를 세계 최초로 개발했다. 개발된 NC-플래시 메모리는 기존 플래시 메모리 대비 전력 소모가 10,000배 이상 낮은 저전력 고성능 특성을 달성했다.
연구팀은 그뿐만 아니라 기존 컴퓨팅 구조인 폰노이만 아키텍처를 대체하여 새롭게 지향하는 인메모리 컴퓨팅을 NC-플래시 메모리를 기반으로 구현해 세계 최고 수준의 에너지 효율 또한 달성했다.
이번 연구 결과는 빠른 스토리지를 필요로 하는 최신 컴퓨팅과 네트워킹의 요구를 충족하는 차세대 낸드 플래시 메모리 개발에 있어 핵심 역할을 할 것이다.
한편, 이번 연구는 연세대학교와 협업을 통해서 이루어졌고, 한국 연구재단 지능형 반도체 기술개발사업의 지원을 받아 수행됐다.
2023.01.18 조회수 9915 -
 차세대 반도체 핵심소재로 열적으로 안정된 강유전체 소재 최초 개발
우리 대학 전기및전자공학부 전상훈 교수 연구팀이 하프니아 강유전체 소재의 물성적 이해를 바탕으로 반도체 3D 집적 공정에서도 열적으로 안정한 *강유전체 소재를 세계 최초로 개발했다고 12일 밝혔다. 현재 반도체 제조 업계에서 고집적, 고효율의 3D 메모리 소자에 대한 필요성이 꾸준하게 대두되고 있다는 점을 고려할 때, 이번 연구는 강유전체 기반의 3D 메모리 집적 공정에서 핵심 기술로 평가받을 것이라 예상된다.
*강유전체: 외부의 전기장 없이도 스스로 분극을 가지는 재료로서 외부 전기장에 의해 분극의 방향이 바뀔 수 있는 소재를 말한다. 비휘발성 특성이 있어, 기능성 소재로서 메모리 소자에 활용이 가능하지만, 고온에서 열적으로 안정성을 확보해야하는 도전 목표가 남아 있으며, 일반 유전체를 일컫는 상유전체는 외부의 전기장이 없으면 분극 특성을 유지하지 못한다는 점에서 다르다.
하프니아 강유전체 소재는 비휘발성 절연막으로, CMOS 공정 호환성, 동작 속도, 내구성 등의 우수한 물리적 특성을 바탕으로 차세대 반도체의 핵심 소재로써 활발하게 연구되고 있는 물질이다. 하지만 하프니아 소재는 필연적으로 고온에서 비휘발성 특성을 잃고 누설전류가 증가하는 한계를 가진다. 이를 억제하기 위해 세계 유수의 기관들에서 다양한 접근방법들이 보고됐지만, 3D 집적 공정 시에 발생하는 고온의 열처리 조건 (750℃ 이상, 30분)에서 강유전체 박막 내의 일반 유전체 (상유전체) 형성을 억제할 수 없었다.
전상훈 교수 연구팀은 세계 최초로 3D 집적 공정에서 요구되는 고온의 열처리 조건에서도 강유전체 박막 내의 상유전체의 형성을 완벽하게 억제하고 비휘발성 기능을 유지하며 우수한 내구성을 가지는 하프니아 강유전체 소재 및 공정 기술을 개발하는 데에 성공했다. 연구팀은 강유전체 박막 내에 이온 반지름이 작은 원소를 고용하는 도핑 기술을 활용해 강유전체 박막의 결정화 온도를 제어함과 동시에 도펀트의 농도에 따른 운동학적 에너지를 고려해 강유전체 소재의 비휘발성 및 기능성과 열적 안정성을 획기적으로 개선했다.
전상훈 교수 연구팀은 CMOS 공정을 이용해 강유전체 기반의 메모리 소자를 집적했고 고온의 열적 에너지(750℃ 이상, 30분)를 가한 후에도 우수한 강유전성이 발현되는 것을 확인했다. 또한 열적 에너지에 따른 강유전체 소재의 도메인 스위칭 동작을 전기적 측정을 통해 직관적으로 분석할 수 있는 시스템을 개발해 추후, 강유전체 소재의 열적 안정성 연구의 프레임 워크를 구축 및 제시했다. 해당 연구는 학계에서 활발하게 연구되고 있는 강유전체 소재의 기능성과 반도체 제조 업계에서 필요로 했던 강유전체 소재 기반의 3D 메모리 소자 집적 공정 사이의 간극을 줄였다는 점에서 큰 의미를 가진다.
전상훈 교수는 “이번 연구 결과는 답보상태에 있던 강유전체 소재 기반의 3D 메모리 및 회로 집적 기술 개발에 대한 돌파구가 되는 기술이 될 것으로 판단되며, 향후 고집적/고효율의 시스템 개발에 있어 핵심 역할을 할 것”이라고 설명했다.
전기및전자공학부 김기욱 박사 과정이 제1 저자로 수행한 이번 연구는 반도체 소자 및 회로 분야의 최고 권위 학회인‘IEEE 국제전자소자학회(International Electron Devices Meeting) 2022 (IEDM 2022)’에 12월 5일 발표를 마쳤다. 한편 이번 연구는 삼성전자(Samsung Electronics)와 차세대 지능형 반도체 사업단의 지능형 반도체 선도기술개발의 지원을 받아 진행됐다.
2022.12.12 조회수 10417
차세대 반도체 핵심소재로 열적으로 안정된 강유전체 소재 최초 개발
우리 대학 전기및전자공학부 전상훈 교수 연구팀이 하프니아 강유전체 소재의 물성적 이해를 바탕으로 반도체 3D 집적 공정에서도 열적으로 안정한 *강유전체 소재를 세계 최초로 개발했다고 12일 밝혔다. 현재 반도체 제조 업계에서 고집적, 고효율의 3D 메모리 소자에 대한 필요성이 꾸준하게 대두되고 있다는 점을 고려할 때, 이번 연구는 강유전체 기반의 3D 메모리 집적 공정에서 핵심 기술로 평가받을 것이라 예상된다.
*강유전체: 외부의 전기장 없이도 스스로 분극을 가지는 재료로서 외부 전기장에 의해 분극의 방향이 바뀔 수 있는 소재를 말한다. 비휘발성 특성이 있어, 기능성 소재로서 메모리 소자에 활용이 가능하지만, 고온에서 열적으로 안정성을 확보해야하는 도전 목표가 남아 있으며, 일반 유전체를 일컫는 상유전체는 외부의 전기장이 없으면 분극 특성을 유지하지 못한다는 점에서 다르다.
하프니아 강유전체 소재는 비휘발성 절연막으로, CMOS 공정 호환성, 동작 속도, 내구성 등의 우수한 물리적 특성을 바탕으로 차세대 반도체의 핵심 소재로써 활발하게 연구되고 있는 물질이다. 하지만 하프니아 소재는 필연적으로 고온에서 비휘발성 특성을 잃고 누설전류가 증가하는 한계를 가진다. 이를 억제하기 위해 세계 유수의 기관들에서 다양한 접근방법들이 보고됐지만, 3D 집적 공정 시에 발생하는 고온의 열처리 조건 (750℃ 이상, 30분)에서 강유전체 박막 내의 일반 유전체 (상유전체) 형성을 억제할 수 없었다.
전상훈 교수 연구팀은 세계 최초로 3D 집적 공정에서 요구되는 고온의 열처리 조건에서도 강유전체 박막 내의 상유전체의 형성을 완벽하게 억제하고 비휘발성 기능을 유지하며 우수한 내구성을 가지는 하프니아 강유전체 소재 및 공정 기술을 개발하는 데에 성공했다. 연구팀은 강유전체 박막 내에 이온 반지름이 작은 원소를 고용하는 도핑 기술을 활용해 강유전체 박막의 결정화 온도를 제어함과 동시에 도펀트의 농도에 따른 운동학적 에너지를 고려해 강유전체 소재의 비휘발성 및 기능성과 열적 안정성을 획기적으로 개선했다.
전상훈 교수 연구팀은 CMOS 공정을 이용해 강유전체 기반의 메모리 소자를 집적했고 고온의 열적 에너지(750℃ 이상, 30분)를 가한 후에도 우수한 강유전성이 발현되는 것을 확인했다. 또한 열적 에너지에 따른 강유전체 소재의 도메인 스위칭 동작을 전기적 측정을 통해 직관적으로 분석할 수 있는 시스템을 개발해 추후, 강유전체 소재의 열적 안정성 연구의 프레임 워크를 구축 및 제시했다. 해당 연구는 학계에서 활발하게 연구되고 있는 강유전체 소재의 기능성과 반도체 제조 업계에서 필요로 했던 강유전체 소재 기반의 3D 메모리 소자 집적 공정 사이의 간극을 줄였다는 점에서 큰 의미를 가진다.
전상훈 교수는 “이번 연구 결과는 답보상태에 있던 강유전체 소재 기반의 3D 메모리 및 회로 집적 기술 개발에 대한 돌파구가 되는 기술이 될 것으로 판단되며, 향후 고집적/고효율의 시스템 개발에 있어 핵심 역할을 할 것”이라고 설명했다.
전기및전자공학부 김기욱 박사 과정이 제1 저자로 수행한 이번 연구는 반도체 소자 및 회로 분야의 최고 권위 학회인‘IEEE 국제전자소자학회(International Electron Devices Meeting) 2022 (IEDM 2022)’에 12월 5일 발표를 마쳤다. 한편 이번 연구는 삼성전자(Samsung Electronics)와 차세대 지능형 반도체 사업단의 지능형 반도체 선도기술개발의 지원을 받아 진행됐다.
2022.12.12 조회수 10417 -
 대규모 한국인 자폐증 가족 유전체 연구를 통한 새로운 자폐 유전변이 최초 발견
우리 대학 의과학대학원 이정호 교수와 바이오및뇌공학과 최정균 교수, 생명과학과 김은준 교수(IBS 시냅스뇌질환연구단장), 분당서울대병원 유희정 교수, KISTI 공동 연구팀이 아시아 최초로 대규모 한국인 자폐증 가족 코호트를 모집하고 전장 유전체 분석을 실시해 자폐증 유발 유전변이가 단백질을 암호화하지 않는 유전체 영역인 비-부호화 영역에서 발생할 수 있다는 사실을 규명했고, 이를 통해 자폐증 원인의 새로운 이해와 치료 전기를 마련했다고 19일 밝혔다.
이번 연구내용은 세계적 정신의학 학술지 ‘분자 정신의학(Molecular Psychiatry)’에 7월 15일 자에 게재됐다.
자폐증은 사회적 의사소통 결핍이나 이상, 반복적이거나 틀에 박힌 행동 문제가 유아 시절 시작돼 거의 평생 지속되는 뇌 신경 발달장애로, 질환 발생의 근본적인 원인에 대한 이해가 매우 부족하며, 공식적으로 인정된 치료 약제가 전무하다. 자폐증 원인에 대한 이해의 필요성은 대중들의 높은 관심을 통해서도 가늠해볼 수 있는데, 예를 들어 최근 세간의 이목이 집중된 드라마 ‘이상한 변호사 우영우’의 주인공이 자폐증을 앓고 있다.
연구진은 자폐증 유발 유전변이가 비-부호화 유전체 영역에서 발생한다는 사실을 발견했으며, 이를 세계 최초로 한국인 자폐증 샘플로 제작한 인간 줄기세포를 이용해 증명했다. 자폐증의 근본 원인을 규명한 획기적인 연구 결과로서, 기존 연구의 한계를 뛰어넘어 그간 유전체 분야의 난공불락으로 여겨졌던 비-부호화 영역에 초점을 맞춘 혁신적인 발상으로 자폐증 치료의 새로운 전기가 마련될 것으로 예상된다.
연구진은 IBS와 한국연구재단, 국가바이오빅데이터 사업단의 지원을 통해 2011년부터 현재 3,708명에 달하는 자폐 환자와 그 가족들로 구성된 대규모 한국인 코호트를 구축하고 유전체 분석을 진행하고 있으며, 이번 연구 결과는 813명의 전장 유전체 염기서열 분석을 바탕으로 이뤄졌다. (그림 1)
유전체 데이터의 98% 이상을 차지하고 있으나 그간 자폐증 유전체 연구에서 조명받지 못했던 비-부호화 영역을 집중적으로 규명하고자, 연구진은 3차원 공간상의 염색질 상호작용(three-dimensional chromatin interaction)이라는 새로운 분석 방식을 사용했으며 (그림 2), 비-부호화 영역에서 발생한 유전변이가 멀리 떨어져 있는 자폐 유전자의 기능에 심각한 이상을 초래할 수 있음을 증명했다. (그림 3)
특히, 본 코호트의 한국인 자폐증 가족으로부터 직접 인간 줄기세포를 제작해 태아기 신경세포를 재현했으며, 이러한 생애 초기 신경 발달단계에서 비-부호화 영역의 유전변이에 의해 최대 500,000 base-pair(유전체 거리 단위) 이상 떨어져 있는 유전자의 발현이 비정상적으로 낮아지거나 높아질 수 있음을 세계 최초로 증명했다 (그림 4)
이번 연구 성과는 자폐증 유발 유전변이가 단백질을 부호화하지 않는 비-부호화 영역에서 발생해, 멀리 떨어져 있는 유전자의 기능에 영향을 미침으로써 신경 발달단계 초기부터 질병 발병에 기여한다는 획기적인 자폐증 원인에 대한 발견이다. 연구팀은 그간 단백질을 부호화하는 영역에만 쏠려 있던 정신질환 연구 풍토 속에서, 비-부호화 영역을 규명하는 방향으로 전환해야 자폐증 치료의 비밀을 풀 수 있다는 새로운 접근법을 제시했다.
IBS 시냅스뇌질환연구단(김은준 교수팀 프로젝트 제안 및 개시), 서울의대 및 분당서울대병원(유희정교수팀 코호트 구축 및 임상 평가), KISTI(대용량 컴퓨팅 리소스 및 유전체 데이터 분석 파이프라인 제공), KAIST (이정호 교수팀, 최정균 교수팀 비-부호화 영역 유전변이 분석) 공동 연구팀이 통합된 유전체-임상 데이터에 대해 3차원 공간상의 염색질 상호작용 분석을 통해 비-부호화 영역에서 발생한 유전변이가 자폐증 발병에 기여함을 규명했다.
이는 순수 국내의 임상가와 기초과학자, 생물정보학 전문가의 융합연구로 이루어낸 성과이며, 아시아 최초의 대규모 전장-유전체 데이터 기반 코호트 구축과 유전체 분석 모델의 기틀을 마련함으로써 대한민국 유전체 연구의 선도적인 역할을 한 것이다. 자폐 유전체 연구는 지난 10년간 북미와 유럽을 위주로 대규모로 진행됐으나, 한국을 비롯한 아시아에서는 상대적으로 연구가 덜 진행됐다.
논문의 공동 제1 저자인 KAIST 의과학대학원 졸업생 김일빈 박사는 “신경발달장애 중 자폐증은 특히 치료가 어려운 것으로 알려져 있는데, 발병 원인 중 하나로 지목되는 유전체 영역의 이상을 한국인 고유의 데이터를 사용해 순수 국내 연구진들의 힘으로 발견해냈다는 데 큰 의미가 있으며, 이 연구 성과가 언젠가는 이루어질 자폐증 치료제 개발을 위한 작은 발판이 되길 바란다”라고 말했다. 분당서울대병원의 유희정 교수도 “우리나라 연구진의 힘을 모아 자폐증의 비밀을 풀기 위한 첫걸음을 내딛었다. 연구에 참여해 준 당사자와 가족들의 헌신으로 이룬 일이라고 생각한다. 하지만 우리가 자폐증의 발병 기전을 완전히 이해하고 나아가 치료제를 개발하기 위해서는 아직 연구해야 할 것이 많다. 유전체 연구에 대한 국가 차원의 지원이 절실하며, 자폐증을 가진 분들과 가족들의 관심도 꼭 필요하다”는 점을 강조했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원사업을 통해 수행됐다.
2022.07.19 조회수 12830
대규모 한국인 자폐증 가족 유전체 연구를 통한 새로운 자폐 유전변이 최초 발견
우리 대학 의과학대학원 이정호 교수와 바이오및뇌공학과 최정균 교수, 생명과학과 김은준 교수(IBS 시냅스뇌질환연구단장), 분당서울대병원 유희정 교수, KISTI 공동 연구팀이 아시아 최초로 대규모 한국인 자폐증 가족 코호트를 모집하고 전장 유전체 분석을 실시해 자폐증 유발 유전변이가 단백질을 암호화하지 않는 유전체 영역인 비-부호화 영역에서 발생할 수 있다는 사실을 규명했고, 이를 통해 자폐증 원인의 새로운 이해와 치료 전기를 마련했다고 19일 밝혔다.
이번 연구내용은 세계적 정신의학 학술지 ‘분자 정신의학(Molecular Psychiatry)’에 7월 15일 자에 게재됐다.
자폐증은 사회적 의사소통 결핍이나 이상, 반복적이거나 틀에 박힌 행동 문제가 유아 시절 시작돼 거의 평생 지속되는 뇌 신경 발달장애로, 질환 발생의 근본적인 원인에 대한 이해가 매우 부족하며, 공식적으로 인정된 치료 약제가 전무하다. 자폐증 원인에 대한 이해의 필요성은 대중들의 높은 관심을 통해서도 가늠해볼 수 있는데, 예를 들어 최근 세간의 이목이 집중된 드라마 ‘이상한 변호사 우영우’의 주인공이 자폐증을 앓고 있다.
연구진은 자폐증 유발 유전변이가 비-부호화 유전체 영역에서 발생한다는 사실을 발견했으며, 이를 세계 최초로 한국인 자폐증 샘플로 제작한 인간 줄기세포를 이용해 증명했다. 자폐증의 근본 원인을 규명한 획기적인 연구 결과로서, 기존 연구의 한계를 뛰어넘어 그간 유전체 분야의 난공불락으로 여겨졌던 비-부호화 영역에 초점을 맞춘 혁신적인 발상으로 자폐증 치료의 새로운 전기가 마련될 것으로 예상된다.
연구진은 IBS와 한국연구재단, 국가바이오빅데이터 사업단의 지원을 통해 2011년부터 현재 3,708명에 달하는 자폐 환자와 그 가족들로 구성된 대규모 한국인 코호트를 구축하고 유전체 분석을 진행하고 있으며, 이번 연구 결과는 813명의 전장 유전체 염기서열 분석을 바탕으로 이뤄졌다. (그림 1)
유전체 데이터의 98% 이상을 차지하고 있으나 그간 자폐증 유전체 연구에서 조명받지 못했던 비-부호화 영역을 집중적으로 규명하고자, 연구진은 3차원 공간상의 염색질 상호작용(three-dimensional chromatin interaction)이라는 새로운 분석 방식을 사용했으며 (그림 2), 비-부호화 영역에서 발생한 유전변이가 멀리 떨어져 있는 자폐 유전자의 기능에 심각한 이상을 초래할 수 있음을 증명했다. (그림 3)
특히, 본 코호트의 한국인 자폐증 가족으로부터 직접 인간 줄기세포를 제작해 태아기 신경세포를 재현했으며, 이러한 생애 초기 신경 발달단계에서 비-부호화 영역의 유전변이에 의해 최대 500,000 base-pair(유전체 거리 단위) 이상 떨어져 있는 유전자의 발현이 비정상적으로 낮아지거나 높아질 수 있음을 세계 최초로 증명했다 (그림 4)
이번 연구 성과는 자폐증 유발 유전변이가 단백질을 부호화하지 않는 비-부호화 영역에서 발생해, 멀리 떨어져 있는 유전자의 기능에 영향을 미침으로써 신경 발달단계 초기부터 질병 발병에 기여한다는 획기적인 자폐증 원인에 대한 발견이다. 연구팀은 그간 단백질을 부호화하는 영역에만 쏠려 있던 정신질환 연구 풍토 속에서, 비-부호화 영역을 규명하는 방향으로 전환해야 자폐증 치료의 비밀을 풀 수 있다는 새로운 접근법을 제시했다.
IBS 시냅스뇌질환연구단(김은준 교수팀 프로젝트 제안 및 개시), 서울의대 및 분당서울대병원(유희정교수팀 코호트 구축 및 임상 평가), KISTI(대용량 컴퓨팅 리소스 및 유전체 데이터 분석 파이프라인 제공), KAIST (이정호 교수팀, 최정균 교수팀 비-부호화 영역 유전변이 분석) 공동 연구팀이 통합된 유전체-임상 데이터에 대해 3차원 공간상의 염색질 상호작용 분석을 통해 비-부호화 영역에서 발생한 유전변이가 자폐증 발병에 기여함을 규명했다.
이는 순수 국내의 임상가와 기초과학자, 생물정보학 전문가의 융합연구로 이루어낸 성과이며, 아시아 최초의 대규모 전장-유전체 데이터 기반 코호트 구축과 유전체 분석 모델의 기틀을 마련함으로써 대한민국 유전체 연구의 선도적인 역할을 한 것이다. 자폐 유전체 연구는 지난 10년간 북미와 유럽을 위주로 대규모로 진행됐으나, 한국을 비롯한 아시아에서는 상대적으로 연구가 덜 진행됐다.
논문의 공동 제1 저자인 KAIST 의과학대학원 졸업생 김일빈 박사는 “신경발달장애 중 자폐증은 특히 치료가 어려운 것으로 알려져 있는데, 발병 원인 중 하나로 지목되는 유전체 영역의 이상을 한국인 고유의 데이터를 사용해 순수 국내 연구진들의 힘으로 발견해냈다는 데 큰 의미가 있으며, 이 연구 성과가 언젠가는 이루어질 자폐증 치료제 개발을 위한 작은 발판이 되길 바란다”라고 말했다. 분당서울대병원의 유희정 교수도 “우리나라 연구진의 힘을 모아 자폐증의 비밀을 풀기 위한 첫걸음을 내딛었다. 연구에 참여해 준 당사자와 가족들의 헌신으로 이룬 일이라고 생각한다. 하지만 우리가 자폐증의 발병 기전을 완전히 이해하고 나아가 치료제를 개발하기 위해서는 아직 연구해야 할 것이 많다. 유전체 연구에 대한 국가 차원의 지원이 절실하며, 자폐증을 가진 분들과 가족들의 관심도 꼭 필요하다”는 점을 강조했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원사업을 통해 수행됐다.
2022.07.19 조회수 12830 -
 최초 머신러닝 기반 유전체 정렬 소프트웨어 개발
우리 대학 전기및전자공학부 한동수 교수 연구팀이 머신러닝(기계학습)에 기반한 *유전체 정렬 소프트웨어를 개발했다고 12일 밝혔다.
☞ 유전체(genome): 생명체가 가지고 있는 염기서열 정보의 총합이며, 유전자는 생물학적 특징을 발현하는 염기서열들을 지칭한다. 유전체를 한 권의 책이라고 비유하면 유전자는 공백을 제외한 모든 글자라고 비유할 수 있다.
차세대 염기서열 분석은 유전체 정보를 해독하는 방법으로 유전체를 무수히 많은 조각으로 잘라낸 후 각 조각을 참조 유전체(reference genome)에 기반해 조립하는 과정을 거친다. 조립된 유전체 정보는 암을 포함한 여러 질병의 예측과 맞춤형 치료, 백신 개발 등 다양한 분야에서 사용된다.
유전체 정렬 소프트웨어는 차세대 염기서열 분석 방법으로 생성한 유전체 조각 데이터를 온전한 유전체 정보로 조립하기 위해 사용되는 소프트웨어다. 유전체 정렬 작업에는 많은 연산이 들어가며, 속도를 높이고 비용을 낮추는 방법에 관한 관심이 계속해서 증가하고 있다. 머신러닝(기계학습) 기반의 인덱싱(색인) 기법(Learned-index)을 유전체 정렬 소프트웨어에 적용한 사례는 이번이 최초다.
전기및전자공학부 정영목 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `옥스포드 바이오인포메틱스(Oxford Bioinformatics)' 2022년 3월에 공개됐다. (논문명 : BWA-MEME: BWA-MEM emulated with a machine learning approach)
유전체 정렬 작업은 정렬해야 하는 유전체 조각의 양이 많고 참조 유전체의 길이도 길어 많은 연산량이 요구되는 작업이다. 또한, 유전체 정렬 소프트웨어에서 정렬 결과의 정확도에 따라 추후의 유전체 분석의 정확도가 영향을 받는다. 이러한 특성 때문에 유전체 정렬 소프트웨어는 높은 정확성을 유지하며 빠르게 연산하는 것이 중요하다.
일반적으로 유전체 분석에는 하버드 브로드 연구소(Broad Institute)에서 개발한 유전체 분석 도구 키트(Genome Analysis Tool Kit, 이하 GATK)를 이용한 데이터 처리 방법을 표준으로 사용한다. 이들 키트 중 BWA-MEM은 GATK에서 표준으로 채택한 유전체 정렬 소프트웨어이며, 2019년에 하버드 대학과 인텔(Intel)의 공동 연구로 BWA-MEM2가 개발됐다.
연구팀이 개발한 머신러닝 기반의 유전체 정렬 소프트웨어는 연산량을 대폭 줄이면서도 표준 유전체 정렬 소프트웨어 BWA-MEM2과 동일한 결과를 만들어 정확도를 유지했다. 사용한 머신러닝 기반의 인덱싱 기법은 주어진 데이터의 분포를 머신러닝 모델이 학습해, 데이터 분포에 최적화된 인덱싱을 찾는 방법론이다. 데이터에 적합하다고 생각되는 인덱싱 방법을 사람이 정하던 기존의 방법과 대비된다.
BWA-MEM과 BWA-MEM2에서 사용하는 인덱싱 기법(FM-index)은 유전자 조각의 위치를 찾기 위해 유전자 조각 길이만큼의 연산이 필요하지만, 연구팀이 제안한 알고리즘은 머신러닝 기반의 인덱싱 기법(Learned-index)을 활용해, 유전자 조각 길이와 상관없이 적은 연산량으로도 유전자 조각의 위치를 찾을 수 있다. 연구팀이 제안한 인덱싱 기법은 기존 인덱싱 기법과 비교해 3.4배 정도 가속화됐고, 이로 인해 유전체 정렬 소프트웨어는 1.4 배 가속화됐다.
연구팀이 이번 연구에서 개발한 유전체 정렬 소프트웨어는 오픈소스 (https://github.com/kaist-ina/BWA-MEME)로 공개돼 많은 분야에 사용될 것으로 기대되며, 유전체 분석에서 사용되는 다양한 소프트웨어를 머신러닝 기술로 가속화하는 연구들의 초석이 될 것으로 기대된다.
한동수 교수는 "이번 연구를 통해 기계학습 기술을 접목해 전장 유전체 빅데이터 분석을 기존 방식보다 빠르고 적은 비용으로 할 수 있다는 것을 보여줬으며, 앞으로 인공지능 기술을 활용해 전장 유전체 빅데이터 분석을 효율화, 고도화할 수 있을 것이라 기대된다ˮ고 말했다.
한편 이번 연구는 과학기술정보통신부의 재원으로 한국연구재단의 지원을 받아 데이터 스테이션 구축·운영 사업으로서 수행됐다.
2022.04.17 조회수 12535
최초 머신러닝 기반 유전체 정렬 소프트웨어 개발
우리 대학 전기및전자공학부 한동수 교수 연구팀이 머신러닝(기계학습)에 기반한 *유전체 정렬 소프트웨어를 개발했다고 12일 밝혔다.
☞ 유전체(genome): 생명체가 가지고 있는 염기서열 정보의 총합이며, 유전자는 생물학적 특징을 발현하는 염기서열들을 지칭한다. 유전체를 한 권의 책이라고 비유하면 유전자는 공백을 제외한 모든 글자라고 비유할 수 있다.
차세대 염기서열 분석은 유전체 정보를 해독하는 방법으로 유전체를 무수히 많은 조각으로 잘라낸 후 각 조각을 참조 유전체(reference genome)에 기반해 조립하는 과정을 거친다. 조립된 유전체 정보는 암을 포함한 여러 질병의 예측과 맞춤형 치료, 백신 개발 등 다양한 분야에서 사용된다.
유전체 정렬 소프트웨어는 차세대 염기서열 분석 방법으로 생성한 유전체 조각 데이터를 온전한 유전체 정보로 조립하기 위해 사용되는 소프트웨어다. 유전체 정렬 작업에는 많은 연산이 들어가며, 속도를 높이고 비용을 낮추는 방법에 관한 관심이 계속해서 증가하고 있다. 머신러닝(기계학습) 기반의 인덱싱(색인) 기법(Learned-index)을 유전체 정렬 소프트웨어에 적용한 사례는 이번이 최초다.
전기및전자공학부 정영목 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `옥스포드 바이오인포메틱스(Oxford Bioinformatics)' 2022년 3월에 공개됐다. (논문명 : BWA-MEME: BWA-MEM emulated with a machine learning approach)
유전체 정렬 작업은 정렬해야 하는 유전체 조각의 양이 많고 참조 유전체의 길이도 길어 많은 연산량이 요구되는 작업이다. 또한, 유전체 정렬 소프트웨어에서 정렬 결과의 정확도에 따라 추후의 유전체 분석의 정확도가 영향을 받는다. 이러한 특성 때문에 유전체 정렬 소프트웨어는 높은 정확성을 유지하며 빠르게 연산하는 것이 중요하다.
일반적으로 유전체 분석에는 하버드 브로드 연구소(Broad Institute)에서 개발한 유전체 분석 도구 키트(Genome Analysis Tool Kit, 이하 GATK)를 이용한 데이터 처리 방법을 표준으로 사용한다. 이들 키트 중 BWA-MEM은 GATK에서 표준으로 채택한 유전체 정렬 소프트웨어이며, 2019년에 하버드 대학과 인텔(Intel)의 공동 연구로 BWA-MEM2가 개발됐다.
연구팀이 개발한 머신러닝 기반의 유전체 정렬 소프트웨어는 연산량을 대폭 줄이면서도 표준 유전체 정렬 소프트웨어 BWA-MEM2과 동일한 결과를 만들어 정확도를 유지했다. 사용한 머신러닝 기반의 인덱싱 기법은 주어진 데이터의 분포를 머신러닝 모델이 학습해, 데이터 분포에 최적화된 인덱싱을 찾는 방법론이다. 데이터에 적합하다고 생각되는 인덱싱 방법을 사람이 정하던 기존의 방법과 대비된다.
BWA-MEM과 BWA-MEM2에서 사용하는 인덱싱 기법(FM-index)은 유전자 조각의 위치를 찾기 위해 유전자 조각 길이만큼의 연산이 필요하지만, 연구팀이 제안한 알고리즘은 머신러닝 기반의 인덱싱 기법(Learned-index)을 활용해, 유전자 조각 길이와 상관없이 적은 연산량으로도 유전자 조각의 위치를 찾을 수 있다. 연구팀이 제안한 인덱싱 기법은 기존 인덱싱 기법과 비교해 3.4배 정도 가속화됐고, 이로 인해 유전체 정렬 소프트웨어는 1.4 배 가속화됐다.
연구팀이 이번 연구에서 개발한 유전체 정렬 소프트웨어는 오픈소스 (https://github.com/kaist-ina/BWA-MEME)로 공개돼 많은 분야에 사용될 것으로 기대되며, 유전체 분석에서 사용되는 다양한 소프트웨어를 머신러닝 기술로 가속화하는 연구들의 초석이 될 것으로 기대된다.
한동수 교수는 "이번 연구를 통해 기계학습 기술을 접목해 전장 유전체 빅데이터 분석을 기존 방식보다 빠르고 적은 비용으로 할 수 있다는 것을 보여줬으며, 앞으로 인공지능 기술을 활용해 전장 유전체 빅데이터 분석을 효율화, 고도화할 수 있을 것이라 기대된다ˮ고 말했다.
한편 이번 연구는 과학기술정보통신부의 재원으로 한국연구재단의 지원을 받아 데이터 스테이션 구축·운영 사업으로서 수행됐다.
2022.04.17 조회수 12535