%EB%A9%B4%EC%97%AD%ED%95%99
-
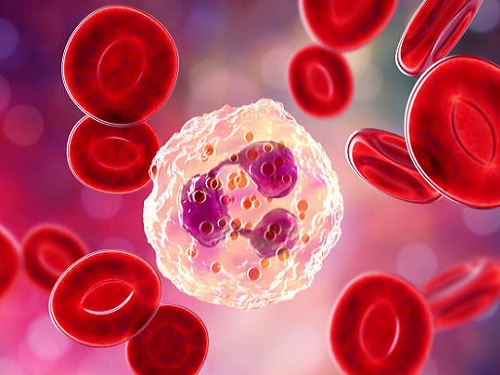 이행 호염구, 알레르기 매개 세포에 대한 새로운 이해
우리 대학 생명과학과 강석조 교수 연구팀이 알레르기를 매개하는 중요한 면역세포인 호염구의 새로운 전구세포를 발견하고, 호염구 말단 분화단계에서 그 고유 기능을 획득하는 데 중요한 전사인자를 규명했다고 7일 밝혔다.
호염구(basophil)는 체내에 극소수로 존재하는 백혈구지만, 알레르기와 같이 제2형 면역 반응으로 매개되는 질환의 주된 작용 세포다. 호염구의 혈액 내 증감을 통해서 알레르기 반응 정도를 판별할 수 있고, 질환의 면역 반응의 중증도에도 영향을 미친다. 호염구는 인체 내로 유입된 알레르기 유발 물질에 특이적인 Immunoglobulin E (IgE)에 대한 수용체를 통해 활성화되면 탈과립(degranulation)과 면역조절 물질인 사이토카인(cytokine)을 비롯해 다양한 염증 유도 물질들을 분비한다. 이를 통하여 호염구는 알레르기 반응을 매개하고 다른 면역세포들의 침윤을 도와 염증 반응을 심화시킨다. 하지만, 이러한 호염구의 초기 분화 과정 연구에 비해 그 고유 기능을 획득하는 말단 분화 과정과 이를 조절하는 인자에 대해서는 알려진 바가 없었다.
강 교수 연구팀은 마우스 골수 내에서 호염구 전구세포(basophil progenitor, BaP)가 세포분열이 없는 최종 분화단계의 성숙한 호염구(mature basophil)로 분화하는 과정 중간에 위치한, 세포분열 능력을 보유한 새로운 전구세포를 발견하였으며 그 특성을 다양한 실험으로 규명하고 ‘이행 호염구(transitional basophil, tBaso)’로 명명하였다. 이행 호염구의 발견을 통하여 강 교수팀은 호염구의 분화과정에서 변화하는 유전자 발현을 더욱 세밀하게 분석할 수 있었으며 세포분열 및 주기 조절과 호염구의 고유한 기능의 조절에 관계하는 유전자의 발현은 분화단계에 따라 다르게 조절됨을 확인하였다.
이어, 호염구의 분화단계에 따라 발현이 변화하는 전사인자 NFIL3를 확인하였고, NFIL3 단백질이 호염구의 말단 분화단계에서 IgE 수용체 활성화에 따라 유도된 호염구의 기능적 특징을 부여하는 중요 인자임을 규명하여 보고하였다. 또한, 호염구 특이적으로 NFIL3가 결손된 마우스를 이용하여, 호염구 내 NFIL3 단백질이 아토피성 피부 질환의 염증 반응을 조절함을 밝혔다.
연구팀은 이행 호염구가 성숙 호염구에 비해 사이토카인 생성 능력이 뛰어남을 추가로 확인하였으며, 사이토카인 자극의 종류에 따라 다른 종류의 제2형 면역반응 사이토카인을 생성함을 밝혔다. 이러한 차별적 사이토카인 생성 능력은 호염구에서는 최초로 발견된 것으로, 추후 호염구 매개 질환에서 그 작용기전을 설명하는 데 중요한 지식을 제공할 것으로 기대한다.
강석조 교수는 “호염구의 말단 분화과정의 중요 전구세포를 발견하고 호염구의 기능적 전문성을 획득하는 다이나믹한 과정을 밝힌 연구”라고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 호염구가 매개하는 알레르기 질환에 대한 이해와 치료제 개발에 활용될 것으로 기대한다”고 전했다.
이번 연구는 면역학 및 알레르기 분야의 세계 최고 국제 학술지 ‘알레르기 및 임상면역학 저널 (The Journal of Allergy and Clinical Immunology)’에 10월 1일 字 온라인판에 게재됐다 (논문명: The transcription factor NFIL3/E4BP4 regulates the developmental stage-specific acquisition of basophil function). KAIST 생명과학과 강석조 교수 연구팀 박지연 박사, 조유리 박사(現 LG화학)가 공동 제1 저자로 연구를 주도하였고, 바이오및뇌공학과 양동찬 박사, 생명과학과 양한슬, 이대엽 교수팀, RIKEN Masato Kubo 교수 연구팀이 함께 참여하였다.
한편 이번 연구는 한국연구재단의 선도연구센터사업의 지원을 받아 수행됐다.
2023.11.07 조회수 5524
이행 호염구, 알레르기 매개 세포에 대한 새로운 이해
우리 대학 생명과학과 강석조 교수 연구팀이 알레르기를 매개하는 중요한 면역세포인 호염구의 새로운 전구세포를 발견하고, 호염구 말단 분화단계에서 그 고유 기능을 획득하는 데 중요한 전사인자를 규명했다고 7일 밝혔다.
호염구(basophil)는 체내에 극소수로 존재하는 백혈구지만, 알레르기와 같이 제2형 면역 반응으로 매개되는 질환의 주된 작용 세포다. 호염구의 혈액 내 증감을 통해서 알레르기 반응 정도를 판별할 수 있고, 질환의 면역 반응의 중증도에도 영향을 미친다. 호염구는 인체 내로 유입된 알레르기 유발 물질에 특이적인 Immunoglobulin E (IgE)에 대한 수용체를 통해 활성화되면 탈과립(degranulation)과 면역조절 물질인 사이토카인(cytokine)을 비롯해 다양한 염증 유도 물질들을 분비한다. 이를 통하여 호염구는 알레르기 반응을 매개하고 다른 면역세포들의 침윤을 도와 염증 반응을 심화시킨다. 하지만, 이러한 호염구의 초기 분화 과정 연구에 비해 그 고유 기능을 획득하는 말단 분화 과정과 이를 조절하는 인자에 대해서는 알려진 바가 없었다.
강 교수 연구팀은 마우스 골수 내에서 호염구 전구세포(basophil progenitor, BaP)가 세포분열이 없는 최종 분화단계의 성숙한 호염구(mature basophil)로 분화하는 과정 중간에 위치한, 세포분열 능력을 보유한 새로운 전구세포를 발견하였으며 그 특성을 다양한 실험으로 규명하고 ‘이행 호염구(transitional basophil, tBaso)’로 명명하였다. 이행 호염구의 발견을 통하여 강 교수팀은 호염구의 분화과정에서 변화하는 유전자 발현을 더욱 세밀하게 분석할 수 있었으며 세포분열 및 주기 조절과 호염구의 고유한 기능의 조절에 관계하는 유전자의 발현은 분화단계에 따라 다르게 조절됨을 확인하였다.
이어, 호염구의 분화단계에 따라 발현이 변화하는 전사인자 NFIL3를 확인하였고, NFIL3 단백질이 호염구의 말단 분화단계에서 IgE 수용체 활성화에 따라 유도된 호염구의 기능적 특징을 부여하는 중요 인자임을 규명하여 보고하였다. 또한, 호염구 특이적으로 NFIL3가 결손된 마우스를 이용하여, 호염구 내 NFIL3 단백질이 아토피성 피부 질환의 염증 반응을 조절함을 밝혔다.
연구팀은 이행 호염구가 성숙 호염구에 비해 사이토카인 생성 능력이 뛰어남을 추가로 확인하였으며, 사이토카인 자극의 종류에 따라 다른 종류의 제2형 면역반응 사이토카인을 생성함을 밝혔다. 이러한 차별적 사이토카인 생성 능력은 호염구에서는 최초로 발견된 것으로, 추후 호염구 매개 질환에서 그 작용기전을 설명하는 데 중요한 지식을 제공할 것으로 기대한다.
강석조 교수는 “호염구의 말단 분화과정의 중요 전구세포를 발견하고 호염구의 기능적 전문성을 획득하는 다이나믹한 과정을 밝힌 연구”라고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 호염구가 매개하는 알레르기 질환에 대한 이해와 치료제 개발에 활용될 것으로 기대한다”고 전했다.
이번 연구는 면역학 및 알레르기 분야의 세계 최고 국제 학술지 ‘알레르기 및 임상면역학 저널 (The Journal of Allergy and Clinical Immunology)’에 10월 1일 字 온라인판에 게재됐다 (논문명: The transcription factor NFIL3/E4BP4 regulates the developmental stage-specific acquisition of basophil function). KAIST 생명과학과 강석조 교수 연구팀 박지연 박사, 조유리 박사(現 LG화학)가 공동 제1 저자로 연구를 주도하였고, 바이오및뇌공학과 양동찬 박사, 생명과학과 양한슬, 이대엽 교수팀, RIKEN Masato Kubo 교수 연구팀이 함께 참여하였다.
한편 이번 연구는 한국연구재단의 선도연구센터사업의 지원을 받아 수행됐다.
2023.11.07 조회수 5524 -
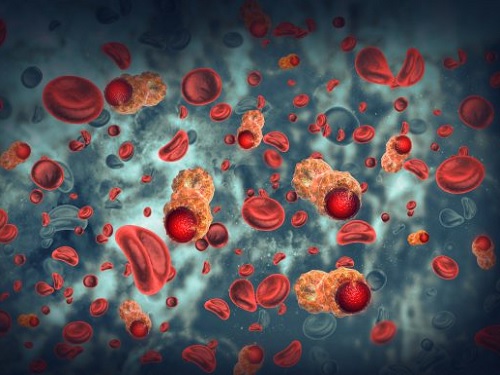 천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
2023.04.26 조회수 7712
천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
2023.04.26 조회수 7712 -
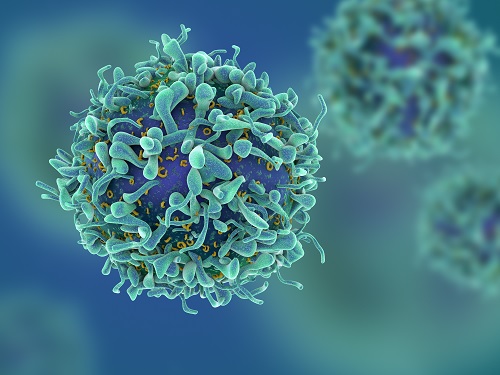 기존 개념을 깬 새로운 면역 T 세포 발견
우리 대학 의과학대학원 신의철 교수 연구팀이 우리 대학 의과학대학원 박수형 교수, 연세대학교 의과대학 주동진, 박준용 교수팀과 공동 연구를 통해 선천면역과 적응면역의 특성을 모두 지니는 새로운 유형의 `NK 유사 T 세포'를 간에서 발견하고 그 작용 특성을 규명했다고 8일 밝혔다.
이번 연구는, 그동안 면역학의 영역에서 이분법적으로 나눠져 있던 선천면역과 적응면역의 경계에서 작동하는 새로운 면역세포를 발견하고 그 특성을 밝힘으로써 인체의 면역 반응을 새로운 시각에서 바라볼 수 있게 했다는 점에서 큰 의의가 있다.
의과학대학원 고준영 박사, 나민석 박사, 최승진 박사가 공동 제1 저자로 참여한 이번 연구 결과는 간장(肝腸)학 분야의 최고 국제 학술지 `간장학 저널(Journal of Hepatology)' 5월 26일 字 온라인판에 게재됐다 (논문명: Identification of a distinct NK-like hepatic T-cell population activated by NKG2C in a TCR-independent manner).
인체에 세균이나 바이러스 같은 병원성 미생물이 침입하면 먼저 선천면역이 작동한다. 선천면역은 신속하게 작동하는 장점이 있지만, 병원성 미생물의 종류를 구분하지 못하고 기억면역을 형성하지 못하는 단점이 있다. 한편 감염 후 4~5일 후부터는 적응면역이 서서히 작동한다. 적응면역은 느리게 활성화되는 대신 각각의 병원성 미생물을 구분하는 능력이 있고 회복 후에는 기억 면역 세포를 만들어 같은 미생물이 재침입하였을 때 재빠른 반응을 할 수 있다.
특히 바이러스 감염 시에는 바이러스에 감염된 세포를 제거하는 기능에 특화된 면역세포들이 중요한 역할을 하는데, 이들 중 NK 세포(자연살해 세포)는 선천면역, T 세포는 적응면역의 특성이 있는 대표적인 면역 세포다. 이 2가지 면역 세포는 바이러스에 감염된 세포를 인식하는 방식도 달라, T 세포는 바이러스 단백질 조각을 항원으로 감지하는 반면, NK 세포는 스트레스 분자 발현이 증가한 것을 통해 바이러스 감염 세포를 감지한다.
지금까지 면역학계에서는 이렇게 NK 세포와 T 세포를 명확히 구분되는 면역 세포로서 나누어 연구를 진행해 왔는데, 연구팀은 이번 연구를 통해 NK 세포와 T 세포의 특성을 모두 지니는 `NK 유사 T 세포'를 새롭게 발견한 것이다. 그리고 이러한 NK 유사 T 세포는 T 세포 수용체를 통해 바이러스 단백질 항원을 인식하는 대신에 NK 세포 수용체인 `NKG2C'를 통해 비정상 세포들을 감지하고 제거할 수 있다는 사실을 발견했다.
연구팀은 이번 연구에서 간에 존재하는 면역세포를 주로 분석했는데, 간은 면역학적으로 특이한 장기로 여겨지고 있다. 소장이나 대장으로부터 들어오는 혈액은 전신 순환계에 합류하기 전에 간을 먼저 지나게 된다. 이 과정에서 장으로부터 들어온 많은 외부 물질이나 병원성 미생물들은 간에서 걸러지게 되어, 간은 면역학적 1차 관문의 역할을 하게 된다. 한편 간은 면역학적 관용을 나타내는 장기로도 잘 알려져, 병원성 미생물에 대한 과도한 면역 반응을 조절하기도 한다. 연구팀은 이처럼 복잡하고 정교하게 조절되는 간의 면역학적 특성을 상세히 분석하기 위해 단일세포 전사체 분석이라는 최신 연구기법을 적용해 분석한 결과, 간 내에서 선천면역과 적응면역의 특성을 모두 지니는 NK 유사 T 세포를 발견했다. 그리고 B형간염 바이러스에 의한 만성 간 질환을 앓는 환자의 간에서는 이러한 NK 유사 T 세포의 수가 증가해 있는 것도 발견했다.
연구팀이 이번에 새롭게 발견한 NK 유사 T 세포가 바이러스 감염 등의 각종 질환에서 어떤 역할을 하는지는 아직 분명하지 않다. 현재 연구팀은 NK 유사 T 세포가 체내에서 감염뿐만 아니라 각종 원인에 의해 비정상적으로 변한 세포들을 선택적으로 제거해 체내 항상성을 유지하는 데 중요한 역할을 한다는 가설을 가지고 후속 연구를 활발히 진행하고 있다. 한편, 미국 스탠퍼드 의대의 마크 데이비스 교수 연구팀이 최근 NK 수용체를 발현하는 T 세포는 다른 면역세포의 기능을 억제한다는 논문을 사이언스지에 발표함에 따라, 연구팀은 이번에 발견한 NK 유사 T 세포가 체내 상황에 따라 면역억제 기능을 수행하는지에 대한 분석도 진행하고 있다.
이번 연구 결과는 연세의대 세브란스병원 외과 및 내과 연구팀과 KAIST 의과학대학원이 간의 면역학적 특성을 규명하기 위해 수행한 협동 연구의 성과로서, 중개 연구(translational research)를 통해 인간 면역학을 새롭게 이해하는 계기를 마련했다는 평가를 받는다.
의과학대학원 신의철 교수는 "최신 연구 방법인 단일세포 전사체 분석 기술을 이용해 복잡한 간장 내 면역세포들을 상세히 분석할 수 있었고, 그 결과로 새로운 유형의 면역 세포인 NK 유사 T 세포를 발견하게 된 중요한 연구ˮ라며 "앞으로 NK 유사 T 세포의 생리 및 병리적 기능을 밝히는 연구를 지속하겠다ˮ라고 말했다.
2022.06.08 조회수 10376
기존 개념을 깬 새로운 면역 T 세포 발견
우리 대학 의과학대학원 신의철 교수 연구팀이 우리 대학 의과학대학원 박수형 교수, 연세대학교 의과대학 주동진, 박준용 교수팀과 공동 연구를 통해 선천면역과 적응면역의 특성을 모두 지니는 새로운 유형의 `NK 유사 T 세포'를 간에서 발견하고 그 작용 특성을 규명했다고 8일 밝혔다.
이번 연구는, 그동안 면역학의 영역에서 이분법적으로 나눠져 있던 선천면역과 적응면역의 경계에서 작동하는 새로운 면역세포를 발견하고 그 특성을 밝힘으로써 인체의 면역 반응을 새로운 시각에서 바라볼 수 있게 했다는 점에서 큰 의의가 있다.
의과학대학원 고준영 박사, 나민석 박사, 최승진 박사가 공동 제1 저자로 참여한 이번 연구 결과는 간장(肝腸)학 분야의 최고 국제 학술지 `간장학 저널(Journal of Hepatology)' 5월 26일 字 온라인판에 게재됐다 (논문명: Identification of a distinct NK-like hepatic T-cell population activated by NKG2C in a TCR-independent manner).
인체에 세균이나 바이러스 같은 병원성 미생물이 침입하면 먼저 선천면역이 작동한다. 선천면역은 신속하게 작동하는 장점이 있지만, 병원성 미생물의 종류를 구분하지 못하고 기억면역을 형성하지 못하는 단점이 있다. 한편 감염 후 4~5일 후부터는 적응면역이 서서히 작동한다. 적응면역은 느리게 활성화되는 대신 각각의 병원성 미생물을 구분하는 능력이 있고 회복 후에는 기억 면역 세포를 만들어 같은 미생물이 재침입하였을 때 재빠른 반응을 할 수 있다.
특히 바이러스 감염 시에는 바이러스에 감염된 세포를 제거하는 기능에 특화된 면역세포들이 중요한 역할을 하는데, 이들 중 NK 세포(자연살해 세포)는 선천면역, T 세포는 적응면역의 특성이 있는 대표적인 면역 세포다. 이 2가지 면역 세포는 바이러스에 감염된 세포를 인식하는 방식도 달라, T 세포는 바이러스 단백질 조각을 항원으로 감지하는 반면, NK 세포는 스트레스 분자 발현이 증가한 것을 통해 바이러스 감염 세포를 감지한다.
지금까지 면역학계에서는 이렇게 NK 세포와 T 세포를 명확히 구분되는 면역 세포로서 나누어 연구를 진행해 왔는데, 연구팀은 이번 연구를 통해 NK 세포와 T 세포의 특성을 모두 지니는 `NK 유사 T 세포'를 새롭게 발견한 것이다. 그리고 이러한 NK 유사 T 세포는 T 세포 수용체를 통해 바이러스 단백질 항원을 인식하는 대신에 NK 세포 수용체인 `NKG2C'를 통해 비정상 세포들을 감지하고 제거할 수 있다는 사실을 발견했다.
연구팀은 이번 연구에서 간에 존재하는 면역세포를 주로 분석했는데, 간은 면역학적으로 특이한 장기로 여겨지고 있다. 소장이나 대장으로부터 들어오는 혈액은 전신 순환계에 합류하기 전에 간을 먼저 지나게 된다. 이 과정에서 장으로부터 들어온 많은 외부 물질이나 병원성 미생물들은 간에서 걸러지게 되어, 간은 면역학적 1차 관문의 역할을 하게 된다. 한편 간은 면역학적 관용을 나타내는 장기로도 잘 알려져, 병원성 미생물에 대한 과도한 면역 반응을 조절하기도 한다. 연구팀은 이처럼 복잡하고 정교하게 조절되는 간의 면역학적 특성을 상세히 분석하기 위해 단일세포 전사체 분석이라는 최신 연구기법을 적용해 분석한 결과, 간 내에서 선천면역과 적응면역의 특성을 모두 지니는 NK 유사 T 세포를 발견했다. 그리고 B형간염 바이러스에 의한 만성 간 질환을 앓는 환자의 간에서는 이러한 NK 유사 T 세포의 수가 증가해 있는 것도 발견했다.
연구팀이 이번에 새롭게 발견한 NK 유사 T 세포가 바이러스 감염 등의 각종 질환에서 어떤 역할을 하는지는 아직 분명하지 않다. 현재 연구팀은 NK 유사 T 세포가 체내에서 감염뿐만 아니라 각종 원인에 의해 비정상적으로 변한 세포들을 선택적으로 제거해 체내 항상성을 유지하는 데 중요한 역할을 한다는 가설을 가지고 후속 연구를 활발히 진행하고 있다. 한편, 미국 스탠퍼드 의대의 마크 데이비스 교수 연구팀이 최근 NK 수용체를 발현하는 T 세포는 다른 면역세포의 기능을 억제한다는 논문을 사이언스지에 발표함에 따라, 연구팀은 이번에 발견한 NK 유사 T 세포가 체내 상황에 따라 면역억제 기능을 수행하는지에 대한 분석도 진행하고 있다.
이번 연구 결과는 연세의대 세브란스병원 외과 및 내과 연구팀과 KAIST 의과학대학원이 간의 면역학적 특성을 규명하기 위해 수행한 협동 연구의 성과로서, 중개 연구(translational research)를 통해 인간 면역학을 새롭게 이해하는 계기를 마련했다는 평가를 받는다.
의과학대학원 신의철 교수는 "최신 연구 방법인 단일세포 전사체 분석 기술을 이용해 복잡한 간장 내 면역세포들을 상세히 분석할 수 있었고, 그 결과로 새로운 유형의 면역 세포인 NK 유사 T 세포를 발견하게 된 중요한 연구ˮ라며 "앞으로 NK 유사 T 세포의 생리 및 병리적 기능을 밝히는 연구를 지속하겠다ˮ라고 말했다.
2022.06.08 조회수 10376 -
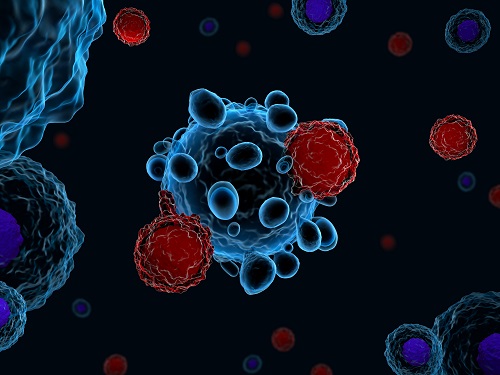 방관자 T세포에 의한 질병 발생 이론 발표
우리 대학 의과학대학원 신의철 교수, 이호영 박사, 정성주 대학원생이 감염질환에서 방관자 (bystander) T세포 활성화의 중요성을 강조하는 주제로 세계적인 면역학 권위지인 `네이처 이뮤놀로지(Nature Immunology)' 8월호에 초청 리뷰 논문을 게재했다고 31일 밝혔다.
인간 질병에서 방관자 T세포의 역할에 관한 연구를 세계적으로 선도하고 있는 신의철 교수 연구팀은 이번 리뷰 논문을 통해 다양한 감염질환에서 방관자 T세포의 역할과 이를 조절하는 기전들을 총체적으로 고찰하고 인간 질병 치료에 응용할 수 있는 미래 연구의 방향을 제시했다.
일반적으로 인체는 바이러스에 감염되면 항바이러스 작용을 하는 T세포가 활성화되어 질병으로부터의 회복을 촉진한다고 알려져 있다. 이때 특정 바이러스에 대응하는 T세포만 활성화되고 관련 없는 T세포들은 활성화되지 않는데, 이러한 현상을 선택적 면역반응이라고 한다. 선택적 면역반응은 T세포가 바이러스의 항원 펩타이드를 인식하면서 이뤄진다.
하지만 바이러스의 종류 및 환자의 면역 체계에 따라, 감염을 일으키는 바이러스와는 상관없는 T세포의 활성화가 일어나게 되는데 이를 방관자 T세포의 활성화라고 이야기한다. 방관자 T세포의 활성화는 바이러스 항원 펩타이드의 존재와는 상관없이 사이토카인(cytokine)에 의해 유발된다고 알려져 있다. 이러한 방관자 T세포의 활성화는 복잡한 감염 이력을 가진 사람의 면역반응을 더 정교하게 이해하기 위해 반드시 고려해야 하는 현상이다.
과거 신의철 교수 연구팀은 2010년대에 한국에서 유행했던 A형 간염 바이러스 감염환자에서 간세포가 심하게 파괴되는 원인으로 방관자 T세포의 활성화 현상을 새롭게 발견해 그 결과를 2018년 권위 있는 면역학 학술지 `이뮤니티(Immunity)'에 보고한 바 있다. 이는 인간 질병에서 방관자 T세포의 역할을 체계적으로 증명한 세계 첫 논문으로 인정받고 있다.
이후 연구팀은 관련 연구를 활발히 지속하며 더 상세한 기전들을 발견해왔다. 간 조직에 상주하며 방관자 활성화를 일으킬 수 있는 T세포를 조절하는 분자를 발견하여 2020년 국제적 학술지 `저널 오브 헤파톨로지 (Journal of Hepatology)'에 보고했고, 특수한 T세포인 점막연관 불변사슬 T세포(MAIT: Mucosal-associated invariant T)도 유사한 활성 과정을 거쳐 간 손상에 기여할 수 있음을 발견해 같은 해 동일 저널에 발표했다.
또한, 최근에는 활성화된 방관자 T세포들이 감염된 조직으로 이동하는데 필요한 세포이동 관련 기전을 발견하여 국제학술지 `셀 리포트 (Cell Reports)'에 보고한 바도 있다.
현재 연구팀은 방관자 T세포 활성화 특성 및 관련 기전을 바이러스 질환 그리고 종양질환에서 밝혀내는 후속 연구를 진행 중이다. 또한, 현재 전 세계적으로 유행 중인 코로나19 감염상황에서 방관자 T세포 활성화 및 역할에 관한 연구도 진행하고 있다.
신의철 교수 연구팀은 방관자 T세포 활성화 연구 분야를 개척하고 확장해 나가고 있는 공로를 인정받아 이번 초청 리뷰 논문을 게재하게 됐다.
이러한 그동안의 연구는 2014년부터 삼성미래기술육성재단의 지속적인 지원을 받아 수행될 수 있었다. 연구팀의 이번 리뷰 논문은 국제 면역학 저명 학술지인 네이처 이뮤놀로지 (Nature Immunology) 誌 8월 5일 字에 게재됐다(논문명: Significance of bystander T cell activation in microbial infection).
이번 연구의 제1 저자인 우리 대학 이호영 박사(박사후 연구원)는 "그동안 면역학계에서 그 중요성을 몰랐던 방관자 T세포 활성화 현상이 이번 리뷰 논문을 통해 크게 주목받기를 기대한다며, 앞으로 다양한 질병에서의 방관자 T세포의 역할 및 관련 기전들의 규명을 위해 노력하겠다ˮ고 말했다.
신의철 교수는 "한국에서 개척한 연구 분야가 국제 면역학계에서 인정을 받는 것이 기쁘다며, 방관자 T세포의 연구가 논문에서만 그치지 않고 신약개발의 단초가 되도록 노력하겠다ˮ 라고 말했다.
2021.09.01 조회수 11737
방관자 T세포에 의한 질병 발생 이론 발표
우리 대학 의과학대학원 신의철 교수, 이호영 박사, 정성주 대학원생이 감염질환에서 방관자 (bystander) T세포 활성화의 중요성을 강조하는 주제로 세계적인 면역학 권위지인 `네이처 이뮤놀로지(Nature Immunology)' 8월호에 초청 리뷰 논문을 게재했다고 31일 밝혔다.
인간 질병에서 방관자 T세포의 역할에 관한 연구를 세계적으로 선도하고 있는 신의철 교수 연구팀은 이번 리뷰 논문을 통해 다양한 감염질환에서 방관자 T세포의 역할과 이를 조절하는 기전들을 총체적으로 고찰하고 인간 질병 치료에 응용할 수 있는 미래 연구의 방향을 제시했다.
일반적으로 인체는 바이러스에 감염되면 항바이러스 작용을 하는 T세포가 활성화되어 질병으로부터의 회복을 촉진한다고 알려져 있다. 이때 특정 바이러스에 대응하는 T세포만 활성화되고 관련 없는 T세포들은 활성화되지 않는데, 이러한 현상을 선택적 면역반응이라고 한다. 선택적 면역반응은 T세포가 바이러스의 항원 펩타이드를 인식하면서 이뤄진다.
하지만 바이러스의 종류 및 환자의 면역 체계에 따라, 감염을 일으키는 바이러스와는 상관없는 T세포의 활성화가 일어나게 되는데 이를 방관자 T세포의 활성화라고 이야기한다. 방관자 T세포의 활성화는 바이러스 항원 펩타이드의 존재와는 상관없이 사이토카인(cytokine)에 의해 유발된다고 알려져 있다. 이러한 방관자 T세포의 활성화는 복잡한 감염 이력을 가진 사람의 면역반응을 더 정교하게 이해하기 위해 반드시 고려해야 하는 현상이다.
과거 신의철 교수 연구팀은 2010년대에 한국에서 유행했던 A형 간염 바이러스 감염환자에서 간세포가 심하게 파괴되는 원인으로 방관자 T세포의 활성화 현상을 새롭게 발견해 그 결과를 2018년 권위 있는 면역학 학술지 `이뮤니티(Immunity)'에 보고한 바 있다. 이는 인간 질병에서 방관자 T세포의 역할을 체계적으로 증명한 세계 첫 논문으로 인정받고 있다.
이후 연구팀은 관련 연구를 활발히 지속하며 더 상세한 기전들을 발견해왔다. 간 조직에 상주하며 방관자 활성화를 일으킬 수 있는 T세포를 조절하는 분자를 발견하여 2020년 국제적 학술지 `저널 오브 헤파톨로지 (Journal of Hepatology)'에 보고했고, 특수한 T세포인 점막연관 불변사슬 T세포(MAIT: Mucosal-associated invariant T)도 유사한 활성 과정을 거쳐 간 손상에 기여할 수 있음을 발견해 같은 해 동일 저널에 발표했다.
또한, 최근에는 활성화된 방관자 T세포들이 감염된 조직으로 이동하는데 필요한 세포이동 관련 기전을 발견하여 국제학술지 `셀 리포트 (Cell Reports)'에 보고한 바도 있다.
현재 연구팀은 방관자 T세포 활성화 특성 및 관련 기전을 바이러스 질환 그리고 종양질환에서 밝혀내는 후속 연구를 진행 중이다. 또한, 현재 전 세계적으로 유행 중인 코로나19 감염상황에서 방관자 T세포 활성화 및 역할에 관한 연구도 진행하고 있다.
신의철 교수 연구팀은 방관자 T세포 활성화 연구 분야를 개척하고 확장해 나가고 있는 공로를 인정받아 이번 초청 리뷰 논문을 게재하게 됐다.
이러한 그동안의 연구는 2014년부터 삼성미래기술육성재단의 지속적인 지원을 받아 수행될 수 있었다. 연구팀의 이번 리뷰 논문은 국제 면역학 저명 학술지인 네이처 이뮤놀로지 (Nature Immunology) 誌 8월 5일 字에 게재됐다(논문명: Significance of bystander T cell activation in microbial infection).
이번 연구의 제1 저자인 우리 대학 이호영 박사(박사후 연구원)는 "그동안 면역학계에서 그 중요성을 몰랐던 방관자 T세포 활성화 현상이 이번 리뷰 논문을 통해 크게 주목받기를 기대한다며, 앞으로 다양한 질병에서의 방관자 T세포의 역할 및 관련 기전들의 규명을 위해 노력하겠다ˮ고 말했다.
신의철 교수는 "한국에서 개척한 연구 분야가 국제 면역학계에서 인정을 받는 것이 기쁘다며, 방관자 T세포의 연구가 논문에서만 그치지 않고 신약개발의 단초가 되도록 노력하겠다ˮ 라고 말했다.
2021.09.01 조회수 11737 -
 중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 33377
중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 33377 -
 항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
2020.06.16 조회수 24813
항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
2020.06.16 조회수 24813 -
 신의철 교수, 암세포의 면역세포 억제 핵심원리 규명
〈 신의철 교수, 김창곤 연구원 〉
우리 대학 의과학대학원 신의철 교수, 연세대학교 의과대학 민병소, 김호근 교수 공동 연구팀이 암 환자의 암세포가 면역세포를 억제해 면역반응을 회피하게 만드는 핵심원리를 발견했다.
이번 연구를 통해 최근 유행하는 면역항암제의 치료 효율을 높일 수 있는 효과적인 암 치료 전략을 제시할 수 있을 것으로 기대된다.
김창곤 연구원, 장미 연구교수가 공동 1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 ‘사이언스 면역학(Science Immunology)’ 11월 8일 자 온라인판에 게재됐다 (논문명 : VEGF-A drives TOX-dependent T cell exhaustion in anti–PD-1–resistant microsatellite stable colorectal cancers).
암 환자는 암세포에 대항하는 면역세포, 특히 T세포의 기능이 현저히 약해져 있다. 이렇게 T세포의 기능이 약해지는 주된 이유는 T세포가 PD-1이라는 억제 수용체를 과다하게 발현하기 때문이다.
최근 유행하고 있는 면역항암제도 바로 이 PD-1 억제 수용체의 기능을 차단해 T세포의 기능을 회복시키는 원리로 작동하는 것이다. 하지만 면역항암제는 아직 부족한 부분이 많아 투여받은 암 환자 중 일부에게만 치료 반응이 나타나는 현실이다. 이러한 이유로 많은 연구자가 암 환자의 T세포 기능이 약해지는 다른 이유를 활발히 찾고 있다.
이번 연구에서 공동 연구팀은, 그간 혈관형성인자로만 알려졌던 혈관내피성장인자(vascular endothelial growth factor; VEGF)라는 혈관형성인자 단백질이 암세포에 대항하는 T세포의 기능을 약하게 만드는 주요 원인임을 새롭게 밝혔다.
종양의 지속적인 성장을 위해 암세포는 혈관내피성장인자를 과다 생성하고, 이로 인해 암 조직에는 혈관이 과다 생성된다는 사실은 이미 잘 알려져 있었다. 연구팀은 이번 연구를 통해 혈관내피성장인자가 혈관 형성 이외에도 T세포 억제라는 중요한 작용을 통해 암의 성장을 돕는다는 사실을 새롭게 규명했다.
암세포에서 생성된 혈관내피성장인자는 암세포에 대항하는 T세포 표면에 발현하는 수용체에 결합해 T세포에 톡스(TOX)라 불리는 단백질의 발현을 유도하고, 톡스는 T세포의 기능을 억제하고 약화하는 유전자 발현 프로그램을 작동시킨다는 것이 이번 연구의 핵심이다.
연구팀은 기초적인 발견에 그치지 않고 암 환자의 면역항암제 치료 효율을 높이는 전략을 제시했다. 암 성장을 막을 목적으로 혈관내피성장인자 저해제가 이미 개발됐기 때문에, 연구팀이 새로 발견한 혈관내피성장인자의 T세포 기능 억제작용을 근거로 혈관내피성장인자 저해제를 면역항암제와 함께 사용한다면 치료 효율을 극대화할 수 있을 것으로 기대하고 있다.
실제 이번 연구에서도 면역항암제와 혈관내피성장인자 저해제를 병합 치료하면 우수한 항암 효과가 있음을 동물 모델에서 증명했다.
이번 연구는 연세대학교 의과대학 외과 및 병리학과 연구팀과 KAIST 의과학대학원이 암 환자의 면역학적 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로 중개 연구(translational research)의 주요 성과로 평가받는다.
신 교수는 “암세포와 면역세포 사이에서 어떤 일이 벌어지는지를 상세히 연구함으로써 임상 치료 전략을 제시하게 된 중요한 연구이다”라며 “향후 암 환자의 생존율을 높일 수 있는 새로운 면역기전 연구 및 면역항암제 개발 연구를 계속하겠다”라고 말했다.
이번 연구는 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 신의철 교수 연구팀 연구성과 개념도
2019.11.13 조회수 12784
신의철 교수, 암세포의 면역세포 억제 핵심원리 규명
〈 신의철 교수, 김창곤 연구원 〉
우리 대학 의과학대학원 신의철 교수, 연세대학교 의과대학 민병소, 김호근 교수 공동 연구팀이 암 환자의 암세포가 면역세포를 억제해 면역반응을 회피하게 만드는 핵심원리를 발견했다.
이번 연구를 통해 최근 유행하는 면역항암제의 치료 효율을 높일 수 있는 효과적인 암 치료 전략을 제시할 수 있을 것으로 기대된다.
김창곤 연구원, 장미 연구교수가 공동 1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 ‘사이언스 면역학(Science Immunology)’ 11월 8일 자 온라인판에 게재됐다 (논문명 : VEGF-A drives TOX-dependent T cell exhaustion in anti–PD-1–resistant microsatellite stable colorectal cancers).
암 환자는 암세포에 대항하는 면역세포, 특히 T세포의 기능이 현저히 약해져 있다. 이렇게 T세포의 기능이 약해지는 주된 이유는 T세포가 PD-1이라는 억제 수용체를 과다하게 발현하기 때문이다.
최근 유행하고 있는 면역항암제도 바로 이 PD-1 억제 수용체의 기능을 차단해 T세포의 기능을 회복시키는 원리로 작동하는 것이다. 하지만 면역항암제는 아직 부족한 부분이 많아 투여받은 암 환자 중 일부에게만 치료 반응이 나타나는 현실이다. 이러한 이유로 많은 연구자가 암 환자의 T세포 기능이 약해지는 다른 이유를 활발히 찾고 있다.
이번 연구에서 공동 연구팀은, 그간 혈관형성인자로만 알려졌던 혈관내피성장인자(vascular endothelial growth factor; VEGF)라는 혈관형성인자 단백질이 암세포에 대항하는 T세포의 기능을 약하게 만드는 주요 원인임을 새롭게 밝혔다.
종양의 지속적인 성장을 위해 암세포는 혈관내피성장인자를 과다 생성하고, 이로 인해 암 조직에는 혈관이 과다 생성된다는 사실은 이미 잘 알려져 있었다. 연구팀은 이번 연구를 통해 혈관내피성장인자가 혈관 형성 이외에도 T세포 억제라는 중요한 작용을 통해 암의 성장을 돕는다는 사실을 새롭게 규명했다.
암세포에서 생성된 혈관내피성장인자는 암세포에 대항하는 T세포 표면에 발현하는 수용체에 결합해 T세포에 톡스(TOX)라 불리는 단백질의 발현을 유도하고, 톡스는 T세포의 기능을 억제하고 약화하는 유전자 발현 프로그램을 작동시킨다는 것이 이번 연구의 핵심이다.
연구팀은 기초적인 발견에 그치지 않고 암 환자의 면역항암제 치료 효율을 높이는 전략을 제시했다. 암 성장을 막을 목적으로 혈관내피성장인자 저해제가 이미 개발됐기 때문에, 연구팀이 새로 발견한 혈관내피성장인자의 T세포 기능 억제작용을 근거로 혈관내피성장인자 저해제를 면역항암제와 함께 사용한다면 치료 효율을 극대화할 수 있을 것으로 기대하고 있다.
실제 이번 연구에서도 면역항암제와 혈관내피성장인자 저해제를 병합 치료하면 우수한 항암 효과가 있음을 동물 모델에서 증명했다.
이번 연구는 연세대학교 의과대학 외과 및 병리학과 연구팀과 KAIST 의과학대학원이 암 환자의 면역학적 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로 중개 연구(translational research)의 주요 성과로 평가받는다.
신 교수는 “암세포와 면역세포 사이에서 어떤 일이 벌어지는지를 상세히 연구함으로써 임상 치료 전략을 제시하게 된 중요한 연구이다”라며 “향후 암 환자의 생존율을 높일 수 있는 새로운 면역기전 연구 및 면역항암제 개발 연구를 계속하겠다”라고 말했다.
이번 연구는 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 신의철 교수 연구팀 연구성과 개념도
2019.11.13 조회수 12784 -
 신의철 교수, 한국과학기술한림원 2019년도 정회원 선정
〈 신 의 철 교수 〉
우리대학 의과학대학원 신의철 교수 등 26명의 국내 과학자가 한국과학기술한림원(원장 이명철) 2019년 신입 정회원으로 선정됐다. 신의철 교수는 네이처 리뷰 면역학에 초청 리뷰논문을 게재한 국내 대표적인 바이러스 면역학자로 꼽힌다.
이밖에 과기한림원은 만 43세 이하 젊은 과학자 중 잠재력과 창의성이 높은 차세대연구자 26명도 선발, 발표했는데 우리대학에서는 이지운 교수(수리과학과)와 임미희 교수(화학과), 김신현 교수(생명화학공학과), 이정률 교수(항공우주공학과), 이현주 교수(생명화학공학과), 정연식 교수(신소재공학과) 등 6명이 학계와 산업계로부터 주목받는 2019년 신입 차세대회원으로 선정됐다.
한국과학기술한림원은 21일 서울 양재동 엘타워에서 2019년도 신년 하례식을 갖고 이들 신입정회원 및 차세대회원을 대상으로 신입회원 회원패 수여식을 가졌다. 이날 하례식에는 이명철 과기한림원장과 문미옥 과학기술정보통신부 제1차관 등 과학기술계 인사 150여명이 같이했다.
2019.01.21 조회수 9620
신의철 교수, 한국과학기술한림원 2019년도 정회원 선정
〈 신 의 철 교수 〉
우리대학 의과학대학원 신의철 교수 등 26명의 국내 과학자가 한국과학기술한림원(원장 이명철) 2019년 신입 정회원으로 선정됐다. 신의철 교수는 네이처 리뷰 면역학에 초청 리뷰논문을 게재한 국내 대표적인 바이러스 면역학자로 꼽힌다.
이밖에 과기한림원은 만 43세 이하 젊은 과학자 중 잠재력과 창의성이 높은 차세대연구자 26명도 선발, 발표했는데 우리대학에서는 이지운 교수(수리과학과)와 임미희 교수(화학과), 김신현 교수(생명화학공학과), 이정률 교수(항공우주공학과), 이현주 교수(생명화학공학과), 정연식 교수(신소재공학과) 등 6명이 학계와 산업계로부터 주목받는 2019년 신입 차세대회원으로 선정됐다.
한국과학기술한림원은 21일 서울 양재동 엘타워에서 2019년도 신년 하례식을 갖고 이들 신입정회원 및 차세대회원을 대상으로 신입회원 회원패 수여식을 가졌다. 이날 하례식에는 이명철 과기한림원장과 문미옥 과학기술정보통신부 제1차관 등 과학기술계 인사 150여명이 같이했다.
2019.01.21 조회수 9620 -
 신의철, 박수형 교수, 네이처 리뷰 면역학에 초청 리뷰논문 게재
우리 대학 의과학대학원 신의철, 박수형 교수와 카톨릭의대 서울성모병원의 성필수 박사가 국내 과학자로는 최초로 ‘네이처 리뷰 면역학(Nature Reviews Immunology)’8월호에 초청 리뷰논문을 게재했다.
‘네이처 리뷰’저널은 네이처 리뷰로부터 초청받은 세계적 석학들이 해당 분야의 전반적인 내용을 총정리 하는 저널이다. 그 중 ‘네이처 리뷰 면역학’은 면역학 분야의 최고 학술지 중 하나로 불린다.
신 교수와 박 교수는 간염 바이러스 면역에 대한 리뷰논문을 작성했다. 사람에게 간염을 일으키는 A형 및 B형, C형 간염 바이러스에 대한 면역반응의 유사점과 차이점을 총체적으로 고찰하고 미래 연구의 방향을 제시했다.
전 세계에서 3억 5천만 명이 B형 간염 바이러스에, 1억 7천만 명이 C형 간염 바이러스에 감염돼 있다. 그러나 B형 간염 바이러스는 체내에서 바이러스를 완전히 제거하는 치료제가 개발되지 않았고 C형 간염은 예방 백신이 개발되지 않았다.
반면 A형 간염은 간 손상을 일으키는 경우가 있긴 하지만 B, C형과 달리 저절로 완치되는 경우가 많다.
신 교수, 박 교수, 성 박사는 이에 주목해 이번 논문에서 A형 간염 바이러스에 대한 면역반응의 특성을 기반으로 B형 간염 바이러스 완치 치료제 및 C형 간염 바이러스 예방 백신을 개발할 수 있음을 논리적으로 제시했다.
신 교수와 박 교수는 지난 15년간 C형 간염 바이러스에 대한 인체 면역반응 연구에 매진했다. 최근에는 국내에서도 유행했던 A형 간염 바이러스 면역에 대한 새 연구 결과들을 발표했고 공로를 인정받아 초청 리뷰논문을 게재했다.
신 교수는 “이번 초청 리뷰는 KAIST 의과학대학원의 면역학 연구가 세계적 수준으로 도약하고 있음을 증명한 것이다” 며 “면역학 연구에 정진해 인간 질병 해결에 도움이 되겠다”고 말했다.
이번 연구의 C형 간염 관련 연구는 한국연구재단의 지원으로 이뤄졌고, 신 교수는 삼성미래기술육성재단의 지원을 통해 A형 간염 바이러스까지 연구를 확장했다.
2016.08.10 조회수 13408
신의철, 박수형 교수, 네이처 리뷰 면역학에 초청 리뷰논문 게재
우리 대학 의과학대학원 신의철, 박수형 교수와 카톨릭의대 서울성모병원의 성필수 박사가 국내 과학자로는 최초로 ‘네이처 리뷰 면역학(Nature Reviews Immunology)’8월호에 초청 리뷰논문을 게재했다.
‘네이처 리뷰’저널은 네이처 리뷰로부터 초청받은 세계적 석학들이 해당 분야의 전반적인 내용을 총정리 하는 저널이다. 그 중 ‘네이처 리뷰 면역학’은 면역학 분야의 최고 학술지 중 하나로 불린다.
신 교수와 박 교수는 간염 바이러스 면역에 대한 리뷰논문을 작성했다. 사람에게 간염을 일으키는 A형 및 B형, C형 간염 바이러스에 대한 면역반응의 유사점과 차이점을 총체적으로 고찰하고 미래 연구의 방향을 제시했다.
전 세계에서 3억 5천만 명이 B형 간염 바이러스에, 1억 7천만 명이 C형 간염 바이러스에 감염돼 있다. 그러나 B형 간염 바이러스는 체내에서 바이러스를 완전히 제거하는 치료제가 개발되지 않았고 C형 간염은 예방 백신이 개발되지 않았다.
반면 A형 간염은 간 손상을 일으키는 경우가 있긴 하지만 B, C형과 달리 저절로 완치되는 경우가 많다.
신 교수, 박 교수, 성 박사는 이에 주목해 이번 논문에서 A형 간염 바이러스에 대한 면역반응의 특성을 기반으로 B형 간염 바이러스 완치 치료제 및 C형 간염 바이러스 예방 백신을 개발할 수 있음을 논리적으로 제시했다.
신 교수와 박 교수는 지난 15년간 C형 간염 바이러스에 대한 인체 면역반응 연구에 매진했다. 최근에는 국내에서도 유행했던 A형 간염 바이러스 면역에 대한 새 연구 결과들을 발표했고 공로를 인정받아 초청 리뷰논문을 게재했다.
신 교수는 “이번 초청 리뷰는 KAIST 의과학대학원의 면역학 연구가 세계적 수준으로 도약하고 있음을 증명한 것이다” 며 “면역학 연구에 정진해 인간 질병 해결에 도움이 되겠다”고 말했다.
이번 연구의 C형 간염 관련 연구는 한국연구재단의 지원으로 이뤄졌고, 신 교수는 삼성미래기술육성재단의 지원을 통해 A형 간염 바이러스까지 연구를 확장했다.
2016.08.10 조회수 13408