%EB%A6%AC%ED%94%84%EB%A1%9C%EA%B7%B8%EB%9E%98%EB%B0%8D
-
 지방세포 이용해 체중 감소 가능하다
우리 연구진이 지방세포를 지방세포 전 단계인 줄기세포로 변화(탈분화)시키며 지방조직의 물리적인 크기를 줄이는 등 체중을 감소시키고 지방세포의 활성화를 통해 체내 신진에너지 대사 변화를 통해 비만이나 당뇨 등 대사성 질환의 제어 방법을 제시하여 화제다.
의과학대학원 서재명 교수 연구팀과 생명과학과 임대식 교수 연구팀의 공동연구를 통해 대사성 질환의 새로운 치료 전략을 규명했다고 1일 밝혔다.
지방조직은 식사 후 여분의 칼로리를 지방 형태로 저장하는 저장고 역할과 호르몬을 분비하는 내분비기관의 역할을 한다. 이 두 가지의 역할 중 하나라도 이상이 생기면 우리의 대사 체계는 무너지고 당뇨 혹은 비만과 같은 대사질환이 걸리게 된다. 그러나 우리 몸이 이 두 가지의 기능을 조화롭게 관장하는지 분자 수준에서의 기전이 알려지지 않았다.
연구팀은 히포 신호전달체계*의 얍타즈(YAP/TAZ) 단백질에 주목, 이 단백질의 지방세포 관련 기능을 규명했다. 1) 식사 유무에 따라 지방조직 안에 있는 얍타즈 단백질의 활성상태가 변한다는 점, 2) 동 단백질의 활성이 지방조직의 크기를 직접적으로 조절한다는 점 3) 에너지소비 및 포만감을 관장하는 렙틴이라는 호르몬의 생성에 얍타즈가 직접적으로 관여를 한다는 점을 밝혔다.
*히포 신호전달체계: 다세포 생물의 조직, 신체 기관의 크기를 결정하는 데 중요한 역할을 하는 세포 내 신호전달체계임.
특히 생체 내에서 활성화된 얍타즈의 역할을 규명하기 위해 라츠1/라츠2(LATS1/LATS2) 유전자를 생쥐의 지방세포에서 특이적으로 결손시켰는데, 지방세포 안에 있는 얍타즈의 지속적인 활성은 지방세포를 지방세포의 전구체, 즉 줄기세포와 같은 세포로 변화(탈분화)시키며 지방조직의 물리적인 크기를 줄인다는 점을 확인할 수 있었다.
탈분화를 통한 체지방의 감소는 에너지소비에 집중된 갈색지방의 활성화 혹은 운동과 같은 기존의 방법과 차별되는 방법이다. 또한 렙틴이라는 호르몬은 지방세포에서 만들어져 식욕을 억제하고 에너지 소비를 증가시키는 핵심적인 대사체계 조절 호르몬으로 30년 전에 처음으로 유전자 서열이 밝혀졌지만, 어떻게 생성이 되는지 분자 수준에서의 기전이 알려지지 않았다.
이번 연구는 1994년 렙틴의 유전자의 서열이 밝혀진 후 최초로 렙틴 발현의 전사 조절 기전*을 밝혔다는 점에서 세계의 주목을 받고 있다. 금번 연구는 지방세포의 압타즈의 활성 증가를 통해 혁신적인 비만 대사질환 치료제 개발의 새로운 가능성을 제시하였다.
*전사 조절 기전: DNA로부터 RNA를 만들어내는 과정을 조절하는 기전을 의미한다.
우리 대학 의과학대학원/생명과학과 최성우 박사 (현 버클리 캘리포니아 주립대학) 와 생명과학과 강주경 박사가 공동 제1 저자로 참여한 이번 연구는 세계적인 국제 학술지 `네이처 대사(Nature Metabolism)' 5월 29일 자 온라인판에 출판됐다. (논문명 : Hippo–YAP/TAZ signalling coordinates adipose plasticity and energy balance by uncoupling leptin expression from fat mass).
한편 이번 연구는 과기정통부 리더연구자 지원사업, 중견연구자 지원사업, 바이오·의료기술개발사업, 해외우수과학자 유치사업, 카이스트 국제공동연구지원사업의 지원으로 수행됐다.
2024.07.01 조회수 5942
지방세포 이용해 체중 감소 가능하다
우리 연구진이 지방세포를 지방세포 전 단계인 줄기세포로 변화(탈분화)시키며 지방조직의 물리적인 크기를 줄이는 등 체중을 감소시키고 지방세포의 활성화를 통해 체내 신진에너지 대사 변화를 통해 비만이나 당뇨 등 대사성 질환의 제어 방법을 제시하여 화제다.
의과학대학원 서재명 교수 연구팀과 생명과학과 임대식 교수 연구팀의 공동연구를 통해 대사성 질환의 새로운 치료 전략을 규명했다고 1일 밝혔다.
지방조직은 식사 후 여분의 칼로리를 지방 형태로 저장하는 저장고 역할과 호르몬을 분비하는 내분비기관의 역할을 한다. 이 두 가지의 역할 중 하나라도 이상이 생기면 우리의 대사 체계는 무너지고 당뇨 혹은 비만과 같은 대사질환이 걸리게 된다. 그러나 우리 몸이 이 두 가지의 기능을 조화롭게 관장하는지 분자 수준에서의 기전이 알려지지 않았다.
연구팀은 히포 신호전달체계*의 얍타즈(YAP/TAZ) 단백질에 주목, 이 단백질의 지방세포 관련 기능을 규명했다. 1) 식사 유무에 따라 지방조직 안에 있는 얍타즈 단백질의 활성상태가 변한다는 점, 2) 동 단백질의 활성이 지방조직의 크기를 직접적으로 조절한다는 점 3) 에너지소비 및 포만감을 관장하는 렙틴이라는 호르몬의 생성에 얍타즈가 직접적으로 관여를 한다는 점을 밝혔다.
*히포 신호전달체계: 다세포 생물의 조직, 신체 기관의 크기를 결정하는 데 중요한 역할을 하는 세포 내 신호전달체계임.
특히 생체 내에서 활성화된 얍타즈의 역할을 규명하기 위해 라츠1/라츠2(LATS1/LATS2) 유전자를 생쥐의 지방세포에서 특이적으로 결손시켰는데, 지방세포 안에 있는 얍타즈의 지속적인 활성은 지방세포를 지방세포의 전구체, 즉 줄기세포와 같은 세포로 변화(탈분화)시키며 지방조직의 물리적인 크기를 줄인다는 점을 확인할 수 있었다.
탈분화를 통한 체지방의 감소는 에너지소비에 집중된 갈색지방의 활성화 혹은 운동과 같은 기존의 방법과 차별되는 방법이다. 또한 렙틴이라는 호르몬은 지방세포에서 만들어져 식욕을 억제하고 에너지 소비를 증가시키는 핵심적인 대사체계 조절 호르몬으로 30년 전에 처음으로 유전자 서열이 밝혀졌지만, 어떻게 생성이 되는지 분자 수준에서의 기전이 알려지지 않았다.
이번 연구는 1994년 렙틴의 유전자의 서열이 밝혀진 후 최초로 렙틴 발현의 전사 조절 기전*을 밝혔다는 점에서 세계의 주목을 받고 있다. 금번 연구는 지방세포의 압타즈의 활성 증가를 통해 혁신적인 비만 대사질환 치료제 개발의 새로운 가능성을 제시하였다.
*전사 조절 기전: DNA로부터 RNA를 만들어내는 과정을 조절하는 기전을 의미한다.
우리 대학 의과학대학원/생명과학과 최성우 박사 (현 버클리 캘리포니아 주립대학) 와 생명과학과 강주경 박사가 공동 제1 저자로 참여한 이번 연구는 세계적인 국제 학술지 `네이처 대사(Nature Metabolism)' 5월 29일 자 온라인판에 출판됐다. (논문명 : Hippo–YAP/TAZ signalling coordinates adipose plasticity and energy balance by uncoupling leptin expression from fat mass).
한편 이번 연구는 과기정통부 리더연구자 지원사업, 중견연구자 지원사업, 바이오·의료기술개발사업, 해외우수과학자 유치사업, 카이스트 국제공동연구지원사업의 지원으로 수행됐다.
2024.07.01 조회수 5942 -
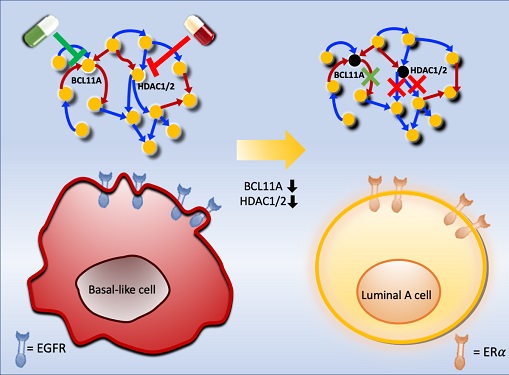 악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12878
악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12878 -
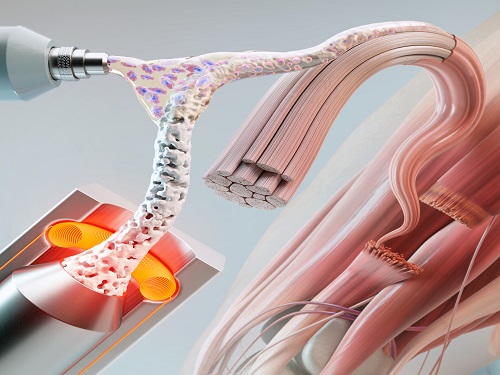 인공근육 재생을 위한 세포기반 3D 파이버 구조체 개발
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이 연세대학교, MIT 공동 연구팀과 함께 광섬유 제작 방법을 이용해 근육 및 혈관, 신경조직을 재생시키기 위한 맞춤형 3D 구조체(세포 기반 인공근육)를 개발했다고 19일 밝혔다.
외상 및 종양 절제 후에 발생하는 근육 손실은 장기적으로 환자의 움직임을 제한하는 가장 큰 원인 중의 하나다. 현재 치료를 위해 이식 기반의 수술법이 시행되고 있으나, 이는 조직을 제공한 부위에 문제를 일으킬 여지가 있을 뿐만 아니라, 이식한 부위에서도 근육의 효과적인 재생력 및 기능성이 충분히 나타나지 않는 문제점을 가지고 있다. 이에 대한 대안으로 손상 부위에 세포를 직접 이식해 골격근(skeletal muscle)의 재생을 유도하는 연구가 진행되고 있지만, 현재의 기술로는 세포의 장기 생존율 및 기능성이 많이 떨어져 실제 임상에 적용하기 어려운 상황이다.
연구팀은 문제 해결을 위해, 섬유아세포(fibroblast)를 리프로그래밍(direct reprogramming)해 유도 근육전구세포(induced myogenic progenitor cells, iMPCs)로 바꾸는 방법을 사용했다. 또한, 세포의 효과적인 분화 및 성장을 위해서는 이상적인 기계적/생화학적 마이크로환경을 제공해야 하므로, 연구팀은 이를 적절한 인공/자연 고분자의 조합을 통한 하이브리드 3D 구조체를 제공하는 방법을 통해 해결했다.
구조체 제작을 위해 첫 번째로 이용한 재료는 우수한 생체적합성 및 강도를 가진 PCL(polycarpolactone) 고분자다. 연구팀은 주로 광섬유를 제작하는데 사용되는 열 인발 공정(thermal drawing process, TDP) 및 다공성 구조 형성을 위한 염침출법(salt leaching)을 이용해, 파이버 기반의 3D PCL 구조체를 제작하는데 성공했다. 해당 공정은 구조체의 사이즈, 강도, 다공성을 자유롭게 조절할 수 있으면서도 구조체의 대량생산을 가능하게 한다는 장점이 있다. 두 번째 재료는 탈세포화(de-cellularization) 과정을 통해 만든 세포외기질(extracellular matrix, ECM)로써, 연구진은 두 재료의 적절한 조합을 통해 이식한 세포에게 최적의 분화 환경을 제공하는데 성공했다.
그 결과, 연구팀은 생체 외(in vitro) 및 생체 내(in vivo) 모델에서 근육 세포의 분화 및 형성이 촉진될 뿐만 아니라, 근육 이외에 주변 신경 및 혈관 분포율이 증가하는 것을 확인했다. 또한 연구팀은 마우스를 대상으로 한 체적 근육 손실 모델에서, 개발한 구조체와 세포를 함께 이식했을 경우 세포만을 이식했을 때에 비해 재생된 근육의 능력이 비약적으로 상승함을 확인했다.
연구를 주도한 박성준 교수는 "이번 연구는 향후 근육 이외에도 다양한 조직의 재생을 위한 맞춤형 3D 구조체를 대량생산 할 수 있는 새로운 방법을 개발했다는 데에 의의가 있다. 이후 본 기술이 여러 가지 생체재료 및 줄기세포 기술과 결합할 경우, 조직 공학 및 인공근육 개발 분야에서 큰 시너지를 낼 수 있으리라 기대한다.ˮ 라고 말했다.
이번 연구결과는 국제 학술지 `어드벤스드 머터리얼즈(Advanced Materials)' 2021년 2월 19일 자에 출판됐다. (논문명: Functional skeletal muscle regeneration with thermally drawn porous fibers and reprogrammed muscle progenitors for volumetric muscle injury)
2021.02.22 조회수 93890
인공근육 재생을 위한 세포기반 3D 파이버 구조체 개발
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이 연세대학교, MIT 공동 연구팀과 함께 광섬유 제작 방법을 이용해 근육 및 혈관, 신경조직을 재생시키기 위한 맞춤형 3D 구조체(세포 기반 인공근육)를 개발했다고 19일 밝혔다.
외상 및 종양 절제 후에 발생하는 근육 손실은 장기적으로 환자의 움직임을 제한하는 가장 큰 원인 중의 하나다. 현재 치료를 위해 이식 기반의 수술법이 시행되고 있으나, 이는 조직을 제공한 부위에 문제를 일으킬 여지가 있을 뿐만 아니라, 이식한 부위에서도 근육의 효과적인 재생력 및 기능성이 충분히 나타나지 않는 문제점을 가지고 있다. 이에 대한 대안으로 손상 부위에 세포를 직접 이식해 골격근(skeletal muscle)의 재생을 유도하는 연구가 진행되고 있지만, 현재의 기술로는 세포의 장기 생존율 및 기능성이 많이 떨어져 실제 임상에 적용하기 어려운 상황이다.
연구팀은 문제 해결을 위해, 섬유아세포(fibroblast)를 리프로그래밍(direct reprogramming)해 유도 근육전구세포(induced myogenic progenitor cells, iMPCs)로 바꾸는 방법을 사용했다. 또한, 세포의 효과적인 분화 및 성장을 위해서는 이상적인 기계적/생화학적 마이크로환경을 제공해야 하므로, 연구팀은 이를 적절한 인공/자연 고분자의 조합을 통한 하이브리드 3D 구조체를 제공하는 방법을 통해 해결했다.
구조체 제작을 위해 첫 번째로 이용한 재료는 우수한 생체적합성 및 강도를 가진 PCL(polycarpolactone) 고분자다. 연구팀은 주로 광섬유를 제작하는데 사용되는 열 인발 공정(thermal drawing process, TDP) 및 다공성 구조 형성을 위한 염침출법(salt leaching)을 이용해, 파이버 기반의 3D PCL 구조체를 제작하는데 성공했다. 해당 공정은 구조체의 사이즈, 강도, 다공성을 자유롭게 조절할 수 있으면서도 구조체의 대량생산을 가능하게 한다는 장점이 있다. 두 번째 재료는 탈세포화(de-cellularization) 과정을 통해 만든 세포외기질(extracellular matrix, ECM)로써, 연구진은 두 재료의 적절한 조합을 통해 이식한 세포에게 최적의 분화 환경을 제공하는데 성공했다.
그 결과, 연구팀은 생체 외(in vitro) 및 생체 내(in vivo) 모델에서 근육 세포의 분화 및 형성이 촉진될 뿐만 아니라, 근육 이외에 주변 신경 및 혈관 분포율이 증가하는 것을 확인했다. 또한 연구팀은 마우스를 대상으로 한 체적 근육 손실 모델에서, 개발한 구조체와 세포를 함께 이식했을 경우 세포만을 이식했을 때에 비해 재생된 근육의 능력이 비약적으로 상승함을 확인했다.
연구를 주도한 박성준 교수는 "이번 연구는 향후 근육 이외에도 다양한 조직의 재생을 위한 맞춤형 3D 구조체를 대량생산 할 수 있는 새로운 방법을 개발했다는 데에 의의가 있다. 이후 본 기술이 여러 가지 생체재료 및 줄기세포 기술과 결합할 경우, 조직 공학 및 인공근육 개발 분야에서 큰 시너지를 낼 수 있으리라 기대한다.ˮ 라고 말했다.
이번 연구결과는 국제 학술지 `어드벤스드 머터리얼즈(Advanced Materials)' 2021년 2월 19일 자에 출판됐다. (논문명: Functional skeletal muscle regeneration with thermally drawn porous fibers and reprogrammed muscle progenitors for volumetric muscle injury)
2021.02.22 조회수 93890