-
 극미량 돌연변이 세포로도 뇌질환 발생한다
뇌를 포함한 모든 신체 기관은 세포 분열 과정에서 발생하는 돌연변이(모자이시즘)을 피할 수 없다. 그렇다면 과연 몇 개의 신경세포에 질병 유발 돌연변이가 생겨났을 때부터 전체 뇌신경 회로를 망가트려 뇌 기능 이상을 일으킬 수 있을까?
우리 대학 의과학대학원 이정호 교수팀이 뇌세포 특이적 돌연변이(뇌 체성 모자이시즘)에 의한 소아 난치성 뇌전증 동물 모델과 환자 뇌 조직 연구를 통해 0.1퍼센트 이하 비율의 극미량 돌연변이 신경세포에 의해서도 뇌 전체 기능 이상을 유발해 뇌전증 발작이 발생할 수 있음을 규명했다고 9일 밝혔다.
이를 통해 난치성 뇌전증의 돌연변이 유전자 진단에 있어 새로운 기준을 마련하는 한편, 극미량의 돌연변이 신경세포가 다양한 뇌 질환 유발에 관여할 수 있음을 밝혔다. 이번 연구의 결과는 세계적 신경 의학 학술지 `브레인(Brain)'에 지난 6월 25일 字 게재됐다.
연구팀은 이번 연구에서 과연 얼마나 적은 수의 세포에서 특정 유전자 모자이시즘이 누적됐을 때 이것이 전체 뇌 기능 이상을 유도하는 뇌 질환 발생으로 이어질 것인가라는 질문에 대답하고자, 마우스 질병 모델과 인체 조직을 이용한 중개의학적 연구를 수행했다.
연구팀은 실험용 쥐의 뇌 조직에 뇌전증 유발 체성 모자이시즘*을 최소 수백 개에서 최대 수만 개의 세포에 유발했다. 이때 고작 8천에서 9천 개 수준의 돌연변이 신경세포가 나타날 때부터, 실험용 쥐가 뇌전증 발작을 일으키고, 관련된 병리가 나타남을 관찰했다. 더 나아가, 난치성 뇌전증 환자 뇌 조직에서 대용량 유전정보 증폭 시퀀싱을 수행해(ultra-high depth amplicon sequencing) 정확한 변이 모자이시즘 비율을 측정했고, 최소 0.07%에 이르는 뇌전증 유발 체성 모자이시즘을 관찰했다.
*체성 모자이시즘(Somatic Mosaicism): 하나의 수정란에서 분열 및 분화를 통해 우리 몸을 이루는 약 30조 개의 세포들이 만들어지는 과정에서 세포마다 돌연변이가 발생할 수 있다는 것으로 암의 진화뿐만 아니라 비암성 질환에서도 중요한 질병 원인으로 최근 주목을 받고 있음.
이 발견은 약물 치료에 반응하지 않아 수술에 이르게 되는 난치성 뇌전증의 유전적 정밀 진단에 도움을 줄 수 있으며, 또한 아직 원인이 밝혀지지 않은 수많은 난치성 신경 정신의학적 질환들이 뇌의 발생과 분화 과정에서 일어나는 극소량의 미세 돌연변이들과 밀접한 관련이 있음을 시사한다.
이번 연구는 국소 피질이형성증*의 진단법 향상 및 체성 모자이시즘에 의한 뇌 질환 원인 발견에 있어서 중요한 기초를 마련할 것으로 예상된다. 이번 연구 성과는 KAIST 교원 창업 기업인 소바젠㈜(대표 박철원, 김병태)을 통해 난치성 뇌전증 환자의 체성 모자이시즘 변이를 정밀 타겟하는 혁신 RNA 치료제 개발에 이용될 예정이다.
*국소 피질이형성증: 뇌 발달 과정 중 대뇌 피질에 국소적으로 신경세포이상이 발생하는 질환으로 기존 항뇌전증 약물에 전혀 반응하지 않는 소아 난치성 뇌전증을 일으키는 가장 중요한 원인으로 알려져 있다.
우리 대학 의과학대학원 졸업생 의사과학자이자 논문의 제1 저자 김진태 박사는 "극미량의 체성 돌연변이라도 뇌의 기능 이상을 유발할 수 있음이 알려졌고, 이를 통해 난치성 뇌전증 등의 유전적 진단과 치료제 개발에 도움이 될 수 있기를 바란다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원 사업의 지원을 받아 수행됐다.
극미량 돌연변이 세포로도 뇌질환 발생한다
뇌를 포함한 모든 신체 기관은 세포 분열 과정에서 발생하는 돌연변이(모자이시즘)을 피할 수 없다. 그렇다면 과연 몇 개의 신경세포에 질병 유발 돌연변이가 생겨났을 때부터 전체 뇌신경 회로를 망가트려 뇌 기능 이상을 일으킬 수 있을까?
우리 대학 의과학대학원 이정호 교수팀이 뇌세포 특이적 돌연변이(뇌 체성 모자이시즘)에 의한 소아 난치성 뇌전증 동물 모델과 환자 뇌 조직 연구를 통해 0.1퍼센트 이하 비율의 극미량 돌연변이 신경세포에 의해서도 뇌 전체 기능 이상을 유발해 뇌전증 발작이 발생할 수 있음을 규명했다고 9일 밝혔다.
이를 통해 난치성 뇌전증의 돌연변이 유전자 진단에 있어 새로운 기준을 마련하는 한편, 극미량의 돌연변이 신경세포가 다양한 뇌 질환 유발에 관여할 수 있음을 밝혔다. 이번 연구의 결과는 세계적 신경 의학 학술지 `브레인(Brain)'에 지난 6월 25일 字 게재됐다.
연구팀은 이번 연구에서 과연 얼마나 적은 수의 세포에서 특정 유전자 모자이시즘이 누적됐을 때 이것이 전체 뇌 기능 이상을 유도하는 뇌 질환 발생으로 이어질 것인가라는 질문에 대답하고자, 마우스 질병 모델과 인체 조직을 이용한 중개의학적 연구를 수행했다.
연구팀은 실험용 쥐의 뇌 조직에 뇌전증 유발 체성 모자이시즘*을 최소 수백 개에서 최대 수만 개의 세포에 유발했다. 이때 고작 8천에서 9천 개 수준의 돌연변이 신경세포가 나타날 때부터, 실험용 쥐가 뇌전증 발작을 일으키고, 관련된 병리가 나타남을 관찰했다. 더 나아가, 난치성 뇌전증 환자 뇌 조직에서 대용량 유전정보 증폭 시퀀싱을 수행해(ultra-high depth amplicon sequencing) 정확한 변이 모자이시즘 비율을 측정했고, 최소 0.07%에 이르는 뇌전증 유발 체성 모자이시즘을 관찰했다.
*체성 모자이시즘(Somatic Mosaicism): 하나의 수정란에서 분열 및 분화를 통해 우리 몸을 이루는 약 30조 개의 세포들이 만들어지는 과정에서 세포마다 돌연변이가 발생할 수 있다는 것으로 암의 진화뿐만 아니라 비암성 질환에서도 중요한 질병 원인으로 최근 주목을 받고 있음.
이 발견은 약물 치료에 반응하지 않아 수술에 이르게 되는 난치성 뇌전증의 유전적 정밀 진단에 도움을 줄 수 있으며, 또한 아직 원인이 밝혀지지 않은 수많은 난치성 신경 정신의학적 질환들이 뇌의 발생과 분화 과정에서 일어나는 극소량의 미세 돌연변이들과 밀접한 관련이 있음을 시사한다.
이번 연구는 국소 피질이형성증*의 진단법 향상 및 체성 모자이시즘에 의한 뇌 질환 원인 발견에 있어서 중요한 기초를 마련할 것으로 예상된다. 이번 연구 성과는 KAIST 교원 창업 기업인 소바젠㈜(대표 박철원, 김병태)을 통해 난치성 뇌전증 환자의 체성 모자이시즘 변이를 정밀 타겟하는 혁신 RNA 치료제 개발에 이용될 예정이다.
*국소 피질이형성증: 뇌 발달 과정 중 대뇌 피질에 국소적으로 신경세포이상이 발생하는 질환으로 기존 항뇌전증 약물에 전혀 반응하지 않는 소아 난치성 뇌전증을 일으키는 가장 중요한 원인으로 알려져 있다.
우리 대학 의과학대학원 졸업생 의사과학자이자 논문의 제1 저자 김진태 박사는 "극미량의 체성 돌연변이라도 뇌의 기능 이상을 유발할 수 있음이 알려졌고, 이를 통해 난치성 뇌전증 등의 유전적 진단과 치료제 개발에 도움이 될 수 있기를 바란다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원 사업의 지원을 받아 수행됐다.
2024.07.09
조회수 690
-
 화학적, 전기적 양방향 소통이 가능한 파이버형 뇌-컴퓨터 인터페이스 개발
뇌 속 뉴런은 화학적, 전기적 신호가 동시에 작동하면서 정교한 시스템을 만들어내지만 현재까지는 이러한 신호를 동시에 주고받으면서 신경의 작동 원리를 확인할 수 있는 장치가 존재하지 않았다. 한국 연구진이 화학적 신호와 전기적 신호를 양 방향적으로 주고받으며 세부적인 신호 전달 체계를 탐사할 수 있는 다기능 신경 인터페이스를 개발하여 앞으로 신경 체계 연구, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이, 초소형 와이어 병합 열 인발공정(Microwire Co-drawing Thermal Drawing Process, MC-TDP)*을 통해 카본, 폴리머, 금속의 다양한 재료를 통합하여 4가지 기능성을 가진 다기능 섬유형 신경 인터페이스를 개발했다고 13일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공
뇌신경 시스템 조사를 위한 삽입형 인터페이스는 전기적 성능에 중점을 두고 발전해 왔다. 하지만 전기적, 화학적 신호의 시너지 효과를 연구하기 위해서는 전기적 신호뿐만 아니라 화학적 신호의 역학을 기록하고 화학적 자극 또한 할 수 있는 신경 디바이스가 필요했다. 그러나 기존의 제작 방법으로는 다양한 자극과 기록을 수행할 수 있는 다양한 재료를 융합하는 것이 어려웠고, 특히 마이크로미터 스케일로 정교한 다기능성 신경 인터페이스를 만드는 것이 어렵다는 문제가 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 초소형 와이어 병합 열 인발공정을 통해 머리카락 크기의 다기능 섬유를 뽑아내는 동안 초소형 와이어를 병합하고 카본 파이버를 융합하여 뉴런 사이에서 일어나는 대표적인 신호 전달을 동시에 조사할 수 있는 다기능 섬유를 제작했다. 연구팀은 제작된 하나의 섬유가 카본 파이버를 통한 도파민 모니터링, 마이크로 유체관을 통한 약물 주입, 폴리머 광 도파관을 통한 광 유전학적 신경 자극, 그리고 초소형 와이어를 통한 전기신호 측정을 할 수 있음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에서 광유전학적 자극에 따른 화학적 신경전달물질 중 도파민과 전기적 신경 활성 신호를 효과적으로 측정하고 약물에 따른 도파민 방출량의 변화를 확인할 수 있음을 보였다. 또한 연구팀은 개발된 섬유가 자발적인 신경 신호를 측정할 수 있음을 보여주며 신경 인터페이스로써의 범용적 사용성도 확인했다.
이번 연구 결과는 국제 학술지 '에이씨에스 나노(ACS Nano)'에 2024년 5월 온라인 출판됐다. (논문명: A Multifunctional and Flexible Neural Probe with Thermally Drawn Fibers for Bidirectional Synaptic Probing in the Brain)
박성준 교수는 "화학적 신경전달물질 기록 및 화학적 자극, 전기적 신경 활성신호 기록, 그리고 광학적 조절 기능을 갖춘 차세대 초다기능성 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 다양한 신경 회로에의 적용을 통해 신경 회로의 작동원리 규명과 뇌 질환의 세부적인 메커니즘 파악에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 기초연구실, STEAM연구사업 및 범부처재생의료기술사업의 지원을 받아 수행됐다.
화학적, 전기적 양방향 소통이 가능한 파이버형 뇌-컴퓨터 인터페이스 개발
뇌 속 뉴런은 화학적, 전기적 신호가 동시에 작동하면서 정교한 시스템을 만들어내지만 현재까지는 이러한 신호를 동시에 주고받으면서 신경의 작동 원리를 확인할 수 있는 장치가 존재하지 않았다. 한국 연구진이 화학적 신호와 전기적 신호를 양 방향적으로 주고받으며 세부적인 신호 전달 체계를 탐사할 수 있는 다기능 신경 인터페이스를 개발하여 앞으로 신경 체계 연구, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이, 초소형 와이어 병합 열 인발공정(Microwire Co-drawing Thermal Drawing Process, MC-TDP)*을 통해 카본, 폴리머, 금속의 다양한 재료를 통합하여 4가지 기능성을 가진 다기능 섬유형 신경 인터페이스를 개발했다고 13일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공
뇌신경 시스템 조사를 위한 삽입형 인터페이스는 전기적 성능에 중점을 두고 발전해 왔다. 하지만 전기적, 화학적 신호의 시너지 효과를 연구하기 위해서는 전기적 신호뿐만 아니라 화학적 신호의 역학을 기록하고 화학적 자극 또한 할 수 있는 신경 디바이스가 필요했다. 그러나 기존의 제작 방법으로는 다양한 자극과 기록을 수행할 수 있는 다양한 재료를 융합하는 것이 어려웠고, 특히 마이크로미터 스케일로 정교한 다기능성 신경 인터페이스를 만드는 것이 어렵다는 문제가 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 초소형 와이어 병합 열 인발공정을 통해 머리카락 크기의 다기능 섬유를 뽑아내는 동안 초소형 와이어를 병합하고 카본 파이버를 융합하여 뉴런 사이에서 일어나는 대표적인 신호 전달을 동시에 조사할 수 있는 다기능 섬유를 제작했다. 연구팀은 제작된 하나의 섬유가 카본 파이버를 통한 도파민 모니터링, 마이크로 유체관을 통한 약물 주입, 폴리머 광 도파관을 통한 광 유전학적 신경 자극, 그리고 초소형 와이어를 통한 전기신호 측정을 할 수 있음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에서 광유전학적 자극에 따른 화학적 신경전달물질 중 도파민과 전기적 신경 활성 신호를 효과적으로 측정하고 약물에 따른 도파민 방출량의 변화를 확인할 수 있음을 보였다. 또한 연구팀은 개발된 섬유가 자발적인 신경 신호를 측정할 수 있음을 보여주며 신경 인터페이스로써의 범용적 사용성도 확인했다.
이번 연구 결과는 국제 학술지 '에이씨에스 나노(ACS Nano)'에 2024년 5월 온라인 출판됐다. (논문명: A Multifunctional and Flexible Neural Probe with Thermally Drawn Fibers for Bidirectional Synaptic Probing in the Brain)
박성준 교수는 "화학적 신경전달물질 기록 및 화학적 자극, 전기적 신경 활성신호 기록, 그리고 광학적 조절 기능을 갖춘 차세대 초다기능성 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 다양한 신경 회로에의 적용을 통해 신경 회로의 작동원리 규명과 뇌 질환의 세부적인 메커니즘 파악에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 기초연구실, STEAM연구사업 및 범부처재생의료기술사업의 지원을 받아 수행됐다.
2024.05.13
조회수 1510
-
 KAIST 첨단 연구의 체험·전시·제품을 짜릿하게 만나다
우리 대학이 4월 과학의 달을 맞아 첨단 연구성과를 체험형 전시 프로그램으로 구성해 시민과 소통에 나선다. 25일부터 28일까지 4일간 대전 엑스포 시민광장 및 과학공원 일대에서 열리는 '2024 대한민국 과학축제 & 과학기술대전'에 6개 연구팀 및 3개 창업기업이 참여해 기술을 선보인다. '과학 실험실' 구역에서는 수면·퍼스널 컬러·뇌구조 분야의 연구진이 체험형 전시로 관람객을 맞는다. 석현정 산업디자인학과 교수 연구팀은 인공지능 기반 퍼스널컬러 진단 서비스를 제공하는 '나의 퍼스널 컬러 찾기(The Authentic Color Play)' 부스를 설치한다. 방문객들은 현장에서 피부색 자동 측정 기술을 직접 체험해보고 개인 피부에 최적화된 색상을 추천받을 수 있다. 김재경 수리과학과 교수 연구팀은 방문객이 양질의 수면을 하고 있는지 3분 만에 알아볼 수 있는 '슬립스(SLEEPS)' 프로그램을 운영한다. 머신러닝 기반의 수면장애 예측 알고리즘을 활용해 간단한 설문과 신체 측정만으로 수면장애 위험도를 계산해보는 체험이다. 검사 결과를 바탕으로 수면장애 위험도를 낮출 수 있는 생활 습관도 함께 알아볼 수 있다. 최민이 뇌인지과학과 교수 연구팀은 '미니 브레인' 체험을 진행한다. 가상현실(VR) 프로그램을 이용해 뇌의 주요 부위들을 해체·조립하며 뇌의 구조를 학습할 수 있다. 또한, 주요 기능과 역할이 다른 뇌 모형의 각 부분을 색칠로 구분하고 스티커를 붙이는 ‘뇌 컬러링’과 세포로부터 미니 브레인이 생겨나는 과정을 시뮬레이션 한 동영상도 관람할 수 있다.
국가 12대 전략기술 성과를 모아놓은 '과학 뮤지엄' 구역에서는 첨단바이오·첨단로봇제조·첨단모빌리티 분야의 연구성과를 전시한다.
조병관 공학생물학대학원 교수 연구팀은 '합성생물학 기반 CO2-to-바이오소재 전환 미생물 세포공장 기술'을 전시한다. 쓰레기 매립 가스, 산업 부생가스 등 환경 오염의 주요 원인인 온실가스를 미생물에 흡수시킨 뒤, 합성생물학을 기반으로 하는 유전적 개량기술을 적용해 다양한 바이오소재로 전환할 수 있는 고효율 생체촉매 개발 기술이다.
박해원 기계공학과 교수 연구팀은 험지탐사용 4족보행 로봇인 '하운드(HOUND)'를 공개한다. 하운드는 시각 및 촉각 센서의 도움 없이도 계단이나 험지 같은 비정형 장애물 환경에서도 안정적인 동작이 가능한 로봇이다. 실내 최대 속도 6.5m/s까지 낼 수 있으며, 100m를 19.87초 주파한 기네스 기록도 가지고 있다. 하운드는 축제 기간 내내 행사 현장을 활보하며 방문객을 맞을 예정이다.
장기태 조천식모빌리티 대학원 교수 연구팀은 '디젤 트럭 개조용 박(薄)형 모터' 기술을 선보인다. 택배차량용 디젤 트럭을 하이브리드 방식으로 개조하는 기술이다. 기존 디젤 차량에 모터를 추가해 저속 주행에는 모터를 사용하고 고속 주행에는 기존 엔진을 활용하는 방식이다. 정차와 가속이 잦은 국내 택배 차량에 이 기술을 도입할 경우 연비와 미세먼지를 동시에 저감할 수 있어 국토교통부 우수물류신기술 1호로도 지정된 바 있다. 이 밖에도 KAIST 혁신 창업기업의 기술도 전시된다. 화학과 창업기업 '폴리페놀팩토리(대표 이해신)'는 폴리페놀 기술을 활용해 탈모의 진행을 완화하고 모발의 풍성함을 더해주는 '그래비티' 샴푸를 소개한다. 연구팀이 개발한 특허 성분이 샴푸 과정에서 순간적인 보호막을 만들어 모발을 보호하는 동시에 가늘어진 모발을 힘 있게 잡아주는 원리다. 부스 방문객에게는 기술을 체험할 수 있는 시제품을 선착순으로 제공할 예정이다.
기계공학과 창업기업 '㈜A2US(대표 이승섭)'는 ‘마법의 전기 물방울(Magic Electro Water droplets)' 기술을 사용해 세계 최초로 개발한 제품을 선보인다. 인체에는 해가 없으면서도 공기 중의 유기물과 세균 등을 없애는 천연물질인 '하이드록실 라디칼'을 포함한 물방울을 만들어내는 가습기 '뮤(MEW, Magic Electro Water droplets)'다. 미세한 노즐에 전기를 가해 만들어진 이 물방울을 분무하면 공기 중의 유해물질과 냄새를 제거할 수 있어 가습과 공기정화 기능이 동시에 가능하다.
문화기술대학원 창업기업 '㈜카이(대표 김범기)'는 '밍글 AI(Mingle AI)'을 전시한다. 이미지, 오디오, 비디오 등 다양한 유형의 데이터를 입력하면 3차원의 아바타나 오브젝트를 만들어주는 생성형 인공지능 툴이다. 전문 지식이 없는 일반 사용자도 손쉽게 디지털 휴먼을 제작할 수 있으며, 게임·엔터테인먼트·소셜미디어 등의 분야에서 활용할 수 있다.이광형 KAIST 총장은 "대중과 눈높이를 맞춘 체험 프로그램을 구성해 KAIST의 우수한 기술을 시민과 공유할 수 있어 뜻깊게 생각한다"라고 전했다. 이어, 이 총장은 "우수한 성과와 함께 과학기술로 사회 문제를 해결하기 위해 매진하는 연구자들의 노력과 진심이 함께 전달될 수 있는 자리가 되길 기대한다"라고 덧붙였다.
KAIST 첨단 연구의 체험·전시·제품을 짜릿하게 만나다
우리 대학이 4월 과학의 달을 맞아 첨단 연구성과를 체험형 전시 프로그램으로 구성해 시민과 소통에 나선다. 25일부터 28일까지 4일간 대전 엑스포 시민광장 및 과학공원 일대에서 열리는 '2024 대한민국 과학축제 & 과학기술대전'에 6개 연구팀 및 3개 창업기업이 참여해 기술을 선보인다. '과학 실험실' 구역에서는 수면·퍼스널 컬러·뇌구조 분야의 연구진이 체험형 전시로 관람객을 맞는다. 석현정 산업디자인학과 교수 연구팀은 인공지능 기반 퍼스널컬러 진단 서비스를 제공하는 '나의 퍼스널 컬러 찾기(The Authentic Color Play)' 부스를 설치한다. 방문객들은 현장에서 피부색 자동 측정 기술을 직접 체험해보고 개인 피부에 최적화된 색상을 추천받을 수 있다. 김재경 수리과학과 교수 연구팀은 방문객이 양질의 수면을 하고 있는지 3분 만에 알아볼 수 있는 '슬립스(SLEEPS)' 프로그램을 운영한다. 머신러닝 기반의 수면장애 예측 알고리즘을 활용해 간단한 설문과 신체 측정만으로 수면장애 위험도를 계산해보는 체험이다. 검사 결과를 바탕으로 수면장애 위험도를 낮출 수 있는 생활 습관도 함께 알아볼 수 있다. 최민이 뇌인지과학과 교수 연구팀은 '미니 브레인' 체험을 진행한다. 가상현실(VR) 프로그램을 이용해 뇌의 주요 부위들을 해체·조립하며 뇌의 구조를 학습할 수 있다. 또한, 주요 기능과 역할이 다른 뇌 모형의 각 부분을 색칠로 구분하고 스티커를 붙이는 ‘뇌 컬러링’과 세포로부터 미니 브레인이 생겨나는 과정을 시뮬레이션 한 동영상도 관람할 수 있다.
국가 12대 전략기술 성과를 모아놓은 '과학 뮤지엄' 구역에서는 첨단바이오·첨단로봇제조·첨단모빌리티 분야의 연구성과를 전시한다.
조병관 공학생물학대학원 교수 연구팀은 '합성생물학 기반 CO2-to-바이오소재 전환 미생물 세포공장 기술'을 전시한다. 쓰레기 매립 가스, 산업 부생가스 등 환경 오염의 주요 원인인 온실가스를 미생물에 흡수시킨 뒤, 합성생물학을 기반으로 하는 유전적 개량기술을 적용해 다양한 바이오소재로 전환할 수 있는 고효율 생체촉매 개발 기술이다.
박해원 기계공학과 교수 연구팀은 험지탐사용 4족보행 로봇인 '하운드(HOUND)'를 공개한다. 하운드는 시각 및 촉각 센서의 도움 없이도 계단이나 험지 같은 비정형 장애물 환경에서도 안정적인 동작이 가능한 로봇이다. 실내 최대 속도 6.5m/s까지 낼 수 있으며, 100m를 19.87초 주파한 기네스 기록도 가지고 있다. 하운드는 축제 기간 내내 행사 현장을 활보하며 방문객을 맞을 예정이다.
장기태 조천식모빌리티 대학원 교수 연구팀은 '디젤 트럭 개조용 박(薄)형 모터' 기술을 선보인다. 택배차량용 디젤 트럭을 하이브리드 방식으로 개조하는 기술이다. 기존 디젤 차량에 모터를 추가해 저속 주행에는 모터를 사용하고 고속 주행에는 기존 엔진을 활용하는 방식이다. 정차와 가속이 잦은 국내 택배 차량에 이 기술을 도입할 경우 연비와 미세먼지를 동시에 저감할 수 있어 국토교통부 우수물류신기술 1호로도 지정된 바 있다. 이 밖에도 KAIST 혁신 창업기업의 기술도 전시된다. 화학과 창업기업 '폴리페놀팩토리(대표 이해신)'는 폴리페놀 기술을 활용해 탈모의 진행을 완화하고 모발의 풍성함을 더해주는 '그래비티' 샴푸를 소개한다. 연구팀이 개발한 특허 성분이 샴푸 과정에서 순간적인 보호막을 만들어 모발을 보호하는 동시에 가늘어진 모발을 힘 있게 잡아주는 원리다. 부스 방문객에게는 기술을 체험할 수 있는 시제품을 선착순으로 제공할 예정이다.
기계공학과 창업기업 '㈜A2US(대표 이승섭)'는 ‘마법의 전기 물방울(Magic Electro Water droplets)' 기술을 사용해 세계 최초로 개발한 제품을 선보인다. 인체에는 해가 없으면서도 공기 중의 유기물과 세균 등을 없애는 천연물질인 '하이드록실 라디칼'을 포함한 물방울을 만들어내는 가습기 '뮤(MEW, Magic Electro Water droplets)'다. 미세한 노즐에 전기를 가해 만들어진 이 물방울을 분무하면 공기 중의 유해물질과 냄새를 제거할 수 있어 가습과 공기정화 기능이 동시에 가능하다.
문화기술대학원 창업기업 '㈜카이(대표 김범기)'는 '밍글 AI(Mingle AI)'을 전시한다. 이미지, 오디오, 비디오 등 다양한 유형의 데이터를 입력하면 3차원의 아바타나 오브젝트를 만들어주는 생성형 인공지능 툴이다. 전문 지식이 없는 일반 사용자도 손쉽게 디지털 휴먼을 제작할 수 있으며, 게임·엔터테인먼트·소셜미디어 등의 분야에서 활용할 수 있다.이광형 KAIST 총장은 "대중과 눈높이를 맞춘 체험 프로그램을 구성해 KAIST의 우수한 기술을 시민과 공유할 수 있어 뜻깊게 생각한다"라고 전했다. 이어, 이 총장은 "우수한 성과와 함께 과학기술로 사회 문제를 해결하기 위해 매진하는 연구자들의 노력과 진심이 함께 전달될 수 있는 자리가 되길 기대한다"라고 덧붙였다.
2024.04.25
조회수 2005
-
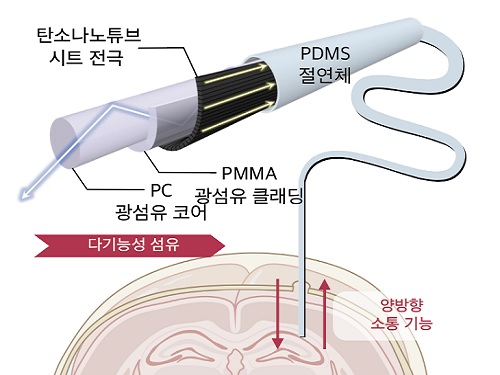 초장기간 작동 뇌-기계 인터페이스 개발
수술이 불가피한 삽입형 신경 인터페이스의 경우, 한 번의 수술로도 최대한 많은 정보를 얻을 수 있고 장기간 사용가능한 디바이스의 개발이 필요하다. 한국 연구진이 1년 이상 사용가능한 다기능성 신경 인터페이스를 개발하여 향후 뇌 지도, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀과 한양대학교(총장 이기정) 바이오메디컬공학과 최창순 교수 연구팀이, 열 인발공정(Thermal Drawing Process, TDP)*과 탄소나노튜브 시트를 병합해 장기간 사용 가능한 다기능성 섬유형 신경 인터페이스를 개발했다고 24일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공.
뇌신경 시스템 탐구를 위한 삽입형 인터페이스는 생체 시스템의 면역 반응을 줄이기 위해 생체 친화적이며 부드러운 물질을 사용하면서도, 다양한 기능을 병합하는 방향으로 발전해 왔다. 하지만 기존의 재료와 제작 방법으로는 다양한 기능을 구현할 수 있으면서도 장기간 사용가능한 디바이스를 만들기 어려웠고, 특히 탄소 기반 전극의 경우 제조 및 병합 과정이 복잡하고 금속 전극에 비해 기능적 수행 능력이 떨어진다는 문제점이 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 탄소나노튜브 시트 전극과 고분자 광섬유를 병합했다. 탄소나노튜브 섬유가 한 방향으로 배열된 탄소나노튜브 시트 전극을 통해 신경세포 활동을 효과적으로 기록했고, 광 전달을 담당하는 고분자 광섬유에 이를 감아 머리카락 크기의 다기능 섬유를 제작했다. 연구팀은 제작된 섬유는 우수한 전기적, 광학적, 기계적 성질을 보였음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에 삽입한 결과, 전기적 신경 활성신호, 화학적 신경전달물질(도파민)을 잘 측정하고 광유전학적 조절을 통해 행동학적 산출을 이끌어낼 수 있음을 확인했다. 또한 연구팀은 1년 이상 광학적으로 발화된 신경 신호와 자발적으로 발화된 신경 신호를 측정함으로써 초장기간 사용 가능성도 보여줬다.
이번 연구 결과는 국제 학술지 `어드밴스드 머터리얼스(Advanced Materials)'에 2024년 3월 29일 字로 출판됐다. (논문명: Structurally Aligned Multifunctional neural Probe (SAMP) using forest-drawn CNT sheet onto thermally drawn polymer fiber for long-term in vivo operation)
박성준 교수는 "전기적 신경 활성신호와 더불어 화학적 신경전달물질 기록 및 광학적 조절 기능을 갖춘 초장기간 사용가능한 차세대 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 대동물 적용 및 자기공명영상 장비와 동시 사용을 통해 뇌 질환의 세부적인 메커니즘 파악과 전뇌적(Whole brain) 기록 및 조절 분야에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 과학기술정보통신부, 한국연구재단 나노및소재기술개발사업, 경찰청 미래치안도전기술개발사업의 지원을 받아 수행됐다.
초장기간 작동 뇌-기계 인터페이스 개발
수술이 불가피한 삽입형 신경 인터페이스의 경우, 한 번의 수술로도 최대한 많은 정보를 얻을 수 있고 장기간 사용가능한 디바이스의 개발이 필요하다. 한국 연구진이 1년 이상 사용가능한 다기능성 신경 인터페이스를 개발하여 향후 뇌 지도, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀과 한양대학교(총장 이기정) 바이오메디컬공학과 최창순 교수 연구팀이, 열 인발공정(Thermal Drawing Process, TDP)*과 탄소나노튜브 시트를 병합해 장기간 사용 가능한 다기능성 섬유형 신경 인터페이스를 개발했다고 24일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공.
뇌신경 시스템 탐구를 위한 삽입형 인터페이스는 생체 시스템의 면역 반응을 줄이기 위해 생체 친화적이며 부드러운 물질을 사용하면서도, 다양한 기능을 병합하는 방향으로 발전해 왔다. 하지만 기존의 재료와 제작 방법으로는 다양한 기능을 구현할 수 있으면서도 장기간 사용가능한 디바이스를 만들기 어려웠고, 특히 탄소 기반 전극의 경우 제조 및 병합 과정이 복잡하고 금속 전극에 비해 기능적 수행 능력이 떨어진다는 문제점이 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 탄소나노튜브 시트 전극과 고분자 광섬유를 병합했다. 탄소나노튜브 섬유가 한 방향으로 배열된 탄소나노튜브 시트 전극을 통해 신경세포 활동을 효과적으로 기록했고, 광 전달을 담당하는 고분자 광섬유에 이를 감아 머리카락 크기의 다기능 섬유를 제작했다. 연구팀은 제작된 섬유는 우수한 전기적, 광학적, 기계적 성질을 보였음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에 삽입한 결과, 전기적 신경 활성신호, 화학적 신경전달물질(도파민)을 잘 측정하고 광유전학적 조절을 통해 행동학적 산출을 이끌어낼 수 있음을 확인했다. 또한 연구팀은 1년 이상 광학적으로 발화된 신경 신호와 자발적으로 발화된 신경 신호를 측정함으로써 초장기간 사용 가능성도 보여줬다.
이번 연구 결과는 국제 학술지 `어드밴스드 머터리얼스(Advanced Materials)'에 2024년 3월 29일 字로 출판됐다. (논문명: Structurally Aligned Multifunctional neural Probe (SAMP) using forest-drawn CNT sheet onto thermally drawn polymer fiber for long-term in vivo operation)
박성준 교수는 "전기적 신경 활성신호와 더불어 화학적 신경전달물질 기록 및 광학적 조절 기능을 갖춘 초장기간 사용가능한 차세대 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 대동물 적용 및 자기공명영상 장비와 동시 사용을 통해 뇌 질환의 세부적인 메커니즘 파악과 전뇌적(Whole brain) 기록 및 조절 분야에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 과학기술정보통신부, 한국연구재단 나노및소재기술개발사업, 경찰청 미래치안도전기술개발사업의 지원을 받아 수행됐다.
2024.04.24
조회수 1931
-
 뇌인지과학과 1주년 기념 심포지엄 개최
우리 대학이 다음 달 2일부터 4일까지 총 3일간 대전 본원 의과학연구센터(E7)에서 '뇌인지과학과 국제심포지엄'을 개최한다.
이번 심포지엄은 뇌인지과학과(학과장 정재승)의 설립 1주년을 기념하는 행사로 국내 뇌인지과학 분야의 저변확대와 차세대 인력양성 등을 논의하기 위해 마련됐다. 이를 위해, 미국 UC 버클리(UC Berkeley), 뉴욕대학교(New York University, 이하 NYU), 스위스 로잔연방공과대학교(EPFL) 등 유수 대학의 세계적 석학들과 구글 딥마인드(Google DeepMind), 아이비엠 리서치(IBM Research) 등에서 활발하게 활동 중인 뇌기반 인공지능연구자 등 13명의 해외 뇌과학자·뇌공학자를 초청했다. 또한, 국내 관련 분야의 리더들과 학술교류 및 공동연구를 논의하고, 우리 대학의 비전에 부합하는 향후 50년의 미래 연구 계획을 함께 모색할 예정이다. '뇌인지 분야의 난제'를 주제로 다루는 심포지엄 첫날에는 양단(Yang Dan) 미국 캘리포니아 대학교-버클리(UC-Berkeley) 신경생물학 석좌교수와 올라프 브랑케(Olaf Blanke) 스위스 로잔연방공과대학교(EPFL) 신경보철센터 교수가 개회 기조 연사를 맡는다. 이들은 각각 '하향식 주의 및 전역 점화: 마우스의 회로 해부'와 '자의식의 신경과학'을 주제로 강연한다. 첫 번째 세션에서는 '뇌인지과학 분야에서 가장 중요한 질문은 무엇일까?'라는 질문을 바탕으로 미국 뇌과학 연구의 중심축 중 하나인 뉴욕대 신경과학 센터(NYU Center for Neural Science)를 설립한 앤소니 모비숀(J. Anthony Movshon) 뉴욕대학교 신경과학 및 생리학 교수가 기조 연설한다. '기술을 확장할 때 우리는 어떻게 이해를 확장할 수 있을까'라는 주제로 강연과 함께 뇌인지과학 분야가 향후 집중해야 하는 연구 방향성을 논의하기 위한 해외 석학들의 발표와 토론이 이어질 예정이다. '뇌와 인지과학 분야의 인재를 어떻게 교육할 것인가?'를 주제로 열리는 둘째 날 오전 세션에서는 문제일 DGIST 뇌과학과 교수, 이상훈 서울대 뇌인지과학과 교수, 조제원 이화여대 뇌인지과학부 교수, 서민아 성균관대 글로벌바이오메디컬공학과 교수 등이 참여해 인재상·교육 커리큘럼·뇌인지과학과 운영 현황·뇌과학 연구의 필요성 등에 대해 강연 및 토론한다. 또한, ‘뇌×헬스케어’와 ‘뇌×인공지능(AI)’을 다루는 세션에서는 뇌 질환 관련 현황 및 연구 동향과 인공지능 기술 개발 동향 등을 공유한다.
심포지엄 마지막 날에는 뇌인지과학 분야에서 우리 대학과 뉴욕대의 공동협력 방안이 논의된다. 신경경제학 분야를 선도하는 뉴욕대 신경경제학 센터(Centre for Neuroeconomics)를 설립한 폴 글림처(Paul Glimcher) 뉴욕대학교 신경과학 및 생리학 석좌교수는 '생명 의료 신경과학의 첨단 기술 협력'을 주제로 기조연설을 한다.
이 세션에서는 미국 뉴욕 맨해튼 소재의 KAIST-NYU 조인트 캠퍼스를 기반으로 추진할 인공지능 융합 뇌과학분야(뇌-기계 상호작용, 뇌기반 기계학습) 국제 공동연구를 위해 뉴욕대의 캐서린 하틀리(Catherine A. Hartley) 교수, 브렌든 레이크(Brenden Lake) 교수와 데이비드 멜처(David Melcher) 뉴욕대-아부다비 교수가 최근 연구성과를 공유하고 토론을 진행한다. 정재승 KAIST 뇌인지과학과 학과장은 "국내에서는 좀처럼 만나기 힘든 세계적인 석학들이 설립 1년 차 학과가 첫 번째로 개최하는 학술 심포지엄의 연사로 참여한다는 것 자체가 KAIST 뇌인지과학과를 향한 학계의 관심과 기대라고 생각한다"라고 말했다. 이어, 정 학과장은 "10년 내 교수진 50명을 보유한 아시아 최대 뇌인지과학과로 성장하는 것을 목표로 신경생물학과 인지과학, 뇌공학과 뇌의학을 두루 아우르는 뇌인지과학 연구의 교두보가 되기 위해 최선을 다하겠다"라고 전했다.한편, KAIST 뇌인지과학과는 단순히 뇌의 생물학적 구조와 인지기능을 연구하는 것을 넘어 뇌와 몸, 인간과 인간, 인간과 세계가 어떻게 상호작용하는지를 탐구하고 이를 바탕으로 공학적이고 의학적인 응용을 실현하기 위해 지난해 설립됐다. 신경과학과 인지과학의의 탄탄한 기초를 바탕으로 뇌공학과 뇌의학 분야로 연구 영역 확장을 시도하고 있으며, KAIST-NYU 조인트 캠퍼스를 통해 학부생과 대학원생, 박사후 연구원, 교수들이 뉴욕에 상주하면서 뉴욕대·콜롬비아대·코넬대·록펠러대 등 유수의 대학들과 공동연구를 수행할 수 있는 세계적 연구 및 교육 협업 시스템을 갖추고 있다.이번 행사는 국제심포지엄의 특성상 일부 세션이 영어로 진행되며, 뇌인지과학 분야에 관심 있는 사람이라면 누구나 무료로 참관할 수 있다.
뇌인지과학과 1주년 기념 심포지엄 개최
우리 대학이 다음 달 2일부터 4일까지 총 3일간 대전 본원 의과학연구센터(E7)에서 '뇌인지과학과 국제심포지엄'을 개최한다.
이번 심포지엄은 뇌인지과학과(학과장 정재승)의 설립 1주년을 기념하는 행사로 국내 뇌인지과학 분야의 저변확대와 차세대 인력양성 등을 논의하기 위해 마련됐다. 이를 위해, 미국 UC 버클리(UC Berkeley), 뉴욕대학교(New York University, 이하 NYU), 스위스 로잔연방공과대학교(EPFL) 등 유수 대학의 세계적 석학들과 구글 딥마인드(Google DeepMind), 아이비엠 리서치(IBM Research) 등에서 활발하게 활동 중인 뇌기반 인공지능연구자 등 13명의 해외 뇌과학자·뇌공학자를 초청했다. 또한, 국내 관련 분야의 리더들과 학술교류 및 공동연구를 논의하고, 우리 대학의 비전에 부합하는 향후 50년의 미래 연구 계획을 함께 모색할 예정이다. '뇌인지 분야의 난제'를 주제로 다루는 심포지엄 첫날에는 양단(Yang Dan) 미국 캘리포니아 대학교-버클리(UC-Berkeley) 신경생물학 석좌교수와 올라프 브랑케(Olaf Blanke) 스위스 로잔연방공과대학교(EPFL) 신경보철센터 교수가 개회 기조 연사를 맡는다. 이들은 각각 '하향식 주의 및 전역 점화: 마우스의 회로 해부'와 '자의식의 신경과학'을 주제로 강연한다. 첫 번째 세션에서는 '뇌인지과학 분야에서 가장 중요한 질문은 무엇일까?'라는 질문을 바탕으로 미국 뇌과학 연구의 중심축 중 하나인 뉴욕대 신경과학 센터(NYU Center for Neural Science)를 설립한 앤소니 모비숀(J. Anthony Movshon) 뉴욕대학교 신경과학 및 생리학 교수가 기조 연설한다. '기술을 확장할 때 우리는 어떻게 이해를 확장할 수 있을까'라는 주제로 강연과 함께 뇌인지과학 분야가 향후 집중해야 하는 연구 방향성을 논의하기 위한 해외 석학들의 발표와 토론이 이어질 예정이다. '뇌와 인지과학 분야의 인재를 어떻게 교육할 것인가?'를 주제로 열리는 둘째 날 오전 세션에서는 문제일 DGIST 뇌과학과 교수, 이상훈 서울대 뇌인지과학과 교수, 조제원 이화여대 뇌인지과학부 교수, 서민아 성균관대 글로벌바이오메디컬공학과 교수 등이 참여해 인재상·교육 커리큘럼·뇌인지과학과 운영 현황·뇌과학 연구의 필요성 등에 대해 강연 및 토론한다. 또한, ‘뇌×헬스케어’와 ‘뇌×인공지능(AI)’을 다루는 세션에서는 뇌 질환 관련 현황 및 연구 동향과 인공지능 기술 개발 동향 등을 공유한다.
심포지엄 마지막 날에는 뇌인지과학 분야에서 우리 대학과 뉴욕대의 공동협력 방안이 논의된다. 신경경제학 분야를 선도하는 뉴욕대 신경경제학 센터(Centre for Neuroeconomics)를 설립한 폴 글림처(Paul Glimcher) 뉴욕대학교 신경과학 및 생리학 석좌교수는 '생명 의료 신경과학의 첨단 기술 협력'을 주제로 기조연설을 한다.
이 세션에서는 미국 뉴욕 맨해튼 소재의 KAIST-NYU 조인트 캠퍼스를 기반으로 추진할 인공지능 융합 뇌과학분야(뇌-기계 상호작용, 뇌기반 기계학습) 국제 공동연구를 위해 뉴욕대의 캐서린 하틀리(Catherine A. Hartley) 교수, 브렌든 레이크(Brenden Lake) 교수와 데이비드 멜처(David Melcher) 뉴욕대-아부다비 교수가 최근 연구성과를 공유하고 토론을 진행한다. 정재승 KAIST 뇌인지과학과 학과장은 "국내에서는 좀처럼 만나기 힘든 세계적인 석학들이 설립 1년 차 학과가 첫 번째로 개최하는 학술 심포지엄의 연사로 참여한다는 것 자체가 KAIST 뇌인지과학과를 향한 학계의 관심과 기대라고 생각한다"라고 말했다. 이어, 정 학과장은 "10년 내 교수진 50명을 보유한 아시아 최대 뇌인지과학과로 성장하는 것을 목표로 신경생물학과 인지과학, 뇌공학과 뇌의학을 두루 아우르는 뇌인지과학 연구의 교두보가 되기 위해 최선을 다하겠다"라고 전했다.한편, KAIST 뇌인지과학과는 단순히 뇌의 생물학적 구조와 인지기능을 연구하는 것을 넘어 뇌와 몸, 인간과 인간, 인간과 세계가 어떻게 상호작용하는지를 탐구하고 이를 바탕으로 공학적이고 의학적인 응용을 실현하기 위해 지난해 설립됐다. 신경과학과 인지과학의의 탄탄한 기초를 바탕으로 뇌공학과 뇌의학 분야로 연구 영역 확장을 시도하고 있으며, KAIST-NYU 조인트 캠퍼스를 통해 학부생과 대학원생, 박사후 연구원, 교수들이 뉴욕에 상주하면서 뉴욕대·콜롬비아대·코넬대·록펠러대 등 유수의 대학들과 공동연구를 수행할 수 있는 세계적 연구 및 교육 협업 시스템을 갖추고 있다.이번 행사는 국제심포지엄의 특성상 일부 세션이 영어로 진행되며, 뇌인지과학 분야에 관심 있는 사람이라면 누구나 무료로 참관할 수 있다.
2023.10.27
조회수 2998
-
 식품의약품안전처와 연구협력 MOU 체결
우리 대학은 16일 오후 식품의약품안전처(처장 오유경)와 식품·의약품·마약류 등 분야에서 연구를 포함한 포괄적인 협력을 강화하는 MOU를 체결했다.
이번 협약을 바탕으로 두 기관은 ▴식품·의약품·마약류 등 분야의 공동연구 발굴·추진 ▴국가연구개발사업 상호협력 및 공동연구 추진 ▴양 기관 교육프로그램 연계·공유 ▴국내외 최신 식·의약 연구 정보·동향 공유 등에 적극적으로 협력할 예정이다.
특히, 'KAIST-원진 세포치료센터(센터장, 김대수)'를 주축으로 뇌 오가노이드(인공장기) 기술을 개발해 약물중독 및 금단증상, 재활에 관해 연구하고 국제적인 표준을 마련할 계획이다.
날로 증가하는 신종 마약의 위협을 신속하게 진단하고 대응하기 위해 우리 대학의 인공지능 기술을 활용해 마약류가 뇌와 행동에 미치는 영향을 초고속으로 정밀 진단할 수 있는 시스템 개발도 진행한다.
이와 함께, mRNA 백신·치료제 기술·플랫폼 개발 등 식품 및 의료 관련 신물질과 제품 안전성에 대한 첨단 평가기술 개발 분야에서도 폭넓게 협력할 예정이다.
오유경 식약처장은 "이번 업무협약을 계기로 식약처와 KAIST가 함께 연구를 수행하게 되어 국민 안전이 한층 더 강화될 수 있을 것으로 기대한다"며 "식약처는 앞으로도 과학적 근거에 기반하여 식품, 의료제품의 안전을 더욱 철저히 관리하겠다"고 말했다.이광형 총장은 "이번 협약이 식약처와 KAIST의 유기적인 협력관계 구축으로 이어져 양 기관이 상호 발전하는 계기가 되길 바란다"며 "앞으로 KAIST의 첨단과학 연구 역량을 바탕으로 식약처와 공동연구를 수행하여 규제과학 전문성을 높이기 위해 지속해서 노력하겠다"고 밝혔다.
식품의약품안전처와 연구협력 MOU 체결
우리 대학은 16일 오후 식품의약품안전처(처장 오유경)와 식품·의약품·마약류 등 분야에서 연구를 포함한 포괄적인 협력을 강화하는 MOU를 체결했다.
이번 협약을 바탕으로 두 기관은 ▴식품·의약품·마약류 등 분야의 공동연구 발굴·추진 ▴국가연구개발사업 상호협력 및 공동연구 추진 ▴양 기관 교육프로그램 연계·공유 ▴국내외 최신 식·의약 연구 정보·동향 공유 등에 적극적으로 협력할 예정이다.
특히, 'KAIST-원진 세포치료센터(센터장, 김대수)'를 주축으로 뇌 오가노이드(인공장기) 기술을 개발해 약물중독 및 금단증상, 재활에 관해 연구하고 국제적인 표준을 마련할 계획이다.
날로 증가하는 신종 마약의 위협을 신속하게 진단하고 대응하기 위해 우리 대학의 인공지능 기술을 활용해 마약류가 뇌와 행동에 미치는 영향을 초고속으로 정밀 진단할 수 있는 시스템 개발도 진행한다.
이와 함께, mRNA 백신·치료제 기술·플랫폼 개발 등 식품 및 의료 관련 신물질과 제품 안전성에 대한 첨단 평가기술 개발 분야에서도 폭넓게 협력할 예정이다.
오유경 식약처장은 "이번 업무협약을 계기로 식약처와 KAIST가 함께 연구를 수행하게 되어 국민 안전이 한층 더 강화될 수 있을 것으로 기대한다"며 "식약처는 앞으로도 과학적 근거에 기반하여 식품, 의료제품의 안전을 더욱 철저히 관리하겠다"고 말했다.이광형 총장은 "이번 협약이 식약처와 KAIST의 유기적인 협력관계 구축으로 이어져 양 기관이 상호 발전하는 계기가 되길 바란다"며 "앞으로 KAIST의 첨단과학 연구 역량을 바탕으로 식약처와 공동연구를 수행하여 규제과학 전문성을 높이기 위해 지속해서 노력하겠다"고 밝혔다.
2023.10.17
조회수 1846
-
 뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16
조회수 2531
-
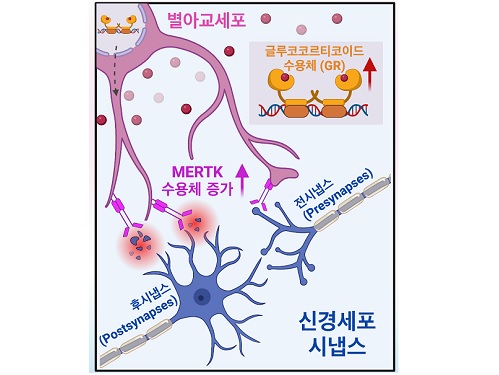 아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
2023.08.01
조회수 3151
-
 150% 쭉쭉 늘어나는 전자 섬유 개발
전자 섬유는 최근 각광받고 있는 사용자 친화 웨어러블 소자, 헬스케어 소자, 최소 침습형 임플란터블 전자소자에 핵심 요소로 여겨져 활발하게 연구가 진행되고 있다. 하지만 고체 금속 전도체 필러(Conductive filler)를 사용한 전자 섬유를 늘려서 사용하려 할 경우, 전기전도성이 급격하게 감소해 전기적 성질이 망가진다는 단점이 있다.
우리 대학 신소재공학과 스티브 박, 전기및전자공학부 정재웅, 바이오및뇌공학과 박성준 교수 공동 연구팀이 높은 전도도와 내구성을 가지는 액체금속 복합체를 이용해 신축성이 우수한 전자 섬유를 개발했다고 25일 밝혔다.
전자 섬유의 늘어나지 않는 단점을 해결하기 위해 연구팀은 고체처럼 형상이 고정된 것이 아닌 기계적 변형에 맞춰 형태가 변형될 수 있는 액체금속 입자 기반의 전도체 필러를 제시했다. 액체금속 마이크로 입자는 인장이 가해질 경우에 그 형태가 타원형으로 늘어나면서 전기 저항 변화를 최소화할 수 있다. 하지만 그 크기가 수 마이크로미터이기 때문에, 기존에 이용된 딥-코팅(dip-coating)과 같은 단순한 방법으로 실에 코팅하는 것이 불가능하다. 연구진은 액체금속 입자가 높은 밀도로 실 위에 전달될 수 있고, 블레이드와 기판 사이에서 현탁액의 조성을 실시간으로 바꾸면서 화학적 변성을 통해 액체금속 입자를 실과 접착시킬 수 있는 새로운 방법인 현탁액 전단(suspension shearing) 방법을 통해 이를 해결했다. 추가로 기계적 안정성이 우수한 탄소나노튜브(CNT)가 포함된 액체금속 입자를 한층 더 코팅하는 방식으로, 액체금속 복합체의 기계적 안정성도 확보할 수 있었다.
제작된 신축성 전자 섬유는 추가적인 공정이 필요 없이 우수한 초기전도성을 보였고(2.2x10^6 S/m), 기존의 고체 금속 전도체 기반 섬유들과는 다르게 150% 늘려도 전기저항 변화가 거의 없다. 기계적 안정성도 우수해 반복되는 변형 실험에도 전기적 성질을 유지할 수 있었고, 다양한 전자 부품들과 쉽게 통합될 수 있다. 연구팀은 이를 이용해 실제 상용화된 옷에 다양한 전자회로를 구현했다.
나아가서 연구팀은 액체금속 복합체를 코팅하는 방법이 다양한 실에 호환 가능하고, 재료의 생친화성이 우수하기 때문에, 이를 이용해 신경과학 연구에 사용할 수 있는 섬유형 바이오 전자 섬유를 구현했다. 연구팀은 제안된 코팅 방법을 이용해 기계적 변형에 영향을 받지 않는 뇌 활동 전극, 신경 자극 전극, 다기능성 옵토지네틱 프로브를 제작해 넓은 범용성과 높은 공정 신뢰성을 갖는다는 것을 보였다.
우리 대학 이건희 박사, 이도훈 박사과정, 전우진 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 온라인 판에 7월 13일자 출판됐다. (논문명: Conductance stable and mechanically durable bi-layer EGaIn composite-coated stretchable fiber for 1D bioelectronics)
스티브박 교수는 "옷에 다양한 전자 공학적인 기능을 웨어러블 형태로 구현하는 가능성을 보여준 연구로 최근에 각광받고 있는 환자 편의성을 높인 웨어러블 헬스케어 소자나 최소침습형 임플란터블 전자소자 개발의 새로운 방향성을 제시한 의미있는 결과ˮ 라고 말했다.
한편 이번 연구는 한국연구재단, KAIST의 지원을 받아 수행됐다. 이건희 박사는 포스코청압재단의 지원을 받고 있다.
150% 쭉쭉 늘어나는 전자 섬유 개발
전자 섬유는 최근 각광받고 있는 사용자 친화 웨어러블 소자, 헬스케어 소자, 최소 침습형 임플란터블 전자소자에 핵심 요소로 여겨져 활발하게 연구가 진행되고 있다. 하지만 고체 금속 전도체 필러(Conductive filler)를 사용한 전자 섬유를 늘려서 사용하려 할 경우, 전기전도성이 급격하게 감소해 전기적 성질이 망가진다는 단점이 있다.
우리 대학 신소재공학과 스티브 박, 전기및전자공학부 정재웅, 바이오및뇌공학과 박성준 교수 공동 연구팀이 높은 전도도와 내구성을 가지는 액체금속 복합체를 이용해 신축성이 우수한 전자 섬유를 개발했다고 25일 밝혔다.
전자 섬유의 늘어나지 않는 단점을 해결하기 위해 연구팀은 고체처럼 형상이 고정된 것이 아닌 기계적 변형에 맞춰 형태가 변형될 수 있는 액체금속 입자 기반의 전도체 필러를 제시했다. 액체금속 마이크로 입자는 인장이 가해질 경우에 그 형태가 타원형으로 늘어나면서 전기 저항 변화를 최소화할 수 있다. 하지만 그 크기가 수 마이크로미터이기 때문에, 기존에 이용된 딥-코팅(dip-coating)과 같은 단순한 방법으로 실에 코팅하는 것이 불가능하다. 연구진은 액체금속 입자가 높은 밀도로 실 위에 전달될 수 있고, 블레이드와 기판 사이에서 현탁액의 조성을 실시간으로 바꾸면서 화학적 변성을 통해 액체금속 입자를 실과 접착시킬 수 있는 새로운 방법인 현탁액 전단(suspension shearing) 방법을 통해 이를 해결했다. 추가로 기계적 안정성이 우수한 탄소나노튜브(CNT)가 포함된 액체금속 입자를 한층 더 코팅하는 방식으로, 액체금속 복합체의 기계적 안정성도 확보할 수 있었다.
제작된 신축성 전자 섬유는 추가적인 공정이 필요 없이 우수한 초기전도성을 보였고(2.2x10^6 S/m), 기존의 고체 금속 전도체 기반 섬유들과는 다르게 150% 늘려도 전기저항 변화가 거의 없다. 기계적 안정성도 우수해 반복되는 변형 실험에도 전기적 성질을 유지할 수 있었고, 다양한 전자 부품들과 쉽게 통합될 수 있다. 연구팀은 이를 이용해 실제 상용화된 옷에 다양한 전자회로를 구현했다.
나아가서 연구팀은 액체금속 복합체를 코팅하는 방법이 다양한 실에 호환 가능하고, 재료의 생친화성이 우수하기 때문에, 이를 이용해 신경과학 연구에 사용할 수 있는 섬유형 바이오 전자 섬유를 구현했다. 연구팀은 제안된 코팅 방법을 이용해 기계적 변형에 영향을 받지 않는 뇌 활동 전극, 신경 자극 전극, 다기능성 옵토지네틱 프로브를 제작해 넓은 범용성과 높은 공정 신뢰성을 갖는다는 것을 보였다.
우리 대학 이건희 박사, 이도훈 박사과정, 전우진 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 온라인 판에 7월 13일자 출판됐다. (논문명: Conductance stable and mechanically durable bi-layer EGaIn composite-coated stretchable fiber for 1D bioelectronics)
스티브박 교수는 "옷에 다양한 전자 공학적인 기능을 웨어러블 형태로 구현하는 가능성을 보여준 연구로 최근에 각광받고 있는 환자 편의성을 높인 웨어러블 헬스케어 소자나 최소침습형 임플란터블 전자소자 개발의 새로운 방향성을 제시한 의미있는 결과ˮ 라고 말했다.
한편 이번 연구는 한국연구재단, KAIST의 지원을 받아 수행됐다. 이건희 박사는 포스코청압재단의 지원을 받고 있다.
2023.07.25
조회수 4117
-
 고규영 특훈교수, 올해 대한민국최고과학기술인상 수상
과학기술정보통신부와 한국과학기술단체총연합회는 올해 대한민국최고과학기술인상 수상자로 고규영 우리 대학 의과학대학원 특훈교수를 선정했다고 2일 밝혔다.
고 교수는 치매 등 퇴행성 뇌 질환을 유발하는 뇌 속 노폐물이 뇌 밖으로 배출되는 주요 경로가 뇌 하부에 있는 뇌막 림프관임을 세계 최초로 규명하고 나이가 들수록 이 뇌막 림프관의 기능이 저하돼 노폐물 배출 능력이 떨어짐을 확인했다. 이전에는 뇌척수액에 녹아든 노폐물과 독성이 뇌 밖으로 배출되는 경로가 베일에 싸여 있었다.
이 연구 결과는 퇴행성 뇌 질환의 예방과 치료에 있어 새로운 방향을 제시했다는 평가를 받으며 최고 권위의 국제 학술지 '네이처'와 '사이언스' 등에 게재돼 자주 인용되고 있다.
고 교수는 연구 중심 의사과학자로서 전북대 의대에서 학사, 동 대학원에서 석사와 박사 학위를 받았다. 이후 포항공대 생명과학과 부교수 등을 거쳐 현재 KAIST 의과학대학원 특훈교수와 IBS 혈관연구단장을 지내고 있다.
고 교수는 지난달 30일 정부서울청사에서 진행된 브리핑에서 "수상해 매우 기쁘다"며 "계속 연구를 진행해 뇌 림프관을 통해 노폐물이나 독성 물질이 원활하게 빠져나갈 수 있게 하는 방법을 찾아내 언젠가는 치매 예방과 치료에 크게 기여할 것"이라고 포부를 밝혔다.
또 그는 지금까지 성과를 바탕으로 현재 영장류에 대한 실험을 진행하고 있다며 확증되면 환자를 대상으로도 연구하고 싶다고 말했다.
과기정통부는 고 교수가 이 밖에도 림프관 경유 암세포가 림프절로 전이하기 위해 지방산을 핵심 연료로 활용한다는 사실과 녹내장의 발생 원인 등을 규명하는 등 선도적인 성과를 도출했다고 밝혔다.
또 현재까지 35명의 박사와 3명의 석사를 배출하는 등 인재 양성에도 이바지하고 있다고 덧붙였다.
한편 그는 브리핑에서 국내 의사과학자의 필요성에 대해서도 입을 열었다. 그는 "국내 의사 13만명 중 성형이나 미용 분야에 3만명이 있는데 그것도 필요한 부분이지만 국가 발전이나 미래를 위해서 연구해야 한다"며 "의대·치의대·한의대에 4천명이 있는 것으로 아는데 1%인 40명만 중계 연구나 기초 연구를 하면 블록버스터 약도 만드는 리더가 될거라 본다"고 말했다.
이어 그는 "KAIST에서 1년에 의사과학자를 30명씩 배출해도 이들이 다시 병원으로 돌아가 교수가 된다"며 "연구할 수 있도록 분위기를 만들어주고 병원이나 부처에서 지원해야 한다"고 강조했다.
대한민국최고과학기술인상은 2003년부터 우리나라를 대표할 수 있는 탁월한 연구성과를 이룬 과학기술인에 부여되고 있다. 올해에는 후보자 총 23명을 대상으로 세 단계의 심사 과정을 거쳐 수상자를 선정했다.
과기정통부는 오는 5일 서울 강남구 한국과학기술회관에서 열리는 '제1회 세계 한인과학기술인대회' 개회식에서 고 교수에게 대통령 상장과 상금 3억 원을 수여할 계획이다.
고규영 특훈교수, 올해 대한민국최고과학기술인상 수상
과학기술정보통신부와 한국과학기술단체총연합회는 올해 대한민국최고과학기술인상 수상자로 고규영 우리 대학 의과학대학원 특훈교수를 선정했다고 2일 밝혔다.
고 교수는 치매 등 퇴행성 뇌 질환을 유발하는 뇌 속 노폐물이 뇌 밖으로 배출되는 주요 경로가 뇌 하부에 있는 뇌막 림프관임을 세계 최초로 규명하고 나이가 들수록 이 뇌막 림프관의 기능이 저하돼 노폐물 배출 능력이 떨어짐을 확인했다. 이전에는 뇌척수액에 녹아든 노폐물과 독성이 뇌 밖으로 배출되는 경로가 베일에 싸여 있었다.
이 연구 결과는 퇴행성 뇌 질환의 예방과 치료에 있어 새로운 방향을 제시했다는 평가를 받으며 최고 권위의 국제 학술지 '네이처'와 '사이언스' 등에 게재돼 자주 인용되고 있다.
고 교수는 연구 중심 의사과학자로서 전북대 의대에서 학사, 동 대학원에서 석사와 박사 학위를 받았다. 이후 포항공대 생명과학과 부교수 등을 거쳐 현재 KAIST 의과학대학원 특훈교수와 IBS 혈관연구단장을 지내고 있다.
고 교수는 지난달 30일 정부서울청사에서 진행된 브리핑에서 "수상해 매우 기쁘다"며 "계속 연구를 진행해 뇌 림프관을 통해 노폐물이나 독성 물질이 원활하게 빠져나갈 수 있게 하는 방법을 찾아내 언젠가는 치매 예방과 치료에 크게 기여할 것"이라고 포부를 밝혔다.
또 그는 지금까지 성과를 바탕으로 현재 영장류에 대한 실험을 진행하고 있다며 확증되면 환자를 대상으로도 연구하고 싶다고 말했다.
과기정통부는 고 교수가 이 밖에도 림프관 경유 암세포가 림프절로 전이하기 위해 지방산을 핵심 연료로 활용한다는 사실과 녹내장의 발생 원인 등을 규명하는 등 선도적인 성과를 도출했다고 밝혔다.
또 현재까지 35명의 박사와 3명의 석사를 배출하는 등 인재 양성에도 이바지하고 있다고 덧붙였다.
한편 그는 브리핑에서 국내 의사과학자의 필요성에 대해서도 입을 열었다. 그는 "국내 의사 13만명 중 성형이나 미용 분야에 3만명이 있는데 그것도 필요한 부분이지만 국가 발전이나 미래를 위해서 연구해야 한다"며 "의대·치의대·한의대에 4천명이 있는 것으로 아는데 1%인 40명만 중계 연구나 기초 연구를 하면 블록버스터 약도 만드는 리더가 될거라 본다"고 말했다.
이어 그는 "KAIST에서 1년에 의사과학자를 30명씩 배출해도 이들이 다시 병원으로 돌아가 교수가 된다"며 "연구할 수 있도록 분위기를 만들어주고 병원이나 부처에서 지원해야 한다"고 강조했다.
대한민국최고과학기술인상은 2003년부터 우리나라를 대표할 수 있는 탁월한 연구성과를 이룬 과학기술인에 부여되고 있다. 올해에는 후보자 총 23명을 대상으로 세 단계의 심사 과정을 거쳐 수상자를 선정했다.
과기정통부는 오는 5일 서울 강남구 한국과학기술회관에서 열리는 '제1회 세계 한인과학기술인대회' 개회식에서 고 교수에게 대통령 상장과 상금 3억 원을 수여할 계획이다.
2023.07.03
조회수 2993
-
 염증없이 체내·외 측정 가능한 전자 신소재 개발
생체전자 의료기기는 체내에서 발생하는 신호를 읽어 생물학적 활동을 감지하거나, 조직을 자극해 질병 등을 치료하는 데 사용된다. 하지만 의료기기에 사용되는 전극 물질은 딱딱한 물성을 가지고 있어 체내에 염증반응을 일으키고 조직에 다량의 손상으로 이어질 수 있다. 따라서 조직과 같이 부드러운 성질을 가지면서도 전도성을 띠는 하이드로겔과 같은 연성 물질에 생체적합성이 높은 전도성 고분자를 체내 전극으로 사용하는 연구들이 활발하게 진행되고 있다.
우리 대학 신소재공학과 강지형 교수와 바이오및뇌공학과 박성준 교수 공동연구팀이 기존에 없었던 고전도성, 유사 조직 접착성 하이드로겔이란 신소재를 개발해 고성능 생체전자 기기를 구현했다고 4일 밝혔다.
대부분 전기 전도도가 높을수록 전도성 도메인들의 결정성이 높아지는 원리에 의해, 전도성이 높은 하이드로겔은 딱딱해지고, 부드러운 하이드로겔은 전도성이 낮을 수밖에 없다는 한계를 가진다. 이에 따라 전도성 고분자를 사용하는 하이드로겔 중, 전기 전도도가 높으면서도(10 S/cm 이상) 부드러운 물성(100 kPa 이하)을 가진 하이드로겔은 지금까지 보고된 바 없었다.
강지형 교수 연구팀은 기존에 없었던 고전도성, 유사 조직 물성 하이드로겔을 개발했다. 이 하이드로겔은 보고된 전도성 고분자 하이드로겔 중 가장 높은 전기 전도도(247 S/cm)를 띄며, 조직과 비슷한 물성(탄성율 = 60 kPa, 파괴변형률 = 410%)을 갖는다. 또한, 본 재료는 지속적인 움직임과 팽창, 수축이 있는 심장, 위와 같은 조직에서 안정적으로 기기가 작동하기 위해 필수조건인 조직에 쉽게 접착되는 장점을 가지고 있다.
공동연구팀은 원하는 생체 조직에 맞게 조정하고 그 형태에 맞추는 주형의 그물 구조에 따라 높은 질서도를 가지는 고분자 주형 네트워크를 도입했다.
따라서 주형에 맞추어 형성된 그물 네트워크는 기존 네트워크 대비 100배 이상 높은 전기 전도도를 보이며, 동시에 주형 고분자의 부드러운 특성 때문에 조직과 비슷한 물성을 지니게 된다. 변형에도 저항이 바뀌지 않아 생체전극으로서 최적의 성능을 갖는다.
또한 연구팀은 개발한 하이드로겔을 전극을 기반으로 한 높은 전기 전도도를 가진 다양한 고성능 생체전자 기기를 제작, 그 기능성을 검증했다. 높은 전기 전도도를 가진 특성으로 좌골신경 자극을 대상으로 하는 디바이스의 경우, 매우 낮은 전압(40 mV)에서 다리 근육의 움직임을 성공적으로 유도할 수 있었다. 또한 심전도 측정(ECG)을 위한 디바이스의 경우에도 매우 높은 신호 대 잡음 비(61 dB)로 신호를 측정하는 데 성공함으로써, 초고품질 생체 신호 측정을 위한 연성 기기 개발 가능성을 입증하였다.
이번 연구를 주도한 강지형 교수는 "이번 연구는 고전도성을 갖고 생체조직과 유사한 기계적 물성을 갖는 하이드로겔 개발을 위한 합성 방향을 새롭게 제시했다는 점에서 의미가 있다고 하면서, "이번에 개발된 전도성 하이드로겔은 급속도로 성장하고 있는 전자약 시장에 게임 체인저가 될 것으로 기대된다고 말했다.
우리 대학 신소재공학과 정주은 박사과정과 바이오및뇌공학과 성창훈 박사과정이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 4월 18일 게재됐다. (논문명: Highly conductive tissue-like hydrogel interface through template-directed assembly)
한편 이번 연구는 한국연구재단의 나노소재기술개발 미래기술연구실 사업을 받아 수행됐다.
염증없이 체내·외 측정 가능한 전자 신소재 개발
생체전자 의료기기는 체내에서 발생하는 신호를 읽어 생물학적 활동을 감지하거나, 조직을 자극해 질병 등을 치료하는 데 사용된다. 하지만 의료기기에 사용되는 전극 물질은 딱딱한 물성을 가지고 있어 체내에 염증반응을 일으키고 조직에 다량의 손상으로 이어질 수 있다. 따라서 조직과 같이 부드러운 성질을 가지면서도 전도성을 띠는 하이드로겔과 같은 연성 물질에 생체적합성이 높은 전도성 고분자를 체내 전극으로 사용하는 연구들이 활발하게 진행되고 있다.
우리 대학 신소재공학과 강지형 교수와 바이오및뇌공학과 박성준 교수 공동연구팀이 기존에 없었던 고전도성, 유사 조직 접착성 하이드로겔이란 신소재를 개발해 고성능 생체전자 기기를 구현했다고 4일 밝혔다.
대부분 전기 전도도가 높을수록 전도성 도메인들의 결정성이 높아지는 원리에 의해, 전도성이 높은 하이드로겔은 딱딱해지고, 부드러운 하이드로겔은 전도성이 낮을 수밖에 없다는 한계를 가진다. 이에 따라 전도성 고분자를 사용하는 하이드로겔 중, 전기 전도도가 높으면서도(10 S/cm 이상) 부드러운 물성(100 kPa 이하)을 가진 하이드로겔은 지금까지 보고된 바 없었다.
강지형 교수 연구팀은 기존에 없었던 고전도성, 유사 조직 물성 하이드로겔을 개발했다. 이 하이드로겔은 보고된 전도성 고분자 하이드로겔 중 가장 높은 전기 전도도(247 S/cm)를 띄며, 조직과 비슷한 물성(탄성율 = 60 kPa, 파괴변형률 = 410%)을 갖는다. 또한, 본 재료는 지속적인 움직임과 팽창, 수축이 있는 심장, 위와 같은 조직에서 안정적으로 기기가 작동하기 위해 필수조건인 조직에 쉽게 접착되는 장점을 가지고 있다.
공동연구팀은 원하는 생체 조직에 맞게 조정하고 그 형태에 맞추는 주형의 그물 구조에 따라 높은 질서도를 가지는 고분자 주형 네트워크를 도입했다.
따라서 주형에 맞추어 형성된 그물 네트워크는 기존 네트워크 대비 100배 이상 높은 전기 전도도를 보이며, 동시에 주형 고분자의 부드러운 특성 때문에 조직과 비슷한 물성을 지니게 된다. 변형에도 저항이 바뀌지 않아 생체전극으로서 최적의 성능을 갖는다.
또한 연구팀은 개발한 하이드로겔을 전극을 기반으로 한 높은 전기 전도도를 가진 다양한 고성능 생체전자 기기를 제작, 그 기능성을 검증했다. 높은 전기 전도도를 가진 특성으로 좌골신경 자극을 대상으로 하는 디바이스의 경우, 매우 낮은 전압(40 mV)에서 다리 근육의 움직임을 성공적으로 유도할 수 있었다. 또한 심전도 측정(ECG)을 위한 디바이스의 경우에도 매우 높은 신호 대 잡음 비(61 dB)로 신호를 측정하는 데 성공함으로써, 초고품질 생체 신호 측정을 위한 연성 기기 개발 가능성을 입증하였다.
이번 연구를 주도한 강지형 교수는 "이번 연구는 고전도성을 갖고 생체조직과 유사한 기계적 물성을 갖는 하이드로겔 개발을 위한 합성 방향을 새롭게 제시했다는 점에서 의미가 있다고 하면서, "이번에 개발된 전도성 하이드로겔은 급속도로 성장하고 있는 전자약 시장에 게임 체인저가 될 것으로 기대된다고 말했다.
우리 대학 신소재공학과 정주은 박사과정과 바이오및뇌공학과 성창훈 박사과정이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 4월 18일 게재됐다. (논문명: Highly conductive tissue-like hydrogel interface through template-directed assembly)
한편 이번 연구는 한국연구재단의 나노소재기술개발 미래기술연구실 사업을 받아 수행됐다.
2023.05.04
조회수 4480
-
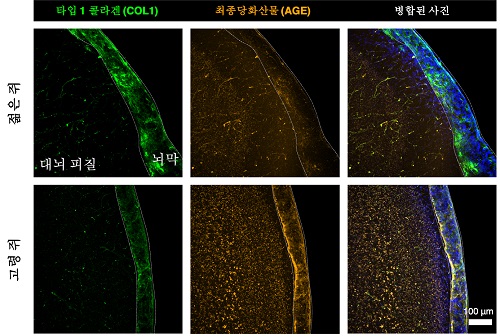 노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15
조회수 3592
 극미량 돌연변이 세포로도 뇌질환 발생한다
뇌를 포함한 모든 신체 기관은 세포 분열 과정에서 발생하는 돌연변이(모자이시즘)을 피할 수 없다. 그렇다면 과연 몇 개의 신경세포에 질병 유발 돌연변이가 생겨났을 때부터 전체 뇌신경 회로를 망가트려 뇌 기능 이상을 일으킬 수 있을까?
우리 대학 의과학대학원 이정호 교수팀이 뇌세포 특이적 돌연변이(뇌 체성 모자이시즘)에 의한 소아 난치성 뇌전증 동물 모델과 환자 뇌 조직 연구를 통해 0.1퍼센트 이하 비율의 극미량 돌연변이 신경세포에 의해서도 뇌 전체 기능 이상을 유발해 뇌전증 발작이 발생할 수 있음을 규명했다고 9일 밝혔다.
이를 통해 난치성 뇌전증의 돌연변이 유전자 진단에 있어 새로운 기준을 마련하는 한편, 극미량의 돌연변이 신경세포가 다양한 뇌 질환 유발에 관여할 수 있음을 밝혔다. 이번 연구의 결과는 세계적 신경 의학 학술지 `브레인(Brain)'에 지난 6월 25일 字 게재됐다.
연구팀은 이번 연구에서 과연 얼마나 적은 수의 세포에서 특정 유전자 모자이시즘이 누적됐을 때 이것이 전체 뇌 기능 이상을 유도하는 뇌 질환 발생으로 이어질 것인가라는 질문에 대답하고자, 마우스 질병 모델과 인체 조직을 이용한 중개의학적 연구를 수행했다.
연구팀은 실험용 쥐의 뇌 조직에 뇌전증 유발 체성 모자이시즘*을 최소 수백 개에서 최대 수만 개의 세포에 유발했다. 이때 고작 8천에서 9천 개 수준의 돌연변이 신경세포가 나타날 때부터, 실험용 쥐가 뇌전증 발작을 일으키고, 관련된 병리가 나타남을 관찰했다. 더 나아가, 난치성 뇌전증 환자 뇌 조직에서 대용량 유전정보 증폭 시퀀싱을 수행해(ultra-high depth amplicon sequencing) 정확한 변이 모자이시즘 비율을 측정했고, 최소 0.07%에 이르는 뇌전증 유발 체성 모자이시즘을 관찰했다.
*체성 모자이시즘(Somatic Mosaicism): 하나의 수정란에서 분열 및 분화를 통해 우리 몸을 이루는 약 30조 개의 세포들이 만들어지는 과정에서 세포마다 돌연변이가 발생할 수 있다는 것으로 암의 진화뿐만 아니라 비암성 질환에서도 중요한 질병 원인으로 최근 주목을 받고 있음.
이 발견은 약물 치료에 반응하지 않아 수술에 이르게 되는 난치성 뇌전증의 유전적 정밀 진단에 도움을 줄 수 있으며, 또한 아직 원인이 밝혀지지 않은 수많은 난치성 신경 정신의학적 질환들이 뇌의 발생과 분화 과정에서 일어나는 극소량의 미세 돌연변이들과 밀접한 관련이 있음을 시사한다.
이번 연구는 국소 피질이형성증*의 진단법 향상 및 체성 모자이시즘에 의한 뇌 질환 원인 발견에 있어서 중요한 기초를 마련할 것으로 예상된다. 이번 연구 성과는 KAIST 교원 창업 기업인 소바젠㈜(대표 박철원, 김병태)을 통해 난치성 뇌전증 환자의 체성 모자이시즘 변이를 정밀 타겟하는 혁신 RNA 치료제 개발에 이용될 예정이다.
*국소 피질이형성증: 뇌 발달 과정 중 대뇌 피질에 국소적으로 신경세포이상이 발생하는 질환으로 기존 항뇌전증 약물에 전혀 반응하지 않는 소아 난치성 뇌전증을 일으키는 가장 중요한 원인으로 알려져 있다.
우리 대학 의과학대학원 졸업생 의사과학자이자 논문의 제1 저자 김진태 박사는 "극미량의 체성 돌연변이라도 뇌의 기능 이상을 유발할 수 있음이 알려졌고, 이를 통해 난치성 뇌전증 등의 유전적 진단과 치료제 개발에 도움이 될 수 있기를 바란다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원 사업의 지원을 받아 수행됐다.
2024.07.09 조회수 690
극미량 돌연변이 세포로도 뇌질환 발생한다
뇌를 포함한 모든 신체 기관은 세포 분열 과정에서 발생하는 돌연변이(모자이시즘)을 피할 수 없다. 그렇다면 과연 몇 개의 신경세포에 질병 유발 돌연변이가 생겨났을 때부터 전체 뇌신경 회로를 망가트려 뇌 기능 이상을 일으킬 수 있을까?
우리 대학 의과학대학원 이정호 교수팀이 뇌세포 특이적 돌연변이(뇌 체성 모자이시즘)에 의한 소아 난치성 뇌전증 동물 모델과 환자 뇌 조직 연구를 통해 0.1퍼센트 이하 비율의 극미량 돌연변이 신경세포에 의해서도 뇌 전체 기능 이상을 유발해 뇌전증 발작이 발생할 수 있음을 규명했다고 9일 밝혔다.
이를 통해 난치성 뇌전증의 돌연변이 유전자 진단에 있어 새로운 기준을 마련하는 한편, 극미량의 돌연변이 신경세포가 다양한 뇌 질환 유발에 관여할 수 있음을 밝혔다. 이번 연구의 결과는 세계적 신경 의학 학술지 `브레인(Brain)'에 지난 6월 25일 字 게재됐다.
연구팀은 이번 연구에서 과연 얼마나 적은 수의 세포에서 특정 유전자 모자이시즘이 누적됐을 때 이것이 전체 뇌 기능 이상을 유도하는 뇌 질환 발생으로 이어질 것인가라는 질문에 대답하고자, 마우스 질병 모델과 인체 조직을 이용한 중개의학적 연구를 수행했다.
연구팀은 실험용 쥐의 뇌 조직에 뇌전증 유발 체성 모자이시즘*을 최소 수백 개에서 최대 수만 개의 세포에 유발했다. 이때 고작 8천에서 9천 개 수준의 돌연변이 신경세포가 나타날 때부터, 실험용 쥐가 뇌전증 발작을 일으키고, 관련된 병리가 나타남을 관찰했다. 더 나아가, 난치성 뇌전증 환자 뇌 조직에서 대용량 유전정보 증폭 시퀀싱을 수행해(ultra-high depth amplicon sequencing) 정확한 변이 모자이시즘 비율을 측정했고, 최소 0.07%에 이르는 뇌전증 유발 체성 모자이시즘을 관찰했다.
*체성 모자이시즘(Somatic Mosaicism): 하나의 수정란에서 분열 및 분화를 통해 우리 몸을 이루는 약 30조 개의 세포들이 만들어지는 과정에서 세포마다 돌연변이가 발생할 수 있다는 것으로 암의 진화뿐만 아니라 비암성 질환에서도 중요한 질병 원인으로 최근 주목을 받고 있음.
이 발견은 약물 치료에 반응하지 않아 수술에 이르게 되는 난치성 뇌전증의 유전적 정밀 진단에 도움을 줄 수 있으며, 또한 아직 원인이 밝혀지지 않은 수많은 난치성 신경 정신의학적 질환들이 뇌의 발생과 분화 과정에서 일어나는 극소량의 미세 돌연변이들과 밀접한 관련이 있음을 시사한다.
이번 연구는 국소 피질이형성증*의 진단법 향상 및 체성 모자이시즘에 의한 뇌 질환 원인 발견에 있어서 중요한 기초를 마련할 것으로 예상된다. 이번 연구 성과는 KAIST 교원 창업 기업인 소바젠㈜(대표 박철원, 김병태)을 통해 난치성 뇌전증 환자의 체성 모자이시즘 변이를 정밀 타겟하는 혁신 RNA 치료제 개발에 이용될 예정이다.
*국소 피질이형성증: 뇌 발달 과정 중 대뇌 피질에 국소적으로 신경세포이상이 발생하는 질환으로 기존 항뇌전증 약물에 전혀 반응하지 않는 소아 난치성 뇌전증을 일으키는 가장 중요한 원인으로 알려져 있다.
우리 대학 의과학대학원 졸업생 의사과학자이자 논문의 제1 저자 김진태 박사는 "극미량의 체성 돌연변이라도 뇌의 기능 이상을 유발할 수 있음이 알려졌고, 이를 통해 난치성 뇌전증 등의 유전적 진단과 치료제 개발에 도움이 될 수 있기를 바란다ˮ라고 말했다.
한편 이번 연구는 서경배과학재단, 한국연구재단, 보건산업진흥원 사업의 지원을 받아 수행됐다.
2024.07.09 조회수 690 화학적, 전기적 양방향 소통이 가능한 파이버형 뇌-컴퓨터 인터페이스 개발
뇌 속 뉴런은 화학적, 전기적 신호가 동시에 작동하면서 정교한 시스템을 만들어내지만 현재까지는 이러한 신호를 동시에 주고받으면서 신경의 작동 원리를 확인할 수 있는 장치가 존재하지 않았다. 한국 연구진이 화학적 신호와 전기적 신호를 양 방향적으로 주고받으며 세부적인 신호 전달 체계를 탐사할 수 있는 다기능 신경 인터페이스를 개발하여 앞으로 신경 체계 연구, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이, 초소형 와이어 병합 열 인발공정(Microwire Co-drawing Thermal Drawing Process, MC-TDP)*을 통해 카본, 폴리머, 금속의 다양한 재료를 통합하여 4가지 기능성을 가진 다기능 섬유형 신경 인터페이스를 개발했다고 13일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공
뇌신경 시스템 조사를 위한 삽입형 인터페이스는 전기적 성능에 중점을 두고 발전해 왔다. 하지만 전기적, 화학적 신호의 시너지 효과를 연구하기 위해서는 전기적 신호뿐만 아니라 화학적 신호의 역학을 기록하고 화학적 자극 또한 할 수 있는 신경 디바이스가 필요했다. 그러나 기존의 제작 방법으로는 다양한 자극과 기록을 수행할 수 있는 다양한 재료를 융합하는 것이 어려웠고, 특히 마이크로미터 스케일로 정교한 다기능성 신경 인터페이스를 만드는 것이 어렵다는 문제가 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 초소형 와이어 병합 열 인발공정을 통해 머리카락 크기의 다기능 섬유를 뽑아내는 동안 초소형 와이어를 병합하고 카본 파이버를 융합하여 뉴런 사이에서 일어나는 대표적인 신호 전달을 동시에 조사할 수 있는 다기능 섬유를 제작했다. 연구팀은 제작된 하나의 섬유가 카본 파이버를 통한 도파민 모니터링, 마이크로 유체관을 통한 약물 주입, 폴리머 광 도파관을 통한 광 유전학적 신경 자극, 그리고 초소형 와이어를 통한 전기신호 측정을 할 수 있음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에서 광유전학적 자극에 따른 화학적 신경전달물질 중 도파민과 전기적 신경 활성 신호를 효과적으로 측정하고 약물에 따른 도파민 방출량의 변화를 확인할 수 있음을 보였다. 또한 연구팀은 개발된 섬유가 자발적인 신경 신호를 측정할 수 있음을 보여주며 신경 인터페이스로써의 범용적 사용성도 확인했다.
이번 연구 결과는 국제 학술지 '에이씨에스 나노(ACS Nano)'에 2024년 5월 온라인 출판됐다. (논문명: A Multifunctional and Flexible Neural Probe with Thermally Drawn Fibers for Bidirectional Synaptic Probing in the Brain)
박성준 교수는 "화학적 신경전달물질 기록 및 화학적 자극, 전기적 신경 활성신호 기록, 그리고 광학적 조절 기능을 갖춘 차세대 초다기능성 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 다양한 신경 회로에의 적용을 통해 신경 회로의 작동원리 규명과 뇌 질환의 세부적인 메커니즘 파악에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 기초연구실, STEAM연구사업 및 범부처재생의료기술사업의 지원을 받아 수행됐다.
2024.05.13 조회수 1510
화학적, 전기적 양방향 소통이 가능한 파이버형 뇌-컴퓨터 인터페이스 개발
뇌 속 뉴런은 화학적, 전기적 신호가 동시에 작동하면서 정교한 시스템을 만들어내지만 현재까지는 이러한 신호를 동시에 주고받으면서 신경의 작동 원리를 확인할 수 있는 장치가 존재하지 않았다. 한국 연구진이 화학적 신호와 전기적 신호를 양 방향적으로 주고받으며 세부적인 신호 전달 체계를 탐사할 수 있는 다기능 신경 인터페이스를 개발하여 앞으로 신경 체계 연구, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이, 초소형 와이어 병합 열 인발공정(Microwire Co-drawing Thermal Drawing Process, MC-TDP)*을 통해 카본, 폴리머, 금속의 다양한 재료를 통합하여 4가지 기능성을 가진 다기능 섬유형 신경 인터페이스를 개발했다고 13일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공
뇌신경 시스템 조사를 위한 삽입형 인터페이스는 전기적 성능에 중점을 두고 발전해 왔다. 하지만 전기적, 화학적 신호의 시너지 효과를 연구하기 위해서는 전기적 신호뿐만 아니라 화학적 신호의 역학을 기록하고 화학적 자극 또한 할 수 있는 신경 디바이스가 필요했다. 그러나 기존의 제작 방법으로는 다양한 자극과 기록을 수행할 수 있는 다양한 재료를 융합하는 것이 어려웠고, 특히 마이크로미터 스케일로 정교한 다기능성 신경 인터페이스를 만드는 것이 어렵다는 문제가 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 초소형 와이어 병합 열 인발공정을 통해 머리카락 크기의 다기능 섬유를 뽑아내는 동안 초소형 와이어를 병합하고 카본 파이버를 융합하여 뉴런 사이에서 일어나는 대표적인 신호 전달을 동시에 조사할 수 있는 다기능 섬유를 제작했다. 연구팀은 제작된 하나의 섬유가 카본 파이버를 통한 도파민 모니터링, 마이크로 유체관을 통한 약물 주입, 폴리머 광 도파관을 통한 광 유전학적 신경 자극, 그리고 초소형 와이어를 통한 전기신호 측정을 할 수 있음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에서 광유전학적 자극에 따른 화학적 신경전달물질 중 도파민과 전기적 신경 활성 신호를 효과적으로 측정하고 약물에 따른 도파민 방출량의 변화를 확인할 수 있음을 보였다. 또한 연구팀은 개발된 섬유가 자발적인 신경 신호를 측정할 수 있음을 보여주며 신경 인터페이스로써의 범용적 사용성도 확인했다.
이번 연구 결과는 국제 학술지 '에이씨에스 나노(ACS Nano)'에 2024년 5월 온라인 출판됐다. (논문명: A Multifunctional and Flexible Neural Probe with Thermally Drawn Fibers for Bidirectional Synaptic Probing in the Brain)
박성준 교수는 "화학적 신경전달물질 기록 및 화학적 자극, 전기적 신경 활성신호 기록, 그리고 광학적 조절 기능을 갖춘 차세대 초다기능성 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 다양한 신경 회로에의 적용을 통해 신경 회로의 작동원리 규명과 뇌 질환의 세부적인 메커니즘 파악에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 기초연구실, STEAM연구사업 및 범부처재생의료기술사업의 지원을 받아 수행됐다.
2024.05.13 조회수 1510 KAIST 첨단 연구의 체험·전시·제품을 짜릿하게 만나다
우리 대학이 4월 과학의 달을 맞아 첨단 연구성과를 체험형 전시 프로그램으로 구성해 시민과 소통에 나선다. 25일부터 28일까지 4일간 대전 엑스포 시민광장 및 과학공원 일대에서 열리는 '2024 대한민국 과학축제 & 과학기술대전'에 6개 연구팀 및 3개 창업기업이 참여해 기술을 선보인다. '과학 실험실' 구역에서는 수면·퍼스널 컬러·뇌구조 분야의 연구진이 체험형 전시로 관람객을 맞는다. 석현정 산업디자인학과 교수 연구팀은 인공지능 기반 퍼스널컬러 진단 서비스를 제공하는 '나의 퍼스널 컬러 찾기(The Authentic Color Play)' 부스를 설치한다. 방문객들은 현장에서 피부색 자동 측정 기술을 직접 체험해보고 개인 피부에 최적화된 색상을 추천받을 수 있다. 김재경 수리과학과 교수 연구팀은 방문객이 양질의 수면을 하고 있는지 3분 만에 알아볼 수 있는 '슬립스(SLEEPS)' 프로그램을 운영한다. 머신러닝 기반의 수면장애 예측 알고리즘을 활용해 간단한 설문과 신체 측정만으로 수면장애 위험도를 계산해보는 체험이다. 검사 결과를 바탕으로 수면장애 위험도를 낮출 수 있는 생활 습관도 함께 알아볼 수 있다. 최민이 뇌인지과학과 교수 연구팀은 '미니 브레인' 체험을 진행한다. 가상현실(VR) 프로그램을 이용해 뇌의 주요 부위들을 해체·조립하며 뇌의 구조를 학습할 수 있다. 또한, 주요 기능과 역할이 다른 뇌 모형의 각 부분을 색칠로 구분하고 스티커를 붙이는 ‘뇌 컬러링’과 세포로부터 미니 브레인이 생겨나는 과정을 시뮬레이션 한 동영상도 관람할 수 있다.
국가 12대 전략기술 성과를 모아놓은 '과학 뮤지엄' 구역에서는 첨단바이오·첨단로봇제조·첨단모빌리티 분야의 연구성과를 전시한다.
조병관 공학생물학대학원 교수 연구팀은 '합성생물학 기반 CO2-to-바이오소재 전환 미생물 세포공장 기술'을 전시한다. 쓰레기 매립 가스, 산업 부생가스 등 환경 오염의 주요 원인인 온실가스를 미생물에 흡수시킨 뒤, 합성생물학을 기반으로 하는 유전적 개량기술을 적용해 다양한 바이오소재로 전환할 수 있는 고효율 생체촉매 개발 기술이다.
박해원 기계공학과 교수 연구팀은 험지탐사용 4족보행 로봇인 '하운드(HOUND)'를 공개한다. 하운드는 시각 및 촉각 센서의 도움 없이도 계단이나 험지 같은 비정형 장애물 환경에서도 안정적인 동작이 가능한 로봇이다. 실내 최대 속도 6.5m/s까지 낼 수 있으며, 100m를 19.87초 주파한 기네스 기록도 가지고 있다. 하운드는 축제 기간 내내 행사 현장을 활보하며 방문객을 맞을 예정이다.
장기태 조천식모빌리티 대학원 교수 연구팀은 '디젤 트럭 개조용 박(薄)형 모터' 기술을 선보인다. 택배차량용 디젤 트럭을 하이브리드 방식으로 개조하는 기술이다. 기존 디젤 차량에 모터를 추가해 저속 주행에는 모터를 사용하고 고속 주행에는 기존 엔진을 활용하는 방식이다. 정차와 가속이 잦은 국내 택배 차량에 이 기술을 도입할 경우 연비와 미세먼지를 동시에 저감할 수 있어 국토교통부 우수물류신기술 1호로도 지정된 바 있다. 이 밖에도 KAIST 혁신 창업기업의 기술도 전시된다. 화학과 창업기업 '폴리페놀팩토리(대표 이해신)'는 폴리페놀 기술을 활용해 탈모의 진행을 완화하고 모발의 풍성함을 더해주는 '그래비티' 샴푸를 소개한다. 연구팀이 개발한 특허 성분이 샴푸 과정에서 순간적인 보호막을 만들어 모발을 보호하는 동시에 가늘어진 모발을 힘 있게 잡아주는 원리다. 부스 방문객에게는 기술을 체험할 수 있는 시제품을 선착순으로 제공할 예정이다.
기계공학과 창업기업 '㈜A2US(대표 이승섭)'는 ‘마법의 전기 물방울(Magic Electro Water droplets)' 기술을 사용해 세계 최초로 개발한 제품을 선보인다. 인체에는 해가 없으면서도 공기 중의 유기물과 세균 등을 없애는 천연물질인 '하이드록실 라디칼'을 포함한 물방울을 만들어내는 가습기 '뮤(MEW, Magic Electro Water droplets)'다. 미세한 노즐에 전기를 가해 만들어진 이 물방울을 분무하면 공기 중의 유해물질과 냄새를 제거할 수 있어 가습과 공기정화 기능이 동시에 가능하다.
문화기술대학원 창업기업 '㈜카이(대표 김범기)'는 '밍글 AI(Mingle AI)'을 전시한다. 이미지, 오디오, 비디오 등 다양한 유형의 데이터를 입력하면 3차원의 아바타나 오브젝트를 만들어주는 생성형 인공지능 툴이다. 전문 지식이 없는 일반 사용자도 손쉽게 디지털 휴먼을 제작할 수 있으며, 게임·엔터테인먼트·소셜미디어 등의 분야에서 활용할 수 있다.이광형 KAIST 총장은 "대중과 눈높이를 맞춘 체험 프로그램을 구성해 KAIST의 우수한 기술을 시민과 공유할 수 있어 뜻깊게 생각한다"라고 전했다. 이어, 이 총장은 "우수한 성과와 함께 과학기술로 사회 문제를 해결하기 위해 매진하는 연구자들의 노력과 진심이 함께 전달될 수 있는 자리가 되길 기대한다"라고 덧붙였다.
2024.04.25 조회수 2005
KAIST 첨단 연구의 체험·전시·제품을 짜릿하게 만나다
우리 대학이 4월 과학의 달을 맞아 첨단 연구성과를 체험형 전시 프로그램으로 구성해 시민과 소통에 나선다. 25일부터 28일까지 4일간 대전 엑스포 시민광장 및 과학공원 일대에서 열리는 '2024 대한민국 과학축제 & 과학기술대전'에 6개 연구팀 및 3개 창업기업이 참여해 기술을 선보인다. '과학 실험실' 구역에서는 수면·퍼스널 컬러·뇌구조 분야의 연구진이 체험형 전시로 관람객을 맞는다. 석현정 산업디자인학과 교수 연구팀은 인공지능 기반 퍼스널컬러 진단 서비스를 제공하는 '나의 퍼스널 컬러 찾기(The Authentic Color Play)' 부스를 설치한다. 방문객들은 현장에서 피부색 자동 측정 기술을 직접 체험해보고 개인 피부에 최적화된 색상을 추천받을 수 있다. 김재경 수리과학과 교수 연구팀은 방문객이 양질의 수면을 하고 있는지 3분 만에 알아볼 수 있는 '슬립스(SLEEPS)' 프로그램을 운영한다. 머신러닝 기반의 수면장애 예측 알고리즘을 활용해 간단한 설문과 신체 측정만으로 수면장애 위험도를 계산해보는 체험이다. 검사 결과를 바탕으로 수면장애 위험도를 낮출 수 있는 생활 습관도 함께 알아볼 수 있다. 최민이 뇌인지과학과 교수 연구팀은 '미니 브레인' 체험을 진행한다. 가상현실(VR) 프로그램을 이용해 뇌의 주요 부위들을 해체·조립하며 뇌의 구조를 학습할 수 있다. 또한, 주요 기능과 역할이 다른 뇌 모형의 각 부분을 색칠로 구분하고 스티커를 붙이는 ‘뇌 컬러링’과 세포로부터 미니 브레인이 생겨나는 과정을 시뮬레이션 한 동영상도 관람할 수 있다.
국가 12대 전략기술 성과를 모아놓은 '과학 뮤지엄' 구역에서는 첨단바이오·첨단로봇제조·첨단모빌리티 분야의 연구성과를 전시한다.
조병관 공학생물학대학원 교수 연구팀은 '합성생물학 기반 CO2-to-바이오소재 전환 미생물 세포공장 기술'을 전시한다. 쓰레기 매립 가스, 산업 부생가스 등 환경 오염의 주요 원인인 온실가스를 미생물에 흡수시킨 뒤, 합성생물학을 기반으로 하는 유전적 개량기술을 적용해 다양한 바이오소재로 전환할 수 있는 고효율 생체촉매 개발 기술이다.
박해원 기계공학과 교수 연구팀은 험지탐사용 4족보행 로봇인 '하운드(HOUND)'를 공개한다. 하운드는 시각 및 촉각 센서의 도움 없이도 계단이나 험지 같은 비정형 장애물 환경에서도 안정적인 동작이 가능한 로봇이다. 실내 최대 속도 6.5m/s까지 낼 수 있으며, 100m를 19.87초 주파한 기네스 기록도 가지고 있다. 하운드는 축제 기간 내내 행사 현장을 활보하며 방문객을 맞을 예정이다.
장기태 조천식모빌리티 대학원 교수 연구팀은 '디젤 트럭 개조용 박(薄)형 모터' 기술을 선보인다. 택배차량용 디젤 트럭을 하이브리드 방식으로 개조하는 기술이다. 기존 디젤 차량에 모터를 추가해 저속 주행에는 모터를 사용하고 고속 주행에는 기존 엔진을 활용하는 방식이다. 정차와 가속이 잦은 국내 택배 차량에 이 기술을 도입할 경우 연비와 미세먼지를 동시에 저감할 수 있어 국토교통부 우수물류신기술 1호로도 지정된 바 있다. 이 밖에도 KAIST 혁신 창업기업의 기술도 전시된다. 화학과 창업기업 '폴리페놀팩토리(대표 이해신)'는 폴리페놀 기술을 활용해 탈모의 진행을 완화하고 모발의 풍성함을 더해주는 '그래비티' 샴푸를 소개한다. 연구팀이 개발한 특허 성분이 샴푸 과정에서 순간적인 보호막을 만들어 모발을 보호하는 동시에 가늘어진 모발을 힘 있게 잡아주는 원리다. 부스 방문객에게는 기술을 체험할 수 있는 시제품을 선착순으로 제공할 예정이다.
기계공학과 창업기업 '㈜A2US(대표 이승섭)'는 ‘마법의 전기 물방울(Magic Electro Water droplets)' 기술을 사용해 세계 최초로 개발한 제품을 선보인다. 인체에는 해가 없으면서도 공기 중의 유기물과 세균 등을 없애는 천연물질인 '하이드록실 라디칼'을 포함한 물방울을 만들어내는 가습기 '뮤(MEW, Magic Electro Water droplets)'다. 미세한 노즐에 전기를 가해 만들어진 이 물방울을 분무하면 공기 중의 유해물질과 냄새를 제거할 수 있어 가습과 공기정화 기능이 동시에 가능하다.
문화기술대학원 창업기업 '㈜카이(대표 김범기)'는 '밍글 AI(Mingle AI)'을 전시한다. 이미지, 오디오, 비디오 등 다양한 유형의 데이터를 입력하면 3차원의 아바타나 오브젝트를 만들어주는 생성형 인공지능 툴이다. 전문 지식이 없는 일반 사용자도 손쉽게 디지털 휴먼을 제작할 수 있으며, 게임·엔터테인먼트·소셜미디어 등의 분야에서 활용할 수 있다.이광형 KAIST 총장은 "대중과 눈높이를 맞춘 체험 프로그램을 구성해 KAIST의 우수한 기술을 시민과 공유할 수 있어 뜻깊게 생각한다"라고 전했다. 이어, 이 총장은 "우수한 성과와 함께 과학기술로 사회 문제를 해결하기 위해 매진하는 연구자들의 노력과 진심이 함께 전달될 수 있는 자리가 되길 기대한다"라고 덧붙였다.
2024.04.25 조회수 2005 초장기간 작동 뇌-기계 인터페이스 개발
수술이 불가피한 삽입형 신경 인터페이스의 경우, 한 번의 수술로도 최대한 많은 정보를 얻을 수 있고 장기간 사용가능한 디바이스의 개발이 필요하다. 한국 연구진이 1년 이상 사용가능한 다기능성 신경 인터페이스를 개발하여 향후 뇌 지도, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀과 한양대학교(총장 이기정) 바이오메디컬공학과 최창순 교수 연구팀이, 열 인발공정(Thermal Drawing Process, TDP)*과 탄소나노튜브 시트를 병합해 장기간 사용 가능한 다기능성 섬유형 신경 인터페이스를 개발했다고 24일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공.
뇌신경 시스템 탐구를 위한 삽입형 인터페이스는 생체 시스템의 면역 반응을 줄이기 위해 생체 친화적이며 부드러운 물질을 사용하면서도, 다양한 기능을 병합하는 방향으로 발전해 왔다. 하지만 기존의 재료와 제작 방법으로는 다양한 기능을 구현할 수 있으면서도 장기간 사용가능한 디바이스를 만들기 어려웠고, 특히 탄소 기반 전극의 경우 제조 및 병합 과정이 복잡하고 금속 전극에 비해 기능적 수행 능력이 떨어진다는 문제점이 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 탄소나노튜브 시트 전극과 고분자 광섬유를 병합했다. 탄소나노튜브 섬유가 한 방향으로 배열된 탄소나노튜브 시트 전극을 통해 신경세포 활동을 효과적으로 기록했고, 광 전달을 담당하는 고분자 광섬유에 이를 감아 머리카락 크기의 다기능 섬유를 제작했다. 연구팀은 제작된 섬유는 우수한 전기적, 광학적, 기계적 성질을 보였음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에 삽입한 결과, 전기적 신경 활성신호, 화학적 신경전달물질(도파민)을 잘 측정하고 광유전학적 조절을 통해 행동학적 산출을 이끌어낼 수 있음을 확인했다. 또한 연구팀은 1년 이상 광학적으로 발화된 신경 신호와 자발적으로 발화된 신경 신호를 측정함으로써 초장기간 사용 가능성도 보여줬다.
이번 연구 결과는 국제 학술지 `어드밴스드 머터리얼스(Advanced Materials)'에 2024년 3월 29일 字로 출판됐다. (논문명: Structurally Aligned Multifunctional neural Probe (SAMP) using forest-drawn CNT sheet onto thermally drawn polymer fiber for long-term in vivo operation)
박성준 교수는 "전기적 신경 활성신호와 더불어 화학적 신경전달물질 기록 및 광학적 조절 기능을 갖춘 초장기간 사용가능한 차세대 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 대동물 적용 및 자기공명영상 장비와 동시 사용을 통해 뇌 질환의 세부적인 메커니즘 파악과 전뇌적(Whole brain) 기록 및 조절 분야에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 과학기술정보통신부, 한국연구재단 나노및소재기술개발사업, 경찰청 미래치안도전기술개발사업의 지원을 받아 수행됐다.
2024.04.24 조회수 1931
초장기간 작동 뇌-기계 인터페이스 개발
수술이 불가피한 삽입형 신경 인터페이스의 경우, 한 번의 수술로도 최대한 많은 정보를 얻을 수 있고 장기간 사용가능한 디바이스의 개발이 필요하다. 한국 연구진이 1년 이상 사용가능한 다기능성 신경 인터페이스를 개발하여 향후 뇌 지도, 질환 연구 및 치료에 획기적인 발전을 가져올 것으로 기대한다.
우리 대학 바이오및뇌공학과 박성준 교수 연구팀과 한양대학교(총장 이기정) 바이오메디컬공학과 최창순 교수 연구팀이, 열 인발공정(Thermal Drawing Process, TDP)*과 탄소나노튜브 시트를 병합해 장기간 사용 가능한 다기능성 섬유형 신경 인터페이스를 개발했다고 24일 밝혔다.
☞ 열 인발공정 : 열을 가해 큰 구조체의 복잡한 구조체를 빠른 속도로 당겨 같은 모양 및 기능을 갖춘 섬유를 뽑아내는 일 또는 가공.
뇌신경 시스템 탐구를 위한 삽입형 인터페이스는 생체 시스템의 면역 반응을 줄이기 위해 생체 친화적이며 부드러운 물질을 사용하면서도, 다양한 기능을 병합하는 방향으로 발전해 왔다. 하지만 기존의 재료와 제작 방법으로는 다양한 기능을 구현할 수 있으면서도 장기간 사용가능한 디바이스를 만들기 어려웠고, 특히 탄소 기반 전극의 경우 제조 및 병합 과정이 복잡하고 금속 전극에 비해 기능적 수행 능력이 떨어진다는 문제점이 있었다.
연구팀은 문제 해결을 위해 이번 연구에서 탄소나노튜브 시트 전극과 고분자 광섬유를 병합했다. 탄소나노튜브 섬유가 한 방향으로 배열된 탄소나노튜브 시트 전극을 통해 신경세포 활동을 효과적으로 기록했고, 광 전달을 담당하는 고분자 광섬유에 이를 감아 머리카락 크기의 다기능 섬유를 제작했다. 연구팀은 제작된 섬유는 우수한 전기적, 광학적, 기계적 성질을 보였음을 확인했다.
해당 뇌-기계 인터페이스를 실제 쥐 모델에 삽입한 결과, 전기적 신경 활성신호, 화학적 신경전달물질(도파민)을 잘 측정하고 광유전학적 조절을 통해 행동학적 산출을 이끌어낼 수 있음을 확인했다. 또한 연구팀은 1년 이상 광학적으로 발화된 신경 신호와 자발적으로 발화된 신경 신호를 측정함으로써 초장기간 사용 가능성도 보여줬다.
이번 연구 결과는 국제 학술지 `어드밴스드 머터리얼스(Advanced Materials)'에 2024년 3월 29일 字로 출판됐다. (논문명: Structurally Aligned Multifunctional neural Probe (SAMP) using forest-drawn CNT sheet onto thermally drawn polymer fiber for long-term in vivo operation)
박성준 교수는 "전기적 신경 활성신호와 더불어 화학적 신경전달물질 기록 및 광학적 조절 기능을 갖춘 초장기간 사용가능한 차세대 신경 인터페이스의 개발 성과ˮ임을 강조하며, "향후 대동물 적용 및 자기공명영상 장비와 동시 사용을 통해 뇌 질환의 세부적인 메커니즘 파악과 전뇌적(Whole brain) 기록 및 조절 분야에 사용될 수 있을 것ˮ 이라고 말했다.
한편 이번 연구는 과학기술정보통신부, 한국연구재단 나노및소재기술개발사업, 경찰청 미래치안도전기술개발사업의 지원을 받아 수행됐다.
2024.04.24 조회수 1931 뇌인지과학과 1주년 기념 심포지엄 개최
우리 대학이 다음 달 2일부터 4일까지 총 3일간 대전 본원 의과학연구센터(E7)에서 '뇌인지과학과 국제심포지엄'을 개최한다.
이번 심포지엄은 뇌인지과학과(학과장 정재승)의 설립 1주년을 기념하는 행사로 국내 뇌인지과학 분야의 저변확대와 차세대 인력양성 등을 논의하기 위해 마련됐다. 이를 위해, 미국 UC 버클리(UC Berkeley), 뉴욕대학교(New York University, 이하 NYU), 스위스 로잔연방공과대학교(EPFL) 등 유수 대학의 세계적 석학들과 구글 딥마인드(Google DeepMind), 아이비엠 리서치(IBM Research) 등에서 활발하게 활동 중인 뇌기반 인공지능연구자 등 13명의 해외 뇌과학자·뇌공학자를 초청했다. 또한, 국내 관련 분야의 리더들과 학술교류 및 공동연구를 논의하고, 우리 대학의 비전에 부합하는 향후 50년의 미래 연구 계획을 함께 모색할 예정이다. '뇌인지 분야의 난제'를 주제로 다루는 심포지엄 첫날에는 양단(Yang Dan) 미국 캘리포니아 대학교-버클리(UC-Berkeley) 신경생물학 석좌교수와 올라프 브랑케(Olaf Blanke) 스위스 로잔연방공과대학교(EPFL) 신경보철센터 교수가 개회 기조 연사를 맡는다. 이들은 각각 '하향식 주의 및 전역 점화: 마우스의 회로 해부'와 '자의식의 신경과학'을 주제로 강연한다. 첫 번째 세션에서는 '뇌인지과학 분야에서 가장 중요한 질문은 무엇일까?'라는 질문을 바탕으로 미국 뇌과학 연구의 중심축 중 하나인 뉴욕대 신경과학 센터(NYU Center for Neural Science)를 설립한 앤소니 모비숀(J. Anthony Movshon) 뉴욕대학교 신경과학 및 생리학 교수가 기조 연설한다. '기술을 확장할 때 우리는 어떻게 이해를 확장할 수 있을까'라는 주제로 강연과 함께 뇌인지과학 분야가 향후 집중해야 하는 연구 방향성을 논의하기 위한 해외 석학들의 발표와 토론이 이어질 예정이다. '뇌와 인지과학 분야의 인재를 어떻게 교육할 것인가?'를 주제로 열리는 둘째 날 오전 세션에서는 문제일 DGIST 뇌과학과 교수, 이상훈 서울대 뇌인지과학과 교수, 조제원 이화여대 뇌인지과학부 교수, 서민아 성균관대 글로벌바이오메디컬공학과 교수 등이 참여해 인재상·교육 커리큘럼·뇌인지과학과 운영 현황·뇌과학 연구의 필요성 등에 대해 강연 및 토론한다. 또한, ‘뇌×헬스케어’와 ‘뇌×인공지능(AI)’을 다루는 세션에서는 뇌 질환 관련 현황 및 연구 동향과 인공지능 기술 개발 동향 등을 공유한다.
심포지엄 마지막 날에는 뇌인지과학 분야에서 우리 대학과 뉴욕대의 공동협력 방안이 논의된다. 신경경제학 분야를 선도하는 뉴욕대 신경경제학 센터(Centre for Neuroeconomics)를 설립한 폴 글림처(Paul Glimcher) 뉴욕대학교 신경과학 및 생리학 석좌교수는 '생명 의료 신경과학의 첨단 기술 협력'을 주제로 기조연설을 한다.
이 세션에서는 미국 뉴욕 맨해튼 소재의 KAIST-NYU 조인트 캠퍼스를 기반으로 추진할 인공지능 융합 뇌과학분야(뇌-기계 상호작용, 뇌기반 기계학습) 국제 공동연구를 위해 뉴욕대의 캐서린 하틀리(Catherine A. Hartley) 교수, 브렌든 레이크(Brenden Lake) 교수와 데이비드 멜처(David Melcher) 뉴욕대-아부다비 교수가 최근 연구성과를 공유하고 토론을 진행한다. 정재승 KAIST 뇌인지과학과 학과장은 "국내에서는 좀처럼 만나기 힘든 세계적인 석학들이 설립 1년 차 학과가 첫 번째로 개최하는 학술 심포지엄의 연사로 참여한다는 것 자체가 KAIST 뇌인지과학과를 향한 학계의 관심과 기대라고 생각한다"라고 말했다. 이어, 정 학과장은 "10년 내 교수진 50명을 보유한 아시아 최대 뇌인지과학과로 성장하는 것을 목표로 신경생물학과 인지과학, 뇌공학과 뇌의학을 두루 아우르는 뇌인지과학 연구의 교두보가 되기 위해 최선을 다하겠다"라고 전했다.한편, KAIST 뇌인지과학과는 단순히 뇌의 생물학적 구조와 인지기능을 연구하는 것을 넘어 뇌와 몸, 인간과 인간, 인간과 세계가 어떻게 상호작용하는지를 탐구하고 이를 바탕으로 공학적이고 의학적인 응용을 실현하기 위해 지난해 설립됐다. 신경과학과 인지과학의의 탄탄한 기초를 바탕으로 뇌공학과 뇌의학 분야로 연구 영역 확장을 시도하고 있으며, KAIST-NYU 조인트 캠퍼스를 통해 학부생과 대학원생, 박사후 연구원, 교수들이 뉴욕에 상주하면서 뉴욕대·콜롬비아대·코넬대·록펠러대 등 유수의 대학들과 공동연구를 수행할 수 있는 세계적 연구 및 교육 협업 시스템을 갖추고 있다.이번 행사는 국제심포지엄의 특성상 일부 세션이 영어로 진행되며, 뇌인지과학 분야에 관심 있는 사람이라면 누구나 무료로 참관할 수 있다.
2023.10.27 조회수 2998
뇌인지과학과 1주년 기념 심포지엄 개최
우리 대학이 다음 달 2일부터 4일까지 총 3일간 대전 본원 의과학연구센터(E7)에서 '뇌인지과학과 국제심포지엄'을 개최한다.
이번 심포지엄은 뇌인지과학과(학과장 정재승)의 설립 1주년을 기념하는 행사로 국내 뇌인지과학 분야의 저변확대와 차세대 인력양성 등을 논의하기 위해 마련됐다. 이를 위해, 미국 UC 버클리(UC Berkeley), 뉴욕대학교(New York University, 이하 NYU), 스위스 로잔연방공과대학교(EPFL) 등 유수 대학의 세계적 석학들과 구글 딥마인드(Google DeepMind), 아이비엠 리서치(IBM Research) 등에서 활발하게 활동 중인 뇌기반 인공지능연구자 등 13명의 해외 뇌과학자·뇌공학자를 초청했다. 또한, 국내 관련 분야의 리더들과 학술교류 및 공동연구를 논의하고, 우리 대학의 비전에 부합하는 향후 50년의 미래 연구 계획을 함께 모색할 예정이다. '뇌인지 분야의 난제'를 주제로 다루는 심포지엄 첫날에는 양단(Yang Dan) 미국 캘리포니아 대학교-버클리(UC-Berkeley) 신경생물학 석좌교수와 올라프 브랑케(Olaf Blanke) 스위스 로잔연방공과대학교(EPFL) 신경보철센터 교수가 개회 기조 연사를 맡는다. 이들은 각각 '하향식 주의 및 전역 점화: 마우스의 회로 해부'와 '자의식의 신경과학'을 주제로 강연한다. 첫 번째 세션에서는 '뇌인지과학 분야에서 가장 중요한 질문은 무엇일까?'라는 질문을 바탕으로 미국 뇌과학 연구의 중심축 중 하나인 뉴욕대 신경과학 센터(NYU Center for Neural Science)를 설립한 앤소니 모비숀(J. Anthony Movshon) 뉴욕대학교 신경과학 및 생리학 교수가 기조 연설한다. '기술을 확장할 때 우리는 어떻게 이해를 확장할 수 있을까'라는 주제로 강연과 함께 뇌인지과학 분야가 향후 집중해야 하는 연구 방향성을 논의하기 위한 해외 석학들의 발표와 토론이 이어질 예정이다. '뇌와 인지과학 분야의 인재를 어떻게 교육할 것인가?'를 주제로 열리는 둘째 날 오전 세션에서는 문제일 DGIST 뇌과학과 교수, 이상훈 서울대 뇌인지과학과 교수, 조제원 이화여대 뇌인지과학부 교수, 서민아 성균관대 글로벌바이오메디컬공학과 교수 등이 참여해 인재상·교육 커리큘럼·뇌인지과학과 운영 현황·뇌과학 연구의 필요성 등에 대해 강연 및 토론한다. 또한, ‘뇌×헬스케어’와 ‘뇌×인공지능(AI)’을 다루는 세션에서는 뇌 질환 관련 현황 및 연구 동향과 인공지능 기술 개발 동향 등을 공유한다.
심포지엄 마지막 날에는 뇌인지과학 분야에서 우리 대학과 뉴욕대의 공동협력 방안이 논의된다. 신경경제학 분야를 선도하는 뉴욕대 신경경제학 센터(Centre for Neuroeconomics)를 설립한 폴 글림처(Paul Glimcher) 뉴욕대학교 신경과학 및 생리학 석좌교수는 '생명 의료 신경과학의 첨단 기술 협력'을 주제로 기조연설을 한다.
이 세션에서는 미국 뉴욕 맨해튼 소재의 KAIST-NYU 조인트 캠퍼스를 기반으로 추진할 인공지능 융합 뇌과학분야(뇌-기계 상호작용, 뇌기반 기계학습) 국제 공동연구를 위해 뉴욕대의 캐서린 하틀리(Catherine A. Hartley) 교수, 브렌든 레이크(Brenden Lake) 교수와 데이비드 멜처(David Melcher) 뉴욕대-아부다비 교수가 최근 연구성과를 공유하고 토론을 진행한다. 정재승 KAIST 뇌인지과학과 학과장은 "국내에서는 좀처럼 만나기 힘든 세계적인 석학들이 설립 1년 차 학과가 첫 번째로 개최하는 학술 심포지엄의 연사로 참여한다는 것 자체가 KAIST 뇌인지과학과를 향한 학계의 관심과 기대라고 생각한다"라고 말했다. 이어, 정 학과장은 "10년 내 교수진 50명을 보유한 아시아 최대 뇌인지과학과로 성장하는 것을 목표로 신경생물학과 인지과학, 뇌공학과 뇌의학을 두루 아우르는 뇌인지과학 연구의 교두보가 되기 위해 최선을 다하겠다"라고 전했다.한편, KAIST 뇌인지과학과는 단순히 뇌의 생물학적 구조와 인지기능을 연구하는 것을 넘어 뇌와 몸, 인간과 인간, 인간과 세계가 어떻게 상호작용하는지를 탐구하고 이를 바탕으로 공학적이고 의학적인 응용을 실현하기 위해 지난해 설립됐다. 신경과학과 인지과학의의 탄탄한 기초를 바탕으로 뇌공학과 뇌의학 분야로 연구 영역 확장을 시도하고 있으며, KAIST-NYU 조인트 캠퍼스를 통해 학부생과 대학원생, 박사후 연구원, 교수들이 뉴욕에 상주하면서 뉴욕대·콜롬비아대·코넬대·록펠러대 등 유수의 대학들과 공동연구를 수행할 수 있는 세계적 연구 및 교육 협업 시스템을 갖추고 있다.이번 행사는 국제심포지엄의 특성상 일부 세션이 영어로 진행되며, 뇌인지과학 분야에 관심 있는 사람이라면 누구나 무료로 참관할 수 있다.
2023.10.27 조회수 2998 식품의약품안전처와 연구협력 MOU 체결
우리 대학은 16일 오후 식품의약품안전처(처장 오유경)와 식품·의약품·마약류 등 분야에서 연구를 포함한 포괄적인 협력을 강화하는 MOU를 체결했다.
이번 협약을 바탕으로 두 기관은 ▴식품·의약품·마약류 등 분야의 공동연구 발굴·추진 ▴국가연구개발사업 상호협력 및 공동연구 추진 ▴양 기관 교육프로그램 연계·공유 ▴국내외 최신 식·의약 연구 정보·동향 공유 등에 적극적으로 협력할 예정이다.
특히, 'KAIST-원진 세포치료센터(센터장, 김대수)'를 주축으로 뇌 오가노이드(인공장기) 기술을 개발해 약물중독 및 금단증상, 재활에 관해 연구하고 국제적인 표준을 마련할 계획이다.
날로 증가하는 신종 마약의 위협을 신속하게 진단하고 대응하기 위해 우리 대학의 인공지능 기술을 활용해 마약류가 뇌와 행동에 미치는 영향을 초고속으로 정밀 진단할 수 있는 시스템 개발도 진행한다.
이와 함께, mRNA 백신·치료제 기술·플랫폼 개발 등 식품 및 의료 관련 신물질과 제품 안전성에 대한 첨단 평가기술 개발 분야에서도 폭넓게 협력할 예정이다.
오유경 식약처장은 "이번 업무협약을 계기로 식약처와 KAIST가 함께 연구를 수행하게 되어 국민 안전이 한층 더 강화될 수 있을 것으로 기대한다"며 "식약처는 앞으로도 과학적 근거에 기반하여 식품, 의료제품의 안전을 더욱 철저히 관리하겠다"고 말했다.이광형 총장은 "이번 협약이 식약처와 KAIST의 유기적인 협력관계 구축으로 이어져 양 기관이 상호 발전하는 계기가 되길 바란다"며 "앞으로 KAIST의 첨단과학 연구 역량을 바탕으로 식약처와 공동연구를 수행하여 규제과학 전문성을 높이기 위해 지속해서 노력하겠다"고 밝혔다.
2023.10.17 조회수 1846
식품의약품안전처와 연구협력 MOU 체결
우리 대학은 16일 오후 식품의약품안전처(처장 오유경)와 식품·의약품·마약류 등 분야에서 연구를 포함한 포괄적인 협력을 강화하는 MOU를 체결했다.
이번 협약을 바탕으로 두 기관은 ▴식품·의약품·마약류 등 분야의 공동연구 발굴·추진 ▴국가연구개발사업 상호협력 및 공동연구 추진 ▴양 기관 교육프로그램 연계·공유 ▴국내외 최신 식·의약 연구 정보·동향 공유 등에 적극적으로 협력할 예정이다.
특히, 'KAIST-원진 세포치료센터(센터장, 김대수)'를 주축으로 뇌 오가노이드(인공장기) 기술을 개발해 약물중독 및 금단증상, 재활에 관해 연구하고 국제적인 표준을 마련할 계획이다.
날로 증가하는 신종 마약의 위협을 신속하게 진단하고 대응하기 위해 우리 대학의 인공지능 기술을 활용해 마약류가 뇌와 행동에 미치는 영향을 초고속으로 정밀 진단할 수 있는 시스템 개발도 진행한다.
이와 함께, mRNA 백신·치료제 기술·플랫폼 개발 등 식품 및 의료 관련 신물질과 제품 안전성에 대한 첨단 평가기술 개발 분야에서도 폭넓게 협력할 예정이다.
오유경 식약처장은 "이번 업무협약을 계기로 식약처와 KAIST가 함께 연구를 수행하게 되어 국민 안전이 한층 더 강화될 수 있을 것으로 기대한다"며 "식약처는 앞으로도 과학적 근거에 기반하여 식품, 의료제품의 안전을 더욱 철저히 관리하겠다"고 말했다.이광형 총장은 "이번 협약이 식약처와 KAIST의 유기적인 협력관계 구축으로 이어져 양 기관이 상호 발전하는 계기가 되길 바란다"며 "앞으로 KAIST의 첨단과학 연구 역량을 바탕으로 식약처와 공동연구를 수행하여 규제과학 전문성을 높이기 위해 지속해서 노력하겠다"고 밝혔다.
2023.10.17 조회수 1846 뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 2531
뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 2531 아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
2023.08.01 조회수 3151
아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
2023.08.01 조회수 3151 150% 쭉쭉 늘어나는 전자 섬유 개발
전자 섬유는 최근 각광받고 있는 사용자 친화 웨어러블 소자, 헬스케어 소자, 최소 침습형 임플란터블 전자소자에 핵심 요소로 여겨져 활발하게 연구가 진행되고 있다. 하지만 고체 금속 전도체 필러(Conductive filler)를 사용한 전자 섬유를 늘려서 사용하려 할 경우, 전기전도성이 급격하게 감소해 전기적 성질이 망가진다는 단점이 있다.
우리 대학 신소재공학과 스티브 박, 전기및전자공학부 정재웅, 바이오및뇌공학과 박성준 교수 공동 연구팀이 높은 전도도와 내구성을 가지는 액체금속 복합체를 이용해 신축성이 우수한 전자 섬유를 개발했다고 25일 밝혔다.
전자 섬유의 늘어나지 않는 단점을 해결하기 위해 연구팀은 고체처럼 형상이 고정된 것이 아닌 기계적 변형에 맞춰 형태가 변형될 수 있는 액체금속 입자 기반의 전도체 필러를 제시했다. 액체금속 마이크로 입자는 인장이 가해질 경우에 그 형태가 타원형으로 늘어나면서 전기 저항 변화를 최소화할 수 있다. 하지만 그 크기가 수 마이크로미터이기 때문에, 기존에 이용된 딥-코팅(dip-coating)과 같은 단순한 방법으로 실에 코팅하는 것이 불가능하다. 연구진은 액체금속 입자가 높은 밀도로 실 위에 전달될 수 있고, 블레이드와 기판 사이에서 현탁액의 조성을 실시간으로 바꾸면서 화학적 변성을 통해 액체금속 입자를 실과 접착시킬 수 있는 새로운 방법인 현탁액 전단(suspension shearing) 방법을 통해 이를 해결했다. 추가로 기계적 안정성이 우수한 탄소나노튜브(CNT)가 포함된 액체금속 입자를 한층 더 코팅하는 방식으로, 액체금속 복합체의 기계적 안정성도 확보할 수 있었다.
제작된 신축성 전자 섬유는 추가적인 공정이 필요 없이 우수한 초기전도성을 보였고(2.2x10^6 S/m), 기존의 고체 금속 전도체 기반 섬유들과는 다르게 150% 늘려도 전기저항 변화가 거의 없다. 기계적 안정성도 우수해 반복되는 변형 실험에도 전기적 성질을 유지할 수 있었고, 다양한 전자 부품들과 쉽게 통합될 수 있다. 연구팀은 이를 이용해 실제 상용화된 옷에 다양한 전자회로를 구현했다.
나아가서 연구팀은 액체금속 복합체를 코팅하는 방법이 다양한 실에 호환 가능하고, 재료의 생친화성이 우수하기 때문에, 이를 이용해 신경과학 연구에 사용할 수 있는 섬유형 바이오 전자 섬유를 구현했다. 연구팀은 제안된 코팅 방법을 이용해 기계적 변형에 영향을 받지 않는 뇌 활동 전극, 신경 자극 전극, 다기능성 옵토지네틱 프로브를 제작해 넓은 범용성과 높은 공정 신뢰성을 갖는다는 것을 보였다.
우리 대학 이건희 박사, 이도훈 박사과정, 전우진 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 온라인 판에 7월 13일자 출판됐다. (논문명: Conductance stable and mechanically durable bi-layer EGaIn composite-coated stretchable fiber for 1D bioelectronics)
스티브박 교수는 "옷에 다양한 전자 공학적인 기능을 웨어러블 형태로 구현하는 가능성을 보여준 연구로 최근에 각광받고 있는 환자 편의성을 높인 웨어러블 헬스케어 소자나 최소침습형 임플란터블 전자소자 개발의 새로운 방향성을 제시한 의미있는 결과ˮ 라고 말했다.
한편 이번 연구는 한국연구재단, KAIST의 지원을 받아 수행됐다. 이건희 박사는 포스코청압재단의 지원을 받고 있다.
2023.07.25 조회수 4117
150% 쭉쭉 늘어나는 전자 섬유 개발
전자 섬유는 최근 각광받고 있는 사용자 친화 웨어러블 소자, 헬스케어 소자, 최소 침습형 임플란터블 전자소자에 핵심 요소로 여겨져 활발하게 연구가 진행되고 있다. 하지만 고체 금속 전도체 필러(Conductive filler)를 사용한 전자 섬유를 늘려서 사용하려 할 경우, 전기전도성이 급격하게 감소해 전기적 성질이 망가진다는 단점이 있다.
우리 대학 신소재공학과 스티브 박, 전기및전자공학부 정재웅, 바이오및뇌공학과 박성준 교수 공동 연구팀이 높은 전도도와 내구성을 가지는 액체금속 복합체를 이용해 신축성이 우수한 전자 섬유를 개발했다고 25일 밝혔다.
전자 섬유의 늘어나지 않는 단점을 해결하기 위해 연구팀은 고체처럼 형상이 고정된 것이 아닌 기계적 변형에 맞춰 형태가 변형될 수 있는 액체금속 입자 기반의 전도체 필러를 제시했다. 액체금속 마이크로 입자는 인장이 가해질 경우에 그 형태가 타원형으로 늘어나면서 전기 저항 변화를 최소화할 수 있다. 하지만 그 크기가 수 마이크로미터이기 때문에, 기존에 이용된 딥-코팅(dip-coating)과 같은 단순한 방법으로 실에 코팅하는 것이 불가능하다. 연구진은 액체금속 입자가 높은 밀도로 실 위에 전달될 수 있고, 블레이드와 기판 사이에서 현탁액의 조성을 실시간으로 바꾸면서 화학적 변성을 통해 액체금속 입자를 실과 접착시킬 수 있는 새로운 방법인 현탁액 전단(suspension shearing) 방법을 통해 이를 해결했다. 추가로 기계적 안정성이 우수한 탄소나노튜브(CNT)가 포함된 액체금속 입자를 한층 더 코팅하는 방식으로, 액체금속 복합체의 기계적 안정성도 확보할 수 있었다.
제작된 신축성 전자 섬유는 추가적인 공정이 필요 없이 우수한 초기전도성을 보였고(2.2x10^6 S/m), 기존의 고체 금속 전도체 기반 섬유들과는 다르게 150% 늘려도 전기저항 변화가 거의 없다. 기계적 안정성도 우수해 반복되는 변형 실험에도 전기적 성질을 유지할 수 있었고, 다양한 전자 부품들과 쉽게 통합될 수 있다. 연구팀은 이를 이용해 실제 상용화된 옷에 다양한 전자회로를 구현했다.
나아가서 연구팀은 액체금속 복합체를 코팅하는 방법이 다양한 실에 호환 가능하고, 재료의 생친화성이 우수하기 때문에, 이를 이용해 신경과학 연구에 사용할 수 있는 섬유형 바이오 전자 섬유를 구현했다. 연구팀은 제안된 코팅 방법을 이용해 기계적 변형에 영향을 받지 않는 뇌 활동 전극, 신경 자극 전극, 다기능성 옵토지네틱 프로브를 제작해 넓은 범용성과 높은 공정 신뢰성을 갖는다는 것을 보였다.
우리 대학 이건희 박사, 이도훈 박사과정, 전우진 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 온라인 판에 7월 13일자 출판됐다. (논문명: Conductance stable and mechanically durable bi-layer EGaIn composite-coated stretchable fiber for 1D bioelectronics)
스티브박 교수는 "옷에 다양한 전자 공학적인 기능을 웨어러블 형태로 구현하는 가능성을 보여준 연구로 최근에 각광받고 있는 환자 편의성을 높인 웨어러블 헬스케어 소자나 최소침습형 임플란터블 전자소자 개발의 새로운 방향성을 제시한 의미있는 결과ˮ 라고 말했다.
한편 이번 연구는 한국연구재단, KAIST의 지원을 받아 수행됐다. 이건희 박사는 포스코청압재단의 지원을 받고 있다.
2023.07.25 조회수 4117 고규영 특훈교수, 올해 대한민국최고과학기술인상 수상
과학기술정보통신부와 한국과학기술단체총연합회는 올해 대한민국최고과학기술인상 수상자로 고규영 우리 대학 의과학대학원 특훈교수를 선정했다고 2일 밝혔다.
고 교수는 치매 등 퇴행성 뇌 질환을 유발하는 뇌 속 노폐물이 뇌 밖으로 배출되는 주요 경로가 뇌 하부에 있는 뇌막 림프관임을 세계 최초로 규명하고 나이가 들수록 이 뇌막 림프관의 기능이 저하돼 노폐물 배출 능력이 떨어짐을 확인했다. 이전에는 뇌척수액에 녹아든 노폐물과 독성이 뇌 밖으로 배출되는 경로가 베일에 싸여 있었다.
이 연구 결과는 퇴행성 뇌 질환의 예방과 치료에 있어 새로운 방향을 제시했다는 평가를 받으며 최고 권위의 국제 학술지 '네이처'와 '사이언스' 등에 게재돼 자주 인용되고 있다.
고 교수는 연구 중심 의사과학자로서 전북대 의대에서 학사, 동 대학원에서 석사와 박사 학위를 받았다. 이후 포항공대 생명과학과 부교수 등을 거쳐 현재 KAIST 의과학대학원 특훈교수와 IBS 혈관연구단장을 지내고 있다.
고 교수는 지난달 30일 정부서울청사에서 진행된 브리핑에서 "수상해 매우 기쁘다"며 "계속 연구를 진행해 뇌 림프관을 통해 노폐물이나 독성 물질이 원활하게 빠져나갈 수 있게 하는 방법을 찾아내 언젠가는 치매 예방과 치료에 크게 기여할 것"이라고 포부를 밝혔다.
또 그는 지금까지 성과를 바탕으로 현재 영장류에 대한 실험을 진행하고 있다며 확증되면 환자를 대상으로도 연구하고 싶다고 말했다.
과기정통부는 고 교수가 이 밖에도 림프관 경유 암세포가 림프절로 전이하기 위해 지방산을 핵심 연료로 활용한다는 사실과 녹내장의 발생 원인 등을 규명하는 등 선도적인 성과를 도출했다고 밝혔다.
또 현재까지 35명의 박사와 3명의 석사를 배출하는 등 인재 양성에도 이바지하고 있다고 덧붙였다.
한편 그는 브리핑에서 국내 의사과학자의 필요성에 대해서도 입을 열었다. 그는 "국내 의사 13만명 중 성형이나 미용 분야에 3만명이 있는데 그것도 필요한 부분이지만 국가 발전이나 미래를 위해서 연구해야 한다"며 "의대·치의대·한의대에 4천명이 있는 것으로 아는데 1%인 40명만 중계 연구나 기초 연구를 하면 블록버스터 약도 만드는 리더가 될거라 본다"고 말했다.
이어 그는 "KAIST에서 1년에 의사과학자를 30명씩 배출해도 이들이 다시 병원으로 돌아가 교수가 된다"며 "연구할 수 있도록 분위기를 만들어주고 병원이나 부처에서 지원해야 한다"고 강조했다.
대한민국최고과학기술인상은 2003년부터 우리나라를 대표할 수 있는 탁월한 연구성과를 이룬 과학기술인에 부여되고 있다. 올해에는 후보자 총 23명을 대상으로 세 단계의 심사 과정을 거쳐 수상자를 선정했다.
과기정통부는 오는 5일 서울 강남구 한국과학기술회관에서 열리는 '제1회 세계 한인과학기술인대회' 개회식에서 고 교수에게 대통령 상장과 상금 3억 원을 수여할 계획이다.
2023.07.03 조회수 2993
고규영 특훈교수, 올해 대한민국최고과학기술인상 수상
과학기술정보통신부와 한국과학기술단체총연합회는 올해 대한민국최고과학기술인상 수상자로 고규영 우리 대학 의과학대학원 특훈교수를 선정했다고 2일 밝혔다.
고 교수는 치매 등 퇴행성 뇌 질환을 유발하는 뇌 속 노폐물이 뇌 밖으로 배출되는 주요 경로가 뇌 하부에 있는 뇌막 림프관임을 세계 최초로 규명하고 나이가 들수록 이 뇌막 림프관의 기능이 저하돼 노폐물 배출 능력이 떨어짐을 확인했다. 이전에는 뇌척수액에 녹아든 노폐물과 독성이 뇌 밖으로 배출되는 경로가 베일에 싸여 있었다.
이 연구 결과는 퇴행성 뇌 질환의 예방과 치료에 있어 새로운 방향을 제시했다는 평가를 받으며 최고 권위의 국제 학술지 '네이처'와 '사이언스' 등에 게재돼 자주 인용되고 있다.
고 교수는 연구 중심 의사과학자로서 전북대 의대에서 학사, 동 대학원에서 석사와 박사 학위를 받았다. 이후 포항공대 생명과학과 부교수 등을 거쳐 현재 KAIST 의과학대학원 특훈교수와 IBS 혈관연구단장을 지내고 있다.
고 교수는 지난달 30일 정부서울청사에서 진행된 브리핑에서 "수상해 매우 기쁘다"며 "계속 연구를 진행해 뇌 림프관을 통해 노폐물이나 독성 물질이 원활하게 빠져나갈 수 있게 하는 방법을 찾아내 언젠가는 치매 예방과 치료에 크게 기여할 것"이라고 포부를 밝혔다.
또 그는 지금까지 성과를 바탕으로 현재 영장류에 대한 실험을 진행하고 있다며 확증되면 환자를 대상으로도 연구하고 싶다고 말했다.
과기정통부는 고 교수가 이 밖에도 림프관 경유 암세포가 림프절로 전이하기 위해 지방산을 핵심 연료로 활용한다는 사실과 녹내장의 발생 원인 등을 규명하는 등 선도적인 성과를 도출했다고 밝혔다.
또 현재까지 35명의 박사와 3명의 석사를 배출하는 등 인재 양성에도 이바지하고 있다고 덧붙였다.
한편 그는 브리핑에서 국내 의사과학자의 필요성에 대해서도 입을 열었다. 그는 "국내 의사 13만명 중 성형이나 미용 분야에 3만명이 있는데 그것도 필요한 부분이지만 국가 발전이나 미래를 위해서 연구해야 한다"며 "의대·치의대·한의대에 4천명이 있는 것으로 아는데 1%인 40명만 중계 연구나 기초 연구를 하면 블록버스터 약도 만드는 리더가 될거라 본다"고 말했다.
이어 그는 "KAIST에서 1년에 의사과학자를 30명씩 배출해도 이들이 다시 병원으로 돌아가 교수가 된다"며 "연구할 수 있도록 분위기를 만들어주고 병원이나 부처에서 지원해야 한다"고 강조했다.
대한민국최고과학기술인상은 2003년부터 우리나라를 대표할 수 있는 탁월한 연구성과를 이룬 과학기술인에 부여되고 있다. 올해에는 후보자 총 23명을 대상으로 세 단계의 심사 과정을 거쳐 수상자를 선정했다.
과기정통부는 오는 5일 서울 강남구 한국과학기술회관에서 열리는 '제1회 세계 한인과학기술인대회' 개회식에서 고 교수에게 대통령 상장과 상금 3억 원을 수여할 계획이다.
2023.07.03 조회수 2993 염증없이 체내·외 측정 가능한 전자 신소재 개발
생체전자 의료기기는 체내에서 발생하는 신호를 읽어 생물학적 활동을 감지하거나, 조직을 자극해 질병 등을 치료하는 데 사용된다. 하지만 의료기기에 사용되는 전극 물질은 딱딱한 물성을 가지고 있어 체내에 염증반응을 일으키고 조직에 다량의 손상으로 이어질 수 있다. 따라서 조직과 같이 부드러운 성질을 가지면서도 전도성을 띠는 하이드로겔과 같은 연성 물질에 생체적합성이 높은 전도성 고분자를 체내 전극으로 사용하는 연구들이 활발하게 진행되고 있다.
우리 대학 신소재공학과 강지형 교수와 바이오및뇌공학과 박성준 교수 공동연구팀이 기존에 없었던 고전도성, 유사 조직 접착성 하이드로겔이란 신소재를 개발해 고성능 생체전자 기기를 구현했다고 4일 밝혔다.
대부분 전기 전도도가 높을수록 전도성 도메인들의 결정성이 높아지는 원리에 의해, 전도성이 높은 하이드로겔은 딱딱해지고, 부드러운 하이드로겔은 전도성이 낮을 수밖에 없다는 한계를 가진다. 이에 따라 전도성 고분자를 사용하는 하이드로겔 중, 전기 전도도가 높으면서도(10 S/cm 이상) 부드러운 물성(100 kPa 이하)을 가진 하이드로겔은 지금까지 보고된 바 없었다.
강지형 교수 연구팀은 기존에 없었던 고전도성, 유사 조직 물성 하이드로겔을 개발했다. 이 하이드로겔은 보고된 전도성 고분자 하이드로겔 중 가장 높은 전기 전도도(247 S/cm)를 띄며, 조직과 비슷한 물성(탄성율 = 60 kPa, 파괴변형률 = 410%)을 갖는다. 또한, 본 재료는 지속적인 움직임과 팽창, 수축이 있는 심장, 위와 같은 조직에서 안정적으로 기기가 작동하기 위해 필수조건인 조직에 쉽게 접착되는 장점을 가지고 있다.
공동연구팀은 원하는 생체 조직에 맞게 조정하고 그 형태에 맞추는 주형의 그물 구조에 따라 높은 질서도를 가지는 고분자 주형 네트워크를 도입했다.
따라서 주형에 맞추어 형성된 그물 네트워크는 기존 네트워크 대비 100배 이상 높은 전기 전도도를 보이며, 동시에 주형 고분자의 부드러운 특성 때문에 조직과 비슷한 물성을 지니게 된다. 변형에도 저항이 바뀌지 않아 생체전극으로서 최적의 성능을 갖는다.
또한 연구팀은 개발한 하이드로겔을 전극을 기반으로 한 높은 전기 전도도를 가진 다양한 고성능 생체전자 기기를 제작, 그 기능성을 검증했다. 높은 전기 전도도를 가진 특성으로 좌골신경 자극을 대상으로 하는 디바이스의 경우, 매우 낮은 전압(40 mV)에서 다리 근육의 움직임을 성공적으로 유도할 수 있었다. 또한 심전도 측정(ECG)을 위한 디바이스의 경우에도 매우 높은 신호 대 잡음 비(61 dB)로 신호를 측정하는 데 성공함으로써, 초고품질 생체 신호 측정을 위한 연성 기기 개발 가능성을 입증하였다.
이번 연구를 주도한 강지형 교수는 "이번 연구는 고전도성을 갖고 생체조직과 유사한 기계적 물성을 갖는 하이드로겔 개발을 위한 합성 방향을 새롭게 제시했다는 점에서 의미가 있다고 하면서, "이번에 개발된 전도성 하이드로겔은 급속도로 성장하고 있는 전자약 시장에 게임 체인저가 될 것으로 기대된다고 말했다.
우리 대학 신소재공학과 정주은 박사과정과 바이오및뇌공학과 성창훈 박사과정이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 4월 18일 게재됐다. (논문명: Highly conductive tissue-like hydrogel interface through template-directed assembly)
한편 이번 연구는 한국연구재단의 나노소재기술개발 미래기술연구실 사업을 받아 수행됐다.
2023.05.04 조회수 4480
염증없이 체내·외 측정 가능한 전자 신소재 개발
생체전자 의료기기는 체내에서 발생하는 신호를 읽어 생물학적 활동을 감지하거나, 조직을 자극해 질병 등을 치료하는 데 사용된다. 하지만 의료기기에 사용되는 전극 물질은 딱딱한 물성을 가지고 있어 체내에 염증반응을 일으키고 조직에 다량의 손상으로 이어질 수 있다. 따라서 조직과 같이 부드러운 성질을 가지면서도 전도성을 띠는 하이드로겔과 같은 연성 물질에 생체적합성이 높은 전도성 고분자를 체내 전극으로 사용하는 연구들이 활발하게 진행되고 있다.
우리 대학 신소재공학과 강지형 교수와 바이오및뇌공학과 박성준 교수 공동연구팀이 기존에 없었던 고전도성, 유사 조직 접착성 하이드로겔이란 신소재를 개발해 고성능 생체전자 기기를 구현했다고 4일 밝혔다.
대부분 전기 전도도가 높을수록 전도성 도메인들의 결정성이 높아지는 원리에 의해, 전도성이 높은 하이드로겔은 딱딱해지고, 부드러운 하이드로겔은 전도성이 낮을 수밖에 없다는 한계를 가진다. 이에 따라 전도성 고분자를 사용하는 하이드로겔 중, 전기 전도도가 높으면서도(10 S/cm 이상) 부드러운 물성(100 kPa 이하)을 가진 하이드로겔은 지금까지 보고된 바 없었다.
강지형 교수 연구팀은 기존에 없었던 고전도성, 유사 조직 물성 하이드로겔을 개발했다. 이 하이드로겔은 보고된 전도성 고분자 하이드로겔 중 가장 높은 전기 전도도(247 S/cm)를 띄며, 조직과 비슷한 물성(탄성율 = 60 kPa, 파괴변형률 = 410%)을 갖는다. 또한, 본 재료는 지속적인 움직임과 팽창, 수축이 있는 심장, 위와 같은 조직에서 안정적으로 기기가 작동하기 위해 필수조건인 조직에 쉽게 접착되는 장점을 가지고 있다.
공동연구팀은 원하는 생체 조직에 맞게 조정하고 그 형태에 맞추는 주형의 그물 구조에 따라 높은 질서도를 가지는 고분자 주형 네트워크를 도입했다.
따라서 주형에 맞추어 형성된 그물 네트워크는 기존 네트워크 대비 100배 이상 높은 전기 전도도를 보이며, 동시에 주형 고분자의 부드러운 특성 때문에 조직과 비슷한 물성을 지니게 된다. 변형에도 저항이 바뀌지 않아 생체전극으로서 최적의 성능을 갖는다.
또한 연구팀은 개발한 하이드로겔을 전극을 기반으로 한 높은 전기 전도도를 가진 다양한 고성능 생체전자 기기를 제작, 그 기능성을 검증했다. 높은 전기 전도도를 가진 특성으로 좌골신경 자극을 대상으로 하는 디바이스의 경우, 매우 낮은 전압(40 mV)에서 다리 근육의 움직임을 성공적으로 유도할 수 있었다. 또한 심전도 측정(ECG)을 위한 디바이스의 경우에도 매우 높은 신호 대 잡음 비(61 dB)로 신호를 측정하는 데 성공함으로써, 초고품질 생체 신호 측정을 위한 연성 기기 개발 가능성을 입증하였다.
이번 연구를 주도한 강지형 교수는 "이번 연구는 고전도성을 갖고 생체조직과 유사한 기계적 물성을 갖는 하이드로겔 개발을 위한 합성 방향을 새롭게 제시했다는 점에서 의미가 있다고 하면서, "이번에 개발된 전도성 하이드로겔은 급속도로 성장하고 있는 전자약 시장에 게임 체인저가 될 것으로 기대된다고 말했다.
우리 대학 신소재공학과 정주은 박사과정과 바이오및뇌공학과 성창훈 박사과정이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 4월 18일 게재됐다. (논문명: Highly conductive tissue-like hydrogel interface through template-directed assembly)
한편 이번 연구는 한국연구재단의 나노소재기술개발 미래기술연구실 사업을 받아 수행됐다.
2023.05.04 조회수 4480 노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15 조회수 3592
노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15 조회수 3592