연구

< 사진 1. 생명과학과 김윤기 교수 >
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
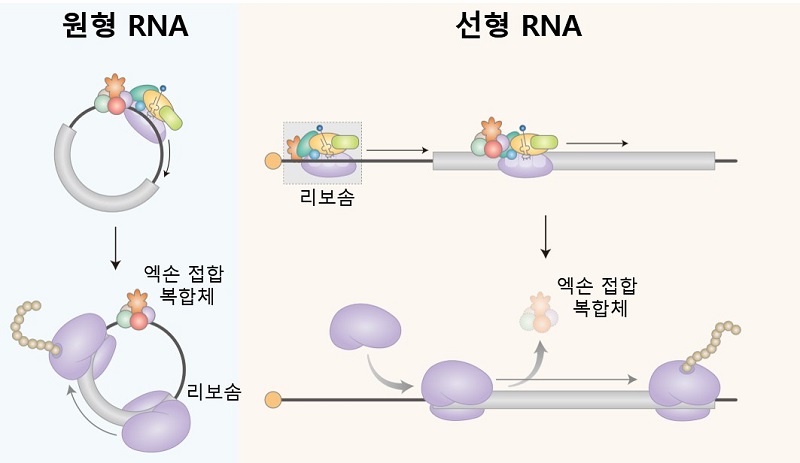
< 그림 1. 원형 RNA의 경우, 엑손 접합 복합체(EJC)가 원형 RNA에 결합하고, eIF3 복합체와 리보좀을 끌어옴으로써 원형 RNA의 단백질 합성을 유도한다. 반면에 선형 mRNA의 경우, 엑손 접합 복합체가 안정하게 선형 mRNA에 결합하지 못하기 때문에, 엑손 접합 복합체를 통한 단백질 합성은 매우 비효율적으로 일어나게 된다. >
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
-
연구 생성형 AI로 혁신적 신약 개발 가능성 열어
최근 자연어나 이미지, 동영상, 음악 등 다양한 분야에서 주목받는 생성형 AI가 신약 설계 분야에서도 기존 신규성 문제를 극복하고 새로운 혁신을 일으키고 있다고 하는데 어떤 기술일까? 우리 대학 화학과 김우연 교수 연구팀이 단백질-분자 사이의 상호작용을 고려해 활성 데이터 없이도 타겟 단백질에 적합한 약물 설계 생성형 AI를 개발했다고 18일 밝혔다. 신규 약물을 발굴하기 위해서는 질병의 원인이 되는 타겟 단백질에 특이적으로 결합하는 분자를 찾는 것이 중요하다. 기존의 약물 설계 생성형 AI는 특정 단백질의 이미 알려진 활성 데이터를 학습에 활용하기 때문에 기존 약물과 유사한 약물을 설계하려는 경향이 있다. 이는 신규성이 중요한 신약 개발 분야에서 치명적인 약점으로 지적되어 왔다. 또한 사업성이 높은 계열 내 최초(First-in-class) 타겟 단백질에 대해서는 실험 데이터가 매우 적거나 전무한데, 이 경우 기존 방식의 생성형 AI를 활용하는 것이 불가능하다. 연구팀
2024-04-18 -
인물 2024 독일 iF 디자인 어워드 5개 상 수상
우리 대학 산업디자인학과 디자인팀이 세계 3대 디자인 어워드 중 하나인 ‘독일 2024 iF 디자인 어워드(International Forum Design Awards)'에서 총 5개의 본상을 수상했다고 5일 밝혔다. iF 디자인 어워드는 독일의 레드닷 어워드, 미국의 IDEA와 함께 세계에서 가장 권위있는 디자인상 중 하나다. 제품 · 패키지 · 커뮤니케이션 · 서비스디자인 · 사용자 경험(UX) · 사용자 인터페이스 (UI ) · 콘셉트 · 인테리어 · 건축 등 총 9개 부문에서 디자인 차별성과 영향력 등을 종합적으로 평가해 혁신적이고 우수한 디자인을 선정하고 매년 상을 수여한다. 대학에서 구성된 디자인팀이 일반 기업 경쟁 부문에 참가해 다수의 상을 받는 것은 국제적으로 매우 드문 사례로, KAIST 산업디자인학과는 2022년 8개, 2023년 7개의 수상 성
2024-04-05 -
연구 화합물 생성AI 기술로 신약 개발 앞당긴다
신약 개발이나 재료과학과 같은 분야에서는 원하는 화학 특성 조건을 갖춘 물질을 발굴하는 것이 중요한 도전으로 부상하고 있다. 우리 대학 연구팀은 화학반응 예측이나 독성 예측, 그리고 화합물 구조 설계 등 다양한 문제를 동시에 풀면서 기존의 인공지능 기술을 뛰어넘는 성능을 보이는 기술을 개발했다. 김재철AI대학원 예종철 교수 연구팀이 분자 데이터에 다중 모달리티 학습(multi-modal learning) 기술을 도입해, 분자 구조와 그 생화학적 특성을 동시에 생성하고 예측이 가능해 다양한 화학적 과제에 광범위하게 활용가능한 인공지능 기술을 개발했다고 25일 밝혔다. 심층신경망 기술을 통한 인공지능의 발달 이래 이러한 분자와 그 특성값 사이의 관계를 파악하려는 시도는 꾸준히 이루어져 왔다. 최근 비 지도 학습(unsupervised training)을 통한 사전학습 기법이 떠오르면서 분자 구조 자체로부터 화합물의 성질을 예측하는 인공지능 연구들이 제시되었으나 새로운 화합물의
2024-03-25 -
행사 생성형 인공지능·가상현실 결합한 3D 스케칭 연구 본격화
우리 대학이 생성형 인공지능(generative AI)과 가상현실(VR)을 활용하여 초고속 생산성 시대를 열어가기 위한 본격적인 도전을 시작한다. 27일 대전 본원에 문을 연 'DRB-KAIST 스케치더퓨처 연구센터(센터장 배석형)'는 생성형 인공지능과 가상현실을 3D(3차원) 스케칭과 결합한 미래형 제품 개발 프로세스를 연구하기 위해 설립됐다. 로봇, 모빌리티, 인공 단백질과 같은 첨단 제조 산업 분야는 제품 개발 주기가 매우 길 뿐만 아니라, 설계 결함이 발견되면 다시 아이디어 발상 단계로 돌아가 실물 제작과 테스트까지의 모든 과정을 반복해야 한다. 또한, 복잡한 3차원 구조체가 한데 맞물려 움직이면서 고도의 기능을 수행하기 때문에, 기존 2차원 스크린 작업 환경에서는 설계 의도를 입력하거나 결과물을 해석하는 데 한계가 있었다.'DRB-KAIST 스케치더퓨처 연구센터'는 사람의 의도를 가장 빠르고 효과적으로 생성형 인공지능에 전달하는 수단으로 최신 가상현실 3D 스케
2024-02-29 -
연구 단백질 ‘생산 설계도’ 보호하는 RNA 조절 기전 찾았다
생명체는 DNA, RNA, 단백질과 같은 바이오분자들의 조절 작용으로 다양한 생물학적 기능을 수행한다. 바이오분자들의 조절로 유전 정보가 전달되고, 잘못 전달된 정보는 유전자 변형이나 감염성 질병의 원인이 된다. 따라서 분자생물학적 조절 연구는 유전자 치료제와 첨단 백신 개발에 중요하다. 특히, 2023년 코로나 mRNA 백신 기술을 개발한 과학자들이 노벨 생리의학상을 수상하면서 RNA 조절 연구에 기반한 첨단신약, 바이오공학 기술이 크게 주목받고 있다. 우리 대학 바이오및뇌공학과 이영석 교수 연구팀이 기초과학연구원(IBS) RNA 연구단 김빛내리 단장(서울대 생명과학부 석좌교수), 미국 국립암연구소 유진 발코프(Eugene Valkov) 박사팀과 공동연구를 통해 자체 개발한 단일핵산 분석법을 적용해 전령 RNA(messenger RNA, 이하 mRNA) 분해의 새로운 조절 기전을 찾았다고 밝혔다. mRNA는 긴 단일 가닥 RNA 분자로, DNA에 보관된 유전 정보를 단백질에
2024-02-28