%ED%97%88%EC%9B%90%EB%8F%84
-
 허원도 교수, 세포의 이동 방향 결정하는 방향타 단백질 발견
〈 허 원 도 교수 〉
우리 몸의 세포는 가만히 멈춰있는 것이 아니라 이동한다. 세포가 특정 방향으로 이동하는 과정은 배아 발달, 상처 치유, 면역 반응 등에 필수적이다. 우리 몸 여러 기관에 암이 전이되는 현상도 암 세포의 이동 때문에 발생한다고 볼 수 있는데 이처럼 세포의 이동은 다양한 생리 및 병리적 조건에서 중요한 역할을 담당한다.
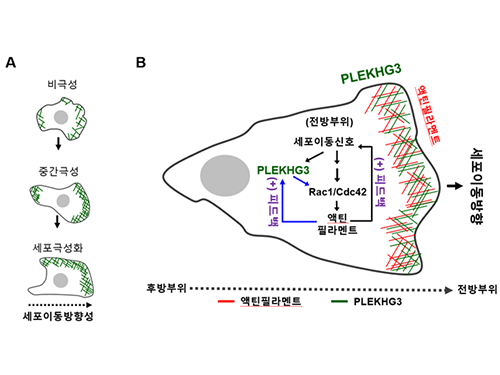
세포 이동에는 여러 종류의 소형 GTP 결합 단백질과 이 단백질의 활성을 조절하는 GEF 단백질들이 관여한다. 세포는 진행 방향 부위의 소형 GTP 결합 단백질(Rac1, Cdc42)이 활성화되면서, 동력을 내는 액틴 섬유를 중합(polymerization)해 지느러미 같은 돌출부를 만들어 앞으로 나아갈 수 있다.
그러나 기존 연구에서는 세포 이동을 관장하는 여러 종류의 GEF 단백질을 세포에 발현시켜도 세포의 이동이 크게 증가하지 않는 한계가 있었고, 세포 이동의 구체적인 작동원리를 밝히지 못했다.
우리 대학 생명과학과 허원도 교수 연구진은 GEF 단백질 중 하나인 ‘PLEKHG3’ 단백질이 세포의 이동 방향을 결정하는 ‘방향타’ 역할을 담당한다는 사실을 처음으로 발견했다.
또한, 독자적으로 개발한 광유전학 기술(광유도 분자 올가미, LARIAT)을 접목, 빛으로 ‘방향타 단백질(PLEKHG3)’ 의 활성을 조절해 세포의 이동을 실시간으로 제어하는 데 성공했다.
연구진은 바이오이미징 기술로 세포 내 63개 GEF 단백질들의 분포양상을 분석해, 세포가 이동하는 동안 세포이동을 조절할 가능성이 높은 GEF 단백질들을 선별했다.
그 중 PLEKHG3가 세포의 진행 방향 부위로 빠르게 이동하는 현상을 확인했다. 방향타 역할을 하는 이 단백질은 해당 부위에서 소형 GTP 결합 단백질을 활성화해 세포 골격을 이루는 액틴 섬유를 형성한다. 액틴 섬유는 그물망을 이루며 지느러미 같은 돌출부를 형성,해 세포를 앞으로 나아가게 한다.
이 과정에서 방향타 단백질은 액틴 섬유 자체와도 매우 강하게 결합하는데, 이 결합이 소형 GTP결합 단백질의 활성을 더욱 촉진시킴으로써 세포의 이동 속도를 더 빠르게 한다는 사실을 발견했다.
또한 연구진은 광유전학 기술로 방향타 단백질의 활성을 조절해 세포가 움직이는 방향을 인위적으로 제어하는 데 성공했다. 청색광 수용체를 이용해 만든 융합 단백질이 발현된 세포에 청색광을 비추면 융합단백질이 PLEKHG3를 올가미처럼 붙잡아 PLEKHG3의 움직임을 방해하는 원리를 활용했다.
이에 따라 빛을 비추면 세포는 이동을 멈추고, 빛을 끄면 PLEKHG3의 활성이 다시 정상화돼, 세포는 움직인다. 빛을 비추는 부위를 조정해서, 세포의 이동방향도 제어할 수 있음을 확인했다.
본 연구는 방향타 단백질인 PLEKHG3가 세포를 움직이게 하는 핵심 단백질임을 밝히고, 광유전학 기술로 빛을 통해 세포의 이동을 자유롭게 제어한 데 의의가 있다.
허원도 교수는 “세포 이동을 극대화하는 새로운 메커니즘을 밝혀 암세포 전이 및 면역 세포 이동을 연구할 수 있을 것으로 기대된다”고 말했다.
이번 연구결과는 국제 학술지 미국국립과학원회보(PNAS) 8월 23일자 온라인 판에 게재됐다.
□ 그림 설명
그림1. 세포내 PLEKHG3의 위치분석
그림2. 세포이동시 PLEKHG3의 세포내 위치추적
그림3. PLEKHG3에 의한 새로운 세포이동 메커니즘
2016.08.24 조회수 9640
허원도 교수, 세포의 이동 방향 결정하는 방향타 단백질 발견
〈 허 원 도 교수 〉
우리 몸의 세포는 가만히 멈춰있는 것이 아니라 이동한다. 세포가 특정 방향으로 이동하는 과정은 배아 발달, 상처 치유, 면역 반응 등에 필수적이다. 우리 몸 여러 기관에 암이 전이되는 현상도 암 세포의 이동 때문에 발생한다고 볼 수 있는데 이처럼 세포의 이동은 다양한 생리 및 병리적 조건에서 중요한 역할을 담당한다.
세포 이동에는 여러 종류의 소형 GTP 결합 단백질과 이 단백질의 활성을 조절하는 GEF 단백질들이 관여한다. 세포는 진행 방향 부위의 소형 GTP 결합 단백질(Rac1, Cdc42)이 활성화되면서, 동력을 내는 액틴 섬유를 중합(polymerization)해 지느러미 같은 돌출부를 만들어 앞으로 나아갈 수 있다.
그러나 기존 연구에서는 세포 이동을 관장하는 여러 종류의 GEF 단백질을 세포에 발현시켜도 세포의 이동이 크게 증가하지 않는 한계가 있었고, 세포 이동의 구체적인 작동원리를 밝히지 못했다.
우리 대학 생명과학과 허원도 교수 연구진은 GEF 단백질 중 하나인 ‘PLEKHG3’ 단백질이 세포의 이동 방향을 결정하는 ‘방향타’ 역할을 담당한다는 사실을 처음으로 발견했다.
또한, 독자적으로 개발한 광유전학 기술(광유도 분자 올가미, LARIAT)을 접목, 빛으로 ‘방향타 단백질(PLEKHG3)’ 의 활성을 조절해 세포의 이동을 실시간으로 제어하는 데 성공했다.
연구진은 바이오이미징 기술로 세포 내 63개 GEF 단백질들의 분포양상을 분석해, 세포가 이동하는 동안 세포이동을 조절할 가능성이 높은 GEF 단백질들을 선별했다.
그 중 PLEKHG3가 세포의 진행 방향 부위로 빠르게 이동하는 현상을 확인했다. 방향타 역할을 하는 이 단백질은 해당 부위에서 소형 GTP 결합 단백질을 활성화해 세포 골격을 이루는 액틴 섬유를 형성한다. 액틴 섬유는 그물망을 이루며 지느러미 같은 돌출부를 형성,해 세포를 앞으로 나아가게 한다.
이 과정에서 방향타 단백질은 액틴 섬유 자체와도 매우 강하게 결합하는데, 이 결합이 소형 GTP결합 단백질의 활성을 더욱 촉진시킴으로써 세포의 이동 속도를 더 빠르게 한다는 사실을 발견했다.
또한 연구진은 광유전학 기술로 방향타 단백질의 활성을 조절해 세포가 움직이는 방향을 인위적으로 제어하는 데 성공했다. 청색광 수용체를 이용해 만든 융합 단백질이 발현된 세포에 청색광을 비추면 융합단백질이 PLEKHG3를 올가미처럼 붙잡아 PLEKHG3의 움직임을 방해하는 원리를 활용했다.
이에 따라 빛을 비추면 세포는 이동을 멈추고, 빛을 끄면 PLEKHG3의 활성이 다시 정상화돼, 세포는 움직인다. 빛을 비추는 부위를 조정해서, 세포의 이동방향도 제어할 수 있음을 확인했다.
본 연구는 방향타 단백질인 PLEKHG3가 세포를 움직이게 하는 핵심 단백질임을 밝히고, 광유전학 기술로 빛을 통해 세포의 이동을 자유롭게 제어한 데 의의가 있다.
허원도 교수는 “세포 이동을 극대화하는 새로운 메커니즘을 밝혀 암세포 전이 및 면역 세포 이동을 연구할 수 있을 것으로 기대된다”고 말했다.
이번 연구결과는 국제 학술지 미국국립과학원회보(PNAS) 8월 23일자 온라인 판에 게재됐다.
□ 그림 설명
그림1. 세포내 PLEKHG3의 위치분석
그림2. 세포이동시 PLEKHG3의 세포내 위치추적
그림3. PLEKHG3에 의한 새로운 세포이동 메커니즘
2016.08.24 조회수 9640 -
 허원도 교수, 세포의 새로운 칼슘 신호 발견
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 세포이동 시 세포의 후방 부위에 새로운 칼슘신호가 있는 것을 발견하고 그 역할을 밝히는 데 성공했다.
허 교수 연구팀은 최근 독자적으로 개발한 광유전학 기법인 광활성세포성장인자수용체(OptoFGFR)와 그 하위 신호전달 단백질을 제어할 수 있는 다른 광유전학 기술을 조합하는 방법을 이용했다.
김진만 박사(의과학대학원), 이민지 박사과정 학생(생명과학과)이 주도한 이번 연구는 ‘미국국립과학원회보(PNAS)’ 온라인 판에 5월 17일자로 게재됐다.
우리 몸을 이루고 있는 세포들은 가만히 멈춰있는 것이 아니라 끊임없이 이동한다. 세포의 이동은 개체의 발달과 유지에 핵심적인 과정이며, 다양한 생리 및 암 전이와 같은 병리적 조건에서 중요한 역할을 담당한다.
특히 배아 발달, 상처 치유, 면역세포 이동 등에서는 세포가 특정 방향으로 이동하는 것이 중요하다. 방향성을 가진 세포는 주변 환경과 상호작용하며 이동하게 되는데 세포의 극성화(Polarization)와 액틴 섬유 등의 세포 골격의 재배열을 통해 이동한다.
방향성을 갖는 세포이동은 복잡한 신호와 신호전달단백질에 의해 매개되는데 신호전달과정은 매우 역동적이며 부위 특이적으로 일어난다.
따라서 이러한 세포의 생화학적인 변화에 중요한 요소와 그 분자적 기전을 밝히는 데에는 어려움이 따른다. 연구진은 원하는 특정 부위에만 자극을 줄 수 있고, 수용체와 같은 상위 신호전달 단백질부터 실제 세포가 움직이도록 작용하는 하위 단백질까지 활성을 각각 조절할 수 있는 광유전학 기술의 장점을 이용했다.
국소적인 빛 자극을 통해 세포의 이동을 유도하는 모델을 구축하고 이를 통해 방향성을 가지는 세포 이동을 개별 세포 수준에서 분석하는데 성공한 것이다.
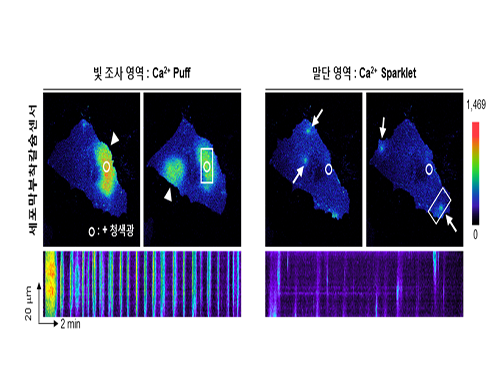
연구진은 광유전학 기술의 적용을 통해 방향성을 가진 세포 이동시에 발생하는 부위 특이적인 칼슘신호(Ca²⁺ sparklet)를 발견했다.
기존 연구에서는 세포 이동시에 세포내 칼슘 농도 경사가 생기는 과정이 전혀 알려져 있지 않았다. 연구진은 세포전방부위에 빛을 비춰 세포성장인자수용체(FGFR)가 활성화돼 여러 신호전달과정이 진행되면서 세포막이 앞으로 팽창하고 세포가 전진하게 되는 것을 확인했다.
신호전달이 세포후방부위까지 전달되면서 세포후방에 있는 세포막칼슘채널의 국소적이고 반복적인 개방을 통해 칼슘이온 농도가 증가, 액틴(Actin)중합을 유도하여 세포후방부위가 수축, 세포이동이 이루어짐을 알게 됐다.
이번 연구는 신호전달 체계의 상, 하위에 있는 단백질들을 특이적으로 조절할 수 있는 다양한 광유전학 기술들을 효과적으로 적용하여 방향성을 가진 세포이동에서 칼슘이온의 새로운 역할을 밝혔다는 점에서 의의가 있다.
세포이동시 세포의 후방 부에 특이적이고 반복적으로 칼슘이 증가하는 현상을 확인, 증가한 칼슘이온이 세포 이동에서 세포의 전방부위와 후방부위의 신호전달단백질의 상호작용에 관여할 뿐만 아니라, 세포 내 전체적인 칼슘의 농도경사를 유지하는데 필수적으로 작용한다는 것을 밝혀낸 것이다.
이 기술은 광유전학 기술의 장점을 극대화한 생물학적 연구의 표본을 제시한다는 점에서 유용할 것으로 기대된다.
□ 그림 설명
그림1. 청색광의 부분 자극에 의해 세포 내에서 발생하는 칼슘신호들
그림2. 광유전학 기술을 이용한 광유도 세포 이동 모델의 구축
2016.05.27 조회수 11422
허원도 교수, 세포의 새로운 칼슘 신호 발견
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 세포이동 시 세포의 후방 부위에 새로운 칼슘신호가 있는 것을 발견하고 그 역할을 밝히는 데 성공했다.
허 교수 연구팀은 최근 독자적으로 개발한 광유전학 기법인 광활성세포성장인자수용체(OptoFGFR)와 그 하위 신호전달 단백질을 제어할 수 있는 다른 광유전학 기술을 조합하는 방법을 이용했다.
김진만 박사(의과학대학원), 이민지 박사과정 학생(생명과학과)이 주도한 이번 연구는 ‘미국국립과학원회보(PNAS)’ 온라인 판에 5월 17일자로 게재됐다.
우리 몸을 이루고 있는 세포들은 가만히 멈춰있는 것이 아니라 끊임없이 이동한다. 세포의 이동은 개체의 발달과 유지에 핵심적인 과정이며, 다양한 생리 및 암 전이와 같은 병리적 조건에서 중요한 역할을 담당한다.
특히 배아 발달, 상처 치유, 면역세포 이동 등에서는 세포가 특정 방향으로 이동하는 것이 중요하다. 방향성을 가진 세포는 주변 환경과 상호작용하며 이동하게 되는데 세포의 극성화(Polarization)와 액틴 섬유 등의 세포 골격의 재배열을 통해 이동한다.
방향성을 갖는 세포이동은 복잡한 신호와 신호전달단백질에 의해 매개되는데 신호전달과정은 매우 역동적이며 부위 특이적으로 일어난다.
따라서 이러한 세포의 생화학적인 변화에 중요한 요소와 그 분자적 기전을 밝히는 데에는 어려움이 따른다. 연구진은 원하는 특정 부위에만 자극을 줄 수 있고, 수용체와 같은 상위 신호전달 단백질부터 실제 세포가 움직이도록 작용하는 하위 단백질까지 활성을 각각 조절할 수 있는 광유전학 기술의 장점을 이용했다.
국소적인 빛 자극을 통해 세포의 이동을 유도하는 모델을 구축하고 이를 통해 방향성을 가지는 세포 이동을 개별 세포 수준에서 분석하는데 성공한 것이다.
연구진은 광유전학 기술의 적용을 통해 방향성을 가진 세포 이동시에 발생하는 부위 특이적인 칼슘신호(Ca²⁺ sparklet)를 발견했다.
기존 연구에서는 세포 이동시에 세포내 칼슘 농도 경사가 생기는 과정이 전혀 알려져 있지 않았다. 연구진은 세포전방부위에 빛을 비춰 세포성장인자수용체(FGFR)가 활성화돼 여러 신호전달과정이 진행되면서 세포막이 앞으로 팽창하고 세포가 전진하게 되는 것을 확인했다.
신호전달이 세포후방부위까지 전달되면서 세포후방에 있는 세포막칼슘채널의 국소적이고 반복적인 개방을 통해 칼슘이온 농도가 증가, 액틴(Actin)중합을 유도하여 세포후방부위가 수축, 세포이동이 이루어짐을 알게 됐다.
이번 연구는 신호전달 체계의 상, 하위에 있는 단백질들을 특이적으로 조절할 수 있는 다양한 광유전학 기술들을 효과적으로 적용하여 방향성을 가진 세포이동에서 칼슘이온의 새로운 역할을 밝혔다는 점에서 의의가 있다.
세포이동시 세포의 후방 부에 특이적이고 반복적으로 칼슘이 증가하는 현상을 확인, 증가한 칼슘이온이 세포 이동에서 세포의 전방부위와 후방부위의 신호전달단백질의 상호작용에 관여할 뿐만 아니라, 세포 내 전체적인 칼슘의 농도경사를 유지하는데 필수적으로 작용한다는 것을 밝혀낸 것이다.
이 기술은 광유전학 기술의 장점을 극대화한 생물학적 연구의 표본을 제시한다는 점에서 유용할 것으로 기대된다.
□ 그림 설명
그림1. 청색광의 부분 자극에 의해 세포 내에서 발생하는 칼슘신호들
그림2. 광유전학 기술을 이용한 광유도 세포 이동 모델의 구축
2016.05.27 조회수 11422 -
 허원도 교수, 빛을 통해 세포내 물질 이동 제어 기술 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 막으로 이루어진 세포내 소기관들의 이동을 빛으로 자유롭게 제어하는데 성공했다. 이로써 세포내 물질 수송의 단계별 메커니즘을 규명해 암과 신경질환 치료에 새로운 해법을 제시할 수 있을 것으로 기대된다.
연구팀은 세포내 물질 수송을 조절하는 새로운 광유전학 기술인 생체막 올가미(IM-LARIAT; Light-Activated Reversible Inhibition by Assembled Trap of Intracellular Membrane) 기술을 개발했다.
세포 내에는 엔도좀(endosome)이나 리소좀(lysosome), 엑소좀(exosome) 등 막으로 이루어진 다양한 막 구조 세포 소기관2)(intracellular membranes)들이 존재한다. 막 구조 세포 소기관들은 세포의 성장과 분열에 밀접한 세포의 기본 기능인 물질 수송과 물질 분비, 신호전달과정 등에 관여한다.
세포내 물질 수송은 매우 역동적으로 움직이는 세포 소기관들에 의해 이루어지는데, 복잡한 움직임을 제어할 방법이 거의 없어 세포 관련 연구가 제한돼 왔다.
이에 허원도 교수는 생체막 올가미 기술을 개발, 빛을 통해 세포 소기관들의 이동을 원하는 때, 원하는 위치에서 일시 정지시켜 세포 소기관들의 이동 메커니즘을 실시간으로 연구하는데 성공했다.
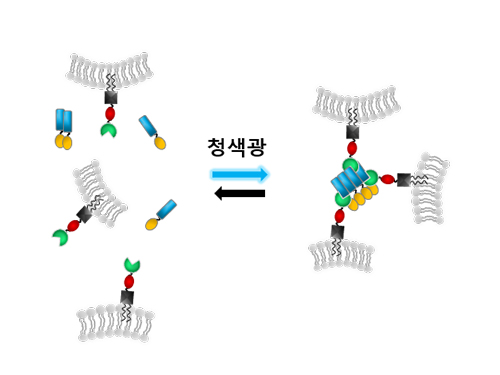
허원도 교수팀은 청색 빛에 반응하는 식물의 청색광 수용 단백질에, 세포 소기관들의 생체막에 존재하는 랩 단백질(Rab small GTPase)을 결합시킨 융합단백질을 개발했다. 이 융합단백질을 실험동물의 암세포와 신경세포에 발현시킨 뒤 청색 빛을 비춘 결과, 많은 막 구조 세포 소기관들이 서로 응집하여 이동이 일시 정지되는 현상을 확인했다.
특히 생체막 올가미 기술을 신경세포에 적용, 엔도좀들의 이동을 일시 정지 시켜, 뇌 신경 세포 성장원추(growth cone)의 성장을 제어하는데 성공했다. 청색 빛을 비추자 일시적으로 성장이 멈췄던 신경세포가, 빛을 끄자 다시 빠르게 자라나는 것을 추가로 확인했다.
이번 연구는 약물이나 전기 자극이 아닌 빛을 비추는 비 침습적(non-invasive) 방식을 고안, 최소 자극으로 막 구조 세포 소기관들의 이동을 제어할 수 있게 된 데 의의가 있다. 신경세포의 분화 및 암세포의 물질 수송을 빛으로 정지시킬 수 있는 생체막 올가미 기술을 응용하면, 다양한 암과 신경질환의 치료 해법을 제시할 수 있을 것으로 기대된다.
허원도 교수는 “이번 연구는 살아있는 세포내에 존재하는 다양한 세포 소기관들을 빛으로 제어한 연구로, 적외선이나 소형 광원을 이용한 생체막 관련 질환 치료법이나 신경세포재생연구로 발전시킬 수 있을 것”이라며 “특히 뇌 신경세포 내 소기관들의 이동과 물질 수송 연구는 기억과 학습 관련 연구 분야에도 새 장을 열어줄 것”이라고 말했다.
이번 연구결과는 생명과학 분야 세계적 학술지인 네이처 케미컬 바이올로지(Nature Chemical Biology, IF 12.996) 온라인판 4월 12일자에 게재됐다.
허원도 교수는 지난 3년 동안 유명학술지에 독자적으로 개발한 광유전학기술들을 연속적으로 발표하고 있으며 현재 수편의 논문들도 해외유명저널에서 심사 중이다. 2014년에 Nature Methods, Nature Communications, Cell 자매지인 Chemistry & Biology 표지논문으로 발표를 시작했다. 2015년 Nature Biotechnology 표지논문에 이어, 이번에는 Nature Chemical Biology에 발표하는 등 세계적으로 광유전학분야를 선도하고 있다.
□ 그림 설명
그림1. 세포 내 물질 수송의 과정
2016.04.18 조회수 12710
허원도 교수, 빛을 통해 세포내 물질 이동 제어 기술 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 막으로 이루어진 세포내 소기관들의 이동을 빛으로 자유롭게 제어하는데 성공했다. 이로써 세포내 물질 수송의 단계별 메커니즘을 규명해 암과 신경질환 치료에 새로운 해법을 제시할 수 있을 것으로 기대된다.
연구팀은 세포내 물질 수송을 조절하는 새로운 광유전학 기술인 생체막 올가미(IM-LARIAT; Light-Activated Reversible Inhibition by Assembled Trap of Intracellular Membrane) 기술을 개발했다.
세포 내에는 엔도좀(endosome)이나 리소좀(lysosome), 엑소좀(exosome) 등 막으로 이루어진 다양한 막 구조 세포 소기관2)(intracellular membranes)들이 존재한다. 막 구조 세포 소기관들은 세포의 성장과 분열에 밀접한 세포의 기본 기능인 물질 수송과 물질 분비, 신호전달과정 등에 관여한다.
세포내 물질 수송은 매우 역동적으로 움직이는 세포 소기관들에 의해 이루어지는데, 복잡한 움직임을 제어할 방법이 거의 없어 세포 관련 연구가 제한돼 왔다.
이에 허원도 교수는 생체막 올가미 기술을 개발, 빛을 통해 세포 소기관들의 이동을 원하는 때, 원하는 위치에서 일시 정지시켜 세포 소기관들의 이동 메커니즘을 실시간으로 연구하는데 성공했다.
허원도 교수팀은 청색 빛에 반응하는 식물의 청색광 수용 단백질에, 세포 소기관들의 생체막에 존재하는 랩 단백질(Rab small GTPase)을 결합시킨 융합단백질을 개발했다. 이 융합단백질을 실험동물의 암세포와 신경세포에 발현시킨 뒤 청색 빛을 비춘 결과, 많은 막 구조 세포 소기관들이 서로 응집하여 이동이 일시 정지되는 현상을 확인했다.
특히 생체막 올가미 기술을 신경세포에 적용, 엔도좀들의 이동을 일시 정지 시켜, 뇌 신경 세포 성장원추(growth cone)의 성장을 제어하는데 성공했다. 청색 빛을 비추자 일시적으로 성장이 멈췄던 신경세포가, 빛을 끄자 다시 빠르게 자라나는 것을 추가로 확인했다.
이번 연구는 약물이나 전기 자극이 아닌 빛을 비추는 비 침습적(non-invasive) 방식을 고안, 최소 자극으로 막 구조 세포 소기관들의 이동을 제어할 수 있게 된 데 의의가 있다. 신경세포의 분화 및 암세포의 물질 수송을 빛으로 정지시킬 수 있는 생체막 올가미 기술을 응용하면, 다양한 암과 신경질환의 치료 해법을 제시할 수 있을 것으로 기대된다.
허원도 교수는 “이번 연구는 살아있는 세포내에 존재하는 다양한 세포 소기관들을 빛으로 제어한 연구로, 적외선이나 소형 광원을 이용한 생체막 관련 질환 치료법이나 신경세포재생연구로 발전시킬 수 있을 것”이라며 “특히 뇌 신경세포 내 소기관들의 이동과 물질 수송 연구는 기억과 학습 관련 연구 분야에도 새 장을 열어줄 것”이라고 말했다.
이번 연구결과는 생명과학 분야 세계적 학술지인 네이처 케미컬 바이올로지(Nature Chemical Biology, IF 12.996) 온라인판 4월 12일자에 게재됐다.
허원도 교수는 지난 3년 동안 유명학술지에 독자적으로 개발한 광유전학기술들을 연속적으로 발표하고 있으며 현재 수편의 논문들도 해외유명저널에서 심사 중이다. 2014년에 Nature Methods, Nature Communications, Cell 자매지인 Chemistry & Biology 표지논문으로 발표를 시작했다. 2015년 Nature Biotechnology 표지논문에 이어, 이번에는 Nature Chemical Biology에 발표하는 등 세계적으로 광유전학분야를 선도하고 있다.
□ 그림 설명
그림1. 세포 내 물질 수송의 과정
2016.04.18 조회수 12710 -
 니콘인스트루먼트코리아, 생명과학과에 발전기금 전달
니콘인스트루먼트코리아(대표 사이토 에이이치)가 본교 생명과학과가 추진하고 있는 ‘신약개발 연구동’ 건립을 위해 써달라며 1천만 원의 발전기금을 전달했다.
발전기금 전달식은 지난달 25일 본교 생명과학과 교수회의실에서 열렸다.
니콘인스트루먼트코리아는 “한국의 생명과학 발전에 크게 기여 할 ‘신약개발연구동’ 설립 취지에 공감하여 기부를 하게 되었다”며 “이번 기부금이 세계적인 연구성과를 창출하는 밑거름이 되길 바란다”라고 뜻을 밝혔다.
<사진설명>니콘 인스트루먼트 코리아가 지난 9월 25일 생명과학과 교수회의실에서 ‘신약개발연구동’ 건립기금으로 1천만 원을 전달했다. 왼쪽부터 생명과학과 허원도 교수, 오병하 학과장, 전상용 교수, 코리아인스텍 장삼섭 대표, 니콘인스트루먼트코리아 유익수 이사.
한편 KAIST 생명과학과는 ‘신약개발 연구동’ 신축을 위한 기금모금을 2015년 8월부터 추진하고 있다. ‘신약개발 연구동’은 첨단 연구기기 지원실을 구축하여 분야가 구별되지 않는 토탈 리서치를 수행하는 연구 공간으로 운영된다. 끝.
2015.10.02 조회수 8615
니콘인스트루먼트코리아, 생명과학과에 발전기금 전달
니콘인스트루먼트코리아(대표 사이토 에이이치)가 본교 생명과학과가 추진하고 있는 ‘신약개발 연구동’ 건립을 위해 써달라며 1천만 원의 발전기금을 전달했다.
발전기금 전달식은 지난달 25일 본교 생명과학과 교수회의실에서 열렸다.
니콘인스트루먼트코리아는 “한국의 생명과학 발전에 크게 기여 할 ‘신약개발연구동’ 설립 취지에 공감하여 기부를 하게 되었다”며 “이번 기부금이 세계적인 연구성과를 창출하는 밑거름이 되길 바란다”라고 뜻을 밝혔다.
<사진설명>니콘 인스트루먼트 코리아가 지난 9월 25일 생명과학과 교수회의실에서 ‘신약개발연구동’ 건립기금으로 1천만 원을 전달했다. 왼쪽부터 생명과학과 허원도 교수, 오병하 학과장, 전상용 교수, 코리아인스텍 장삼섭 대표, 니콘인스트루먼트코리아 유익수 이사.
한편 KAIST 생명과학과는 ‘신약개발 연구동’ 신축을 위한 기금모금을 2015년 8월부터 추진하고 있다. ‘신약개발 연구동’은 첨단 연구기기 지원실을 구축하여 분야가 구별되지 않는 토탈 리서치를 수행하는 연구 공간으로 운영된다. 끝.
2015.10.02 조회수 8615 -
 과학기술계 세계적 리더, 10일 KAIST에 집결
- 제6회 KAIST 총장자문위원회 참석 위해 - - 재학생들과 피자·김밥 먹으면서 대화도 나눠 -
미국 연방정부의 과학기술부 장관격인 미국과학재단(NSF) 총재를 지낸 아든 비먼트(Arden Bement) 박사와 영국의 고등교육 평가기관인 QS의 세계대학 평가에서 수년째 아시아 1위를 차지하고 있는 홍콩과기대 토니 챈(Tony F. Chan) 총장 등 세계 정상급 과학기술계 리더들이 10일 대전 KAIST를 방문했다.
이밖에 MIT 및 칼텍(Caltech, 캘리포니아 공대)과 더불어 세계 3대 공대 중 하나로 꼽히는 독일 베를린공대의 요르그 스타인바크(Jörg Steinbach) 총장을 비롯해 폴 그린필드(Paul Greenfield) 호주 퀸즈랜드대 총장, 라스 펠레슨(Lars Pallesen) 덴마크공대 총장, 요시나오 미시마(Yoshinao Mishima) 동경공대 수석부총장, 모쉐 슈피탈니(Moshe Shpitalni) 이스라엘 테크니언(Technion) 대학원장 등 모두 14명의 해외자문위원과 함께 민계식 현대중공업 회장, 이희국 LG 실트로 사장 등 6명의 국내자문위원도 9일과 10일 속속 KAIST에 합류했다.
이처럼 국내·외의 산·학·연 정상급 유명인사들이 KAIST를 방문한 이유는 10일 서남표 총장이 주관한 제6회 KAIST 총장자문위원회에 참석하기 위해서다.
서 총장은 부임 첫 해인 지난 2006년부터 KAIST를 세계적인 과학기술대학으로 발전시키기 위해 학술 및 교육, 연구 분야에서 다양한 정책자문을 얻고자 매년 총장자문위원회의를 개최해오고 있다.
올 11월 현재 KAIST 총장자문위원회 위원장은 닐 파파랄도(Neil Pappalardo) 미국 메디텍(MEDITECH) 회장이 맡고 있다. 이들 국내·외 자문위원들은 회의 전날인 9일 오후 2시부터는 무선충전 전기자동차(온라인 전기자동차)와 모바일 항구(MH) 연구현장을 방문해 연구 성과를 보고받고 연구진을 격려했다.
이어 10일에는 서남표 총장으로부터 지난 1년간 ‘KAIST의 주요현황 및 비전’을, 백경욱 연구부총장으로부터 ‘KAIST가 나아가야 할 연구방향’에 대해, 그리고 이영훈 학생본부장으로부터는 ‘학생사고 이후 학생지원 계획’ 등을 보고받고 전문가로서 의견을 제시했다.
이어 생명과학과 허원도 교수, 기계공학과 김정 교수 등 6명의 교수의 첨단기술 연구과제에 대한 주제발표와 토론 순으로 자문회의가 진행됐다.
이와 같이 서 총장과 KAIST는 ‘2011 총장자문위원회’에 세계적 연구대학으로서의 국제화 활동 및 교육환경 개선 등 지난 1년간 학교가 중점적으로 추진해온 제반 활동을 보고했으며 각 사안별로 제시된 자문위원들의 의견은 학교정책 등에 적극 반영할 방침이다.
특히, 이날 총장자문위원들은 12시부터 교내 E5빌딩 2층 교수클럽에서 KAIST 재학생들과 김밥, 피자, 치킨 등으로 점심을 먹으면서 대화를 나누는 시간도 가졌다. 쉽게 만나기 어려운 전 세계 과학기술계의 최정상급 인사 20여명이 학생들과 소박하게 점심을 먹으면서 대화와 토론을 나눈 것은 매우 이례적인 일이다.
학교측은 짧은 시간이지만 학생들이 이들 인사들과의 대화와 관심사항에 대한 의견 교환을 통해 과학기술의 중요성을 깨닫는 한편 인생관을 정립하는데 큰 도움을 얻을 것으로 기대하고 있다.
학교는 이를 위해 지난 7일부터 학내공지를 통해 총장자문위원들과 대화를 원하는 학부 및 대학원생 100명을 선착순으로 모집했으며 이날 학생과의 대화시간에는 자문위원단은 물론 학생, 그리고 서 총장을 포함한 보직교수 등 모두 180여명이 참석했다.
10일 본관 1층에서 열린 "제6회 KAIST 총장자문위원회"에서 서남표 총장이 자문위원들에게 발표를 하고 있다.
10일 KAIST E5빌딩 2층 교수클럽에서 KAIST 재학생들과 총장자문위원들이 김밥, 피자, 치킨 등으로 점심을 먹으면서 대화를 나누고 있다.
2011.11.10 조회수 14341
과학기술계 세계적 리더, 10일 KAIST에 집결
- 제6회 KAIST 총장자문위원회 참석 위해 - - 재학생들과 피자·김밥 먹으면서 대화도 나눠 -
미국 연방정부의 과학기술부 장관격인 미국과학재단(NSF) 총재를 지낸 아든 비먼트(Arden Bement) 박사와 영국의 고등교육 평가기관인 QS의 세계대학 평가에서 수년째 아시아 1위를 차지하고 있는 홍콩과기대 토니 챈(Tony F. Chan) 총장 등 세계 정상급 과학기술계 리더들이 10일 대전 KAIST를 방문했다.
이밖에 MIT 및 칼텍(Caltech, 캘리포니아 공대)과 더불어 세계 3대 공대 중 하나로 꼽히는 독일 베를린공대의 요르그 스타인바크(Jörg Steinbach) 총장을 비롯해 폴 그린필드(Paul Greenfield) 호주 퀸즈랜드대 총장, 라스 펠레슨(Lars Pallesen) 덴마크공대 총장, 요시나오 미시마(Yoshinao Mishima) 동경공대 수석부총장, 모쉐 슈피탈니(Moshe Shpitalni) 이스라엘 테크니언(Technion) 대학원장 등 모두 14명의 해외자문위원과 함께 민계식 현대중공업 회장, 이희국 LG 실트로 사장 등 6명의 국내자문위원도 9일과 10일 속속 KAIST에 합류했다.
이처럼 국내·외의 산·학·연 정상급 유명인사들이 KAIST를 방문한 이유는 10일 서남표 총장이 주관한 제6회 KAIST 총장자문위원회에 참석하기 위해서다.
서 총장은 부임 첫 해인 지난 2006년부터 KAIST를 세계적인 과학기술대학으로 발전시키기 위해 학술 및 교육, 연구 분야에서 다양한 정책자문을 얻고자 매년 총장자문위원회의를 개최해오고 있다.
올 11월 현재 KAIST 총장자문위원회 위원장은 닐 파파랄도(Neil Pappalardo) 미국 메디텍(MEDITECH) 회장이 맡고 있다. 이들 국내·외 자문위원들은 회의 전날인 9일 오후 2시부터는 무선충전 전기자동차(온라인 전기자동차)와 모바일 항구(MH) 연구현장을 방문해 연구 성과를 보고받고 연구진을 격려했다.
이어 10일에는 서남표 총장으로부터 지난 1년간 ‘KAIST의 주요현황 및 비전’을, 백경욱 연구부총장으로부터 ‘KAIST가 나아가야 할 연구방향’에 대해, 그리고 이영훈 학생본부장으로부터는 ‘학생사고 이후 학생지원 계획’ 등을 보고받고 전문가로서 의견을 제시했다.
이어 생명과학과 허원도 교수, 기계공학과 김정 교수 등 6명의 교수의 첨단기술 연구과제에 대한 주제발표와 토론 순으로 자문회의가 진행됐다.
이와 같이 서 총장과 KAIST는 ‘2011 총장자문위원회’에 세계적 연구대학으로서의 국제화 활동 및 교육환경 개선 등 지난 1년간 학교가 중점적으로 추진해온 제반 활동을 보고했으며 각 사안별로 제시된 자문위원들의 의견은 학교정책 등에 적극 반영할 방침이다.
특히, 이날 총장자문위원들은 12시부터 교내 E5빌딩 2층 교수클럽에서 KAIST 재학생들과 김밥, 피자, 치킨 등으로 점심을 먹으면서 대화를 나누는 시간도 가졌다. 쉽게 만나기 어려운 전 세계 과학기술계의 최정상급 인사 20여명이 학생들과 소박하게 점심을 먹으면서 대화와 토론을 나눈 것은 매우 이례적인 일이다.
학교측은 짧은 시간이지만 학생들이 이들 인사들과의 대화와 관심사항에 대한 의견 교환을 통해 과학기술의 중요성을 깨닫는 한편 인생관을 정립하는데 큰 도움을 얻을 것으로 기대하고 있다.
학교는 이를 위해 지난 7일부터 학내공지를 통해 총장자문위원들과 대화를 원하는 학부 및 대학원생 100명을 선착순으로 모집했으며 이날 학생과의 대화시간에는 자문위원단은 물론 학생, 그리고 서 총장을 포함한 보직교수 등 모두 180여명이 참석했다.
10일 본관 1층에서 열린 "제6회 KAIST 총장자문위원회"에서 서남표 총장이 자문위원들에게 발표를 하고 있다.
10일 KAIST E5빌딩 2층 교수클럽에서 KAIST 재학생들과 총장자문위원들이 김밥, 피자, 치킨 등으로 점심을 먹으면서 대화를 나누고 있다.
2011.11.10 조회수 14341 -
 심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
2010.12.20 조회수 12672
심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
2010.12.20 조회수 12672 -
 제3회 KI 국제 공동 심포지엄 개최
오는 24일(목) 오전 10시 교내 정문술빌딩 드림홀에서 과학과 공학속의 컬러(Color in Science and Engineering)라는 주제로 ‘제3회 KI 국제 공동심포지엄’을 개최한다.
이번 심포지엄은 전 세계적으로 융합연구의 중요성이 더욱 강조되는 시점에서 과학과 공학뿐만 아니라 심미적이며 감성적인 차원의 컬러를 다양한 분야의 저명한 연사들의 발표를 통하여 새로운 융합연구의 장을 마련하기 위하여 준비됐다.
이를 위해 영국 리드대학교(University of Leeds) 색채과학과 로니어 루오(Ronnier Luo)교수, 교토대학(University of Tokyo) 전자공학과의 수수모 노다(Susumu Noda)교수, 도쿄 대학(University of Tokyo) 산업과학과의 히로시 도시요시(Hiroshi Toshiyoshi)교수 등 저명한 해외 연사가 초청됐다.
특히 루오 교수는 색상, 광택, 촉감 등을 포함한 물리적 형태의 측정에 대한 발표를 통해 과학자와 디자이너 사이에 다리역할을 해 줄 수 있는 효과적인 방법을 발표할 예정이다. 생명과학과 허원도 교수, 산업디자인학과 석현정교수를 포함한 저명한 국내의 5인의 연사들도 각 연구분야에서 컬러와 관련된 주제에 대해 발표할 예정이다.
이번 심포지엄은 기초과학과 공학의 저명한 연구자들뿐만 아니라 색채 인지와 심리, 디자인과 관련된 뛰어난 연구자들의 발표가 포함되어 색채에 대한 다양한 의견과 시각을 교환할 수 있는 기회가 될 것이다. 첨단 기술과 응용 분야에서 단순히 앞선 기술이 아니라 인간의 감성과 휴먼인터페이스를 이해하는 기술이 필요한데 KI(KAIST Institutes)를 중심으로 이러한 통섭의 장을 마련하기 위하여 기획된 본 심포지엄은 기존의 심포지움과 차별화 되는 새로운 시도이다.
김상수 부총장은 “다양한 학문적 배경을 가진 국내외 색채전문가들의 심도 있고 흥미로운 강연과 토론을 통해 전 세계의 학문적 트렌드를 살펴볼 수 있는 좋은 기회가 될 것”이라고 밝혔다.
우리대학은 미국 MIT의 링컨연구소처럼 세계적 수준의 연구개발 성과를 통해 대학의 인지도를 높이고 국가 경쟁력 향상에 기여할 수 있는 발판으로 삼고자, 미래 핵심분야인 바이오, IT, 나노, 광기술 등 8개 연구소로 이뤄진 KI(KAIST Institutes)를 설립했다.
현재 우리대학의 26개 학과의 200여명의 교수가 참여하여 활발한 융합연구를 수행하고 있다.
2009.09.22 조회수 15976
제3회 KI 국제 공동 심포지엄 개최
오는 24일(목) 오전 10시 교내 정문술빌딩 드림홀에서 과학과 공학속의 컬러(Color in Science and Engineering)라는 주제로 ‘제3회 KI 국제 공동심포지엄’을 개최한다.
이번 심포지엄은 전 세계적으로 융합연구의 중요성이 더욱 강조되는 시점에서 과학과 공학뿐만 아니라 심미적이며 감성적인 차원의 컬러를 다양한 분야의 저명한 연사들의 발표를 통하여 새로운 융합연구의 장을 마련하기 위하여 준비됐다.
이를 위해 영국 리드대학교(University of Leeds) 색채과학과 로니어 루오(Ronnier Luo)교수, 교토대학(University of Tokyo) 전자공학과의 수수모 노다(Susumu Noda)교수, 도쿄 대학(University of Tokyo) 산업과학과의 히로시 도시요시(Hiroshi Toshiyoshi)교수 등 저명한 해외 연사가 초청됐다.
특히 루오 교수는 색상, 광택, 촉감 등을 포함한 물리적 형태의 측정에 대한 발표를 통해 과학자와 디자이너 사이에 다리역할을 해 줄 수 있는 효과적인 방법을 발표할 예정이다. 생명과학과 허원도 교수, 산업디자인학과 석현정교수를 포함한 저명한 국내의 5인의 연사들도 각 연구분야에서 컬러와 관련된 주제에 대해 발표할 예정이다.
이번 심포지엄은 기초과학과 공학의 저명한 연구자들뿐만 아니라 색채 인지와 심리, 디자인과 관련된 뛰어난 연구자들의 발표가 포함되어 색채에 대한 다양한 의견과 시각을 교환할 수 있는 기회가 될 것이다. 첨단 기술과 응용 분야에서 단순히 앞선 기술이 아니라 인간의 감성과 휴먼인터페이스를 이해하는 기술이 필요한데 KI(KAIST Institutes)를 중심으로 이러한 통섭의 장을 마련하기 위하여 기획된 본 심포지엄은 기존의 심포지움과 차별화 되는 새로운 시도이다.
김상수 부총장은 “다양한 학문적 배경을 가진 국내외 색채전문가들의 심도 있고 흥미로운 강연과 토론을 통해 전 세계의 학문적 트렌드를 살펴볼 수 있는 좋은 기회가 될 것”이라고 밝혔다.
우리대학은 미국 MIT의 링컨연구소처럼 세계적 수준의 연구개발 성과를 통해 대학의 인지도를 높이고 국가 경쟁력 향상에 기여할 수 있는 발판으로 삼고자, 미래 핵심분야인 바이오, IT, 나노, 광기술 등 8개 연구소로 이뤄진 KI(KAIST Institutes)를 설립했다.
현재 우리대학의 26개 학과의 200여명의 교수가 참여하여 활발한 융합연구를 수행하고 있다.
2009.09.22 조회수 15976