-
 윤동기 교수, 국제액정학회 중견학술상 수상
우리 대학 화학과 윤동기 교수가 국제액정학회(ILCS (The International Liquid Crystal Society))가 수여하는 ILCS 중견학술상(Mid-Career Award(LG))을 받았다고 26일 밝혔다. 시상식은 7월 24일 브라질 리우데자네이루에서 열린 29회 국제액정학회(29th International Liquid Crystal Conference)에서 개최됐다.
2008년 국제액정학회가 제정한 ‘ILCS 중견학술상(Mid-Career Award)’은 액정분야에서 최초 발견이나 커다란 연구 성과를 낸 중견 과학자를 대상으로 2년마다 단 한 명에게만 수여하는 상이다. 윤동기 교수처럼 2012년 동 학회에서 젊은 과학자에게 수여하는 미치 나카타 상(Michi Nakata Prize)에 이어 ILCS 중견학술상(Mid-Career Award)을 동시에 받은 사례는 전 세계적으로도 윤 교수가 처음이다.
윤동기 교수는 평판 디스플레이 시장의 상당 부분을 차지하는 LCD(liquid crystal display, 액정표시장치)의 핵심 물질인 액정물질을 물리, 화학적인 관점에서 융합연구를 주도하고 있는 액정물질 전문 과학자다. 현재까지, 우리나라에서 액정 디스플레이를 많이 생산해 왔음에도 불구하고, 그 핵심 물질인 액정물질에 대한 기초연구는 해외에 비해 국내 연구의 수준이 뒤떨어진 것이 사실이므로 관련 분야의 지속적인 발전을 위해서는 관련 기초 및 융합연구가 중요하다.
산업계에서도 LCD 관련 R&D 분야는 성숙단계라고는 하지만 최근 플렉시블, 폴더블, 스트레처블 디스플레이를 비롯해 OLED 분야에서도 코팅이 가능한 다양한 기능성 박막 필름이 필요한데, 이에 배향된 액정분자체 기반의 보상 필름이 유력한 후보군으로 떠오르고 있고, 자동차용 각종 디스플레이, 증강현실용 소프트 로보틱스뿐만 아니라 차세대 통신, 안테나 분야 등에도 액정물질 기반의 핵심 연구가 필요한 상황이다.
윤 교수는 디스플레이 분야에서 가장 일반적으로 많이 연구되는 방향성만 있는 네마틱(Nematic)이라고 하는 단순한 액정 상(phase)을 비롯해 차세대 디스플레이 및 디스플레이를 넘어서는 새로운 응용 분야를 열 수 있는 판상형 액정(Smectic LC) 분야에서 두각을 나타내어‘사이언스 어드밴시스’ 등 세계적인 수준의 저널들에 150여 편의 연구 결과를 발표하고 특허 또한 30여 편을 출원 및 등록할 정도로 활발한 연구 활동을 펼치고 있다.
윤 교수의 액정물질 기반 나노 및 마이크로패터닝과 관련한 연구 및 최신 응용연구 성과를 통해 국제액정학회가 인정했기 때문에 윤 교수가 ‘ILCS 중견학술상(Mid-Career Award (LG))’ 수상자로 선정됐다고 관계자는 설명했다.
윤 교수는 현재 ‘초분자 액정물질 및 액정고분자 패터닝’이라는 새로운 분야를 개척 중으로, 기초과학연구뿐만 아니라 차세대 통신 분야에 대해서도 액정물질을 기반으로 융합 기술을 개발하는 연구도 함께 진행하고 있다.
윤동기 교수, 국제액정학회 중견학술상 수상
우리 대학 화학과 윤동기 교수가 국제액정학회(ILCS (The International Liquid Crystal Society))가 수여하는 ILCS 중견학술상(Mid-Career Award(LG))을 받았다고 26일 밝혔다. 시상식은 7월 24일 브라질 리우데자네이루에서 열린 29회 국제액정학회(29th International Liquid Crystal Conference)에서 개최됐다.
2008년 국제액정학회가 제정한 ‘ILCS 중견학술상(Mid-Career Award)’은 액정분야에서 최초 발견이나 커다란 연구 성과를 낸 중견 과학자를 대상으로 2년마다 단 한 명에게만 수여하는 상이다. 윤동기 교수처럼 2012년 동 학회에서 젊은 과학자에게 수여하는 미치 나카타 상(Michi Nakata Prize)에 이어 ILCS 중견학술상(Mid-Career Award)을 동시에 받은 사례는 전 세계적으로도 윤 교수가 처음이다.
윤동기 교수는 평판 디스플레이 시장의 상당 부분을 차지하는 LCD(liquid crystal display, 액정표시장치)의 핵심 물질인 액정물질을 물리, 화학적인 관점에서 융합연구를 주도하고 있는 액정물질 전문 과학자다. 현재까지, 우리나라에서 액정 디스플레이를 많이 생산해 왔음에도 불구하고, 그 핵심 물질인 액정물질에 대한 기초연구는 해외에 비해 국내 연구의 수준이 뒤떨어진 것이 사실이므로 관련 분야의 지속적인 발전을 위해서는 관련 기초 및 융합연구가 중요하다.
산업계에서도 LCD 관련 R&D 분야는 성숙단계라고는 하지만 최근 플렉시블, 폴더블, 스트레처블 디스플레이를 비롯해 OLED 분야에서도 코팅이 가능한 다양한 기능성 박막 필름이 필요한데, 이에 배향된 액정분자체 기반의 보상 필름이 유력한 후보군으로 떠오르고 있고, 자동차용 각종 디스플레이, 증강현실용 소프트 로보틱스뿐만 아니라 차세대 통신, 안테나 분야 등에도 액정물질 기반의 핵심 연구가 필요한 상황이다.
윤 교수는 디스플레이 분야에서 가장 일반적으로 많이 연구되는 방향성만 있는 네마틱(Nematic)이라고 하는 단순한 액정 상(phase)을 비롯해 차세대 디스플레이 및 디스플레이를 넘어서는 새로운 응용 분야를 열 수 있는 판상형 액정(Smectic LC) 분야에서 두각을 나타내어‘사이언스 어드밴시스’ 등 세계적인 수준의 저널들에 150여 편의 연구 결과를 발표하고 특허 또한 30여 편을 출원 및 등록할 정도로 활발한 연구 활동을 펼치고 있다.
윤 교수의 액정물질 기반 나노 및 마이크로패터닝과 관련한 연구 및 최신 응용연구 성과를 통해 국제액정학회가 인정했기 때문에 윤 교수가 ‘ILCS 중견학술상(Mid-Career Award (LG))’ 수상자로 선정됐다고 관계자는 설명했다.
윤 교수는 현재 ‘초분자 액정물질 및 액정고분자 패터닝’이라는 새로운 분야를 개척 중으로, 기초과학연구뿐만 아니라 차세대 통신 분야에 대해서도 액정물질을 기반으로 융합 기술을 개발하는 연구도 함께 진행하고 있다.
2024.07.26
조회수 4240
-
 종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16
조회수 6160
-
 맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27
조회수 5835
-
 암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
2023.03.02
조회수 14115
-
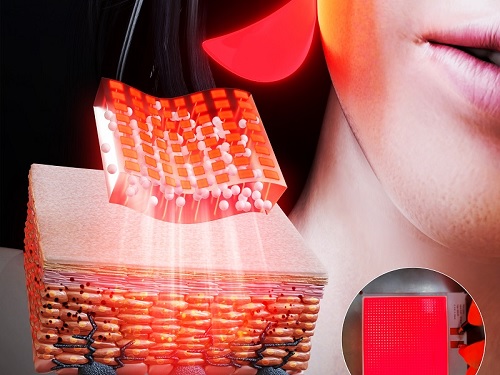 면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10
조회수 9061
-
 창업원, KAIST Startup Tech Plaza 6일 개최
우리 대학 창업원(원장 김영태)은 6일(수) 오후 2시 판교센터에서 KAIST 스타트업 테크 플라자(KAIST Startup Tech Plaza)를 개최한다.
KAIST 스타트업 테크 플라자는 ▲바이오테크/약학/헬스케어(Biotech/Pharmacy/Healthcare) ▲소재/부품/장비 ▲환경·사회·지배구조(ESG) ▲인공지능/디지털 트랜스포메이션(AI/DT) 등 최첨단 기술 트렌드를 공유하는 자리다. 창업원은 스타트업과 투자자 등 인재가 만나 함께 성장하는 기회의 장을 마련하기 위해 이번 행사를 포함해 올 한 해 동안 총 여섯 번의 스타트업 테크 플라자를 개최할 예정이다.6일 열리는 올해 첫 행사는 의과학 분야를 주제로 전문가 강연과 관련 분야 스타트업 IR(Investor Relations) 피칭 및 스타트업-VC 네트워킹 등의 프로그램을 마련했다. 이정석 KAIST 의과학대학원 교수(지놈인사이트 공동 창업자)가 “의사, 과학자, 사업가 그리고?”라는 주제로 강연한다. 또한, 튜론(TULON), 에아스텍(ERSTEQ), 프라미솝(PROMISOPE), 포엔(4N), 소누스(SONUS) 등 5개 창업기업이 IR 피칭을 진행한다. 이어, 스타트업-VC 네트워킹 및 1:1 맞춤 상담 등이 행사 현장에서 진행된다. 우리 대학 교원, 재학생 및 졸업생 중 창업에 관심이 있는 예비창업가라면 누구나 참여할 수 있으며, 현장 네트워킹 행사를 제외한 전체 순서는 ZOOM으로 중계된다.김영태 창업원장은 "최초·최고 기술 기반의 KAIST 창업가들이 코로나-19와 기술혁신 등으로 인한 대격변의 시기에 적기에 창업하고 빠르게 성장할 수 있도록 창업원의 역할을 지속적으로 강화할 것"이라고 밝혔다.
창업원, KAIST Startup Tech Plaza 6일 개최
우리 대학 창업원(원장 김영태)은 6일(수) 오후 2시 판교센터에서 KAIST 스타트업 테크 플라자(KAIST Startup Tech Plaza)를 개최한다.
KAIST 스타트업 테크 플라자는 ▲바이오테크/약학/헬스케어(Biotech/Pharmacy/Healthcare) ▲소재/부품/장비 ▲환경·사회·지배구조(ESG) ▲인공지능/디지털 트랜스포메이션(AI/DT) 등 최첨단 기술 트렌드를 공유하는 자리다. 창업원은 스타트업과 투자자 등 인재가 만나 함께 성장하는 기회의 장을 마련하기 위해 이번 행사를 포함해 올 한 해 동안 총 여섯 번의 스타트업 테크 플라자를 개최할 예정이다.6일 열리는 올해 첫 행사는 의과학 분야를 주제로 전문가 강연과 관련 분야 스타트업 IR(Investor Relations) 피칭 및 스타트업-VC 네트워킹 등의 프로그램을 마련했다. 이정석 KAIST 의과학대학원 교수(지놈인사이트 공동 창업자)가 “의사, 과학자, 사업가 그리고?”라는 주제로 강연한다. 또한, 튜론(TULON), 에아스텍(ERSTEQ), 프라미솝(PROMISOPE), 포엔(4N), 소누스(SONUS) 등 5개 창업기업이 IR 피칭을 진행한다. 이어, 스타트업-VC 네트워킹 및 1:1 맞춤 상담 등이 행사 현장에서 진행된다. 우리 대학 교원, 재학생 및 졸업생 중 창업에 관심이 있는 예비창업가라면 누구나 참여할 수 있으며, 현장 네트워킹 행사를 제외한 전체 순서는 ZOOM으로 중계된다.김영태 창업원장은 "최초·최고 기술 기반의 KAIST 창업가들이 코로나-19와 기술혁신 등으로 인한 대격변의 시기에 적기에 창업하고 빠르게 성장할 수 있도록 창업원의 역할을 지속적으로 강화할 것"이라고 밝혔다.
2022.04.05
조회수 9075
-
 KAIST Crazy Day 전 국민 아이디어 공모전 개최
우리 대학이 파격적으로 실행할 수 있는 도전 과제를 국민의 제안으로 발굴하는 'KAIST Crazy Day 아이디어 공모전’을 개최한다. 올해 5월 중 하루, 파격적(Crazy), 창의적(Creative), 도전적(Challenging)이거나 배려정신(Caring)을 담은 아이디어를 실행하는 `KAIST Crazy Day’”행사를 개최할 예정이다. 일 년에 딱 하루, 평소에는 적용해보기 어려웠던 아이디어를 캠퍼스에서 실행해 혁신문화를 확산하고 구성원들의 창의적인 열정을 장려하겠다는 취지다. 이를 위해, 전 국민을 대상으로 모험적이면서도 창의적인 아이디어를 제안받는 공모전을 이달 14일 시작한다. 상금은 총 1,000만 원 규모다.‘KAIST 1일 총장 되기’, ‘필기 제로 수업해보기’, ‘연구를 위해 연구하지 않기’ ‘직위 대신 이름 부르기’ 등 기존의 관행이나 형식에 얽매이지 않는 혁신적인 시도이면서도 자유로운 사고를 바탕으로 ‘왜’라는 질문을 끊임없이 이끌어내는 아이디어라면 국민 누구나 제안할 수 있다. 다음 달 8일까지 진행되는 공모전은 KAIST 홈페이지(www.kaist.ac.kr) 또는 KAIST 글로벌전략연구소 홈페이지(http://gsi.kaist.ac.kr/)에서 참여할 수 있다. 1인당 1건씩 온라인으로 응모할 수 있으며, 우편 및 방문 신청은 받지 않는다. 우리 대학은 창의성, 혁신성, 진취성, 실행 가능성, 대중의 공감대 등을 평가 기준으로 정하고 내부 및 외부위원이 참여하는 3단계 심사를 통해 최종 수상작을 선정할 예정이다. 대상 1명에게는 상금 500만 원 주어지며, 제안한 아이디어가 5월 개최될 `KAIST Crazy Day‘ 행사에서 실행된다. 이 밖에, 최우수상 1명과 우수상 3명에게는 각각 200만 원과 100만 원의 상금을 수여한다. 이광형 총장은 “하버드대학의 유머 과학잡지 ‘별난 연구 연보(Annals of Improbable Research)’에서는 매년 황당무계한 괴짜 연구에 ‘이그 노벨상(Ig Nobel Prize)’을 수여한다”라고 언급했다. 이어, 이 총장은 “괴짜 아이디어가 노벨상으로 이어진 수많은 사례로 미루어 볼 때 과학기술혁신은 고정관념과 상식의 프레임에서 벗어나는 데서부터 출발한다”라며, “국민이 제안하는 파격적이고도 획기적인 아이디어를 실천해 KAIST의 도전과 실험정신을 계속 이어 나가겠다”라고 밝혔다.
KAIST Crazy Day 전 국민 아이디어 공모전 개최
우리 대학이 파격적으로 실행할 수 있는 도전 과제를 국민의 제안으로 발굴하는 'KAIST Crazy Day 아이디어 공모전’을 개최한다. 올해 5월 중 하루, 파격적(Crazy), 창의적(Creative), 도전적(Challenging)이거나 배려정신(Caring)을 담은 아이디어를 실행하는 `KAIST Crazy Day’”행사를 개최할 예정이다. 일 년에 딱 하루, 평소에는 적용해보기 어려웠던 아이디어를 캠퍼스에서 실행해 혁신문화를 확산하고 구성원들의 창의적인 열정을 장려하겠다는 취지다. 이를 위해, 전 국민을 대상으로 모험적이면서도 창의적인 아이디어를 제안받는 공모전을 이달 14일 시작한다. 상금은 총 1,000만 원 규모다.‘KAIST 1일 총장 되기’, ‘필기 제로 수업해보기’, ‘연구를 위해 연구하지 않기’ ‘직위 대신 이름 부르기’ 등 기존의 관행이나 형식에 얽매이지 않는 혁신적인 시도이면서도 자유로운 사고를 바탕으로 ‘왜’라는 질문을 끊임없이 이끌어내는 아이디어라면 국민 누구나 제안할 수 있다. 다음 달 8일까지 진행되는 공모전은 KAIST 홈페이지(www.kaist.ac.kr) 또는 KAIST 글로벌전략연구소 홈페이지(http://gsi.kaist.ac.kr/)에서 참여할 수 있다. 1인당 1건씩 온라인으로 응모할 수 있으며, 우편 및 방문 신청은 받지 않는다. 우리 대학은 창의성, 혁신성, 진취성, 실행 가능성, 대중의 공감대 등을 평가 기준으로 정하고 내부 및 외부위원이 참여하는 3단계 심사를 통해 최종 수상작을 선정할 예정이다. 대상 1명에게는 상금 500만 원 주어지며, 제안한 아이디어가 5월 개최될 `KAIST Crazy Day‘ 행사에서 실행된다. 이 밖에, 최우수상 1명과 우수상 3명에게는 각각 200만 원과 100만 원의 상금을 수여한다. 이광형 총장은 “하버드대학의 유머 과학잡지 ‘별난 연구 연보(Annals of Improbable Research)’에서는 매년 황당무계한 괴짜 연구에 ‘이그 노벨상(Ig Nobel Prize)’을 수여한다”라고 언급했다. 이어, 이 총장은 “괴짜 아이디어가 노벨상으로 이어진 수많은 사례로 미루어 볼 때 과학기술혁신은 고정관념과 상식의 프레임에서 벗어나는 데서부터 출발한다”라며, “국민이 제안하는 파격적이고도 획기적인 아이디어를 실천해 KAIST의 도전과 실험정신을 계속 이어 나가겠다”라고 밝혔다.
2022.03.11
조회수 10373
-
 면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
2021.10.21
조회수 12983
-
 인공지능 이용 면역항암 세포 3차원 분석기술 개발
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀이 면역항암 세포의 활동을 정밀하게 측정하고 분석할 수 있는 새로운 3차원 인공지능 분석기술을 개발했다고 28일 밝혔다.
체내에서 면역세포를 추출한 후, 외부에서 면역 능력을 강화시키고 다시 환자에게 주입해 암을 치료하는 방식을 `입양전달 면역세포 치료(adoptive immune cell therapy)'라고 부른다. 이 치료방식은 면역세포 치료법 중 가장 많은 주목을 받는 기술이다. `키메릭 항원 수용체' 또는 `CAR(Chimeric Antigen Receptor)'라고도 불리는 데 유전자 재조합기술을 이용해 T세포와 같은 면역세포를 변형해 암세포와의 반응을 유도해 사멸시키는 치료 방법이다.
특히 CAR-T세포 치료는 높은 치료 효과를 보여 차세대 암 치료제로 급부상하고 있다. 2017년 난치성 B세포 급성 림프구성 백혈병 치료제 판매 승인을 시작으로 현재 3종의 CAR-T 치료제가 판매 승인을 받았으며, 전 세계적으로 약 1,000건 이상의 임상 시험이 진행 중이다. 그러나 아직 우리나라에서는 진행 중인 임상 시험이 전무한 실정이다.
CAR-T 기술을 이용한 암 치료 방법들이 속속 개발되고 있지만, CAR-T세포에 대한 세포‧분자 생물학적 메커니즘은 아직 많은 부분이 알려지지 않았다. 특히, CAR-T세포가 표적 암세포를 인지해 결합한 후 `면역 시냅스 (immunological synapse, 이하 IS)'를 형성해 물질을 전달하고 암세포의 사멸을 유도하는데, 두 세포 간의 거리와 같은 IS의 형태 정보는 T세포 활성화 유도와 관련이 높다고 알려져 있지만 구체적인 내용을 파악하기 어렵기 때문에 이에 대한 연구가 활발히 진행 중이다.
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀은 CAR-T세포의 IS를 정밀하고 체계적으로 연구할 수 있는 새로운 기술을 개발했다. 3D 홀로그래피 현미경 기술을 이용해, 염색이나 전처리 없이 살아있는 상태의 CAR-T세포와 표적 암세포 간의 상호작용을 고속으로 측정하고 기존에는 관찰하기 어려운 CAR-T와 암세포 간의 IS를 고해상도로 실시간 측정했다. 또한 이렇게 측정한 3D 세포 영상을 인공지능 신경망(Convolutional Neural Network, CNN)을 이용해 분석하고, 3차원 공간에서 정확하게 IS 정보를 정량적으로 추출할 수 있는 기술을 자체 개발했다.
공동연구팀은 또 이 기술을 활용해 빠른 CAR-T 면역 관문 형성 메커니즘을 추적할 수 있었을 뿐만 아니라, IS의 형태학적 특성이 CAR-T의 항암 효능과 연관이 있음을 확인했다. 연구팀은 3차원 IS 정보가 새로운 표적 항암 치료제의 초기 연구에 필요한 정량적 지표를 제공할 것이라고 기대하고 있다.
이번 연구에는 우리 대학 기술을 바탕으로 창업한 2개 기업이 공동으로 참여했다. 3차원 홀로그래픽 현미경을 상업화한 토모큐브 社의 현미경 장비를 이용해 면역세포를 측정하는 한편 토모큐브 社의 인공지능 연구팀이 알고리즘 개발에 참여했다. 이밖에 국내 최초 CAR-T 기반 치료제 기업인 ㈜큐로셀도 연구에 함께 참여해 이 같은 성과를 거두는 데 성공했다.
물리학과 이무성 박사과정 학생, 생명과학과 이영호 박사, 물리학과 송진엽 학부생 (現 메사추세츠 공과대학(MIT) 물리학과 박사과정)이 공동 제1 저자로 참여한 이번 연구는 국제적으로 권위를 인정받는 생물학술지인 `이라이프(eLife)' 12월 17일 字 온라인판을 통해 공개됐으며 지난 21일 字에 공식 게재됐다.
(논문명 : Deep-learning based three-dimensional label-free tracking and analysis of immunological synapses of CAR-T cells)
한편 이번 연구는 한국연구재단 리더연구사업, 바이오·의료기술개발사업, 중견연구자지원사업, KAIST Up program의 지원을 받아 수행됐다.
인공지능 이용 면역항암 세포 3차원 분석기술 개발
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀이 면역항암 세포의 활동을 정밀하게 측정하고 분석할 수 있는 새로운 3차원 인공지능 분석기술을 개발했다고 28일 밝혔다.
체내에서 면역세포를 추출한 후, 외부에서 면역 능력을 강화시키고 다시 환자에게 주입해 암을 치료하는 방식을 `입양전달 면역세포 치료(adoptive immune cell therapy)'라고 부른다. 이 치료방식은 면역세포 치료법 중 가장 많은 주목을 받는 기술이다. `키메릭 항원 수용체' 또는 `CAR(Chimeric Antigen Receptor)'라고도 불리는 데 유전자 재조합기술을 이용해 T세포와 같은 면역세포를 변형해 암세포와의 반응을 유도해 사멸시키는 치료 방법이다.
특히 CAR-T세포 치료는 높은 치료 효과를 보여 차세대 암 치료제로 급부상하고 있다. 2017년 난치성 B세포 급성 림프구성 백혈병 치료제 판매 승인을 시작으로 현재 3종의 CAR-T 치료제가 판매 승인을 받았으며, 전 세계적으로 약 1,000건 이상의 임상 시험이 진행 중이다. 그러나 아직 우리나라에서는 진행 중인 임상 시험이 전무한 실정이다.
CAR-T 기술을 이용한 암 치료 방법들이 속속 개발되고 있지만, CAR-T세포에 대한 세포‧분자 생물학적 메커니즘은 아직 많은 부분이 알려지지 않았다. 특히, CAR-T세포가 표적 암세포를 인지해 결합한 후 `면역 시냅스 (immunological synapse, 이하 IS)'를 형성해 물질을 전달하고 암세포의 사멸을 유도하는데, 두 세포 간의 거리와 같은 IS의 형태 정보는 T세포 활성화 유도와 관련이 높다고 알려져 있지만 구체적인 내용을 파악하기 어렵기 때문에 이에 대한 연구가 활발히 진행 중이다.
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀은 CAR-T세포의 IS를 정밀하고 체계적으로 연구할 수 있는 새로운 기술을 개발했다. 3D 홀로그래피 현미경 기술을 이용해, 염색이나 전처리 없이 살아있는 상태의 CAR-T세포와 표적 암세포 간의 상호작용을 고속으로 측정하고 기존에는 관찰하기 어려운 CAR-T와 암세포 간의 IS를 고해상도로 실시간 측정했다. 또한 이렇게 측정한 3D 세포 영상을 인공지능 신경망(Convolutional Neural Network, CNN)을 이용해 분석하고, 3차원 공간에서 정확하게 IS 정보를 정량적으로 추출할 수 있는 기술을 자체 개발했다.
공동연구팀은 또 이 기술을 활용해 빠른 CAR-T 면역 관문 형성 메커니즘을 추적할 수 있었을 뿐만 아니라, IS의 형태학적 특성이 CAR-T의 항암 효능과 연관이 있음을 확인했다. 연구팀은 3차원 IS 정보가 새로운 표적 항암 치료제의 초기 연구에 필요한 정량적 지표를 제공할 것이라고 기대하고 있다.
이번 연구에는 우리 대학 기술을 바탕으로 창업한 2개 기업이 공동으로 참여했다. 3차원 홀로그래픽 현미경을 상업화한 토모큐브 社의 현미경 장비를 이용해 면역세포를 측정하는 한편 토모큐브 社의 인공지능 연구팀이 알고리즘 개발에 참여했다. 이밖에 국내 최초 CAR-T 기반 치료제 기업인 ㈜큐로셀도 연구에 함께 참여해 이 같은 성과를 거두는 데 성공했다.
물리학과 이무성 박사과정 학생, 생명과학과 이영호 박사, 물리학과 송진엽 학부생 (現 메사추세츠 공과대학(MIT) 물리학과 박사과정)이 공동 제1 저자로 참여한 이번 연구는 국제적으로 권위를 인정받는 생물학술지인 `이라이프(eLife)' 12월 17일 字 온라인판을 통해 공개됐으며 지난 21일 字에 공식 게재됐다.
(논문명 : Deep-learning based three-dimensional label-free tracking and analysis of immunological synapses of CAR-T cells)
한편 이번 연구는 한국연구재단 리더연구사업, 바이오·의료기술개발사업, 중견연구자지원사업, KAIST Up program의 지원을 받아 수행됐다.
2021.01.29
조회수 77286
-
 차세대 발광 물질 카본닷의 발광 특성 변화 메커니즘을 규명
우리 대학 생명화학공학과 김도현 교수 연구팀이 차세대 발광 물질인 이중 발광 *카본닷의 농도 의존성 발광 특성 변화 메커니즘을 규명했다고 5일 밝혔다.
☞ 카본닷(carbon-dot): 탄소 기반의 발광 물질로 풍부한 원료와 낮은 독성 및 환경친화적인 장점 때문에 기존에 상용화돼 있는 유기 발광체, 양자점(퀀텀닷)을 대체할 수 있는 차세대 발광 물질로 부상하고 있음.
김도현 교수 연구팀은 청색 및 적색을 이중 발광하는 카본닷을 합성한 후 농도에 따른 발광 특성 변화를 관찰해 카본닷 발광 소스 간 상호작용에 따른 현상을 분석했다. 김도현 교수팀의 연구 결과는 카본닷의 발광 특성 제어는 물론 이론적 이해를 가능케 함으로써 이중 발광 카본닷의 복잡한 발광 특성 해석에 새로운 근거를 제시한 것으로 평가받고 있다.
우리 대학 유효정 박사과정, 곽병은 석박사통합과정이 각각 제1, 제2 저자로 참여한 이번 연구는 국제 학술지 `피지컬 케미스트리 케미컬 피직스(Physical Chemistry Chemical Physics, PCCP)' 9월 22권 36호 표지논문으로 선정됐다. (논문명 : Interparticle distance as a key factor for controlling the dual-emission properties of carbon dots)
카본닷은 다양한 발광 준위 에너지를 동시에 갖기 때문에 다색발광이 가능하며 농도 변화에 따른 발광 특성 변화를 보인다. 이 같은 특성은 기존 발광 물질인 유기 발광체, 양자점과는 구별되는 카본닷만이 지닌 독자적이고 유용한 특성이다.
최근 들어 다양한 분야에 카본닷의 발광 특성을 이용하려는 연구가 활발히 진행되고 있다. 특히 백색광 및 광학 센서 분야에서 다색발광은 하나의 형광체만으로도 장치 구현이 가능하고 레퍼런스 신호를 제공해 센서의 정확도를 높일 수 있다는 장점 때문에 카본닷 다색발광의 구현과 제어가 중요한 연구과제로 떠오르고 있다.
카본닷은 다색발광과 농도 변화에 따라 다양한 발광 특성을 보이지만 매우 드물게 만들어진다는 게 약점이다. 또 복수 발광 소스 사이의 복잡한 상호작용으로 인해 카본닷의 다색발광과 농도 변화에 따른 다양한 발광 메커니즘을 규명한 연구가 거의 이뤄지지 않고 있다.
연구팀은 이런 문제해결을 위해 청색·적색 이중 발광 카본닷을 합성해 카본닷의 입자 간 거리가 카본닷 발광 특성 변화에 중요한 역할을 한다는 점을 밝히는 연구를 진행했다.
기존의 농도 변화에 따른 카본닷의 발광 특성 변화를 용매 의존 발색 현상에 빗대 수소 결합 영향에 의한 현상으로 해석한 사례가 있지만, 김 교수 연구팀은 카본닷 발광 현상의 농도 의존성이 수소 결합과는 상관없이 입자 간 거리에 의해 제어되는 현상일 수 있다는 가능성에 주목했다.
연구팀이 농도 변화에 따른 카본닷의 이중 발광 특성의 변화를 관찰한 결과, 임계 농도에서 적색 발광에 가장 적합한 입자 간 거리를 형성하고, 이 농도를 전후로 청색 발광이 강해지면서 카본닷의 농도별 이중 발광 특성이 변화하는 현상을 확인했다.
연구팀은 이를 기반으로 분광 분석을 통해 이중 발광의 청색 및 적색의 두 발광 소스를 각각 표면 작용기와 코어의 결합구조로 구분해 농도 변화에 따라 각 발광 소스의 이중 발광에 대한 기여도가 변화한다는 구체적인 설명을 제시했다. 연구팀은 특히 고농도 영역에서 두 발광 소스의 상호작용에 대한 메커니즘 제시를 통해 입자 간 거리 변화 때문에 이중 발광 특성이 제어된다는 결과를 얻었다.
연구팀이 합성한 이중 발광 카본닷은 단일 형광체로서 청색과 적색 발광을 동시 구현할 수 있고 특성 제어가 가능함에 따라 혼합색 구현은 물론 색 변화에 의한 센싱에 사용할 수 있다.
연구팀은 또 이중 발광 카본닷의 농도 조절을 통해 순수한 백색에 근접한 백색 LED 구현에도 성공하는 한편 색 변화에 의한 pH 센싱에 활용해 pH에 따른 청색·적색의 상대적 발광 세기 변화를 통해 pH 추정이 가능함을 보였다. 기존에 제시됐던 카본닷이 고도화된 기능성을 가진 발광체로써 사용될 수 있다는 가능성을 이번 연구를 통해 다시 한 번 입증한 것이다.
제1 저자인 유효정 박사과정 학생은 "카본닷 입자 간 거리에 따라 발광 소스의 상호작용이 일어나 농도에 따른 발광 특성에 변화가 일어난다는 해석은 기존 연구에서 간과됐던 부분ˮ이라면서 "이중 발광 현상에 대한 분석과 함께 이 연구 결과가 카본닷 발광 현상 규명에 있어 새로운 관점을 제시한 것ˮ이라고 의미를 부여했다.
이번 연구는 한국연구재단 이공분야기초연구사업의 지원을 받아 수행됐다.
차세대 발광 물질 카본닷의 발광 특성 변화 메커니즘을 규명
우리 대학 생명화학공학과 김도현 교수 연구팀이 차세대 발광 물질인 이중 발광 *카본닷의 농도 의존성 발광 특성 변화 메커니즘을 규명했다고 5일 밝혔다.
☞ 카본닷(carbon-dot): 탄소 기반의 발광 물질로 풍부한 원료와 낮은 독성 및 환경친화적인 장점 때문에 기존에 상용화돼 있는 유기 발광체, 양자점(퀀텀닷)을 대체할 수 있는 차세대 발광 물질로 부상하고 있음.
김도현 교수 연구팀은 청색 및 적색을 이중 발광하는 카본닷을 합성한 후 농도에 따른 발광 특성 변화를 관찰해 카본닷 발광 소스 간 상호작용에 따른 현상을 분석했다. 김도현 교수팀의 연구 결과는 카본닷의 발광 특성 제어는 물론 이론적 이해를 가능케 함으로써 이중 발광 카본닷의 복잡한 발광 특성 해석에 새로운 근거를 제시한 것으로 평가받고 있다.
우리 대학 유효정 박사과정, 곽병은 석박사통합과정이 각각 제1, 제2 저자로 참여한 이번 연구는 국제 학술지 `피지컬 케미스트리 케미컬 피직스(Physical Chemistry Chemical Physics, PCCP)' 9월 22권 36호 표지논문으로 선정됐다. (논문명 : Interparticle distance as a key factor for controlling the dual-emission properties of carbon dots)
카본닷은 다양한 발광 준위 에너지를 동시에 갖기 때문에 다색발광이 가능하며 농도 변화에 따른 발광 특성 변화를 보인다. 이 같은 특성은 기존 발광 물질인 유기 발광체, 양자점과는 구별되는 카본닷만이 지닌 독자적이고 유용한 특성이다.
최근 들어 다양한 분야에 카본닷의 발광 특성을 이용하려는 연구가 활발히 진행되고 있다. 특히 백색광 및 광학 센서 분야에서 다색발광은 하나의 형광체만으로도 장치 구현이 가능하고 레퍼런스 신호를 제공해 센서의 정확도를 높일 수 있다는 장점 때문에 카본닷 다색발광의 구현과 제어가 중요한 연구과제로 떠오르고 있다.
카본닷은 다색발광과 농도 변화에 따라 다양한 발광 특성을 보이지만 매우 드물게 만들어진다는 게 약점이다. 또 복수 발광 소스 사이의 복잡한 상호작용으로 인해 카본닷의 다색발광과 농도 변화에 따른 다양한 발광 메커니즘을 규명한 연구가 거의 이뤄지지 않고 있다.
연구팀은 이런 문제해결을 위해 청색·적색 이중 발광 카본닷을 합성해 카본닷의 입자 간 거리가 카본닷 발광 특성 변화에 중요한 역할을 한다는 점을 밝히는 연구를 진행했다.
기존의 농도 변화에 따른 카본닷의 발광 특성 변화를 용매 의존 발색 현상에 빗대 수소 결합 영향에 의한 현상으로 해석한 사례가 있지만, 김 교수 연구팀은 카본닷 발광 현상의 농도 의존성이 수소 결합과는 상관없이 입자 간 거리에 의해 제어되는 현상일 수 있다는 가능성에 주목했다.
연구팀이 농도 변화에 따른 카본닷의 이중 발광 특성의 변화를 관찰한 결과, 임계 농도에서 적색 발광에 가장 적합한 입자 간 거리를 형성하고, 이 농도를 전후로 청색 발광이 강해지면서 카본닷의 농도별 이중 발광 특성이 변화하는 현상을 확인했다.
연구팀은 이를 기반으로 분광 분석을 통해 이중 발광의 청색 및 적색의 두 발광 소스를 각각 표면 작용기와 코어의 결합구조로 구분해 농도 변화에 따라 각 발광 소스의 이중 발광에 대한 기여도가 변화한다는 구체적인 설명을 제시했다. 연구팀은 특히 고농도 영역에서 두 발광 소스의 상호작용에 대한 메커니즘 제시를 통해 입자 간 거리 변화 때문에 이중 발광 특성이 제어된다는 결과를 얻었다.
연구팀이 합성한 이중 발광 카본닷은 단일 형광체로서 청색과 적색 발광을 동시 구현할 수 있고 특성 제어가 가능함에 따라 혼합색 구현은 물론 색 변화에 의한 센싱에 사용할 수 있다.
연구팀은 또 이중 발광 카본닷의 농도 조절을 통해 순수한 백색에 근접한 백색 LED 구현에도 성공하는 한편 색 변화에 의한 pH 센싱에 활용해 pH에 따른 청색·적색의 상대적 발광 세기 변화를 통해 pH 추정이 가능함을 보였다. 기존에 제시됐던 카본닷이 고도화된 기능성을 가진 발광체로써 사용될 수 있다는 가능성을 이번 연구를 통해 다시 한 번 입증한 것이다.
제1 저자인 유효정 박사과정 학생은 "카본닷 입자 간 거리에 따라 발광 소스의 상호작용이 일어나 농도에 따른 발광 특성에 변화가 일어난다는 해석은 기존 연구에서 간과됐던 부분ˮ이라면서 "이중 발광 현상에 대한 분석과 함께 이 연구 결과가 카본닷 발광 현상 규명에 있어 새로운 관점을 제시한 것ˮ이라고 의미를 부여했다.
이번 연구는 한국연구재단 이공분야기초연구사업의 지원을 받아 수행됐다.
2020.11.05
조회수 30106
-
 美 화학공학회 주최 케미카 대회 국내 예선 우승
(좌측부터) 고동연 교수, 정석영, 슈브로닐 센구프토, 홍지현, 이건호, 박규범, 조슈아 훌리오 아디드자자 학생
우리 대학 학부생으로 구성된 카이탈리스트(KAItalyst, 지도교수 생명화학공학과 고동연)팀이 지난 7월 20일(토) 대전 본원에서 열린 미국 화학공학회(AIChE) 케미카(Chem-E-Car) 한국 지역 예선 대회에서 우승을 차지했다.
케미카 대회는 화학반응으로 구동되는 모형 자동차를 제작하고 그 차량을 제어하는 기술 수준을 겨루는 대회다. 지난 1999년 미국 화학공학회에서 첫 대회를 개최한 이후 전 세계 대학생들이 참여하고 있다.
우리대학은 2014년 처음으로 대회에 출전해 2016년에는 최종 우승을 차지했으며, 2017년과 2018년에는 모스트 컨시스턴트 어워드(Most Consistent Award)를 연속으로 수상했다.
미국 화학공학회에는 대회에 기여한 KAIST의 공로와 역량을 인정해 올해는 공식 지역 예선을 유치할 것을 요청해왔다. 이에 생명화학공학과(학과장 이재우)가 주축이 되어 본선 주최 측이 직접 파견한 2명의 스태프가 관리·감독하는 케미카 한국 지역 예선 대회를 국내 최초로 개최했다.
지난 4월 중순부터 약 한 달 반 동안 한국 화학공학회를 통해 지역 예선에 참여할 총 4개의 팀을 선발하는 공모를 진행했다. 대회에 참가하기 위해서는 4인 이상으로 구성된 대학생 팀이 화학반응으로 구동되는 모형 자동차를 제작한 뒤 정확하게 움직여야 하는 기술을 구현해야 한다.
첫 대회 개최 소식에 여러 대학이 참가 의사를 밝혔지만, 기술 구현에 실패해 KAIST 생명화학공학과와 서울대학교 화학생물공학부 두 팀만이 참가할 수 있었다.
생명화학공학과 홍지현(22세), 정석영(20세), 이건호(20세), 박규범(19세), 조슈아 훌리오 아디드자자(21세, Joshua Julio Adidjaja) 씨와 기계공학과 슈브로닐 센구프토(21세, Shubhranil Sengupta) 씨 등 총 6명의 학부생으로 구성된 카이탈리스트팀은 화학 반응이 신속하고 정확한 요오드시계반응(iodine clock reaction)을 이용하는 한편 바나듐 산화환원 화학전지를 통해 안정적인 출력을 갖는 자동차를 제작했다.
케미카 대회 규칙상 반드시 화학반응으로만 자동차를 제어해야 하며, 경연 대회 현장에서 주행할 거리와 수송할 화물의 무게가 결정된다. 당일에 부여받은 조건이 적용된 모형 자동차를 활용해 목표 지점까지 도달한 시간과 정확도를 비교해 승패를 가린다. 즉, 화학 반응을 정밀하게 제어할 수 있어야 좋은 성적을 거둘 수 있다.
KAIST 팀은 경연 당일 미션으로 제시된 22.5m의 주행거리 중 서울대 팀보다 결승지점에 1.5m 이상 근접하게 접근해 승리를 거뒀다.
우승을 차지한 KAIST 팀에는 본선 진출권과 함께 200달러의 상금이 수여됐으며, 서울대 팀에는 100달러의 상금이 주어졌다.
카이탈리스트의 팀 리더인 홍지현 씨는 "이런 차를 제작하고 구동해본 것이 처음이라 여러 문제점이 있었지만 계속된 노력을 통해 좋은 결과를 낼 수 있었다.ˮ며 이어 "11월에 열리는 국제대회에서도 좋은 결과를 내도록 최선을 다하겠다ˮ고 말했다.
본선 대회는 올해 11월 美 플로리다주 올랜도에서 열리는 미국 화학공학회 정기 총회(AIChE Fall Meeting)에서 개최되며 조지아공대, 카네기멜론대학 등 50개 대학이 참여할 예정이다.
카이탈리스트 팀을 지도한 고동연(생명화학공학과) 교수는 "KAIST가 올해 국내 최초로 개최한 케미카 한국 지역 예선이 시작점이 되어 앞으로 보다 많은 대학이 함께 참여하고 선의의 경쟁을 펼치는 대회로 성장하길 바란다ˮ고 전했다.
美 화학공학회 주최 케미카 대회 국내 예선 우승
(좌측부터) 고동연 교수, 정석영, 슈브로닐 센구프토, 홍지현, 이건호, 박규범, 조슈아 훌리오 아디드자자 학생
우리 대학 학부생으로 구성된 카이탈리스트(KAItalyst, 지도교수 생명화학공학과 고동연)팀이 지난 7월 20일(토) 대전 본원에서 열린 미국 화학공학회(AIChE) 케미카(Chem-E-Car) 한국 지역 예선 대회에서 우승을 차지했다.
케미카 대회는 화학반응으로 구동되는 모형 자동차를 제작하고 그 차량을 제어하는 기술 수준을 겨루는 대회다. 지난 1999년 미국 화학공학회에서 첫 대회를 개최한 이후 전 세계 대학생들이 참여하고 있다.
우리대학은 2014년 처음으로 대회에 출전해 2016년에는 최종 우승을 차지했으며, 2017년과 2018년에는 모스트 컨시스턴트 어워드(Most Consistent Award)를 연속으로 수상했다.
미국 화학공학회에는 대회에 기여한 KAIST의 공로와 역량을 인정해 올해는 공식 지역 예선을 유치할 것을 요청해왔다. 이에 생명화학공학과(학과장 이재우)가 주축이 되어 본선 주최 측이 직접 파견한 2명의 스태프가 관리·감독하는 케미카 한국 지역 예선 대회를 국내 최초로 개최했다.
지난 4월 중순부터 약 한 달 반 동안 한국 화학공학회를 통해 지역 예선에 참여할 총 4개의 팀을 선발하는 공모를 진행했다. 대회에 참가하기 위해서는 4인 이상으로 구성된 대학생 팀이 화학반응으로 구동되는 모형 자동차를 제작한 뒤 정확하게 움직여야 하는 기술을 구현해야 한다.
첫 대회 개최 소식에 여러 대학이 참가 의사를 밝혔지만, 기술 구현에 실패해 KAIST 생명화학공학과와 서울대학교 화학생물공학부 두 팀만이 참가할 수 있었다.
생명화학공학과 홍지현(22세), 정석영(20세), 이건호(20세), 박규범(19세), 조슈아 훌리오 아디드자자(21세, Joshua Julio Adidjaja) 씨와 기계공학과 슈브로닐 센구프토(21세, Shubhranil Sengupta) 씨 등 총 6명의 학부생으로 구성된 카이탈리스트팀은 화학 반응이 신속하고 정확한 요오드시계반응(iodine clock reaction)을 이용하는 한편 바나듐 산화환원 화학전지를 통해 안정적인 출력을 갖는 자동차를 제작했다.
케미카 대회 규칙상 반드시 화학반응으로만 자동차를 제어해야 하며, 경연 대회 현장에서 주행할 거리와 수송할 화물의 무게가 결정된다. 당일에 부여받은 조건이 적용된 모형 자동차를 활용해 목표 지점까지 도달한 시간과 정확도를 비교해 승패를 가린다. 즉, 화학 반응을 정밀하게 제어할 수 있어야 좋은 성적을 거둘 수 있다.
KAIST 팀은 경연 당일 미션으로 제시된 22.5m의 주행거리 중 서울대 팀보다 결승지점에 1.5m 이상 근접하게 접근해 승리를 거뒀다.
우승을 차지한 KAIST 팀에는 본선 진출권과 함께 200달러의 상금이 수여됐으며, 서울대 팀에는 100달러의 상금이 주어졌다.
카이탈리스트의 팀 리더인 홍지현 씨는 "이런 차를 제작하고 구동해본 것이 처음이라 여러 문제점이 있었지만 계속된 노력을 통해 좋은 결과를 낼 수 있었다.ˮ며 이어 "11월에 열리는 국제대회에서도 좋은 결과를 내도록 최선을 다하겠다ˮ고 말했다.
본선 대회는 올해 11월 美 플로리다주 올랜도에서 열리는 미국 화학공학회 정기 총회(AIChE Fall Meeting)에서 개최되며 조지아공대, 카네기멜론대학 등 50개 대학이 참여할 예정이다.
카이탈리스트 팀을 지도한 고동연(생명화학공학과) 교수는 "KAIST가 올해 국내 최초로 개최한 케미카 한국 지역 예선이 시작점이 되어 앞으로 보다 많은 대학이 함께 참여하고 선의의 경쟁을 펼치는 대회로 성장하길 바란다ˮ고 전했다.
2019.07.31
조회수 13222
-
 2019 CHIP 해외 자문단 초청 워크숍 개최
〈 (왼쪽부터)데이빗 슈베르트(David Schubert) 라이프 사이언스 파트너스 최고운영책임자,
다니엘 김(Daniel Kim) 텍사스 대학 신경외과 전문의, 베른트 스토바쪄(Bernd Stowasser) 사노피 유럽 민관협력 담당 임원, 조지 맥랜든(George Mclendon) 엠엘바이오 이사 〉
우리 대학 바이오헬스케어 혁신정책센터(Center for Bio-Healthcare Innovation & Policy, 이하 CHIP)가 오는 7월 1일부터 이틀간 서울 강남쉐라톤팰리스 호텔에서 ‘2019 CHIP 해외 자문단 초청 워크숍’ 개최한다.
올해로 5회째를 맞는 이번 국제 워크숍은 ‘글로벌 오픈이노베이션 플랫폼 구축과 지속가능한 바이오투자 생태계 조성’을 주제로 열린다. 국내 제약사·벤처·벤처캐피털·의료기관·정부기관 전문가들이 모여 바이오헬스 산업 육성을 위한 미래전략을 도출하는 자리다.
글로벌 제약사 사노피의 유럽 민관협력 담당 임원인 베른트 스토바쪄(Bernd Stowasser) 박사, 미국의 혁신신약 전문 액셀러레이터 라이프 사이언스 파트너스(Life Science Partners)의 데이빗 슈베르트(David Schubert) 최고운영책임자, 전 캐롤라이나 헬스케어 시스템의 부회장이자 현재 신약개발 벤처 엠엘바이오(MLBio)의 이사인 조지 맥랜든(George Mclendon) 박사, 텍사스 대학 신경외과 전문의이자 의료로봇 전문가인 다니엘 김(Daniel Kim) 등이 자문단으로 참여한다.
7월 1일 오후 2시부터 진행되는 첫날 워크숍은 정호철 이화여대 약대 특임교수와 김태억 범부처신약사업단 사업개발본부장이 좌장을 맡는다. 총 2개의 세션에서 ▲글로벌 신약개발의 동향 및 미래 방향 ▲바이오헬스 산업에서 글로벌 연구개발 협력의 필요성과 글로벌 동향 ▲IMI(Innovative Medicines Initiative(혁신신약이니셔티브),이하 IMI) 3의 거버넌스 및 한국-EU 공동 R&D의 시너지 ▲IMI와 연구개발 협력이 필요한 분야 및 협력방향 등을 세부과제로 다뤄 신약 개발 분야에서의 국제 연구개발 협력을 통한 글로벌 오픈이노베이션 플랫폼 구축을 논의한다.
특히, 국내 신약개발 생태계의 고질적 약점으로 지적되는 중개연구역량·글로벌 수준의 신약개발 연구인력 부족·글로벌 제약기업 및 선진국 인허가 기관과 네트워크 부재에 관한 해법 모색에 나선다.
그동안 국내 신약개발 지원기관 및 관련 기업들이 세계 최대 민관협력 신약개발 네트워크인 EU-IMI에 참여하고 싶다는 의사를 개별적으로 전달했으나 한국이 비 EU국가라는 이유로 성사되지 못했다.
KAIST 바이오헬스케어 혁신정책센터는 국내·외 자문위원들과 함께 IMI 및 유럽제약협회(EFPIA)와 지난 3년간의 논의해왔으며, 연구개발 비용의 자체 부담을 조건으로 한국의 IMI 참여 지지를 확보했다. 또한, 정부관계자와 함께 한국이 IMI에 참여해야 하는 필요성에 대해 논의하는 중이다.
이번 워크숍을 통해 한국-EU IMI 공동 신약연구 프로그램을 구축할 임시추진위원회를 구성하고 오송·대구 첨단의료복합단지를 글로벌 진출의 허브로 육성해 한국이 EU-IMI의 일원으로 활동하는 방안에 대해 본격적으로 논의할 예정이다.
세포·유전자 치료제 등 미래 정밀의료 의약품 개발과 민간 기업이 개발을 회피하거나 실패 위험이 높은 수퍼박테리아 항생제, 치매를 포함한 뇌질환 치료제 등의 국내 개발을 가속하기 위해서다.
7월 2일은 지속가능한 바이오투자 생태계 조성과 국내 신약·의료기기 스타트업의 글로벌 사업화 가능성을 전망해보는 자리로 마련된다.
조영국 글로벌밸류네트웍스 대표, 김종백 법무법인 지안 변호사, 이남구 워터스 코리아 대표가 좌장을 맡아 ▲바이오기업 가치 평가와 기업공개 ▲바이오텍 초기 투자의 다원화 ▲의료기기 혁신을 위한 투자 등의 세부 과제를 다룰 예정이다.
특히, 바이오 분야 창업부터 코스닥 상장까지 경험을 공유하기 위해 유진산 파맵신 대표와 윤원수 티앤알바이오팹 대표도 기업 사례 발표자로 나선다.
둘째 날 오후 행사에서는 신약개발 스타트업과 의료기기 스타트업의 글로벌 사업화 가능성을 탐색하는 기업 소개와 리뷰(Pre-IR) 시간이 마련된다. 작년에 이 세션에서 소개된 5개의 스타트업 중 2곳이 6개월 이내에 시리즈 A 투자 유치에 성공한 바 있다.
이번 행사는 KAIST 바이오헬스케어 혁신정책센터가 주최·주관하고 보건복지부와 보건산업진흥원, 한강서사이어티가 후원한다.
채수찬 KAIST 바이오헬스케어 혁신정책센터장은 “이번 워크숍을 통해 IMI와 같은 민관협력체 활용과 우리나라 바이오헬스 산업의 글로벌 진출 가속과 지속가능한 발전 방안이 마련되기를 기대한다”고 밝혔다.
KAIST 2019 CHIP 해외 자문단 초청 워크숍은 홈페이지( http://chip.kaist.ac.kr )를 통해 참석 신청이 가능하다.(문의:02-3498-7558)
2019 CHIP 해외 자문단 초청 워크숍 개최
〈 (왼쪽부터)데이빗 슈베르트(David Schubert) 라이프 사이언스 파트너스 최고운영책임자,
다니엘 김(Daniel Kim) 텍사스 대학 신경외과 전문의, 베른트 스토바쪄(Bernd Stowasser) 사노피 유럽 민관협력 담당 임원, 조지 맥랜든(George Mclendon) 엠엘바이오 이사 〉
우리 대학 바이오헬스케어 혁신정책센터(Center for Bio-Healthcare Innovation & Policy, 이하 CHIP)가 오는 7월 1일부터 이틀간 서울 강남쉐라톤팰리스 호텔에서 ‘2019 CHIP 해외 자문단 초청 워크숍’ 개최한다.
올해로 5회째를 맞는 이번 국제 워크숍은 ‘글로벌 오픈이노베이션 플랫폼 구축과 지속가능한 바이오투자 생태계 조성’을 주제로 열린다. 국내 제약사·벤처·벤처캐피털·의료기관·정부기관 전문가들이 모여 바이오헬스 산업 육성을 위한 미래전략을 도출하는 자리다.
글로벌 제약사 사노피의 유럽 민관협력 담당 임원인 베른트 스토바쪄(Bernd Stowasser) 박사, 미국의 혁신신약 전문 액셀러레이터 라이프 사이언스 파트너스(Life Science Partners)의 데이빗 슈베르트(David Schubert) 최고운영책임자, 전 캐롤라이나 헬스케어 시스템의 부회장이자 현재 신약개발 벤처 엠엘바이오(MLBio)의 이사인 조지 맥랜든(George Mclendon) 박사, 텍사스 대학 신경외과 전문의이자 의료로봇 전문가인 다니엘 김(Daniel Kim) 등이 자문단으로 참여한다.
7월 1일 오후 2시부터 진행되는 첫날 워크숍은 정호철 이화여대 약대 특임교수와 김태억 범부처신약사업단 사업개발본부장이 좌장을 맡는다. 총 2개의 세션에서 ▲글로벌 신약개발의 동향 및 미래 방향 ▲바이오헬스 산업에서 글로벌 연구개발 협력의 필요성과 글로벌 동향 ▲IMI(Innovative Medicines Initiative(혁신신약이니셔티브),이하 IMI) 3의 거버넌스 및 한국-EU 공동 R&D의 시너지 ▲IMI와 연구개발 협력이 필요한 분야 및 협력방향 등을 세부과제로 다뤄 신약 개발 분야에서의 국제 연구개발 협력을 통한 글로벌 오픈이노베이션 플랫폼 구축을 논의한다.
특히, 국내 신약개발 생태계의 고질적 약점으로 지적되는 중개연구역량·글로벌 수준의 신약개발 연구인력 부족·글로벌 제약기업 및 선진국 인허가 기관과 네트워크 부재에 관한 해법 모색에 나선다.
그동안 국내 신약개발 지원기관 및 관련 기업들이 세계 최대 민관협력 신약개발 네트워크인 EU-IMI에 참여하고 싶다는 의사를 개별적으로 전달했으나 한국이 비 EU국가라는 이유로 성사되지 못했다.
KAIST 바이오헬스케어 혁신정책센터는 국내·외 자문위원들과 함께 IMI 및 유럽제약협회(EFPIA)와 지난 3년간의 논의해왔으며, 연구개발 비용의 자체 부담을 조건으로 한국의 IMI 참여 지지를 확보했다. 또한, 정부관계자와 함께 한국이 IMI에 참여해야 하는 필요성에 대해 논의하는 중이다.
이번 워크숍을 통해 한국-EU IMI 공동 신약연구 프로그램을 구축할 임시추진위원회를 구성하고 오송·대구 첨단의료복합단지를 글로벌 진출의 허브로 육성해 한국이 EU-IMI의 일원으로 활동하는 방안에 대해 본격적으로 논의할 예정이다.
세포·유전자 치료제 등 미래 정밀의료 의약품 개발과 민간 기업이 개발을 회피하거나 실패 위험이 높은 수퍼박테리아 항생제, 치매를 포함한 뇌질환 치료제 등의 국내 개발을 가속하기 위해서다.
7월 2일은 지속가능한 바이오투자 생태계 조성과 국내 신약·의료기기 스타트업의 글로벌 사업화 가능성을 전망해보는 자리로 마련된다.
조영국 글로벌밸류네트웍스 대표, 김종백 법무법인 지안 변호사, 이남구 워터스 코리아 대표가 좌장을 맡아 ▲바이오기업 가치 평가와 기업공개 ▲바이오텍 초기 투자의 다원화 ▲의료기기 혁신을 위한 투자 등의 세부 과제를 다룰 예정이다.
특히, 바이오 분야 창업부터 코스닥 상장까지 경험을 공유하기 위해 유진산 파맵신 대표와 윤원수 티앤알바이오팹 대표도 기업 사례 발표자로 나선다.
둘째 날 오후 행사에서는 신약개발 스타트업과 의료기기 스타트업의 글로벌 사업화 가능성을 탐색하는 기업 소개와 리뷰(Pre-IR) 시간이 마련된다. 작년에 이 세션에서 소개된 5개의 스타트업 중 2곳이 6개월 이내에 시리즈 A 투자 유치에 성공한 바 있다.
이번 행사는 KAIST 바이오헬스케어 혁신정책센터가 주최·주관하고 보건복지부와 보건산업진흥원, 한강서사이어티가 후원한다.
채수찬 KAIST 바이오헬스케어 혁신정책센터장은 “이번 워크숍을 통해 IMI와 같은 민관협력체 활용과 우리나라 바이오헬스 산업의 글로벌 진출 가속과 지속가능한 발전 방안이 마련되기를 기대한다”고 밝혔다.
KAIST 2019 CHIP 해외 자문단 초청 워크숍은 홈페이지( http://chip.kaist.ac.kr )를 통해 참석 신청이 가능하다.(문의:02-3498-7558)
2019.06.27
조회수 15694
 윤동기 교수, 국제액정학회 중견학술상 수상
우리 대학 화학과 윤동기 교수가 국제액정학회(ILCS (The International Liquid Crystal Society))가 수여하는 ILCS 중견학술상(Mid-Career Award(LG))을 받았다고 26일 밝혔다. 시상식은 7월 24일 브라질 리우데자네이루에서 열린 29회 국제액정학회(29th International Liquid Crystal Conference)에서 개최됐다.
2008년 국제액정학회가 제정한 ‘ILCS 중견학술상(Mid-Career Award)’은 액정분야에서 최초 발견이나 커다란 연구 성과를 낸 중견 과학자를 대상으로 2년마다 단 한 명에게만 수여하는 상이다. 윤동기 교수처럼 2012년 동 학회에서 젊은 과학자에게 수여하는 미치 나카타 상(Michi Nakata Prize)에 이어 ILCS 중견학술상(Mid-Career Award)을 동시에 받은 사례는 전 세계적으로도 윤 교수가 처음이다.
윤동기 교수는 평판 디스플레이 시장의 상당 부분을 차지하는 LCD(liquid crystal display, 액정표시장치)의 핵심 물질인 액정물질을 물리, 화학적인 관점에서 융합연구를 주도하고 있는 액정물질 전문 과학자다. 현재까지, 우리나라에서 액정 디스플레이를 많이 생산해 왔음에도 불구하고, 그 핵심 물질인 액정물질에 대한 기초연구는 해외에 비해 국내 연구의 수준이 뒤떨어진 것이 사실이므로 관련 분야의 지속적인 발전을 위해서는 관련 기초 및 융합연구가 중요하다.
산업계에서도 LCD 관련 R&D 분야는 성숙단계라고는 하지만 최근 플렉시블, 폴더블, 스트레처블 디스플레이를 비롯해 OLED 분야에서도 코팅이 가능한 다양한 기능성 박막 필름이 필요한데, 이에 배향된 액정분자체 기반의 보상 필름이 유력한 후보군으로 떠오르고 있고, 자동차용 각종 디스플레이, 증강현실용 소프트 로보틱스뿐만 아니라 차세대 통신, 안테나 분야 등에도 액정물질 기반의 핵심 연구가 필요한 상황이다.
윤 교수는 디스플레이 분야에서 가장 일반적으로 많이 연구되는 방향성만 있는 네마틱(Nematic)이라고 하는 단순한 액정 상(phase)을 비롯해 차세대 디스플레이 및 디스플레이를 넘어서는 새로운 응용 분야를 열 수 있는 판상형 액정(Smectic LC) 분야에서 두각을 나타내어‘사이언스 어드밴시스’ 등 세계적인 수준의 저널들에 150여 편의 연구 결과를 발표하고 특허 또한 30여 편을 출원 및 등록할 정도로 활발한 연구 활동을 펼치고 있다.
윤 교수의 액정물질 기반 나노 및 마이크로패터닝과 관련한 연구 및 최신 응용연구 성과를 통해 국제액정학회가 인정했기 때문에 윤 교수가 ‘ILCS 중견학술상(Mid-Career Award (LG))’ 수상자로 선정됐다고 관계자는 설명했다.
윤 교수는 현재 ‘초분자 액정물질 및 액정고분자 패터닝’이라는 새로운 분야를 개척 중으로, 기초과학연구뿐만 아니라 차세대 통신 분야에 대해서도 액정물질을 기반으로 융합 기술을 개발하는 연구도 함께 진행하고 있다.
2024.07.26 조회수 4240
윤동기 교수, 국제액정학회 중견학술상 수상
우리 대학 화학과 윤동기 교수가 국제액정학회(ILCS (The International Liquid Crystal Society))가 수여하는 ILCS 중견학술상(Mid-Career Award(LG))을 받았다고 26일 밝혔다. 시상식은 7월 24일 브라질 리우데자네이루에서 열린 29회 국제액정학회(29th International Liquid Crystal Conference)에서 개최됐다.
2008년 국제액정학회가 제정한 ‘ILCS 중견학술상(Mid-Career Award)’은 액정분야에서 최초 발견이나 커다란 연구 성과를 낸 중견 과학자를 대상으로 2년마다 단 한 명에게만 수여하는 상이다. 윤동기 교수처럼 2012년 동 학회에서 젊은 과학자에게 수여하는 미치 나카타 상(Michi Nakata Prize)에 이어 ILCS 중견학술상(Mid-Career Award)을 동시에 받은 사례는 전 세계적으로도 윤 교수가 처음이다.
윤동기 교수는 평판 디스플레이 시장의 상당 부분을 차지하는 LCD(liquid crystal display, 액정표시장치)의 핵심 물질인 액정물질을 물리, 화학적인 관점에서 융합연구를 주도하고 있는 액정물질 전문 과학자다. 현재까지, 우리나라에서 액정 디스플레이를 많이 생산해 왔음에도 불구하고, 그 핵심 물질인 액정물질에 대한 기초연구는 해외에 비해 국내 연구의 수준이 뒤떨어진 것이 사실이므로 관련 분야의 지속적인 발전을 위해서는 관련 기초 및 융합연구가 중요하다.
산업계에서도 LCD 관련 R&D 분야는 성숙단계라고는 하지만 최근 플렉시블, 폴더블, 스트레처블 디스플레이를 비롯해 OLED 분야에서도 코팅이 가능한 다양한 기능성 박막 필름이 필요한데, 이에 배향된 액정분자체 기반의 보상 필름이 유력한 후보군으로 떠오르고 있고, 자동차용 각종 디스플레이, 증강현실용 소프트 로보틱스뿐만 아니라 차세대 통신, 안테나 분야 등에도 액정물질 기반의 핵심 연구가 필요한 상황이다.
윤 교수는 디스플레이 분야에서 가장 일반적으로 많이 연구되는 방향성만 있는 네마틱(Nematic)이라고 하는 단순한 액정 상(phase)을 비롯해 차세대 디스플레이 및 디스플레이를 넘어서는 새로운 응용 분야를 열 수 있는 판상형 액정(Smectic LC) 분야에서 두각을 나타내어‘사이언스 어드밴시스’ 등 세계적인 수준의 저널들에 150여 편의 연구 결과를 발표하고 특허 또한 30여 편을 출원 및 등록할 정도로 활발한 연구 활동을 펼치고 있다.
윤 교수의 액정물질 기반 나노 및 마이크로패터닝과 관련한 연구 및 최신 응용연구 성과를 통해 국제액정학회가 인정했기 때문에 윤 교수가 ‘ILCS 중견학술상(Mid-Career Award (LG))’ 수상자로 선정됐다고 관계자는 설명했다.
윤 교수는 현재 ‘초분자 액정물질 및 액정고분자 패터닝’이라는 새로운 분야를 개척 중으로, 기초과학연구뿐만 아니라 차세대 통신 분야에 대해서도 액정물질을 기반으로 융합 기술을 개발하는 연구도 함께 진행하고 있다.
2024.07.26 조회수 4240 종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16 조회수 6160
종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16 조회수 6160 맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27 조회수 5835
맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27 조회수 5835 암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
2023.03.02 조회수 14115
암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
2023.03.02 조회수 14115 면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10 조회수 9061
면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10 조회수 9061 창업원, KAIST Startup Tech Plaza 6일 개최
우리 대학 창업원(원장 김영태)은 6일(수) 오후 2시 판교센터에서 KAIST 스타트업 테크 플라자(KAIST Startup Tech Plaza)를 개최한다.
KAIST 스타트업 테크 플라자는 ▲바이오테크/약학/헬스케어(Biotech/Pharmacy/Healthcare) ▲소재/부품/장비 ▲환경·사회·지배구조(ESG) ▲인공지능/디지털 트랜스포메이션(AI/DT) 등 최첨단 기술 트렌드를 공유하는 자리다. 창업원은 스타트업과 투자자 등 인재가 만나 함께 성장하는 기회의 장을 마련하기 위해 이번 행사를 포함해 올 한 해 동안 총 여섯 번의 스타트업 테크 플라자를 개최할 예정이다.6일 열리는 올해 첫 행사는 의과학 분야를 주제로 전문가 강연과 관련 분야 스타트업 IR(Investor Relations) 피칭 및 스타트업-VC 네트워킹 등의 프로그램을 마련했다. 이정석 KAIST 의과학대학원 교수(지놈인사이트 공동 창업자)가 “의사, 과학자, 사업가 그리고?”라는 주제로 강연한다. 또한, 튜론(TULON), 에아스텍(ERSTEQ), 프라미솝(PROMISOPE), 포엔(4N), 소누스(SONUS) 등 5개 창업기업이 IR 피칭을 진행한다. 이어, 스타트업-VC 네트워킹 및 1:1 맞춤 상담 등이 행사 현장에서 진행된다. 우리 대학 교원, 재학생 및 졸업생 중 창업에 관심이 있는 예비창업가라면 누구나 참여할 수 있으며, 현장 네트워킹 행사를 제외한 전체 순서는 ZOOM으로 중계된다.김영태 창업원장은 "최초·최고 기술 기반의 KAIST 창업가들이 코로나-19와 기술혁신 등으로 인한 대격변의 시기에 적기에 창업하고 빠르게 성장할 수 있도록 창업원의 역할을 지속적으로 강화할 것"이라고 밝혔다.
2022.04.05 조회수 9075
창업원, KAIST Startup Tech Plaza 6일 개최
우리 대학 창업원(원장 김영태)은 6일(수) 오후 2시 판교센터에서 KAIST 스타트업 테크 플라자(KAIST Startup Tech Plaza)를 개최한다.
KAIST 스타트업 테크 플라자는 ▲바이오테크/약학/헬스케어(Biotech/Pharmacy/Healthcare) ▲소재/부품/장비 ▲환경·사회·지배구조(ESG) ▲인공지능/디지털 트랜스포메이션(AI/DT) 등 최첨단 기술 트렌드를 공유하는 자리다. 창업원은 스타트업과 투자자 등 인재가 만나 함께 성장하는 기회의 장을 마련하기 위해 이번 행사를 포함해 올 한 해 동안 총 여섯 번의 스타트업 테크 플라자를 개최할 예정이다.6일 열리는 올해 첫 행사는 의과학 분야를 주제로 전문가 강연과 관련 분야 스타트업 IR(Investor Relations) 피칭 및 스타트업-VC 네트워킹 등의 프로그램을 마련했다. 이정석 KAIST 의과학대학원 교수(지놈인사이트 공동 창업자)가 “의사, 과학자, 사업가 그리고?”라는 주제로 강연한다. 또한, 튜론(TULON), 에아스텍(ERSTEQ), 프라미솝(PROMISOPE), 포엔(4N), 소누스(SONUS) 등 5개 창업기업이 IR 피칭을 진행한다. 이어, 스타트업-VC 네트워킹 및 1:1 맞춤 상담 등이 행사 현장에서 진행된다. 우리 대학 교원, 재학생 및 졸업생 중 창업에 관심이 있는 예비창업가라면 누구나 참여할 수 있으며, 현장 네트워킹 행사를 제외한 전체 순서는 ZOOM으로 중계된다.김영태 창업원장은 "최초·최고 기술 기반의 KAIST 창업가들이 코로나-19와 기술혁신 등으로 인한 대격변의 시기에 적기에 창업하고 빠르게 성장할 수 있도록 창업원의 역할을 지속적으로 강화할 것"이라고 밝혔다.
2022.04.05 조회수 9075 KAIST Crazy Day 전 국민 아이디어 공모전 개최
우리 대학이 파격적으로 실행할 수 있는 도전 과제를 국민의 제안으로 발굴하는 'KAIST Crazy Day 아이디어 공모전’을 개최한다. 올해 5월 중 하루, 파격적(Crazy), 창의적(Creative), 도전적(Challenging)이거나 배려정신(Caring)을 담은 아이디어를 실행하는 `KAIST Crazy Day’”행사를 개최할 예정이다. 일 년에 딱 하루, 평소에는 적용해보기 어려웠던 아이디어를 캠퍼스에서 실행해 혁신문화를 확산하고 구성원들의 창의적인 열정을 장려하겠다는 취지다. 이를 위해, 전 국민을 대상으로 모험적이면서도 창의적인 아이디어를 제안받는 공모전을 이달 14일 시작한다. 상금은 총 1,000만 원 규모다.‘KAIST 1일 총장 되기’, ‘필기 제로 수업해보기’, ‘연구를 위해 연구하지 않기’ ‘직위 대신 이름 부르기’ 등 기존의 관행이나 형식에 얽매이지 않는 혁신적인 시도이면서도 자유로운 사고를 바탕으로 ‘왜’라는 질문을 끊임없이 이끌어내는 아이디어라면 국민 누구나 제안할 수 있다. 다음 달 8일까지 진행되는 공모전은 KAIST 홈페이지(www.kaist.ac.kr) 또는 KAIST 글로벌전략연구소 홈페이지(http://gsi.kaist.ac.kr/)에서 참여할 수 있다. 1인당 1건씩 온라인으로 응모할 수 있으며, 우편 및 방문 신청은 받지 않는다. 우리 대학은 창의성, 혁신성, 진취성, 실행 가능성, 대중의 공감대 등을 평가 기준으로 정하고 내부 및 외부위원이 참여하는 3단계 심사를 통해 최종 수상작을 선정할 예정이다. 대상 1명에게는 상금 500만 원 주어지며, 제안한 아이디어가 5월 개최될 `KAIST Crazy Day‘ 행사에서 실행된다. 이 밖에, 최우수상 1명과 우수상 3명에게는 각각 200만 원과 100만 원의 상금을 수여한다. 이광형 총장은 “하버드대학의 유머 과학잡지 ‘별난 연구 연보(Annals of Improbable Research)’에서는 매년 황당무계한 괴짜 연구에 ‘이그 노벨상(Ig Nobel Prize)’을 수여한다”라고 언급했다. 이어, 이 총장은 “괴짜 아이디어가 노벨상으로 이어진 수많은 사례로 미루어 볼 때 과학기술혁신은 고정관념과 상식의 프레임에서 벗어나는 데서부터 출발한다”라며, “국민이 제안하는 파격적이고도 획기적인 아이디어를 실천해 KAIST의 도전과 실험정신을 계속 이어 나가겠다”라고 밝혔다.
2022.03.11 조회수 10373
KAIST Crazy Day 전 국민 아이디어 공모전 개최
우리 대학이 파격적으로 실행할 수 있는 도전 과제를 국민의 제안으로 발굴하는 'KAIST Crazy Day 아이디어 공모전’을 개최한다. 올해 5월 중 하루, 파격적(Crazy), 창의적(Creative), 도전적(Challenging)이거나 배려정신(Caring)을 담은 아이디어를 실행하는 `KAIST Crazy Day’”행사를 개최할 예정이다. 일 년에 딱 하루, 평소에는 적용해보기 어려웠던 아이디어를 캠퍼스에서 실행해 혁신문화를 확산하고 구성원들의 창의적인 열정을 장려하겠다는 취지다. 이를 위해, 전 국민을 대상으로 모험적이면서도 창의적인 아이디어를 제안받는 공모전을 이달 14일 시작한다. 상금은 총 1,000만 원 규모다.‘KAIST 1일 총장 되기’, ‘필기 제로 수업해보기’, ‘연구를 위해 연구하지 않기’ ‘직위 대신 이름 부르기’ 등 기존의 관행이나 형식에 얽매이지 않는 혁신적인 시도이면서도 자유로운 사고를 바탕으로 ‘왜’라는 질문을 끊임없이 이끌어내는 아이디어라면 국민 누구나 제안할 수 있다. 다음 달 8일까지 진행되는 공모전은 KAIST 홈페이지(www.kaist.ac.kr) 또는 KAIST 글로벌전략연구소 홈페이지(http://gsi.kaist.ac.kr/)에서 참여할 수 있다. 1인당 1건씩 온라인으로 응모할 수 있으며, 우편 및 방문 신청은 받지 않는다. 우리 대학은 창의성, 혁신성, 진취성, 실행 가능성, 대중의 공감대 등을 평가 기준으로 정하고 내부 및 외부위원이 참여하는 3단계 심사를 통해 최종 수상작을 선정할 예정이다. 대상 1명에게는 상금 500만 원 주어지며, 제안한 아이디어가 5월 개최될 `KAIST Crazy Day‘ 행사에서 실행된다. 이 밖에, 최우수상 1명과 우수상 3명에게는 각각 200만 원과 100만 원의 상금을 수여한다. 이광형 총장은 “하버드대학의 유머 과학잡지 ‘별난 연구 연보(Annals of Improbable Research)’에서는 매년 황당무계한 괴짜 연구에 ‘이그 노벨상(Ig Nobel Prize)’을 수여한다”라고 언급했다. 이어, 이 총장은 “괴짜 아이디어가 노벨상으로 이어진 수많은 사례로 미루어 볼 때 과학기술혁신은 고정관념과 상식의 프레임에서 벗어나는 데서부터 출발한다”라며, “국민이 제안하는 파격적이고도 획기적인 아이디어를 실천해 KAIST의 도전과 실험정신을 계속 이어 나가겠다”라고 밝혔다.
2022.03.11 조회수 10373 면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
2021.10.21 조회수 12983
면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
2021.10.21 조회수 12983 인공지능 이용 면역항암 세포 3차원 분석기술 개발
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀이 면역항암 세포의 활동을 정밀하게 측정하고 분석할 수 있는 새로운 3차원 인공지능 분석기술을 개발했다고 28일 밝혔다.
체내에서 면역세포를 추출한 후, 외부에서 면역 능력을 강화시키고 다시 환자에게 주입해 암을 치료하는 방식을 `입양전달 면역세포 치료(adoptive immune cell therapy)'라고 부른다. 이 치료방식은 면역세포 치료법 중 가장 많은 주목을 받는 기술이다. `키메릭 항원 수용체' 또는 `CAR(Chimeric Antigen Receptor)'라고도 불리는 데 유전자 재조합기술을 이용해 T세포와 같은 면역세포를 변형해 암세포와의 반응을 유도해 사멸시키는 치료 방법이다.
특히 CAR-T세포 치료는 높은 치료 효과를 보여 차세대 암 치료제로 급부상하고 있다. 2017년 난치성 B세포 급성 림프구성 백혈병 치료제 판매 승인을 시작으로 현재 3종의 CAR-T 치료제가 판매 승인을 받았으며, 전 세계적으로 약 1,000건 이상의 임상 시험이 진행 중이다. 그러나 아직 우리나라에서는 진행 중인 임상 시험이 전무한 실정이다.
CAR-T 기술을 이용한 암 치료 방법들이 속속 개발되고 있지만, CAR-T세포에 대한 세포‧분자 생물학적 메커니즘은 아직 많은 부분이 알려지지 않았다. 특히, CAR-T세포가 표적 암세포를 인지해 결합한 후 `면역 시냅스 (immunological synapse, 이하 IS)'를 형성해 물질을 전달하고 암세포의 사멸을 유도하는데, 두 세포 간의 거리와 같은 IS의 형태 정보는 T세포 활성화 유도와 관련이 높다고 알려져 있지만 구체적인 내용을 파악하기 어렵기 때문에 이에 대한 연구가 활발히 진행 중이다.
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀은 CAR-T세포의 IS를 정밀하고 체계적으로 연구할 수 있는 새로운 기술을 개발했다. 3D 홀로그래피 현미경 기술을 이용해, 염색이나 전처리 없이 살아있는 상태의 CAR-T세포와 표적 암세포 간의 상호작용을 고속으로 측정하고 기존에는 관찰하기 어려운 CAR-T와 암세포 간의 IS를 고해상도로 실시간 측정했다. 또한 이렇게 측정한 3D 세포 영상을 인공지능 신경망(Convolutional Neural Network, CNN)을 이용해 분석하고, 3차원 공간에서 정확하게 IS 정보를 정량적으로 추출할 수 있는 기술을 자체 개발했다.
공동연구팀은 또 이 기술을 활용해 빠른 CAR-T 면역 관문 형성 메커니즘을 추적할 수 있었을 뿐만 아니라, IS의 형태학적 특성이 CAR-T의 항암 효능과 연관이 있음을 확인했다. 연구팀은 3차원 IS 정보가 새로운 표적 항암 치료제의 초기 연구에 필요한 정량적 지표를 제공할 것이라고 기대하고 있다.
이번 연구에는 우리 대학 기술을 바탕으로 창업한 2개 기업이 공동으로 참여했다. 3차원 홀로그래픽 현미경을 상업화한 토모큐브 社의 현미경 장비를 이용해 면역세포를 측정하는 한편 토모큐브 社의 인공지능 연구팀이 알고리즘 개발에 참여했다. 이밖에 국내 최초 CAR-T 기반 치료제 기업인 ㈜큐로셀도 연구에 함께 참여해 이 같은 성과를 거두는 데 성공했다.
물리학과 이무성 박사과정 학생, 생명과학과 이영호 박사, 물리학과 송진엽 학부생 (現 메사추세츠 공과대학(MIT) 물리학과 박사과정)이 공동 제1 저자로 참여한 이번 연구는 국제적으로 권위를 인정받는 생물학술지인 `이라이프(eLife)' 12월 17일 字 온라인판을 통해 공개됐으며 지난 21일 字에 공식 게재됐다.
(논문명 : Deep-learning based three-dimensional label-free tracking and analysis of immunological synapses of CAR-T cells)
한편 이번 연구는 한국연구재단 리더연구사업, 바이오·의료기술개발사업, 중견연구자지원사업, KAIST Up program의 지원을 받아 수행됐다.
2021.01.29 조회수 77286
인공지능 이용 면역항암 세포 3차원 분석기술 개발
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀이 면역항암 세포의 활동을 정밀하게 측정하고 분석할 수 있는 새로운 3차원 인공지능 분석기술을 개발했다고 28일 밝혔다.
체내에서 면역세포를 추출한 후, 외부에서 면역 능력을 강화시키고 다시 환자에게 주입해 암을 치료하는 방식을 `입양전달 면역세포 치료(adoptive immune cell therapy)'라고 부른다. 이 치료방식은 면역세포 치료법 중 가장 많은 주목을 받는 기술이다. `키메릭 항원 수용체' 또는 `CAR(Chimeric Antigen Receptor)'라고도 불리는 데 유전자 재조합기술을 이용해 T세포와 같은 면역세포를 변형해 암세포와의 반응을 유도해 사멸시키는 치료 방법이다.
특히 CAR-T세포 치료는 높은 치료 효과를 보여 차세대 암 치료제로 급부상하고 있다. 2017년 난치성 B세포 급성 림프구성 백혈병 치료제 판매 승인을 시작으로 현재 3종의 CAR-T 치료제가 판매 승인을 받았으며, 전 세계적으로 약 1,000건 이상의 임상 시험이 진행 중이다. 그러나 아직 우리나라에서는 진행 중인 임상 시험이 전무한 실정이다.
CAR-T 기술을 이용한 암 치료 방법들이 속속 개발되고 있지만, CAR-T세포에 대한 세포‧분자 생물학적 메커니즘은 아직 많은 부분이 알려지지 않았다. 특히, CAR-T세포가 표적 암세포를 인지해 결합한 후 `면역 시냅스 (immunological synapse, 이하 IS)'를 형성해 물질을 전달하고 암세포의 사멸을 유도하는데, 두 세포 간의 거리와 같은 IS의 형태 정보는 T세포 활성화 유도와 관련이 높다고 알려져 있지만 구체적인 내용을 파악하기 어렵기 때문에 이에 대한 연구가 활발히 진행 중이다.
우리 대학 물리학과 박용근, 생명과학과 김찬혁 교수 공동연구팀은 CAR-T세포의 IS를 정밀하고 체계적으로 연구할 수 있는 새로운 기술을 개발했다. 3D 홀로그래피 현미경 기술을 이용해, 염색이나 전처리 없이 살아있는 상태의 CAR-T세포와 표적 암세포 간의 상호작용을 고속으로 측정하고 기존에는 관찰하기 어려운 CAR-T와 암세포 간의 IS를 고해상도로 실시간 측정했다. 또한 이렇게 측정한 3D 세포 영상을 인공지능 신경망(Convolutional Neural Network, CNN)을 이용해 분석하고, 3차원 공간에서 정확하게 IS 정보를 정량적으로 추출할 수 있는 기술을 자체 개발했다.
공동연구팀은 또 이 기술을 활용해 빠른 CAR-T 면역 관문 형성 메커니즘을 추적할 수 있었을 뿐만 아니라, IS의 형태학적 특성이 CAR-T의 항암 효능과 연관이 있음을 확인했다. 연구팀은 3차원 IS 정보가 새로운 표적 항암 치료제의 초기 연구에 필요한 정량적 지표를 제공할 것이라고 기대하고 있다.
이번 연구에는 우리 대학 기술을 바탕으로 창업한 2개 기업이 공동으로 참여했다. 3차원 홀로그래픽 현미경을 상업화한 토모큐브 社의 현미경 장비를 이용해 면역세포를 측정하는 한편 토모큐브 社의 인공지능 연구팀이 알고리즘 개발에 참여했다. 이밖에 국내 최초 CAR-T 기반 치료제 기업인 ㈜큐로셀도 연구에 함께 참여해 이 같은 성과를 거두는 데 성공했다.
물리학과 이무성 박사과정 학생, 생명과학과 이영호 박사, 물리학과 송진엽 학부생 (現 메사추세츠 공과대학(MIT) 물리학과 박사과정)이 공동 제1 저자로 참여한 이번 연구는 국제적으로 권위를 인정받는 생물학술지인 `이라이프(eLife)' 12월 17일 字 온라인판을 통해 공개됐으며 지난 21일 字에 공식 게재됐다.
(논문명 : Deep-learning based three-dimensional label-free tracking and analysis of immunological synapses of CAR-T cells)
한편 이번 연구는 한국연구재단 리더연구사업, 바이오·의료기술개발사업, 중견연구자지원사업, KAIST Up program의 지원을 받아 수행됐다.
2021.01.29 조회수 77286 차세대 발광 물질 카본닷의 발광 특성 변화 메커니즘을 규명
우리 대학 생명화학공학과 김도현 교수 연구팀이 차세대 발광 물질인 이중 발광 *카본닷의 농도 의존성 발광 특성 변화 메커니즘을 규명했다고 5일 밝혔다.
☞ 카본닷(carbon-dot): 탄소 기반의 발광 물질로 풍부한 원료와 낮은 독성 및 환경친화적인 장점 때문에 기존에 상용화돼 있는 유기 발광체, 양자점(퀀텀닷)을 대체할 수 있는 차세대 발광 물질로 부상하고 있음.
김도현 교수 연구팀은 청색 및 적색을 이중 발광하는 카본닷을 합성한 후 농도에 따른 발광 특성 변화를 관찰해 카본닷 발광 소스 간 상호작용에 따른 현상을 분석했다. 김도현 교수팀의 연구 결과는 카본닷의 발광 특성 제어는 물론 이론적 이해를 가능케 함으로써 이중 발광 카본닷의 복잡한 발광 특성 해석에 새로운 근거를 제시한 것으로 평가받고 있다.
우리 대학 유효정 박사과정, 곽병은 석박사통합과정이 각각 제1, 제2 저자로 참여한 이번 연구는 국제 학술지 `피지컬 케미스트리 케미컬 피직스(Physical Chemistry Chemical Physics, PCCP)' 9월 22권 36호 표지논문으로 선정됐다. (논문명 : Interparticle distance as a key factor for controlling the dual-emission properties of carbon dots)
카본닷은 다양한 발광 준위 에너지를 동시에 갖기 때문에 다색발광이 가능하며 농도 변화에 따른 발광 특성 변화를 보인다. 이 같은 특성은 기존 발광 물질인 유기 발광체, 양자점과는 구별되는 카본닷만이 지닌 독자적이고 유용한 특성이다.
최근 들어 다양한 분야에 카본닷의 발광 특성을 이용하려는 연구가 활발히 진행되고 있다. 특히 백색광 및 광학 센서 분야에서 다색발광은 하나의 형광체만으로도 장치 구현이 가능하고 레퍼런스 신호를 제공해 센서의 정확도를 높일 수 있다는 장점 때문에 카본닷 다색발광의 구현과 제어가 중요한 연구과제로 떠오르고 있다.
카본닷은 다색발광과 농도 변화에 따라 다양한 발광 특성을 보이지만 매우 드물게 만들어진다는 게 약점이다. 또 복수 발광 소스 사이의 복잡한 상호작용으로 인해 카본닷의 다색발광과 농도 변화에 따른 다양한 발광 메커니즘을 규명한 연구가 거의 이뤄지지 않고 있다.
연구팀은 이런 문제해결을 위해 청색·적색 이중 발광 카본닷을 합성해 카본닷의 입자 간 거리가 카본닷 발광 특성 변화에 중요한 역할을 한다는 점을 밝히는 연구를 진행했다.
기존의 농도 변화에 따른 카본닷의 발광 특성 변화를 용매 의존 발색 현상에 빗대 수소 결합 영향에 의한 현상으로 해석한 사례가 있지만, 김 교수 연구팀은 카본닷 발광 현상의 농도 의존성이 수소 결합과는 상관없이 입자 간 거리에 의해 제어되는 현상일 수 있다는 가능성에 주목했다.
연구팀이 농도 변화에 따른 카본닷의 이중 발광 특성의 변화를 관찰한 결과, 임계 농도에서 적색 발광에 가장 적합한 입자 간 거리를 형성하고, 이 농도를 전후로 청색 발광이 강해지면서 카본닷의 농도별 이중 발광 특성이 변화하는 현상을 확인했다.
연구팀은 이를 기반으로 분광 분석을 통해 이중 발광의 청색 및 적색의 두 발광 소스를 각각 표면 작용기와 코어의 결합구조로 구분해 농도 변화에 따라 각 발광 소스의 이중 발광에 대한 기여도가 변화한다는 구체적인 설명을 제시했다. 연구팀은 특히 고농도 영역에서 두 발광 소스의 상호작용에 대한 메커니즘 제시를 통해 입자 간 거리 변화 때문에 이중 발광 특성이 제어된다는 결과를 얻었다.
연구팀이 합성한 이중 발광 카본닷은 단일 형광체로서 청색과 적색 발광을 동시 구현할 수 있고 특성 제어가 가능함에 따라 혼합색 구현은 물론 색 변화에 의한 센싱에 사용할 수 있다.
연구팀은 또 이중 발광 카본닷의 농도 조절을 통해 순수한 백색에 근접한 백색 LED 구현에도 성공하는 한편 색 변화에 의한 pH 센싱에 활용해 pH에 따른 청색·적색의 상대적 발광 세기 변화를 통해 pH 추정이 가능함을 보였다. 기존에 제시됐던 카본닷이 고도화된 기능성을 가진 발광체로써 사용될 수 있다는 가능성을 이번 연구를 통해 다시 한 번 입증한 것이다.
제1 저자인 유효정 박사과정 학생은 "카본닷 입자 간 거리에 따라 발광 소스의 상호작용이 일어나 농도에 따른 발광 특성에 변화가 일어난다는 해석은 기존 연구에서 간과됐던 부분ˮ이라면서 "이중 발광 현상에 대한 분석과 함께 이 연구 결과가 카본닷 발광 현상 규명에 있어 새로운 관점을 제시한 것ˮ이라고 의미를 부여했다.
이번 연구는 한국연구재단 이공분야기초연구사업의 지원을 받아 수행됐다.
2020.11.05 조회수 30106
차세대 발광 물질 카본닷의 발광 특성 변화 메커니즘을 규명
우리 대학 생명화학공학과 김도현 교수 연구팀이 차세대 발광 물질인 이중 발광 *카본닷의 농도 의존성 발광 특성 변화 메커니즘을 규명했다고 5일 밝혔다.
☞ 카본닷(carbon-dot): 탄소 기반의 발광 물질로 풍부한 원료와 낮은 독성 및 환경친화적인 장점 때문에 기존에 상용화돼 있는 유기 발광체, 양자점(퀀텀닷)을 대체할 수 있는 차세대 발광 물질로 부상하고 있음.
김도현 교수 연구팀은 청색 및 적색을 이중 발광하는 카본닷을 합성한 후 농도에 따른 발광 특성 변화를 관찰해 카본닷 발광 소스 간 상호작용에 따른 현상을 분석했다. 김도현 교수팀의 연구 결과는 카본닷의 발광 특성 제어는 물론 이론적 이해를 가능케 함으로써 이중 발광 카본닷의 복잡한 발광 특성 해석에 새로운 근거를 제시한 것으로 평가받고 있다.
우리 대학 유효정 박사과정, 곽병은 석박사통합과정이 각각 제1, 제2 저자로 참여한 이번 연구는 국제 학술지 `피지컬 케미스트리 케미컬 피직스(Physical Chemistry Chemical Physics, PCCP)' 9월 22권 36호 표지논문으로 선정됐다. (논문명 : Interparticle distance as a key factor for controlling the dual-emission properties of carbon dots)
카본닷은 다양한 발광 준위 에너지를 동시에 갖기 때문에 다색발광이 가능하며 농도 변화에 따른 발광 특성 변화를 보인다. 이 같은 특성은 기존 발광 물질인 유기 발광체, 양자점과는 구별되는 카본닷만이 지닌 독자적이고 유용한 특성이다.
최근 들어 다양한 분야에 카본닷의 발광 특성을 이용하려는 연구가 활발히 진행되고 있다. 특히 백색광 및 광학 센서 분야에서 다색발광은 하나의 형광체만으로도 장치 구현이 가능하고 레퍼런스 신호를 제공해 센서의 정확도를 높일 수 있다는 장점 때문에 카본닷 다색발광의 구현과 제어가 중요한 연구과제로 떠오르고 있다.
카본닷은 다색발광과 농도 변화에 따라 다양한 발광 특성을 보이지만 매우 드물게 만들어진다는 게 약점이다. 또 복수 발광 소스 사이의 복잡한 상호작용으로 인해 카본닷의 다색발광과 농도 변화에 따른 다양한 발광 메커니즘을 규명한 연구가 거의 이뤄지지 않고 있다.
연구팀은 이런 문제해결을 위해 청색·적색 이중 발광 카본닷을 합성해 카본닷의 입자 간 거리가 카본닷 발광 특성 변화에 중요한 역할을 한다는 점을 밝히는 연구를 진행했다.
기존의 농도 변화에 따른 카본닷의 발광 특성 변화를 용매 의존 발색 현상에 빗대 수소 결합 영향에 의한 현상으로 해석한 사례가 있지만, 김 교수 연구팀은 카본닷 발광 현상의 농도 의존성이 수소 결합과는 상관없이 입자 간 거리에 의해 제어되는 현상일 수 있다는 가능성에 주목했다.
연구팀이 농도 변화에 따른 카본닷의 이중 발광 특성의 변화를 관찰한 결과, 임계 농도에서 적색 발광에 가장 적합한 입자 간 거리를 형성하고, 이 농도를 전후로 청색 발광이 강해지면서 카본닷의 농도별 이중 발광 특성이 변화하는 현상을 확인했다.
연구팀은 이를 기반으로 분광 분석을 통해 이중 발광의 청색 및 적색의 두 발광 소스를 각각 표면 작용기와 코어의 결합구조로 구분해 농도 변화에 따라 각 발광 소스의 이중 발광에 대한 기여도가 변화한다는 구체적인 설명을 제시했다. 연구팀은 특히 고농도 영역에서 두 발광 소스의 상호작용에 대한 메커니즘 제시를 통해 입자 간 거리 변화 때문에 이중 발광 특성이 제어된다는 결과를 얻었다.
연구팀이 합성한 이중 발광 카본닷은 단일 형광체로서 청색과 적색 발광을 동시 구현할 수 있고 특성 제어가 가능함에 따라 혼합색 구현은 물론 색 변화에 의한 센싱에 사용할 수 있다.
연구팀은 또 이중 발광 카본닷의 농도 조절을 통해 순수한 백색에 근접한 백색 LED 구현에도 성공하는 한편 색 변화에 의한 pH 센싱에 활용해 pH에 따른 청색·적색의 상대적 발광 세기 변화를 통해 pH 추정이 가능함을 보였다. 기존에 제시됐던 카본닷이 고도화된 기능성을 가진 발광체로써 사용될 수 있다는 가능성을 이번 연구를 통해 다시 한 번 입증한 것이다.
제1 저자인 유효정 박사과정 학생은 "카본닷 입자 간 거리에 따라 발광 소스의 상호작용이 일어나 농도에 따른 발광 특성에 변화가 일어난다는 해석은 기존 연구에서 간과됐던 부분ˮ이라면서 "이중 발광 현상에 대한 분석과 함께 이 연구 결과가 카본닷 발광 현상 규명에 있어 새로운 관점을 제시한 것ˮ이라고 의미를 부여했다.
이번 연구는 한국연구재단 이공분야기초연구사업의 지원을 받아 수행됐다.
2020.11.05 조회수 30106 美 화학공학회 주최 케미카 대회 국내 예선 우승
(좌측부터) 고동연 교수, 정석영, 슈브로닐 센구프토, 홍지현, 이건호, 박규범, 조슈아 훌리오 아디드자자 학생
우리 대학 학부생으로 구성된 카이탈리스트(KAItalyst, 지도교수 생명화학공학과 고동연)팀이 지난 7월 20일(토) 대전 본원에서 열린 미국 화학공학회(AIChE) 케미카(Chem-E-Car) 한국 지역 예선 대회에서 우승을 차지했다.
케미카 대회는 화학반응으로 구동되는 모형 자동차를 제작하고 그 차량을 제어하는 기술 수준을 겨루는 대회다. 지난 1999년 미국 화학공학회에서 첫 대회를 개최한 이후 전 세계 대학생들이 참여하고 있다.
우리대학은 2014년 처음으로 대회에 출전해 2016년에는 최종 우승을 차지했으며, 2017년과 2018년에는 모스트 컨시스턴트 어워드(Most Consistent Award)를 연속으로 수상했다.
미국 화학공학회에는 대회에 기여한 KAIST의 공로와 역량을 인정해 올해는 공식 지역 예선을 유치할 것을 요청해왔다. 이에 생명화학공학과(학과장 이재우)가 주축이 되어 본선 주최 측이 직접 파견한 2명의 스태프가 관리·감독하는 케미카 한국 지역 예선 대회를 국내 최초로 개최했다.
지난 4월 중순부터 약 한 달 반 동안 한국 화학공학회를 통해 지역 예선에 참여할 총 4개의 팀을 선발하는 공모를 진행했다. 대회에 참가하기 위해서는 4인 이상으로 구성된 대학생 팀이 화학반응으로 구동되는 모형 자동차를 제작한 뒤 정확하게 움직여야 하는 기술을 구현해야 한다.
첫 대회 개최 소식에 여러 대학이 참가 의사를 밝혔지만, 기술 구현에 실패해 KAIST 생명화학공학과와 서울대학교 화학생물공학부 두 팀만이 참가할 수 있었다.
생명화학공학과 홍지현(22세), 정석영(20세), 이건호(20세), 박규범(19세), 조슈아 훌리오 아디드자자(21세, Joshua Julio Adidjaja) 씨와 기계공학과 슈브로닐 센구프토(21세, Shubhranil Sengupta) 씨 등 총 6명의 학부생으로 구성된 카이탈리스트팀은 화학 반응이 신속하고 정확한 요오드시계반응(iodine clock reaction)을 이용하는 한편 바나듐 산화환원 화학전지를 통해 안정적인 출력을 갖는 자동차를 제작했다.
케미카 대회 규칙상 반드시 화학반응으로만 자동차를 제어해야 하며, 경연 대회 현장에서 주행할 거리와 수송할 화물의 무게가 결정된다. 당일에 부여받은 조건이 적용된 모형 자동차를 활용해 목표 지점까지 도달한 시간과 정확도를 비교해 승패를 가린다. 즉, 화학 반응을 정밀하게 제어할 수 있어야 좋은 성적을 거둘 수 있다.
KAIST 팀은 경연 당일 미션으로 제시된 22.5m의 주행거리 중 서울대 팀보다 결승지점에 1.5m 이상 근접하게 접근해 승리를 거뒀다.
우승을 차지한 KAIST 팀에는 본선 진출권과 함께 200달러의 상금이 수여됐으며, 서울대 팀에는 100달러의 상금이 주어졌다.
카이탈리스트의 팀 리더인 홍지현 씨는 "이런 차를 제작하고 구동해본 것이 처음이라 여러 문제점이 있었지만 계속된 노력을 통해 좋은 결과를 낼 수 있었다.ˮ며 이어 "11월에 열리는 국제대회에서도 좋은 결과를 내도록 최선을 다하겠다ˮ고 말했다.
본선 대회는 올해 11월 美 플로리다주 올랜도에서 열리는 미국 화학공학회 정기 총회(AIChE Fall Meeting)에서 개최되며 조지아공대, 카네기멜론대학 등 50개 대학이 참여할 예정이다.
카이탈리스트 팀을 지도한 고동연(생명화학공학과) 교수는 "KAIST가 올해 국내 최초로 개최한 케미카 한국 지역 예선이 시작점이 되어 앞으로 보다 많은 대학이 함께 참여하고 선의의 경쟁을 펼치는 대회로 성장하길 바란다ˮ고 전했다.
2019.07.31 조회수 13222
美 화학공학회 주최 케미카 대회 국내 예선 우승
(좌측부터) 고동연 교수, 정석영, 슈브로닐 센구프토, 홍지현, 이건호, 박규범, 조슈아 훌리오 아디드자자 학생
우리 대학 학부생으로 구성된 카이탈리스트(KAItalyst, 지도교수 생명화학공학과 고동연)팀이 지난 7월 20일(토) 대전 본원에서 열린 미국 화학공학회(AIChE) 케미카(Chem-E-Car) 한국 지역 예선 대회에서 우승을 차지했다.
케미카 대회는 화학반응으로 구동되는 모형 자동차를 제작하고 그 차량을 제어하는 기술 수준을 겨루는 대회다. 지난 1999년 미국 화학공학회에서 첫 대회를 개최한 이후 전 세계 대학생들이 참여하고 있다.
우리대학은 2014년 처음으로 대회에 출전해 2016년에는 최종 우승을 차지했으며, 2017년과 2018년에는 모스트 컨시스턴트 어워드(Most Consistent Award)를 연속으로 수상했다.
미국 화학공학회에는 대회에 기여한 KAIST의 공로와 역량을 인정해 올해는 공식 지역 예선을 유치할 것을 요청해왔다. 이에 생명화학공학과(학과장 이재우)가 주축이 되어 본선 주최 측이 직접 파견한 2명의 스태프가 관리·감독하는 케미카 한국 지역 예선 대회를 국내 최초로 개최했다.
지난 4월 중순부터 약 한 달 반 동안 한국 화학공학회를 통해 지역 예선에 참여할 총 4개의 팀을 선발하는 공모를 진행했다. 대회에 참가하기 위해서는 4인 이상으로 구성된 대학생 팀이 화학반응으로 구동되는 모형 자동차를 제작한 뒤 정확하게 움직여야 하는 기술을 구현해야 한다.
첫 대회 개최 소식에 여러 대학이 참가 의사를 밝혔지만, 기술 구현에 실패해 KAIST 생명화학공학과와 서울대학교 화학생물공학부 두 팀만이 참가할 수 있었다.
생명화학공학과 홍지현(22세), 정석영(20세), 이건호(20세), 박규범(19세), 조슈아 훌리오 아디드자자(21세, Joshua Julio Adidjaja) 씨와 기계공학과 슈브로닐 센구프토(21세, Shubhranil Sengupta) 씨 등 총 6명의 학부생으로 구성된 카이탈리스트팀은 화학 반응이 신속하고 정확한 요오드시계반응(iodine clock reaction)을 이용하는 한편 바나듐 산화환원 화학전지를 통해 안정적인 출력을 갖는 자동차를 제작했다.
케미카 대회 규칙상 반드시 화학반응으로만 자동차를 제어해야 하며, 경연 대회 현장에서 주행할 거리와 수송할 화물의 무게가 결정된다. 당일에 부여받은 조건이 적용된 모형 자동차를 활용해 목표 지점까지 도달한 시간과 정확도를 비교해 승패를 가린다. 즉, 화학 반응을 정밀하게 제어할 수 있어야 좋은 성적을 거둘 수 있다.
KAIST 팀은 경연 당일 미션으로 제시된 22.5m의 주행거리 중 서울대 팀보다 결승지점에 1.5m 이상 근접하게 접근해 승리를 거뒀다.
우승을 차지한 KAIST 팀에는 본선 진출권과 함께 200달러의 상금이 수여됐으며, 서울대 팀에는 100달러의 상금이 주어졌다.
카이탈리스트의 팀 리더인 홍지현 씨는 "이런 차를 제작하고 구동해본 것이 처음이라 여러 문제점이 있었지만 계속된 노력을 통해 좋은 결과를 낼 수 있었다.ˮ며 이어 "11월에 열리는 국제대회에서도 좋은 결과를 내도록 최선을 다하겠다ˮ고 말했다.
본선 대회는 올해 11월 美 플로리다주 올랜도에서 열리는 미국 화학공학회 정기 총회(AIChE Fall Meeting)에서 개최되며 조지아공대, 카네기멜론대학 등 50개 대학이 참여할 예정이다.
카이탈리스트 팀을 지도한 고동연(생명화학공학과) 교수는 "KAIST가 올해 국내 최초로 개최한 케미카 한국 지역 예선이 시작점이 되어 앞으로 보다 많은 대학이 함께 참여하고 선의의 경쟁을 펼치는 대회로 성장하길 바란다ˮ고 전했다.
2019.07.31 조회수 13222 2019 CHIP 해외 자문단 초청 워크숍 개최
〈 (왼쪽부터)데이빗 슈베르트(David Schubert) 라이프 사이언스 파트너스 최고운영책임자,
다니엘 김(Daniel Kim) 텍사스 대학 신경외과 전문의, 베른트 스토바쪄(Bernd Stowasser) 사노피 유럽 민관협력 담당 임원, 조지 맥랜든(George Mclendon) 엠엘바이오 이사 〉
우리 대학 바이오헬스케어 혁신정책센터(Center for Bio-Healthcare Innovation & Policy, 이하 CHIP)가 오는 7월 1일부터 이틀간 서울 강남쉐라톤팰리스 호텔에서 ‘2019 CHIP 해외 자문단 초청 워크숍’ 개최한다.
올해로 5회째를 맞는 이번 국제 워크숍은 ‘글로벌 오픈이노베이션 플랫폼 구축과 지속가능한 바이오투자 생태계 조성’을 주제로 열린다. 국내 제약사·벤처·벤처캐피털·의료기관·정부기관 전문가들이 모여 바이오헬스 산업 육성을 위한 미래전략을 도출하는 자리다.
글로벌 제약사 사노피의 유럽 민관협력 담당 임원인 베른트 스토바쪄(Bernd Stowasser) 박사, 미국의 혁신신약 전문 액셀러레이터 라이프 사이언스 파트너스(Life Science Partners)의 데이빗 슈베르트(David Schubert) 최고운영책임자, 전 캐롤라이나 헬스케어 시스템의 부회장이자 현재 신약개발 벤처 엠엘바이오(MLBio)의 이사인 조지 맥랜든(George Mclendon) 박사, 텍사스 대학 신경외과 전문의이자 의료로봇 전문가인 다니엘 김(Daniel Kim) 등이 자문단으로 참여한다.
7월 1일 오후 2시부터 진행되는 첫날 워크숍은 정호철 이화여대 약대 특임교수와 김태억 범부처신약사업단 사업개발본부장이 좌장을 맡는다. 총 2개의 세션에서 ▲글로벌 신약개발의 동향 및 미래 방향 ▲바이오헬스 산업에서 글로벌 연구개발 협력의 필요성과 글로벌 동향 ▲IMI(Innovative Medicines Initiative(혁신신약이니셔티브),이하 IMI) 3의 거버넌스 및 한국-EU 공동 R&D의 시너지 ▲IMI와 연구개발 협력이 필요한 분야 및 협력방향 등을 세부과제로 다뤄 신약 개발 분야에서의 국제 연구개발 협력을 통한 글로벌 오픈이노베이션 플랫폼 구축을 논의한다.
특히, 국내 신약개발 생태계의 고질적 약점으로 지적되는 중개연구역량·글로벌 수준의 신약개발 연구인력 부족·글로벌 제약기업 및 선진국 인허가 기관과 네트워크 부재에 관한 해법 모색에 나선다.
그동안 국내 신약개발 지원기관 및 관련 기업들이 세계 최대 민관협력 신약개발 네트워크인 EU-IMI에 참여하고 싶다는 의사를 개별적으로 전달했으나 한국이 비 EU국가라는 이유로 성사되지 못했다.
KAIST 바이오헬스케어 혁신정책센터는 국내·외 자문위원들과 함께 IMI 및 유럽제약협회(EFPIA)와 지난 3년간의 논의해왔으며, 연구개발 비용의 자체 부담을 조건으로 한국의 IMI 참여 지지를 확보했다. 또한, 정부관계자와 함께 한국이 IMI에 참여해야 하는 필요성에 대해 논의하는 중이다.
이번 워크숍을 통해 한국-EU IMI 공동 신약연구 프로그램을 구축할 임시추진위원회를 구성하고 오송·대구 첨단의료복합단지를 글로벌 진출의 허브로 육성해 한국이 EU-IMI의 일원으로 활동하는 방안에 대해 본격적으로 논의할 예정이다.
세포·유전자 치료제 등 미래 정밀의료 의약품 개발과 민간 기업이 개발을 회피하거나 실패 위험이 높은 수퍼박테리아 항생제, 치매를 포함한 뇌질환 치료제 등의 국내 개발을 가속하기 위해서다.
7월 2일은 지속가능한 바이오투자 생태계 조성과 국내 신약·의료기기 스타트업의 글로벌 사업화 가능성을 전망해보는 자리로 마련된다.
조영국 글로벌밸류네트웍스 대표, 김종백 법무법인 지안 변호사, 이남구 워터스 코리아 대표가 좌장을 맡아 ▲바이오기업 가치 평가와 기업공개 ▲바이오텍 초기 투자의 다원화 ▲의료기기 혁신을 위한 투자 등의 세부 과제를 다룰 예정이다.
특히, 바이오 분야 창업부터 코스닥 상장까지 경험을 공유하기 위해 유진산 파맵신 대표와 윤원수 티앤알바이오팹 대표도 기업 사례 발표자로 나선다.
둘째 날 오후 행사에서는 신약개발 스타트업과 의료기기 스타트업의 글로벌 사업화 가능성을 탐색하는 기업 소개와 리뷰(Pre-IR) 시간이 마련된다. 작년에 이 세션에서 소개된 5개의 스타트업 중 2곳이 6개월 이내에 시리즈 A 투자 유치에 성공한 바 있다.
이번 행사는 KAIST 바이오헬스케어 혁신정책센터가 주최·주관하고 보건복지부와 보건산업진흥원, 한강서사이어티가 후원한다.
채수찬 KAIST 바이오헬스케어 혁신정책센터장은 “이번 워크숍을 통해 IMI와 같은 민관협력체 활용과 우리나라 바이오헬스 산업의 글로벌 진출 가속과 지속가능한 발전 방안이 마련되기를 기대한다”고 밝혔다.
KAIST 2019 CHIP 해외 자문단 초청 워크숍은 홈페이지( http://chip.kaist.ac.kr )를 통해 참석 신청이 가능하다.(문의:02-3498-7558)
2019.06.27 조회수 15694
2019 CHIP 해외 자문단 초청 워크숍 개최
〈 (왼쪽부터)데이빗 슈베르트(David Schubert) 라이프 사이언스 파트너스 최고운영책임자,
다니엘 김(Daniel Kim) 텍사스 대학 신경외과 전문의, 베른트 스토바쪄(Bernd Stowasser) 사노피 유럽 민관협력 담당 임원, 조지 맥랜든(George Mclendon) 엠엘바이오 이사 〉
우리 대학 바이오헬스케어 혁신정책센터(Center for Bio-Healthcare Innovation & Policy, 이하 CHIP)가 오는 7월 1일부터 이틀간 서울 강남쉐라톤팰리스 호텔에서 ‘2019 CHIP 해외 자문단 초청 워크숍’ 개최한다.
올해로 5회째를 맞는 이번 국제 워크숍은 ‘글로벌 오픈이노베이션 플랫폼 구축과 지속가능한 바이오투자 생태계 조성’을 주제로 열린다. 국내 제약사·벤처·벤처캐피털·의료기관·정부기관 전문가들이 모여 바이오헬스 산업 육성을 위한 미래전략을 도출하는 자리다.
글로벌 제약사 사노피의 유럽 민관협력 담당 임원인 베른트 스토바쪄(Bernd Stowasser) 박사, 미국의 혁신신약 전문 액셀러레이터 라이프 사이언스 파트너스(Life Science Partners)의 데이빗 슈베르트(David Schubert) 최고운영책임자, 전 캐롤라이나 헬스케어 시스템의 부회장이자 현재 신약개발 벤처 엠엘바이오(MLBio)의 이사인 조지 맥랜든(George Mclendon) 박사, 텍사스 대학 신경외과 전문의이자 의료로봇 전문가인 다니엘 김(Daniel Kim) 등이 자문단으로 참여한다.
7월 1일 오후 2시부터 진행되는 첫날 워크숍은 정호철 이화여대 약대 특임교수와 김태억 범부처신약사업단 사업개발본부장이 좌장을 맡는다. 총 2개의 세션에서 ▲글로벌 신약개발의 동향 및 미래 방향 ▲바이오헬스 산업에서 글로벌 연구개발 협력의 필요성과 글로벌 동향 ▲IMI(Innovative Medicines Initiative(혁신신약이니셔티브),이하 IMI) 3의 거버넌스 및 한국-EU 공동 R&D의 시너지 ▲IMI와 연구개발 협력이 필요한 분야 및 협력방향 등을 세부과제로 다뤄 신약 개발 분야에서의 국제 연구개발 협력을 통한 글로벌 오픈이노베이션 플랫폼 구축을 논의한다.
특히, 국내 신약개발 생태계의 고질적 약점으로 지적되는 중개연구역량·글로벌 수준의 신약개발 연구인력 부족·글로벌 제약기업 및 선진국 인허가 기관과 네트워크 부재에 관한 해법 모색에 나선다.
그동안 국내 신약개발 지원기관 및 관련 기업들이 세계 최대 민관협력 신약개발 네트워크인 EU-IMI에 참여하고 싶다는 의사를 개별적으로 전달했으나 한국이 비 EU국가라는 이유로 성사되지 못했다.
KAIST 바이오헬스케어 혁신정책센터는 국내·외 자문위원들과 함께 IMI 및 유럽제약협회(EFPIA)와 지난 3년간의 논의해왔으며, 연구개발 비용의 자체 부담을 조건으로 한국의 IMI 참여 지지를 확보했다. 또한, 정부관계자와 함께 한국이 IMI에 참여해야 하는 필요성에 대해 논의하는 중이다.
이번 워크숍을 통해 한국-EU IMI 공동 신약연구 프로그램을 구축할 임시추진위원회를 구성하고 오송·대구 첨단의료복합단지를 글로벌 진출의 허브로 육성해 한국이 EU-IMI의 일원으로 활동하는 방안에 대해 본격적으로 논의할 예정이다.
세포·유전자 치료제 등 미래 정밀의료 의약품 개발과 민간 기업이 개발을 회피하거나 실패 위험이 높은 수퍼박테리아 항생제, 치매를 포함한 뇌질환 치료제 등의 국내 개발을 가속하기 위해서다.
7월 2일은 지속가능한 바이오투자 생태계 조성과 국내 신약·의료기기 스타트업의 글로벌 사업화 가능성을 전망해보는 자리로 마련된다.
조영국 글로벌밸류네트웍스 대표, 김종백 법무법인 지안 변호사, 이남구 워터스 코리아 대표가 좌장을 맡아 ▲바이오기업 가치 평가와 기업공개 ▲바이오텍 초기 투자의 다원화 ▲의료기기 혁신을 위한 투자 등의 세부 과제를 다룰 예정이다.
특히, 바이오 분야 창업부터 코스닥 상장까지 경험을 공유하기 위해 유진산 파맵신 대표와 윤원수 티앤알바이오팹 대표도 기업 사례 발표자로 나선다.
둘째 날 오후 행사에서는 신약개발 스타트업과 의료기기 스타트업의 글로벌 사업화 가능성을 탐색하는 기업 소개와 리뷰(Pre-IR) 시간이 마련된다. 작년에 이 세션에서 소개된 5개의 스타트업 중 2곳이 6개월 이내에 시리즈 A 투자 유치에 성공한 바 있다.
이번 행사는 KAIST 바이오헬스케어 혁신정책센터가 주최·주관하고 보건복지부와 보건산업진흥원, 한강서사이어티가 후원한다.
채수찬 KAIST 바이오헬스케어 혁신정책센터장은 “이번 워크숍을 통해 IMI와 같은 민관협력체 활용과 우리나라 바이오헬스 산업의 글로벌 진출 가속과 지속가능한 발전 방안이 마련되기를 기대한다”고 밝혔다.
KAIST 2019 CHIP 해외 자문단 초청 워크숍은 홈페이지( http://chip.kaist.ac.kr )를 통해 참석 신청이 가능하다.(문의:02-3498-7558)
2019.06.27 조회수 15694