%EC%9C%A0%EC%A0%84%EC%9E%90
-
 석현정, 최경아 교수 청백색 조명이 아침잠 깨워주는 효과 입증
〈 왼쪽부터 정현정 교수, 석현정 교수, 김태수 박사과정, 최경아 연구교수 〉
출근과 등교. 이 두 단어는 대부분의 직장인과 학생에게 유쾌하지 않다. 회식, 인터넷 강의, 스마트폰, 육아 등으로 인해 부족해진 아침잠은 쉽사리 사라지지 않는다. 하지만 우리가 매일 접하는 빛을 통해 오전의 나른함을 깨우고 생체리듬을 유지할 수 있다는 연구 결과가 발표됐다.
우리 대학 산업디자인학과 석현정 교수, 최경아 연구교수가 높은 색의 온도를 갖는 청백색(blue-enriched white)의 푸른 빛이 아침잠을 깨우는 데 효과적임을 밝혀냈다.
이 연구는 인간 중심의 조명이 나아가야 할 방향을 제시한 것으로, 인공적인 조명 시스템을 변화하는 데 긍정적인 영향을 끼칠 것으로 기대된다.
특히 이번 연구는 산업디자인학과 소속 교수와 연구원이 교신저자 및 1 저자로 참여해 순수과학 분야 저널에 논문을 게재했다. 이는 세계적으로도 찾기 힘든 사례로 디자인학과 자연과학의 우수 융합 연구의 표본이 될 것으로 예상된다.
최경아 연구교수가 1 저자, 나노과학기술대학원 정현정 교수가 참여한 이번 연구는 국제 학술지 ‘사이언티픽 리포트(Scientific Reports)’ 1월 23일 자에 게재됐다. (논문명 : Awakening effects of blue-enriched morning light exposure on university students’ physiological and subjective responses)
2017년도 노벨 생리의학상은 태양의 주기에 따라 아침, 저녁으로 몸의 변화가 규칙적으로 일어나는 서카디안(circadian) 리듬, 즉 생체리듬을 조절하는 유전자를 규명한 미국의 과학자 제프리 홀 메인대(University Of Maine) 교수, 마이클 로스바시 브랜다이스대(Brandeis University) 교수, 마이클 영 록펠러대(Rockefeller University) 교수에게 돌아갔다.
이처럼 수면과 각성 등 인간의 생체리듬 관련 연구는 끊임없이 이뤄지고 있다. 빛이 생리적 작용에 관여한다는 사실은 2000년대 초반 인간의 망막에서 제3의 광수용세포가 발견된 이후 꾸준히 연구되고 있다.
제3의 광수용세포는 기존의 간상세포나 원추세포와는 달리 비 시각적인 것에 반응하고 뇌에 전달되는 경로도 다르다. 특히 이 세포는 빛의 파란색 영역에 가장 민감해 이를 통해 각성 등 여러 생리적 현상이 발생할 뿐 아니라 뇌파, 멜라토닌 분비, 심전도 등에도 영향을 미친다는 사실이 밝혀졌다.
그러나 관련 기존 연구는 푸른 빛의 강한 레이저를 직접 조사하는 한정적인 조건에서 실험이 이뤄지기 때문에 결과를 일상에 접목하기가 어려웠다. 또한 기존 연구 대부분은 푸른 빛을 저녁이나 늦은 오후에 접하면 멜라토닌 분비가 억제돼 숙면을 방해한다는 사실을 규명하는 데에만 주력했다.
연구팀은 푸른 빛이 저녁에는 숙면에 방해될 수 있지만, 때와 장소에 따라서는 이로운 빛으로 활용할 수 있음을 증명하기 위해 노력했다. 오전에 쬐는 청백색의 빛은 인체를 잠에서 깨워 생체리듬을 조절하는 데 긍정적인 영향을 미친다는 사실을 밝혀냈다.
연구팀은 우리 대학 학생 15명을 대상으로 실험을 진행했고 호르몬과 타액 변화 등의 생리적 지표와 설문조사를 통한 주관적 지표를 동시에 관찰했다. 이 결과 빛의 색 변화에 따라 감성 등을 나타낸 주관적 지표와 멜라토닌 분비에 변화가 일어남을 확인했다.
최경아 연구교수는 박사과정 시절 학습 환경의 조명이 학생들의 학습 활동에 미치는 영향을 밝힌 바 있다. (논문명: Dynamic lighting system for the learning environment: performance of elementary students). 이번 연구를 통해 조명의 빛깔이 사람에게 미치는 영향을 하루 주기와 접목해 더욱 심화된 결과를 얻은 것이다.
석현정 교수는 “처음에는 단순히 조명을 다양하게 바꿔가며 구성원들을 편하게 쉬게 해주려는 의도에서 시작해, 호텔이나 레스토랑, 모닥불 등의 조명에서는 편안해지고 흰색 조명에서는 긴장감이 발생하는 이유를 명쾌하게 밝히고자 했다”라며 “과학적 근거와 고도화를 통해 신뢰성이 있는 데이터를 수집했고 많은 사람이 혜택을 볼 수 있는 결과를 얻었다고 생각한다”라고 말했다.
최경아 연구교수는 “이와 같은 조명 시스템의 진화가 실내 건축물뿐 아니라 자동차 내부와 지하주차장 세탁기, 냉장고 등 각종 전자기기에도 적용될 수 있다”고 밝혔다. 또한 스마트 조명 시스템을 달력, 출장 앱과 연동한다면 자동 학습을 통해 인간의 생체리듬과 권장 수면시간 및 기상 시간에 맞춰 조명의 색과 세기를 조절할 수도 있을 것으로 전망했다.
석현정 교수는 “학문마다 중요시하는 관점이 달라 디자인학자로서 자연과학의 기준을 통과하기가 쉽지 않았다. 꼼꼼히 설계하고 유의미한 데이터를 축적하는 데 큰 노력을 기울여 좋은 결과가 나온 것 같다”라며 “인간 중심의 조명이 우리 일상생활에 성공적으로 적용될 기회는 무궁무진하다”라고 말했다.
최경아 연구교수는 “빛을 단순히 공간을 밝히는 용도를 넘어 사용자의 경험을 한층 더 풍요롭게 하는 중요한 도구로 인식하는 데서 시작된 연구이다”라며 “학문 간 경계를 허물고 우리 연구를 읽어주는 독자의 스펙트럼이 확대된다는 데 의의가 있다고 생각한다”라고 말했다.
이번 연구는 한국연구재단의 이공분야 기초연구사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 낮과 밤의 멜라토닌 분비량의 변화 그래프
2019.02.28 조회수 19490
석현정, 최경아 교수 청백색 조명이 아침잠 깨워주는 효과 입증
〈 왼쪽부터 정현정 교수, 석현정 교수, 김태수 박사과정, 최경아 연구교수 〉
출근과 등교. 이 두 단어는 대부분의 직장인과 학생에게 유쾌하지 않다. 회식, 인터넷 강의, 스마트폰, 육아 등으로 인해 부족해진 아침잠은 쉽사리 사라지지 않는다. 하지만 우리가 매일 접하는 빛을 통해 오전의 나른함을 깨우고 생체리듬을 유지할 수 있다는 연구 결과가 발표됐다.
우리 대학 산업디자인학과 석현정 교수, 최경아 연구교수가 높은 색의 온도를 갖는 청백색(blue-enriched white)의 푸른 빛이 아침잠을 깨우는 데 효과적임을 밝혀냈다.
이 연구는 인간 중심의 조명이 나아가야 할 방향을 제시한 것으로, 인공적인 조명 시스템을 변화하는 데 긍정적인 영향을 끼칠 것으로 기대된다.
특히 이번 연구는 산업디자인학과 소속 교수와 연구원이 교신저자 및 1 저자로 참여해 순수과학 분야 저널에 논문을 게재했다. 이는 세계적으로도 찾기 힘든 사례로 디자인학과 자연과학의 우수 융합 연구의 표본이 될 것으로 예상된다.
최경아 연구교수가 1 저자, 나노과학기술대학원 정현정 교수가 참여한 이번 연구는 국제 학술지 ‘사이언티픽 리포트(Scientific Reports)’ 1월 23일 자에 게재됐다. (논문명 : Awakening effects of blue-enriched morning light exposure on university students’ physiological and subjective responses)
2017년도 노벨 생리의학상은 태양의 주기에 따라 아침, 저녁으로 몸의 변화가 규칙적으로 일어나는 서카디안(circadian) 리듬, 즉 생체리듬을 조절하는 유전자를 규명한 미국의 과학자 제프리 홀 메인대(University Of Maine) 교수, 마이클 로스바시 브랜다이스대(Brandeis University) 교수, 마이클 영 록펠러대(Rockefeller University) 교수에게 돌아갔다.
이처럼 수면과 각성 등 인간의 생체리듬 관련 연구는 끊임없이 이뤄지고 있다. 빛이 생리적 작용에 관여한다는 사실은 2000년대 초반 인간의 망막에서 제3의 광수용세포가 발견된 이후 꾸준히 연구되고 있다.
제3의 광수용세포는 기존의 간상세포나 원추세포와는 달리 비 시각적인 것에 반응하고 뇌에 전달되는 경로도 다르다. 특히 이 세포는 빛의 파란색 영역에 가장 민감해 이를 통해 각성 등 여러 생리적 현상이 발생할 뿐 아니라 뇌파, 멜라토닌 분비, 심전도 등에도 영향을 미친다는 사실이 밝혀졌다.
그러나 관련 기존 연구는 푸른 빛의 강한 레이저를 직접 조사하는 한정적인 조건에서 실험이 이뤄지기 때문에 결과를 일상에 접목하기가 어려웠다. 또한 기존 연구 대부분은 푸른 빛을 저녁이나 늦은 오후에 접하면 멜라토닌 분비가 억제돼 숙면을 방해한다는 사실을 규명하는 데에만 주력했다.
연구팀은 푸른 빛이 저녁에는 숙면에 방해될 수 있지만, 때와 장소에 따라서는 이로운 빛으로 활용할 수 있음을 증명하기 위해 노력했다. 오전에 쬐는 청백색의 빛은 인체를 잠에서 깨워 생체리듬을 조절하는 데 긍정적인 영향을 미친다는 사실을 밝혀냈다.
연구팀은 우리 대학 학생 15명을 대상으로 실험을 진행했고 호르몬과 타액 변화 등의 생리적 지표와 설문조사를 통한 주관적 지표를 동시에 관찰했다. 이 결과 빛의 색 변화에 따라 감성 등을 나타낸 주관적 지표와 멜라토닌 분비에 변화가 일어남을 확인했다.
최경아 연구교수는 박사과정 시절 학습 환경의 조명이 학생들의 학습 활동에 미치는 영향을 밝힌 바 있다. (논문명: Dynamic lighting system for the learning environment: performance of elementary students). 이번 연구를 통해 조명의 빛깔이 사람에게 미치는 영향을 하루 주기와 접목해 더욱 심화된 결과를 얻은 것이다.
석현정 교수는 “처음에는 단순히 조명을 다양하게 바꿔가며 구성원들을 편하게 쉬게 해주려는 의도에서 시작해, 호텔이나 레스토랑, 모닥불 등의 조명에서는 편안해지고 흰색 조명에서는 긴장감이 발생하는 이유를 명쾌하게 밝히고자 했다”라며 “과학적 근거와 고도화를 통해 신뢰성이 있는 데이터를 수집했고 많은 사람이 혜택을 볼 수 있는 결과를 얻었다고 생각한다”라고 말했다.
최경아 연구교수는 “이와 같은 조명 시스템의 진화가 실내 건축물뿐 아니라 자동차 내부와 지하주차장 세탁기, 냉장고 등 각종 전자기기에도 적용될 수 있다”고 밝혔다. 또한 스마트 조명 시스템을 달력, 출장 앱과 연동한다면 자동 학습을 통해 인간의 생체리듬과 권장 수면시간 및 기상 시간에 맞춰 조명의 색과 세기를 조절할 수도 있을 것으로 전망했다.
석현정 교수는 “학문마다 중요시하는 관점이 달라 디자인학자로서 자연과학의 기준을 통과하기가 쉽지 않았다. 꼼꼼히 설계하고 유의미한 데이터를 축적하는 데 큰 노력을 기울여 좋은 결과가 나온 것 같다”라며 “인간 중심의 조명이 우리 일상생활에 성공적으로 적용될 기회는 무궁무진하다”라고 말했다.
최경아 연구교수는 “빛을 단순히 공간을 밝히는 용도를 넘어 사용자의 경험을 한층 더 풍요롭게 하는 중요한 도구로 인식하는 데서 시작된 연구이다”라며 “학문 간 경계를 허물고 우리 연구를 읽어주는 독자의 스펙트럼이 확대된다는 데 의의가 있다고 생각한다”라고 말했다.
이번 연구는 한국연구재단의 이공분야 기초연구사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 낮과 밤의 멜라토닌 분비량의 변화 그래프
2019.02.28 조회수 19490 -
 허원도 교수, 빛만 비춰도 유전자 발현 조절하는 효소 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 살아있는 생쥐의 머리에 빛만 비춰도 생쥐 뇌 유전자 발현을 제어할 수 있는 시스템을 개발했다.
매우 약한 빛에도 반응하도록 유전자 재조합 효소를 설계해 원하는 위치와 타이밍에 효소를 활성화할 수 있다. 많은 시간과 재원이 소요되는 유전자 변형 실험 모델을 만들지 않아도 특정 유전자 발현을 유도할 수 있어 활용이 매우 클 것으로 기대된다.
이번 연구결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 1월 19일자 온라인 판에 게재됐다.
연구팀이 개발한 Flp 유전자 재조합 효소는 빛에 민감하게 반응해 활성화된다. 수술이 아닌 LED 빛을 쏘는 비침습성(non-invasive) 방식만으로도 유전자의 발현을 유도할 수 있어 물리적․화학적 손상에 의한 부작용도 최소화할 수 있다.
Flp 유전자 재조합 효소는 말 그대로 유전자를 자르고 재조합하는 기능을 지녀 유전자 형질 전환 실험모델을 만드는 등 다방면으로 활용됐다. 광유전학 기술에 응용하려는 시도가 있었으나 빛 없이도 스스로 조립(auto-assembly)돼버려 제어가 어려웠다. 뇌 속으로 빛을 직접 전달하려면 광섬유를 집어넣는 수술 과정도 필요했다.
연구팀이 개발한 광활성 Flp 유전자 재조합 효소(이하 PA-Flp 단백질)는 비활성화 상태에서도 빛을 받으면 결합되면서 활성화된다. 연구진은 단백질 공학을 통해 기존에는 잘 알려지지 않았던 Flp 재조합 효소를 활성화하는 위치를 찾는 힌트를 얻어 PA-Flp 단백질을 설계했다. PA-Flp 단백질의 발현 정도는 적색 형광단백질을 붙여 쉽게 알아볼 수 있도록 만들었다.
PA-Flp 단백질은 매우 적은 양으로도 반응하는 민감도를 지녔다. 연구진은 기억을 관장하는 쥐의 뇌 해마 부위에 PA-Flp 단백질을 넣은 뒤 약 30초 동안 LED를 머리 부분에 비추는 실험을 진행했다. 그 결과 생쥐 뇌의 깊은 조직 영역에 도달하는 매우 적은 양의 빛으로도 PA-Flp 단백질이 활성화된 것을 확인했다.
생쥐에게 쏜 빛은 1-2mW/mm2로 실생활에서 사용하는 휴대폰의 손전등 혹은 발표 시 이용하는 레이저 포인터 정도의 세기다. 연구진은 물리적 손상을 전혀 일으키지 않는 비침습성 방식으로도 유전자 발현을 조절하는데 성공한 것이다.
또한 연구진은 행동을 재현하고 검증하는 실험에 나섰다. 해마보다 더 깊숙한 곳에 있는 내측 중격(~3.5mm) 뇌 내측 중격(medial septum): 기억의 중추 역할을 담당하는 해마와 연결된 부위에는 칼슘 채널이 존재하는데 이 칼슘 채널의 발현이 억제되면 물체를 탐색하는 능력이 증가한다는 기존의 연구에 착안하여 실험을 설계했다.
연구진은 내측 중격에 PA-Flp 단백질을 도입하고 LED 빛을 쏘자 칼슘 채널의 발현이 억제됨을 확인했다. 실제 PA-Flp 단백질이 활성화된 실험군은 물체를 탐색하는 능력이 대조군에 비해 훨씬 커져 물체 주변으로 더 많은 움직임을 기록했다.
이번 연구는 빛으로 원하는 타이밍에 유전자를 자르고 재조합하는 효소를 개발해 향후 광유전학에 응용가치가 클 것으로 기대된다. 특정 유전자가 변형된 실험모델을 제작하는데 오랜 시일과 연구비가 투입되는데 반해 이 기술을 활용하면 빛만 쏘는 방식으로도 원하는 유전자를 쉽고 빠르게 조절할 수 있기 때문이다. 또한 광섬유를 심는 별도의 수술 없이도 연구자가 사용하기 간편하고 비용도 저렴하다.
허원도 교수는 “실험쥐의 생리학적 현상에 영향을 줄 수 있는 물리적, 화학적 자극이 거의 없이 LED로 원하는 특정 유전자 발현을 조절할 수 있는 것이 큰 장점이다”라며 “향후 다양한 뇌 영역을 탐구하는데 널리 활용될 것으로 기대한다”고 밝혔다.
□ 그림 설명
그림1. PA-Flp 단백질 작동원리 및 발현
그림2. 물체 탐색 능력이 증가함을 실험으로 확인
2019.01.21 조회수 10902
허원도 교수, 빛만 비춰도 유전자 발현 조절하는 효소 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 살아있는 생쥐의 머리에 빛만 비춰도 생쥐 뇌 유전자 발현을 제어할 수 있는 시스템을 개발했다.
매우 약한 빛에도 반응하도록 유전자 재조합 효소를 설계해 원하는 위치와 타이밍에 효소를 활성화할 수 있다. 많은 시간과 재원이 소요되는 유전자 변형 실험 모델을 만들지 않아도 특정 유전자 발현을 유도할 수 있어 활용이 매우 클 것으로 기대된다.
이번 연구결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 1월 19일자 온라인 판에 게재됐다.
연구팀이 개발한 Flp 유전자 재조합 효소는 빛에 민감하게 반응해 활성화된다. 수술이 아닌 LED 빛을 쏘는 비침습성(non-invasive) 방식만으로도 유전자의 발현을 유도할 수 있어 물리적․화학적 손상에 의한 부작용도 최소화할 수 있다.
Flp 유전자 재조합 효소는 말 그대로 유전자를 자르고 재조합하는 기능을 지녀 유전자 형질 전환 실험모델을 만드는 등 다방면으로 활용됐다. 광유전학 기술에 응용하려는 시도가 있었으나 빛 없이도 스스로 조립(auto-assembly)돼버려 제어가 어려웠다. 뇌 속으로 빛을 직접 전달하려면 광섬유를 집어넣는 수술 과정도 필요했다.
연구팀이 개발한 광활성 Flp 유전자 재조합 효소(이하 PA-Flp 단백질)는 비활성화 상태에서도 빛을 받으면 결합되면서 활성화된다. 연구진은 단백질 공학을 통해 기존에는 잘 알려지지 않았던 Flp 재조합 효소를 활성화하는 위치를 찾는 힌트를 얻어 PA-Flp 단백질을 설계했다. PA-Flp 단백질의 발현 정도는 적색 형광단백질을 붙여 쉽게 알아볼 수 있도록 만들었다.
PA-Flp 단백질은 매우 적은 양으로도 반응하는 민감도를 지녔다. 연구진은 기억을 관장하는 쥐의 뇌 해마 부위에 PA-Flp 단백질을 넣은 뒤 약 30초 동안 LED를 머리 부분에 비추는 실험을 진행했다. 그 결과 생쥐 뇌의 깊은 조직 영역에 도달하는 매우 적은 양의 빛으로도 PA-Flp 단백질이 활성화된 것을 확인했다.
생쥐에게 쏜 빛은 1-2mW/mm2로 실생활에서 사용하는 휴대폰의 손전등 혹은 발표 시 이용하는 레이저 포인터 정도의 세기다. 연구진은 물리적 손상을 전혀 일으키지 않는 비침습성 방식으로도 유전자 발현을 조절하는데 성공한 것이다.
또한 연구진은 행동을 재현하고 검증하는 실험에 나섰다. 해마보다 더 깊숙한 곳에 있는 내측 중격(~3.5mm) 뇌 내측 중격(medial septum): 기억의 중추 역할을 담당하는 해마와 연결된 부위에는 칼슘 채널이 존재하는데 이 칼슘 채널의 발현이 억제되면 물체를 탐색하는 능력이 증가한다는 기존의 연구에 착안하여 실험을 설계했다.
연구진은 내측 중격에 PA-Flp 단백질을 도입하고 LED 빛을 쏘자 칼슘 채널의 발현이 억제됨을 확인했다. 실제 PA-Flp 단백질이 활성화된 실험군은 물체를 탐색하는 능력이 대조군에 비해 훨씬 커져 물체 주변으로 더 많은 움직임을 기록했다.
이번 연구는 빛으로 원하는 타이밍에 유전자를 자르고 재조합하는 효소를 개발해 향후 광유전학에 응용가치가 클 것으로 기대된다. 특정 유전자가 변형된 실험모델을 제작하는데 오랜 시일과 연구비가 투입되는데 반해 이 기술을 활용하면 빛만 쏘는 방식으로도 원하는 유전자를 쉽고 빠르게 조절할 수 있기 때문이다. 또한 광섬유를 심는 별도의 수술 없이도 연구자가 사용하기 간편하고 비용도 저렴하다.
허원도 교수는 “실험쥐의 생리학적 현상에 영향을 줄 수 있는 물리적, 화학적 자극이 거의 없이 LED로 원하는 특정 유전자 발현을 조절할 수 있는 것이 큰 장점이다”라며 “향후 다양한 뇌 영역을 탐구하는데 널리 활용될 것으로 기대한다”고 밝혔다.
□ 그림 설명
그림1. PA-Flp 단백질 작동원리 및 발현
그림2. 물체 탐색 능력이 증가함을 실험으로 확인
2019.01.21 조회수 10902 -
 박수형 교수, 간암 복합면역치료 적용 가능성 확인
〈 박 수 형 교수 〉
우리 대학 의과학대학원 박수형 교수와 서울아산병원 황신, 송기원 교수 공동연구팀이 간암 환자의 탈진(exhausted)된 종양 침투 면역세포 구성의 차이에 따른 간암 환자군을 구분하는 데 성공했다.
이번 연구를 통해 간암 환자의 새로운 면역치료법 적용 가능성을 확인함으로써 향후 맞춤 의학의 근거를 제시할 수 있는 기반이 될 것으로 기대된다.
특히 이번 연구는 서울아산병원 임상 연구팀과 KAIST 의과학대학원이 동물 모델이 아닌 임상을 통해 새 면역 항암 치료법을 위한 협업을 진행한 것으로 중개 연구(translational research)의 우수 모델로 평가받는다.
김형돈 박사과정이 1저자로 참여한 이번 연구는 국제 학술지 ‘소화기학(Gastroenterology)’ 12월 4일 자에 게재됐다.
암이 발생하면 인체는 암세포를 제거하기 위해 면역세포인 ‘T세포’를 활성화하는데, 종양은 T세포의 기능을 억제하기 위한 환경을 구성한다. 이때 침투한 T세포들은 ‘피디-1(PD-1)’ 단백질과 같은 면역 관문 수용체를 세포 표면에 발현하면서 활성이 저하되고 탈진된 상태가 된다.
‘PD-1 억제제’로 대표되는 면역 관문 억제제는 PD-1 신호에 의해 저하된 T세포의 활성을 회복시키는 역할을 한다. 암세포는 생존을 위해 면역세포로부터 몸을 숨기는데, 면역 관문 억제제는 암세포가 숨는 데 도움을 주는 PD-1, PD-L1의 작용을 차단함으로써 면역세포가 정상적으로 암세포를 공격할 수 있게 되는 것이다.
그러나 면역 관문 억제제는 약 2~30%의 환자에게만 효능이 있고 70% 이상의 환자에게는 효과가 없어 면역항암제의 치료 효능을 높이기 위한 연구가 계속되고 있다.
연구팀은 간암 환자의 탈진한 T세포 중에서 PD-1 단백질을 많이 발현하는 T세포가 그렇지 않은 T세포에 비해 면역세포의 기능이 더 많이 저하돼 있고, PD-1 이외의 다양한 면역 관문 수용체를 동시에 발현하는 것을 발견했다.
특히 간암 환자 중에서 약 절반 정도의 환자만이 PD-1을 많이 발현하는 탈진 T세포를 갖고 있으며, 이러한 환자들이 복합 면역 관문 억제제에 의해 T세포의 기능이 효과적으로 회복됨을 확인했다.
이번 결과를 통해 복합 면역 관문 억제제의 대상이 되는 환자군을 제시함으로써 효과적인 면역 치료를 효율적으로 적용하는 데 기여할 것으로 예상된다.
박 교수는 “이번에 새롭게 제시된 환자군은 현재 적용 중인 면역 관문 억제제 치료의 반응을 예측할 수 있는 바이오 마커로서 유용하게 활용될 수 있다”라며 “복합 면역 관문 억제제가 특정 환자에게만 효능이 있음을 제시해 맞춤 의학의 근거가 될 수 있다는 임상적 의의를 갖는다”라고 말했다.
이번 연구는 보건복지부 첨단의료기술개발 사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. PD-1 발현에 따른 각 세포군의 특징적인 유전자 발현 양상
그림2. PD-1을 과발현하는 세포군의 존재 유무에 따른 특징적인 두가지 환자군
2018.12.12 조회수 10740
박수형 교수, 간암 복합면역치료 적용 가능성 확인
〈 박 수 형 교수 〉
우리 대학 의과학대학원 박수형 교수와 서울아산병원 황신, 송기원 교수 공동연구팀이 간암 환자의 탈진(exhausted)된 종양 침투 면역세포 구성의 차이에 따른 간암 환자군을 구분하는 데 성공했다.
이번 연구를 통해 간암 환자의 새로운 면역치료법 적용 가능성을 확인함으로써 향후 맞춤 의학의 근거를 제시할 수 있는 기반이 될 것으로 기대된다.
특히 이번 연구는 서울아산병원 임상 연구팀과 KAIST 의과학대학원이 동물 모델이 아닌 임상을 통해 새 면역 항암 치료법을 위한 협업을 진행한 것으로 중개 연구(translational research)의 우수 모델로 평가받는다.
김형돈 박사과정이 1저자로 참여한 이번 연구는 국제 학술지 ‘소화기학(Gastroenterology)’ 12월 4일 자에 게재됐다.
암이 발생하면 인체는 암세포를 제거하기 위해 면역세포인 ‘T세포’를 활성화하는데, 종양은 T세포의 기능을 억제하기 위한 환경을 구성한다. 이때 침투한 T세포들은 ‘피디-1(PD-1)’ 단백질과 같은 면역 관문 수용체를 세포 표면에 발현하면서 활성이 저하되고 탈진된 상태가 된다.
‘PD-1 억제제’로 대표되는 면역 관문 억제제는 PD-1 신호에 의해 저하된 T세포의 활성을 회복시키는 역할을 한다. 암세포는 생존을 위해 면역세포로부터 몸을 숨기는데, 면역 관문 억제제는 암세포가 숨는 데 도움을 주는 PD-1, PD-L1의 작용을 차단함으로써 면역세포가 정상적으로 암세포를 공격할 수 있게 되는 것이다.
그러나 면역 관문 억제제는 약 2~30%의 환자에게만 효능이 있고 70% 이상의 환자에게는 효과가 없어 면역항암제의 치료 효능을 높이기 위한 연구가 계속되고 있다.
연구팀은 간암 환자의 탈진한 T세포 중에서 PD-1 단백질을 많이 발현하는 T세포가 그렇지 않은 T세포에 비해 면역세포의 기능이 더 많이 저하돼 있고, PD-1 이외의 다양한 면역 관문 수용체를 동시에 발현하는 것을 발견했다.
특히 간암 환자 중에서 약 절반 정도의 환자만이 PD-1을 많이 발현하는 탈진 T세포를 갖고 있으며, 이러한 환자들이 복합 면역 관문 억제제에 의해 T세포의 기능이 효과적으로 회복됨을 확인했다.
이번 결과를 통해 복합 면역 관문 억제제의 대상이 되는 환자군을 제시함으로써 효과적인 면역 치료를 효율적으로 적용하는 데 기여할 것으로 예상된다.
박 교수는 “이번에 새롭게 제시된 환자군은 현재 적용 중인 면역 관문 억제제 치료의 반응을 예측할 수 있는 바이오 마커로서 유용하게 활용될 수 있다”라며 “복합 면역 관문 억제제가 특정 환자에게만 효능이 있음을 제시해 맞춤 의학의 근거가 될 수 있다는 임상적 의의를 갖는다”라고 말했다.
이번 연구는 보건복지부 첨단의료기술개발 사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. PD-1 발현에 따른 각 세포군의 특징적인 유전자 발현 양상
그림2. PD-1을 과발현하는 세포군의 존재 유무에 따른 특징적인 두가지 환자군
2018.12.12 조회수 10740 -
 최원호 교수, 박상후 연구교수, 어드밴시스 인 피직스 엑스 초청 리뷰논문 게재
〈 최원호 교수, 박상후 연구교수 〉
우리 대학 원자력및양자공학과 최원호 교수와 박상후 연구교수가 국제 학술지 ‘어드밴시스 인 피직스 엑스(Advances in Physics: X)’ 10월 23일자에 초청 리뷰논문을 게재했다. 모(母) 학술지인 ‘어드밴시스 인 피직스(Advances in Physics)’의 피인용 지수는 2017년 기준 30.917로 물리학 분야에서 최고의 리뷰 학술지로 인정받고 있다.
초청 리뷰논문은 학술지 편집장으로부터 초청받은 세계적 석학들이 해당 분야의 전반적인 연구 내용을 총 정리하는 논문이다. 어드밴시스 인 피직스 엑스는 2016년에 첫 출판된 학술지로 학문의 경계를 뛰어넘어 물리학 외 다른 학문 분야까지 영향력이 있는 연구에 대한 내용을 출판하고 있다. 현재까지 모(母) 학술지를 포함해 우리나라 물리학자의 제1저자 및 교신저자로서 초청 리뷰논문 게재는 이번이 처음이다.
최원호 교수는 지난30년 이상 저온 대기압 플라즈마부터 고온 핵융합 플라즈마까지 플라즈마 물리의 여러 난제 해결 연구에 매진해 왔으며, 이와 더불어 최첨단 플라즈마 진단계 및 플라즈마 응용 기술을 개발해 왔다.
최근에는 3년 전 창업한 교내 창업 기업인 플라즈맵(Plasmapp, 대표 임유봉 박사과정)을 통해 의료용 플라즈마 멸균 기술 등 다양한 플라즈마 기술의 실용화에 힘쓰고 있다. 기초연구부터 실용화 연구에까지 이와 같은 플라즈마 기술 발전의 공로를 국제적으로 인정받아, 대기압 플라즈마 전자의 진단과 특성조사에 관한 리뷰논문을 게재했다.
대기압에서 플라즈마를 발생시키면 자유전자와 중성기체 입자 사이의 충돌이 매우 빈번하게 일어나는 약하게 이온화된 플라즈마가 된다. 이러한 플라즈마 내에 존재하는 전자는 플라즈마 내에서 여러 물리적 및 화학적 반응을 지배하는 중요한 역할을 한다. 전자의 밀도 및 온도를 시공간적으로 정확하게 진단하는 것은 난이도가 높아 지금까지 큰 어려움이 있었고, 이러한 진단의 어려움 때문에 전자의 가열 구조 및 원리를 실험적으로 규명하는데 한계가 있었다.
최원호 교수 연구팀은 전자에 의한 중성입자 제동복사(electron-neutral bremsstrahlung) 원리를 이용해 플라즈마 내 자유전자의 밀도와 온도를 정확히 진단하고, 이를 2차원으로 영상화 하는 기술을 개발했으며 이 기술은 최근 학계의 주목을 받고 있다.
연구팀은 개발된 진단기술을 이용해 대기압 플라즈마에서 자유전자의 가열 구조 및 근본 원리를 밝히고, 특정 플라즈마에서 전자가열 구조의 시공간적 대칭성 소멸을 최초로 확인하는 등 현재까지 실험적으로 확인할 수 없었던 여러 전자 가열 원리를 규명했다.
최 교수는 “소재와 환경분야 뿐만 아니라 최근의 의학, 바이오, 농식품 분야를 위한 활용 가능성 때문에 대기압 플라즈마 연구는 세계적으로 각광을 받고 있으며, 대기압 플라즈마 내에서 일어나는 여러 물리적 및 화학적 현상을 좌지우지하는 전자의 특성을 정확하게 진단하고 이해하는 일은 과학적 측면에서도 중요성이 크다”며 “대기압 플라즈마 전자의 진단과 특성연구에 관한 논문을 세계 저명 저널에 리뷰논문으로 초청받은 것은 그간의 연구 성과에 대해 인정받은 결과라 생각하고, 본 논문은 대기압 플라즈마의 산업적 활용에도 기본이 되는 자료가 될 것이다”고 말했다.
2018.10.25 조회수 8787
최원호 교수, 박상후 연구교수, 어드밴시스 인 피직스 엑스 초청 리뷰논문 게재
〈 최원호 교수, 박상후 연구교수 〉
우리 대학 원자력및양자공학과 최원호 교수와 박상후 연구교수가 국제 학술지 ‘어드밴시스 인 피직스 엑스(Advances in Physics: X)’ 10월 23일자에 초청 리뷰논문을 게재했다. 모(母) 학술지인 ‘어드밴시스 인 피직스(Advances in Physics)’의 피인용 지수는 2017년 기준 30.917로 물리학 분야에서 최고의 리뷰 학술지로 인정받고 있다.
초청 리뷰논문은 학술지 편집장으로부터 초청받은 세계적 석학들이 해당 분야의 전반적인 연구 내용을 총 정리하는 논문이다. 어드밴시스 인 피직스 엑스는 2016년에 첫 출판된 학술지로 학문의 경계를 뛰어넘어 물리학 외 다른 학문 분야까지 영향력이 있는 연구에 대한 내용을 출판하고 있다. 현재까지 모(母) 학술지를 포함해 우리나라 물리학자의 제1저자 및 교신저자로서 초청 리뷰논문 게재는 이번이 처음이다.
최원호 교수는 지난30년 이상 저온 대기압 플라즈마부터 고온 핵융합 플라즈마까지 플라즈마 물리의 여러 난제 해결 연구에 매진해 왔으며, 이와 더불어 최첨단 플라즈마 진단계 및 플라즈마 응용 기술을 개발해 왔다.
최근에는 3년 전 창업한 교내 창업 기업인 플라즈맵(Plasmapp, 대표 임유봉 박사과정)을 통해 의료용 플라즈마 멸균 기술 등 다양한 플라즈마 기술의 실용화에 힘쓰고 있다. 기초연구부터 실용화 연구에까지 이와 같은 플라즈마 기술 발전의 공로를 국제적으로 인정받아, 대기압 플라즈마 전자의 진단과 특성조사에 관한 리뷰논문을 게재했다.
대기압에서 플라즈마를 발생시키면 자유전자와 중성기체 입자 사이의 충돌이 매우 빈번하게 일어나는 약하게 이온화된 플라즈마가 된다. 이러한 플라즈마 내에 존재하는 전자는 플라즈마 내에서 여러 물리적 및 화학적 반응을 지배하는 중요한 역할을 한다. 전자의 밀도 및 온도를 시공간적으로 정확하게 진단하는 것은 난이도가 높아 지금까지 큰 어려움이 있었고, 이러한 진단의 어려움 때문에 전자의 가열 구조 및 원리를 실험적으로 규명하는데 한계가 있었다.
최원호 교수 연구팀은 전자에 의한 중성입자 제동복사(electron-neutral bremsstrahlung) 원리를 이용해 플라즈마 내 자유전자의 밀도와 온도를 정확히 진단하고, 이를 2차원으로 영상화 하는 기술을 개발했으며 이 기술은 최근 학계의 주목을 받고 있다.
연구팀은 개발된 진단기술을 이용해 대기압 플라즈마에서 자유전자의 가열 구조 및 근본 원리를 밝히고, 특정 플라즈마에서 전자가열 구조의 시공간적 대칭성 소멸을 최초로 확인하는 등 현재까지 실험적으로 확인할 수 없었던 여러 전자 가열 원리를 규명했다.
최 교수는 “소재와 환경분야 뿐만 아니라 최근의 의학, 바이오, 농식품 분야를 위한 활용 가능성 때문에 대기압 플라즈마 연구는 세계적으로 각광을 받고 있으며, 대기압 플라즈마 내에서 일어나는 여러 물리적 및 화학적 현상을 좌지우지하는 전자의 특성을 정확하게 진단하고 이해하는 일은 과학적 측면에서도 중요성이 크다”며 “대기압 플라즈마 전자의 진단과 특성연구에 관한 논문을 세계 저명 저널에 리뷰논문으로 초청받은 것은 그간의 연구 성과에 대해 인정받은 결과라 생각하고, 본 논문은 대기압 플라즈마의 산업적 활용에도 기본이 되는 자료가 될 것이다”고 말했다.
2018.10.25 조회수 8787 -
 박범순 교수, 유전체 편집의 글로벌 관측소 설립 제안
〈 박 범 순 교수 〉
우리 대학 과학기술정책대학원 박범순 교수 연구팀의 유전체 편집 관련 ‘글로벌 관측소(Global Observatory)’ 설립 제안 논문이 국제학술지 셀의 자매지인 ‘트렌드 인 바이오테크놀로지(Trends in Biotechnology)’ 6월자 온라인 판에 게재됐다.
유전자가위 기술의 발전으로 인간 생식세포의 손쉬운 편집이 가능해지고 인류의 미래에 직접적인 영향을 줄 수 있다는 점에서 새로운 국제적 협치의 장에 대한 필요성이 커지고 있다.
이에 2015년 12월 영국 왕립학회, 중국 과학한림원, 미국 과학한림원의 공둥 주관으로 열린 ‘인간유전체 편집에 대한 국제 회의’에서 유전체 편집기술의 안전성과 효능의 검증, 기술의 적절성에 대한 폭넓은 사회적 합의 확보, 관련 규제 관리 마련 등에 대해 논의한 바 있다.
그러나 여전히 폭넓은 합의가 무엇을 의미하는지, 이를 어떻게 확보할 지에 대한 합의점은 명확하지 않았다.
박 교수 논문은 이 문제를 세 가지로 정리해 제시했다. ▲ 유전체 편집기술에 대한 국제적 논의에는 지정학적 의미에서 많은 국가의 관점이 적절히 고려돼야 하고 ▲ 기술의 적용이 사회를 지탱하는 규범과 법적 권리 및 의무와 깊이 연관돼 있기 때문에 기술의 미래에 대한 질문은 기술적, 윤리적 영역으로 쉽게 구분할 수 없고 ▲ 무엇이 중요한 이슈이고, 우선적으로 무엇을 다뤄야 하는가, 합의를 어떻게 이룰 것인가에 대한 논의가 이뤄져야 한다고 말했다.
이어 글로벌 관측소의 설립 목적과 목표가 소개됐다. 이 관측소는 인간 유전체편집기술에 대해 보다 포괄적이며 ‘코스모폴리탄 윤리’에 기반한 새로운 형태의 숙의의 장으로 제안됐다. 가장 주된 기능으로는 글로벌 인류 공동체 내의 다양한 관점들을 가시화하고 이를 통해 숙의과정에서 보다 확장된 질문들이 다루어질 수 있도록 하는 것이다.
글로벌 관측소는 ▲유전체편집에 대한 글로벌 수준의 윤리적, 정책적 반응들을 수집하고 가시화하는 작업 ▲‘합의’에 대한 개념적 발전, 긴장관계들, 그리고 합의가 필요한 영역들에 대한 실질적 분석을 제공하고 ▲기존의 논의에서 무시되었던 중요한 질문들, 목소리를 높일 수 없었던 행위자들에게 초점을 맞춰 주기적인 논의가 이루어지는 포럼으로서 역할을 수행하게 될 것이라고 설명했다.
박범순 교수는 “크리스퍼(CRISPR) 유전자 가위로 대표되는 유전체편집기술이 가져올 사회적, 법적, 윤리적, 종교적, 철학적 이슈를 각국의 경험을 바탕으로 논의하고 정보를 공유하기 위한 대화의 장을 마련하자는 취지에서 글로벌 관측소 설립을 제안했다”고 말했다.
2018.07.02 조회수 11948
박범순 교수, 유전체 편집의 글로벌 관측소 설립 제안
〈 박 범 순 교수 〉
우리 대학 과학기술정책대학원 박범순 교수 연구팀의 유전체 편집 관련 ‘글로벌 관측소(Global Observatory)’ 설립 제안 논문이 국제학술지 셀의 자매지인 ‘트렌드 인 바이오테크놀로지(Trends in Biotechnology)’ 6월자 온라인 판에 게재됐다.
유전자가위 기술의 발전으로 인간 생식세포의 손쉬운 편집이 가능해지고 인류의 미래에 직접적인 영향을 줄 수 있다는 점에서 새로운 국제적 협치의 장에 대한 필요성이 커지고 있다.
이에 2015년 12월 영국 왕립학회, 중국 과학한림원, 미국 과학한림원의 공둥 주관으로 열린 ‘인간유전체 편집에 대한 국제 회의’에서 유전체 편집기술의 안전성과 효능의 검증, 기술의 적절성에 대한 폭넓은 사회적 합의 확보, 관련 규제 관리 마련 등에 대해 논의한 바 있다.
그러나 여전히 폭넓은 합의가 무엇을 의미하는지, 이를 어떻게 확보할 지에 대한 합의점은 명확하지 않았다.
박 교수 논문은 이 문제를 세 가지로 정리해 제시했다. ▲ 유전체 편집기술에 대한 국제적 논의에는 지정학적 의미에서 많은 국가의 관점이 적절히 고려돼야 하고 ▲ 기술의 적용이 사회를 지탱하는 규범과 법적 권리 및 의무와 깊이 연관돼 있기 때문에 기술의 미래에 대한 질문은 기술적, 윤리적 영역으로 쉽게 구분할 수 없고 ▲ 무엇이 중요한 이슈이고, 우선적으로 무엇을 다뤄야 하는가, 합의를 어떻게 이룰 것인가에 대한 논의가 이뤄져야 한다고 말했다.
이어 글로벌 관측소의 설립 목적과 목표가 소개됐다. 이 관측소는 인간 유전체편집기술에 대해 보다 포괄적이며 ‘코스모폴리탄 윤리’에 기반한 새로운 형태의 숙의의 장으로 제안됐다. 가장 주된 기능으로는 글로벌 인류 공동체 내의 다양한 관점들을 가시화하고 이를 통해 숙의과정에서 보다 확장된 질문들이 다루어질 수 있도록 하는 것이다.
글로벌 관측소는 ▲유전체편집에 대한 글로벌 수준의 윤리적, 정책적 반응들을 수집하고 가시화하는 작업 ▲‘합의’에 대한 개념적 발전, 긴장관계들, 그리고 합의가 필요한 영역들에 대한 실질적 분석을 제공하고 ▲기존의 논의에서 무시되었던 중요한 질문들, 목소리를 높일 수 없었던 행위자들에게 초점을 맞춰 주기적인 논의가 이루어지는 포럼으로서 역할을 수행하게 될 것이라고 설명했다.
박범순 교수는 “크리스퍼(CRISPR) 유전자 가위로 대표되는 유전체편집기술이 가져올 사회적, 법적, 윤리적, 종교적, 철학적 이슈를 각국의 경험을 바탕으로 논의하고 정보를 공유하기 위한 대화의 장을 마련하자는 취지에서 글로벌 관측소 설립을 제안했다”고 말했다.
2018.07.02 조회수 11948 -
 조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
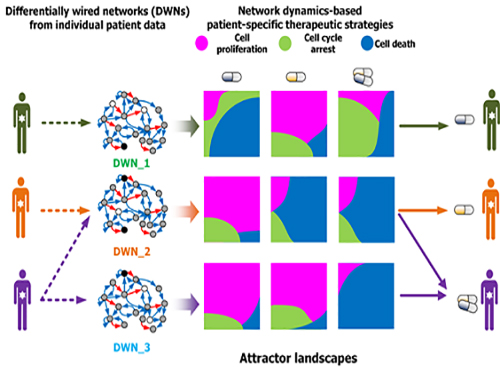
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 24049
조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 24049 -
 조광현 교수, 대장암 유발하는 돌연변이 유전자의 네트워크 원리 규명
〈 왼쪽위부터 시계방향으로 이종훈 박사과정, 공정렬 박사과정, 조광현 교수, 신동관 연구교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암이 발병하는 과정에서 생기는 유전자 네트워크의 원리를 규명하는 데 성공했다.
이를 통해 대장암의 근본적인 발병 원리를 밝혀낼 뿐 아니라 향후 새로운 개념의 효과적인 항암제의 분자표적을 찾는데 활용될 것으로 기대된다. 또한 4차 산업혁명의 핵심 기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명해냈다는 의의를 갖는다.
신동관 박사, 이종훈, 공정렬 학생연구원 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 2일자 온라인 판에 게재됐다.
인간의 암은 유전자 돌연변이에 의해 발생한다. 이 돌연변이의 빈도는 암종에 따라 차이가 나는데 백혈병, 소아암은 10여 개 정도이지만 성인 고형암은 평균 50여 개, 폐암 등의 외부인자로 인한 경우는 수백 개에 이른다.
전 세계 암연구자들은 암 치료를 위해 환자들에게서 빈번하게 발견되는 유전자 돌연변이들을 파악하고 이 중 주요 암 유발 유전자를 찾아내 표적 항암제를 개발하고자 노력했다.
그러나 유전자 돌연변이는 해당 유전자의 기능에만 영향을 주는 게 아니라 그 유전자와 상호작용하는 다른 유전자에게도 영향을 끼친다. 따라서 이러한 유전자 네트워크의 원리를 모른 채 소수의 암 유발 유전자를 대상으로 하는 현재의 치료법은 일부에게만 효과가 있고 쉽게 약물의 내성을 일으키는 한계가 있다.
조 교수 연구팀은 대장암 환자의 대규모 유전체 데이터를 이용해 유전자 상호작용 네트워크에서 나타나는 다중 돌연변이의 협력적 효과에 대한 수학모형을 구축했다.
이는 국제 암유전체컨소시엄에서 발표한 전암 유전체데이터베이스(TCGA: The Cancer Genome Atlas)를 토대로 구축한 것으로, 유전자 네트워크에서 나타나는 돌연변이의 영향력을 정량화하고 이를 이용해 대장암 환자 군을 임상 특징에 따라 군집화 하는데 성공했다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 암 발생 과정에서 나타나는 임계전이(critical transition) 현상을 밝혀내 숨겨진 유전자 네트워크의 원리를 최초로 규명했다.
임계전이란 상전이와 같이 물질의 상태가 갑작스럽게 변화하는 현상을 말한다. 암 발생 과정에서는 유전자 돌연변이의 발생 순서를 추적하기 어렵기 때문에 전이 현상이 존재하는지 확인할 수 없었다.
연구팀은 시스템생물학 기반의 연구방법을 이용해 확인한 결과 기존의 대장암에서 잘 알려진 암 유발 유전자 돌연변이의 발생 순서를 따르는 경우에 임계전이 현상을 보임을 발견했다.
이번에 개발한 수학모형을 활용하면 암환자에게 발생하는 다수 유전자 돌연변이의 영향을 가장 효과적으로 저해할 수 있는 새로운 항암 표적 약물이 개발될 것으로 기대된다.
특히 주요 암 유발 유전자 뿐 아니라 돌연변이의 영향을 받는 다른 모든 유전자들을 대상으로 종합적으로 평가해 효과적인 약물 표적을 찾아낼 수 있다.
조 교수는 “지금껏 다수 유전자들의 돌연변이가 암 발생에 어떻게 기여하는지 밝혀진 바가 없었다”며 “이번 연구에서는 시스템생물학으로 암세포의 발달과정에서 유전자 네트워크의 원리를 최초로 밝힘으로써 새로운 차원의 항암제 표적을 발굴할 수 있는 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유전자 돌연변이의 영향력 전파에 의한 거대 클러스터의 형성
그림2. 암발생 과정에서 돌연변이 협력효과의 임계전이 현상
2017.11.07 조회수 24426
조광현 교수, 대장암 유발하는 돌연변이 유전자의 네트워크 원리 규명
〈 왼쪽위부터 시계방향으로 이종훈 박사과정, 공정렬 박사과정, 조광현 교수, 신동관 연구교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암이 발병하는 과정에서 생기는 유전자 네트워크의 원리를 규명하는 데 성공했다.
이를 통해 대장암의 근본적인 발병 원리를 밝혀낼 뿐 아니라 향후 새로운 개념의 효과적인 항암제의 분자표적을 찾는데 활용될 것으로 기대된다. 또한 4차 산업혁명의 핵심 기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명해냈다는 의의를 갖는다.
신동관 박사, 이종훈, 공정렬 학생연구원 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 2일자 온라인 판에 게재됐다.
인간의 암은 유전자 돌연변이에 의해 발생한다. 이 돌연변이의 빈도는 암종에 따라 차이가 나는데 백혈병, 소아암은 10여 개 정도이지만 성인 고형암은 평균 50여 개, 폐암 등의 외부인자로 인한 경우는 수백 개에 이른다.
전 세계 암연구자들은 암 치료를 위해 환자들에게서 빈번하게 발견되는 유전자 돌연변이들을 파악하고 이 중 주요 암 유발 유전자를 찾아내 표적 항암제를 개발하고자 노력했다.
그러나 유전자 돌연변이는 해당 유전자의 기능에만 영향을 주는 게 아니라 그 유전자와 상호작용하는 다른 유전자에게도 영향을 끼친다. 따라서 이러한 유전자 네트워크의 원리를 모른 채 소수의 암 유발 유전자를 대상으로 하는 현재의 치료법은 일부에게만 효과가 있고 쉽게 약물의 내성을 일으키는 한계가 있다.
조 교수 연구팀은 대장암 환자의 대규모 유전체 데이터를 이용해 유전자 상호작용 네트워크에서 나타나는 다중 돌연변이의 협력적 효과에 대한 수학모형을 구축했다.
이는 국제 암유전체컨소시엄에서 발표한 전암 유전체데이터베이스(TCGA: The Cancer Genome Atlas)를 토대로 구축한 것으로, 유전자 네트워크에서 나타나는 돌연변이의 영향력을 정량화하고 이를 이용해 대장암 환자 군을 임상 특징에 따라 군집화 하는데 성공했다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 암 발생 과정에서 나타나는 임계전이(critical transition) 현상을 밝혀내 숨겨진 유전자 네트워크의 원리를 최초로 규명했다.
임계전이란 상전이와 같이 물질의 상태가 갑작스럽게 변화하는 현상을 말한다. 암 발생 과정에서는 유전자 돌연변이의 발생 순서를 추적하기 어렵기 때문에 전이 현상이 존재하는지 확인할 수 없었다.
연구팀은 시스템생물학 기반의 연구방법을 이용해 확인한 결과 기존의 대장암에서 잘 알려진 암 유발 유전자 돌연변이의 발생 순서를 따르는 경우에 임계전이 현상을 보임을 발견했다.
이번에 개발한 수학모형을 활용하면 암환자에게 발생하는 다수 유전자 돌연변이의 영향을 가장 효과적으로 저해할 수 있는 새로운 항암 표적 약물이 개발될 것으로 기대된다.
특히 주요 암 유발 유전자 뿐 아니라 돌연변이의 영향을 받는 다른 모든 유전자들을 대상으로 종합적으로 평가해 효과적인 약물 표적을 찾아낼 수 있다.
조 교수는 “지금껏 다수 유전자들의 돌연변이가 암 발생에 어떻게 기여하는지 밝혀진 바가 없었다”며 “이번 연구에서는 시스템생물학으로 암세포의 발달과정에서 유전자 네트워크의 원리를 최초로 밝힘으로써 새로운 차원의 항암제 표적을 발굴할 수 있는 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유전자 돌연변이의 영향력 전파에 의한 거대 클러스터의 형성
그림2. 암발생 과정에서 돌연변이 협력효과의 임계전이 현상
2017.11.07 조회수 24426 -
 생명과학과 임대식 교수, 과학기술혁신본부장으로 임명돼
우리대학 생명과학과 임대식 교수(52)가 과학기술정보통신부 과학기술혁신본부장으로 임명됐다. 서울 출신인 임대식 교수는 영일고와 서울대 미생물학과를 졸업하고 미국 텍사스주립대에서 생화학·분자유전학 박사학위를 취득했다. 이후 한국분자세포생물학회 학술위원장과 우리대학 생명과학과 지정 석좌교수를 거쳐 히포(Hippo) 세포분열·분화창의연구단 단장으로 일해왔다.
박수현 청와대 대변인은 31일 과학기술혁신본부장 등에 관한 인선내용을 발표를 하면서 "임 본부장은 암 억제 유전자 기능을 규명한 생명과학 권위자로, 기초과학기술 발전을 위한 연구지원체제를 구축하고 과기분야 혁신을 이끌 적임자"라고 말했다. 문재인정부 들어 신설된 과학기술혁신본부장 직은 차관급 자리로 국가 연구개발(R&D)사업에 대한 막강한 예산 심의 권한을 갖고 있어 과학기술계의 관심이 높았다.
■ 임대식 과학기술정보통신부 과학기술혁신본부장
▲1965년생, 서울 ▲영일고 ▲서울대 미생물학과 ▲미국 텍사스주립대 생화학 및 분자유전학 박사 ▲한국분자세포생물학회 학술위원장 ▲KAIST 생명과학과 교수(現) ▲KAIST 히포(Hippo) 세포분열분화창의연구단 단장(現)
2017.09.03 조회수 11355
생명과학과 임대식 교수, 과학기술혁신본부장으로 임명돼
우리대학 생명과학과 임대식 교수(52)가 과학기술정보통신부 과학기술혁신본부장으로 임명됐다. 서울 출신인 임대식 교수는 영일고와 서울대 미생물학과를 졸업하고 미국 텍사스주립대에서 생화학·분자유전학 박사학위를 취득했다. 이후 한국분자세포생물학회 학술위원장과 우리대학 생명과학과 지정 석좌교수를 거쳐 히포(Hippo) 세포분열·분화창의연구단 단장으로 일해왔다.
박수현 청와대 대변인은 31일 과학기술혁신본부장 등에 관한 인선내용을 발표를 하면서 "임 본부장은 암 억제 유전자 기능을 규명한 생명과학 권위자로, 기초과학기술 발전을 위한 연구지원체제를 구축하고 과기분야 혁신을 이끌 적임자"라고 말했다. 문재인정부 들어 신설된 과학기술혁신본부장 직은 차관급 자리로 국가 연구개발(R&D)사업에 대한 막강한 예산 심의 권한을 갖고 있어 과학기술계의 관심이 높았다.
■ 임대식 과학기술정보통신부 과학기술혁신본부장
▲1965년생, 서울 ▲영일고 ▲서울대 미생물학과 ▲미국 텍사스주립대 생화학 및 분자유전학 박사 ▲한국분자세포생물학회 학술위원장 ▲KAIST 생명과학과 교수(現) ▲KAIST 히포(Hippo) 세포분열분화창의연구단 단장(現)
2017.09.03 조회수 11355 -
 (재)유전자동의보감사업단, 제2회 바이오시너지 기업파트너스 심포지엄 개최
인공지능 시스템을 이용한 천연물 소재 개발기술 발표와 사업단 및 관련기업 간 상호협력 방안 논의를 위한 ‘바이오시너지 기업파트너스 심포지엄’이 17일 열린다.
우리대학과 미래창조과학부 산하 (재)유전자동의보감사업단(단장 이도헌 교수·바이오및뇌공학과)은 한국건강기능식품협회 후원으로 17일 오후 2시30분부터 이화여자대학교 LG컨벤션센터에서 ‘바이오시너지 기업파트너스 심포지엄’을 개최한다.
올 심포지엄은 작년 5월에 열린 ‘바이오시너지 워크숍’행사에 이어 (재)유전자동의보감사업단이 두 번째로 주관, 개최하는 행사다. 이 심포지엄에는 미래부와 식약처·사업단 연구책임자들은 물론 바이오헬스케어 분야의 국내·외 학자와 관련 기업인·전문가들이 대거 참가해서 향후 기술개발 방향과 시장수요 예측·시장중심의 맞춤형 기술이전과 사업화 유망기술 발굴 등에 관해 심도 있게 논의한다.
이번 심포지엄에서는 특히 사업단과 공동연구를 수행 중인 네덜란드의 대표적인 식품연구소인 니조(NIZO)의 엘스 반 호펜(Els Van Hoffen) 실장(Senior Project Manager), 네덜란드 국립응용과학연구소 TNO의 수잔 워페리스(Suzan Wopereis) 책임연구원(Senior Scientist)이 참석해 각각 니조(NIZO)와 TNO의 최신 연구내용과 지난 5년 동안의 기술개발 내용 등에 관해 중점 소개한다.
OECD 발표자료에 따르면 2014년 글로벌 식품산업의 규모는 약 5.5조 달러(약 6,152조원)이며 매년 4.4% 성장하고 있는데 이는 세계 식품시장의 트렌드가 음식을 소비하는 차원에서 유기농 등 안전식품, 기능성 건강식품 위주로 변화하고 있기 때문이다. 농·식품 R&D로 경제성장을 견인한 대표적인 네덜란드는 니조(NIZO)와 TNO 등 시장 친화적인 식품관련 연구소를 중심으로 연구가 이뤄지고 있는데 1948년 낙농업체들이 공동 설립한 니조(NIZO)와 약 30년 전 네덜란드 정부가 세운 TNO는 전체 운영비의 70% 이상을 민간업체들과의 협력이나 개인투자자들과 프로젝트를 진행해서 벌어들이고 있다.
두 전문가의 발표가 끝난 후에는 권오란 이화여대 교수가 사업단이 개발한 기술과 천연물 분야 관련기업 등 산업계와의 상호 연계방안을 모색하는 등 기업인들과 연구 책임자들 간의 관심방안에 대한 토론을 주관, 진행한다. 이밖에 강연 홀 복도에는 발표와 토론이 끝난 후 참석자들이 사업단이 보유중인 기술을 한 눈에 볼 수 있도록 전시관을 꾸며놨으며 기업인들 간에 자연스럽게 상담을 할 수 있는 자리도 함께 마련했다.
이도헌 사업단장은 “2013년 11월 출범이후 사업단은 5개 연구 분야인 모델·소재·표적 마커·인체 연구에 역량을 집중한 결과, 성분기반의 바이오 헬스케어와 관련한 방대한 규모의 DB를 구축하고 이를 기반으로 천연물 성분의 인체작용을 분석할 수 있는 세계 최대 규모의 가상인체(인공지능) 시스템을 구축했다” 며 “이번 심포지엄에서 사업단과 관련기업들 간에 공동연구 및 연구 성과에 대한 공동 활용방안에 대한 심층적인 논의가 이뤄졌으면 한다”고 말했다. 참가 문의 042-350-8651.
2017.07.14 조회수 16262
(재)유전자동의보감사업단, 제2회 바이오시너지 기업파트너스 심포지엄 개최
인공지능 시스템을 이용한 천연물 소재 개발기술 발표와 사업단 및 관련기업 간 상호협력 방안 논의를 위한 ‘바이오시너지 기업파트너스 심포지엄’이 17일 열린다.
우리대학과 미래창조과학부 산하 (재)유전자동의보감사업단(단장 이도헌 교수·바이오및뇌공학과)은 한국건강기능식품협회 후원으로 17일 오후 2시30분부터 이화여자대학교 LG컨벤션센터에서 ‘바이오시너지 기업파트너스 심포지엄’을 개최한다.
올 심포지엄은 작년 5월에 열린 ‘바이오시너지 워크숍’행사에 이어 (재)유전자동의보감사업단이 두 번째로 주관, 개최하는 행사다. 이 심포지엄에는 미래부와 식약처·사업단 연구책임자들은 물론 바이오헬스케어 분야의 국내·외 학자와 관련 기업인·전문가들이 대거 참가해서 향후 기술개발 방향과 시장수요 예측·시장중심의 맞춤형 기술이전과 사업화 유망기술 발굴 등에 관해 심도 있게 논의한다.
이번 심포지엄에서는 특히 사업단과 공동연구를 수행 중인 네덜란드의 대표적인 식품연구소인 니조(NIZO)의 엘스 반 호펜(Els Van Hoffen) 실장(Senior Project Manager), 네덜란드 국립응용과학연구소 TNO의 수잔 워페리스(Suzan Wopereis) 책임연구원(Senior Scientist)이 참석해 각각 니조(NIZO)와 TNO의 최신 연구내용과 지난 5년 동안의 기술개발 내용 등에 관해 중점 소개한다.
OECD 발표자료에 따르면 2014년 글로벌 식품산업의 규모는 약 5.5조 달러(약 6,152조원)이며 매년 4.4% 성장하고 있는데 이는 세계 식품시장의 트렌드가 음식을 소비하는 차원에서 유기농 등 안전식품, 기능성 건강식품 위주로 변화하고 있기 때문이다. 농·식품 R&D로 경제성장을 견인한 대표적인 네덜란드는 니조(NIZO)와 TNO 등 시장 친화적인 식품관련 연구소를 중심으로 연구가 이뤄지고 있는데 1948년 낙농업체들이 공동 설립한 니조(NIZO)와 약 30년 전 네덜란드 정부가 세운 TNO는 전체 운영비의 70% 이상을 민간업체들과의 협력이나 개인투자자들과 프로젝트를 진행해서 벌어들이고 있다.
두 전문가의 발표가 끝난 후에는 권오란 이화여대 교수가 사업단이 개발한 기술과 천연물 분야 관련기업 등 산업계와의 상호 연계방안을 모색하는 등 기업인들과 연구 책임자들 간의 관심방안에 대한 토론을 주관, 진행한다. 이밖에 강연 홀 복도에는 발표와 토론이 끝난 후 참석자들이 사업단이 보유중인 기술을 한 눈에 볼 수 있도록 전시관을 꾸며놨으며 기업인들 간에 자연스럽게 상담을 할 수 있는 자리도 함께 마련했다.
이도헌 사업단장은 “2013년 11월 출범이후 사업단은 5개 연구 분야인 모델·소재·표적 마커·인체 연구에 역량을 집중한 결과, 성분기반의 바이오 헬스케어와 관련한 방대한 규모의 DB를 구축하고 이를 기반으로 천연물 성분의 인체작용을 분석할 수 있는 세계 최대 규모의 가상인체(인공지능) 시스템을 구축했다” 며 “이번 심포지엄에서 사업단과 관련기업들 간에 공동연구 및 연구 성과에 대한 공동 활용방안에 대한 심층적인 논의가 이뤄졌으면 한다”고 말했다. 참가 문의 042-350-8651.
2017.07.14 조회수 16262 -
 이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
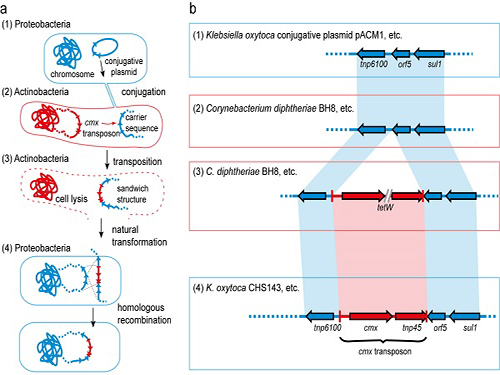
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 23681
이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 23681 -
 전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
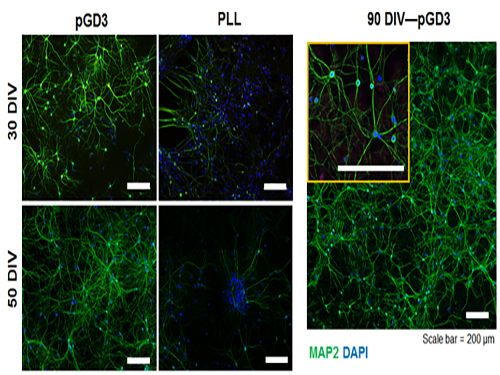
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 25885
전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 25885 -
 유전자동의보감 사업단, 녹십자HS의 천연물 신약 글로벌 시장 진출 지원
메르스 여파로 면역력을 강화하는 인삼과 홍삼 제품의 매출이 크게 증가하고 있다. 인삼은 한국의 대표적인 특산물이자 수출효자 품목이었으나 과학적인 작용 원리는 아직 정확히 규명되지 못하고 있으며 현재 해외시장의 2%도 점유하지 못하고 있는 상황이다.
이러한 가운데 유전자동의보감사업단(단장 이도헌 KAIST 교수)과 ㈜녹십자HS(대표이사 유영효)는 6월 10일 KAIST에서 특정 진세노사이드가 강화된 BST204 천연물신약의 글로벌 시장 진출을 위한 협력연구협약(MOU) 및 비밀유지계약(NDA)을 체결했다.
유전자동의보감사업단은 MCMT(multi-component multi-target, 다중성분 다중표적) 기반 천연물 신약개발 플랫폼을 활용하여 ㈜녹십자HS가 개발 중인 BST204 천연물신약 개발 연구에 협력하기로 하였으며 이는 해당 제품의 유럽시장 진출에 큰 도움이 될 것으로 기대되고 있다.
㈜녹십자HS가 개발 중인 BST204 천연물신약은 인삼에 바이오변환기술을 적용하여 특정 진세노사이드 유효성분의 효능을 강화시킨 조성물로서 국내 제약사가 개발한 천연물신약 중 최초로 독일에서 임상1상 시험을 완료하고 임상2상 시험을 앞두고 있다.
이도헌 교수(사업단장)는 “유전자동의보감 사업단은 천연물 복합성분이 인체에서 작용하는 원리를 가상인체 컴퓨터 모델과 멀티오믹스 등 융합원천기술로 규명하여 미래 창조형 헬스케어 신소재를 발굴한다는 것을 목표로 하고 있다”며 “특히, 가상인체 컴퓨터모델은 독창적인 신기술로서 국내 제약기업의 글로벌 시장 진출에 효자역할을 할 플랫폼 기술이 될 것”으로 전망했다.
유영효 대표이사는 “천연물 신약이 유럽, 미국 등 글로벌 시장에서 인정받기 위해서는 효능과 안전성을 입증하는 것은 물론 정확한 작용원리까지도 제시해야 한다”며 “하지만 다양한 성분의 혼합물인 천연물의 특성상 작용원리를 규명하는 것이 매우 어렵고 시간과 비용이 많이 들기 때문에 이 문제를 해결하기 위해서는 획기적인 기술혁신이 필요한 상황이다”이라고 밝혔다. 끝.
2015.06.10 조회수 12194
유전자동의보감 사업단, 녹십자HS의 천연물 신약 글로벌 시장 진출 지원
메르스 여파로 면역력을 강화하는 인삼과 홍삼 제품의 매출이 크게 증가하고 있다. 인삼은 한국의 대표적인 특산물이자 수출효자 품목이었으나 과학적인 작용 원리는 아직 정확히 규명되지 못하고 있으며 현재 해외시장의 2%도 점유하지 못하고 있는 상황이다.
이러한 가운데 유전자동의보감사업단(단장 이도헌 KAIST 교수)과 ㈜녹십자HS(대표이사 유영효)는 6월 10일 KAIST에서 특정 진세노사이드가 강화된 BST204 천연물신약의 글로벌 시장 진출을 위한 협력연구협약(MOU) 및 비밀유지계약(NDA)을 체결했다.
유전자동의보감사업단은 MCMT(multi-component multi-target, 다중성분 다중표적) 기반 천연물 신약개발 플랫폼을 활용하여 ㈜녹십자HS가 개발 중인 BST204 천연물신약 개발 연구에 협력하기로 하였으며 이는 해당 제품의 유럽시장 진출에 큰 도움이 될 것으로 기대되고 있다.
㈜녹십자HS가 개발 중인 BST204 천연물신약은 인삼에 바이오변환기술을 적용하여 특정 진세노사이드 유효성분의 효능을 강화시킨 조성물로서 국내 제약사가 개발한 천연물신약 중 최초로 독일에서 임상1상 시험을 완료하고 임상2상 시험을 앞두고 있다.
이도헌 교수(사업단장)는 “유전자동의보감 사업단은 천연물 복합성분이 인체에서 작용하는 원리를 가상인체 컴퓨터 모델과 멀티오믹스 등 융합원천기술로 규명하여 미래 창조형 헬스케어 신소재를 발굴한다는 것을 목표로 하고 있다”며 “특히, 가상인체 컴퓨터모델은 독창적인 신기술로서 국내 제약기업의 글로벌 시장 진출에 효자역할을 할 플랫폼 기술이 될 것”으로 전망했다.
유영효 대표이사는 “천연물 신약이 유럽, 미국 등 글로벌 시장에서 인정받기 위해서는 효능과 안전성을 입증하는 것은 물론 정확한 작용원리까지도 제시해야 한다”며 “하지만 다양한 성분의 혼합물인 천연물의 특성상 작용원리를 규명하는 것이 매우 어렵고 시간과 비용이 많이 들기 때문에 이 문제를 해결하기 위해서는 획기적인 기술혁신이 필요한 상황이다”이라고 밝혔다. 끝.
2015.06.10 조회수 12194