%EC%95%8C%EC%B8%A0%ED%95%98%EC%9D%B4%EB%A8%B8
-
 알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 27281
알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 27281 -
 알츠하이머 치료제 개발을 위한 새로운 가능성 제시
우리 연구진이 알츠하이머 발병 원인을 동시다발적으로 억제 가능한 치료제 개발 원리를 증명하고 또 동물실험에서 효능을 입증하는 등 알츠하이머병에 관한 새로운 치료제 개발에 대한 가능성을 제시함으로써 많은 주목을 받고 있다.
우리 대학 화학과 임미희 교수 연구팀이 알츠하이머 발병의 원인으로 알려진 ‘활성 산소종’과 ‘아밀로이드 베타’, ‘금속 이온’ 등을 손쉽고도 동시다발적으로 억제할 수 있는 치료제 개발 원리를 새롭게 증명하고 알츠하이머 질환에 걸린 동물 모델(실험용 쥐) 치료를 통해 이를 입증하는 데 성공했다고 11일 밝혔다.
이번 연구에는 KAIST 백무현 교수와 서울아산병원 이주영 교수도 함께 참여했으며 저명 국제 학술지인 미국 화학회지(Journal of the American Chemical Society) 4월 1일 字에 게재됐다. 이 논문은 특히 4월 26일 字 ‘편집장 선정 우수 논문(Editors’Choice Paper)’으로 꼽혀 많은 주목을 받고 있다. (논문명 : Minimalistic Principles for Designing Small Molecules with Multiple Reactivities against Pathological Factors in Dementia)
알츠하이머병은 치매를 일으키는 대표적인 뇌 질환이다. 이 질환의 원인으로 다양한 요소들이 제시됐지만, 원인 인자들 사이의 원리들은 아직도 명확하게 밝혀지지 않고 있다.
알츠하이머병을 일으키는 대표적인 원인 인자로는, 활성 산소종과 아밀로이드 베타, 금속 이온이 알려져 있다. 이 요인들은 개별적으로 질병을 유발할 뿐만 아니라, 상호 작용을 통해 뇌 질환을 더욱 악화시킬 수 있다. 예를 들어, 금속 이온들은 아밀로이드 베타와 결합해 아밀로이드 베타의 응집 속도를 촉진시킬 뿐만 아니라, 활성 산소종들을 과다하게 생성하여 신경독성을 유발할 수 있다. 따라서 이처럼 복잡하게 얽힌 여러 원인 인자들을 동시에 겨냥할 수 있는 새로운 알츠하이머병 치료제 개발이 필요하다.
임 교수 연구팀은 단순한 저분자 화합물의 산화 환원 반응을 이용해 알츠하이머병의 원인 인자들을 손쉽게 조절할 수 있음을 증명했다. 임 교수팀은 산화되는 정도가 다른 화합물들의 합리적 설계를 통해 쉽게 산화되는 화합물들은 알츠하이머 질병의 여러 원인 인자들을 한꺼번에 조절할 수 있다는 사실을 확인했다.
연구 결과, 임 교수 연구팀은 저분자 화합물의 산화 환원 반응으로 활성 산소종에 대한 항산화 작용의 가능성을 확인했을 뿐만 아니라 아밀로이드 베타 또는 금속-아밀로이드 베타의 응집 및 섬유 형성 정도 또한 확연히 감소되는 것을 실험적으로 증명했다.
이 밖에 알츠하이머병에 걸린 동물 모델(실험용 쥐)에 체외 반응성이 좋고 바이오 응용에 적합한 성질을 가지고 있는 대표 저분자 화합물을 주입한 한 결과, 뇌 속에 축적된 아밀로이드 베타의 양이 크게 줄어드는 현상과 함께 알츠하이머 동물 모델의 손상된 인지 능력과 기억력이 향상되는 결과를 확인했다.
이번 연구가 크게 주목받는 이유는 알츠하이머병을 치료하기 위한 화합물을 개발하는 데 있어 아주 단순한 방향족 저분자 화합물의 구조변화를 통해 산화 환원 정도를 조절하여 여러 원인 인자들을 동시에 조절할 수 있고 이러한 간단한 원리를 통해 누구나 손쉽게 치료제를 디자인할 수 있기 때문이다.
임미희 교수는“이번 연구는 아주 단순한 방향족 저분자 화합물의 산화 정도의 차이를 이용해 여러 원인 인자들과의 반응성 유무를 확연히 구분할 수 있다는 점을 증명한 데 의미가 있다”며, “이 방법을 신약 개발의 디자인 방법으로 사용한다면, 비용과 시간을 훨씬 단축시켜 최대의 효과를 가질 수 있다”고 덧붙였다. 임 교수는 이와 함께 “제시된 치료제의 디자인 방법은 다양한 퇴행성 뇌 질환 치료제들의 개발 성공 가능성을 높일 것으로 기대된다”라고 강조했다.
한편 이번 연구는 한국연구재단, 기초과학연구원과 서울아산병원 등의 지원을 받아 수행됐다.
2020.05.11 조회수 19823
알츠하이머 치료제 개발을 위한 새로운 가능성 제시
우리 연구진이 알츠하이머 발병 원인을 동시다발적으로 억제 가능한 치료제 개발 원리를 증명하고 또 동물실험에서 효능을 입증하는 등 알츠하이머병에 관한 새로운 치료제 개발에 대한 가능성을 제시함으로써 많은 주목을 받고 있다.
우리 대학 화학과 임미희 교수 연구팀이 알츠하이머 발병의 원인으로 알려진 ‘활성 산소종’과 ‘아밀로이드 베타’, ‘금속 이온’ 등을 손쉽고도 동시다발적으로 억제할 수 있는 치료제 개발 원리를 새롭게 증명하고 알츠하이머 질환에 걸린 동물 모델(실험용 쥐) 치료를 통해 이를 입증하는 데 성공했다고 11일 밝혔다.
이번 연구에는 KAIST 백무현 교수와 서울아산병원 이주영 교수도 함께 참여했으며 저명 국제 학술지인 미국 화학회지(Journal of the American Chemical Society) 4월 1일 字에 게재됐다. 이 논문은 특히 4월 26일 字 ‘편집장 선정 우수 논문(Editors’Choice Paper)’으로 꼽혀 많은 주목을 받고 있다. (논문명 : Minimalistic Principles for Designing Small Molecules with Multiple Reactivities against Pathological Factors in Dementia)
알츠하이머병은 치매를 일으키는 대표적인 뇌 질환이다. 이 질환의 원인으로 다양한 요소들이 제시됐지만, 원인 인자들 사이의 원리들은 아직도 명확하게 밝혀지지 않고 있다.
알츠하이머병을 일으키는 대표적인 원인 인자로는, 활성 산소종과 아밀로이드 베타, 금속 이온이 알려져 있다. 이 요인들은 개별적으로 질병을 유발할 뿐만 아니라, 상호 작용을 통해 뇌 질환을 더욱 악화시킬 수 있다. 예를 들어, 금속 이온들은 아밀로이드 베타와 결합해 아밀로이드 베타의 응집 속도를 촉진시킬 뿐만 아니라, 활성 산소종들을 과다하게 생성하여 신경독성을 유발할 수 있다. 따라서 이처럼 복잡하게 얽힌 여러 원인 인자들을 동시에 겨냥할 수 있는 새로운 알츠하이머병 치료제 개발이 필요하다.
임 교수 연구팀은 단순한 저분자 화합물의 산화 환원 반응을 이용해 알츠하이머병의 원인 인자들을 손쉽게 조절할 수 있음을 증명했다. 임 교수팀은 산화되는 정도가 다른 화합물들의 합리적 설계를 통해 쉽게 산화되는 화합물들은 알츠하이머 질병의 여러 원인 인자들을 한꺼번에 조절할 수 있다는 사실을 확인했다.
연구 결과, 임 교수 연구팀은 저분자 화합물의 산화 환원 반응으로 활성 산소종에 대한 항산화 작용의 가능성을 확인했을 뿐만 아니라 아밀로이드 베타 또는 금속-아밀로이드 베타의 응집 및 섬유 형성 정도 또한 확연히 감소되는 것을 실험적으로 증명했다.
이 밖에 알츠하이머병에 걸린 동물 모델(실험용 쥐)에 체외 반응성이 좋고 바이오 응용에 적합한 성질을 가지고 있는 대표 저분자 화합물을 주입한 한 결과, 뇌 속에 축적된 아밀로이드 베타의 양이 크게 줄어드는 현상과 함께 알츠하이머 동물 모델의 손상된 인지 능력과 기억력이 향상되는 결과를 확인했다.
이번 연구가 크게 주목받는 이유는 알츠하이머병을 치료하기 위한 화합물을 개발하는 데 있어 아주 단순한 방향족 저분자 화합물의 구조변화를 통해 산화 환원 정도를 조절하여 여러 원인 인자들을 동시에 조절할 수 있고 이러한 간단한 원리를 통해 누구나 손쉽게 치료제를 디자인할 수 있기 때문이다.
임미희 교수는“이번 연구는 아주 단순한 방향족 저분자 화합물의 산화 정도의 차이를 이용해 여러 원인 인자들과의 반응성 유무를 확연히 구분할 수 있다는 점을 증명한 데 의미가 있다”며, “이 방법을 신약 개발의 디자인 방법으로 사용한다면, 비용과 시간을 훨씬 단축시켜 최대의 효과를 가질 수 있다”고 덧붙였다. 임 교수는 이와 함께 “제시된 치료제의 디자인 방법은 다양한 퇴행성 뇌 질환 치료제들의 개발 성공 가능성을 높일 것으로 기대된다”라고 강조했다.
한편 이번 연구는 한국연구재단, 기초과학연구원과 서울아산병원 등의 지원을 받아 수행됐다.
2020.05.11 조회수 19823 -
 두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17891
두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17891 -
 산소 이용해 알츠하이머 유발 단백질 독성 개선
화학과 임미희 교수 연구팀이 공기 중의 산소를 이용해 알츠하이머 유발에 관여하는 단백질의 독성을 개선할 수 있는 화학적 도구를 설계하는 데 성공했다.
연구팀은 알츠하이머 발병에 관여한다고 알려진 구리-아밀로이드 베타 복합체의 응집과 이에 의한 발생한 세포 독성을 개선할 수 있는 화학적 도구를 설계하고, 구리 배위권 이중 변형을 통한 작용 원리를 분자적 수준에서 밝혀냈다.
한지연 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지인 미국 국립과학원회보(PNAS)에 2월 27일 자로 게재됐다.(논문명 : Mechanistic approaches for chemically modifying the coordination sphere of copper-amyloid-β complexes)
전이 금속 중 구리 이온은 항산화 작용과 신경전달물질 생성 등 신체에 필수적인 생리적 기능에 관여한다. 건강한 사람의 뇌와 달리 알츠하이머병 같은 퇴행성 뇌 질환 환자의 뇌에서는 이러한 구리 이온의 항상성이 완전히 무너져있다고 알려져 있다.
알츠하이머 발병에 밀접하게 관계가 있다고 알려진 아밀로이드 베타 펩타이드는 구리 이온과 강하게 결합할 수 있다. 구리 이온은 아밀로이드 베타의 응집을 촉진할 뿐만 아니라, 활성산소를 과다하게 생성해 신경독성을 일으킨다. 따라서 구리-아밀로이드 베타 복합체를 표적하고 그 배위 결합을 효과적으로 막을 수 있는 화학적 접근 기법이 최근 주목받고 있다.
연구팀은 알츠하이머 발병 원리에 직간접적으로 관여하는 구리 이온이 공기 중 산소와 반응할 수 있다는 점을 이용했다. 이에 구리-아밀로이드 베타 복합체와 상호작용할 수 있도록 화합물을 합리적으로 설계하고, 해당분자가 산소가 존재하는 환경에서 구리 배위권에 위치한 특정 아미노산에 결합 및 산화에 의한 이중 변형을 일으킨 것을 확인했다.
연구팀은 연구팀이 개발한 배위권 이중 변형 기법에 따라 구리-아밀로이드 베타의 응집 과정 및 섬유 형성 정도가 확연히 달라짐을 확인했다. 이 기법을 통해 구리 이온의 병리학적 특성 중 하나인 활성산소 생성 정도 또한 두드러지게 개선된 것을 관찰했다.
나아가 기존의 기법과 비교했을 때 구리-아밀로이드 베타 복합체에 의한 세포 독성을 더욱 효과적으로 회복시키는 것으로 나타났다.
이번 연구는 산소의 유무, 전이 금속의 종류, 산화 활성 금속의 산화수, 아밀로이드성 단백질의 종류 등 다양한 변수의 통제를 통해 해당 화합물이 아밀로이드 베타의 구리 배위권을 어떻게 변형시켰는지에 대한 작용 원리를 분자적 수준에서 제안했다는 의의가 있다.
임미희 교수는 “알츠하이머 발병에 관여한다고 알려진 구리 이온이 산소와 반응할 수 있다는 점을 역으로 이용했다”라며 “이번 연구에서 최초로 발표한 단백질 내 구리 배위권 이중 변형 기법을 바탕으로, 다른 퇴행성 뇌질환의 치료제 개발에도 더욱 박차를 가할 수 있을 것이다”라고 말했다.
이번 연구는 한국연구재단과 KAIST의 지원으로 수행됐다.
2020.03.03 조회수 17808
산소 이용해 알츠하이머 유발 단백질 독성 개선
화학과 임미희 교수 연구팀이 공기 중의 산소를 이용해 알츠하이머 유발에 관여하는 단백질의 독성을 개선할 수 있는 화학적 도구를 설계하는 데 성공했다.
연구팀은 알츠하이머 발병에 관여한다고 알려진 구리-아밀로이드 베타 복합체의 응집과 이에 의한 발생한 세포 독성을 개선할 수 있는 화학적 도구를 설계하고, 구리 배위권 이중 변형을 통한 작용 원리를 분자적 수준에서 밝혀냈다.
한지연 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지인 미국 국립과학원회보(PNAS)에 2월 27일 자로 게재됐다.(논문명 : Mechanistic approaches for chemically modifying the coordination sphere of copper-amyloid-β complexes)
전이 금속 중 구리 이온은 항산화 작용과 신경전달물질 생성 등 신체에 필수적인 생리적 기능에 관여한다. 건강한 사람의 뇌와 달리 알츠하이머병 같은 퇴행성 뇌 질환 환자의 뇌에서는 이러한 구리 이온의 항상성이 완전히 무너져있다고 알려져 있다.
알츠하이머 발병에 밀접하게 관계가 있다고 알려진 아밀로이드 베타 펩타이드는 구리 이온과 강하게 결합할 수 있다. 구리 이온은 아밀로이드 베타의 응집을 촉진할 뿐만 아니라, 활성산소를 과다하게 생성해 신경독성을 일으킨다. 따라서 구리-아밀로이드 베타 복합체를 표적하고 그 배위 결합을 효과적으로 막을 수 있는 화학적 접근 기법이 최근 주목받고 있다.
연구팀은 알츠하이머 발병 원리에 직간접적으로 관여하는 구리 이온이 공기 중 산소와 반응할 수 있다는 점을 이용했다. 이에 구리-아밀로이드 베타 복합체와 상호작용할 수 있도록 화합물을 합리적으로 설계하고, 해당분자가 산소가 존재하는 환경에서 구리 배위권에 위치한 특정 아미노산에 결합 및 산화에 의한 이중 변형을 일으킨 것을 확인했다.
연구팀은 연구팀이 개발한 배위권 이중 변형 기법에 따라 구리-아밀로이드 베타의 응집 과정 및 섬유 형성 정도가 확연히 달라짐을 확인했다. 이 기법을 통해 구리 이온의 병리학적 특성 중 하나인 활성산소 생성 정도 또한 두드러지게 개선된 것을 관찰했다.
나아가 기존의 기법과 비교했을 때 구리-아밀로이드 베타 복합체에 의한 세포 독성을 더욱 효과적으로 회복시키는 것으로 나타났다.
이번 연구는 산소의 유무, 전이 금속의 종류, 산화 활성 금속의 산화수, 아밀로이드성 단백질의 종류 등 다양한 변수의 통제를 통해 해당 화합물이 아밀로이드 베타의 구리 배위권을 어떻게 변형시켰는지에 대한 작용 원리를 분자적 수준에서 제안했다는 의의가 있다.
임미희 교수는 “알츠하이머 발병에 관여한다고 알려진 구리 이온이 산소와 반응할 수 있다는 점을 역으로 이용했다”라며 “이번 연구에서 최초로 발표한 단백질 내 구리 배위권 이중 변형 기법을 바탕으로, 다른 퇴행성 뇌질환의 치료제 개발에도 더욱 박차를 가할 수 있을 것이다”라고 말했다.
이번 연구는 한국연구재단과 KAIST의 지원으로 수행됐다.
2020.03.03 조회수 17808 -
 박찬범, 스티브 박 교수, 혈액 기반 알츠하이머병 멀티플렉스 진단센서 개발
KAIST(총장 신성철) 신소재공학과 박찬범 교수와 스티브 박 교수 공동 연구팀이 혈액으로 알츠하이머병을 진단할 수 있는 센서를 개발하는 데 성공했다.
연구팀이 개발한 진단 센서를 활용해 혈액 내에 존재하는 베타-아밀로이드 및 타우 단백질 등 알츠하이머병과 관련한 4종의 바이오마커 농도를 측정·비교하면 민감도는 90%, 정확도 88.6%로 중증 알츠하이머 환자를 구별해 낼 수 있다.
김가영 박사과정·김민지 석사과정이 공동 1저자로 참여한 이번 연구 결과는 국제 학술지‘네이처 커뮤니케이션스(Nature communications)’1월 8일 자 온라인판에 게재됐다. (논문명: Clinically accurate diagnosis of Alzheimer’s disease via multiplexed sensing of core biomarkers in human plasma)
알츠하이머병은 치매의 약 70%를 차지하는 대표적인 치매 질환이다. 현재 전 세계 65세 이상 인구 중 10% 이상이 이 질병으로 인해 고통을 받고 있다. 하지만 현재의 진단 방법은 고가의 양전자 단층촬영(PET) 또는 자기공명영상진단(MRI) 장비를 사용해야만 하기에 많은 환자를 진단하기 위해서는 저렴하면서도 정확한 진단 기술개발의 필요성이 제기돼 왔다.
연구팀은 랑뮤어 블라젯(Langmuir-blodgett)이라는 기술을 이용해 고밀도로 정렬한 탄소 나노튜브(Carbon nanotube)를 기반으로 한 고민감성의 저항 센서를 개발했다. 탄소 나노튜브를 고밀도로 정렬하게 되면 무작위의 방향성을 가질 때 생성되는 접합 저항(Tube-to-tube junction resistance)을 최소화할 수 있어 분석물을 더 민감하게 검출할 수 있다.
실제로 고밀도로 정렬된 탄소 나노튜브를 이용한 저항 센서는 기존에 개발된 탄소 나노튜브 기반의 바이오센서들 대비 100배 이상의 높은 민감도를 보였다.
연구팀은 고밀도로 정렬된 탄소 나노튜브를 이용해 혈액에 존재하는 알츠하이머병의 바이오마커 4종류를 동시에 측정할 수 있는 저항 센서 칩을 제작했다. 알츠하이머병의 대표적인 바이오마커인 베타-아밀로이드 42 (β-amyloid42,), 베타-아밀로이드 40 (β-amyloid40), 총-타우 단백질 (Total tau proteins) 및 과인산화된 타우 단백질 (Phosphorylated tau proteins)은 그 양이 알츠하이머병의 병리와 직접적인 상관관계를 가지기 때문에 알츠하이머병 환자를 구별해 내는 데 매우 유용하다.
고밀도로 정렬된 탄소 나노튜브 기반 센서 칩을 이용해 실제 알츠하이머 환자와 정상인의 혈액 샘플 내에 존재하는 4종의 바이오마커 농도를 측정 하고 비교한 결과, 민감도와 선택성은 각각 90%, 그리고 88.6%의 정확도를 지녀 중증 알츠하이머 환자를 상당히 정확하게 진단할 수 있음을 확인했다. 연구팀이 개발한 고밀도로 정렬된 탄소 나노튜브 센서는 측정방식이 간편하고, 제작비용도 저렴하다.
박찬범 교수는“본 연구는 알츠하이머병으로 이미 확정된 중증환자들을 대상으로 진행하였다. 향후 실제 진료 환경에 활용하기 위해서는 경도인지장애 (Mild cognitive impairment) 환자의 진단 가능성을 테스트하는 것이 필요하다”며“이를 위하여 경도인지장애 코호트, 치매 코호트 등의 범국가적인 인프라 구축이 필수적이며, 국가 공공기관의 적극적인 연구 네트워크 구축 및 지원의 장기성 보장이 요구된다”고 강조했다.
한편 이번 연구는 과학기술정보통신부 리더연구자 지원사업과 충남대병원 및 충북대병원 인체자원은행의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 혈액 내에 존재하는 총 4종의 바이오마커 농도를 측정해 알츠하이머병 환자를 구별하는 고밀도로 정렬된 카본 나노튜브 기반 저항 센서의 모식도
그림 2. 진단 센서 성능
2020.01.15 조회수 22682
박찬범, 스티브 박 교수, 혈액 기반 알츠하이머병 멀티플렉스 진단센서 개발
KAIST(총장 신성철) 신소재공학과 박찬범 교수와 스티브 박 교수 공동 연구팀이 혈액으로 알츠하이머병을 진단할 수 있는 센서를 개발하는 데 성공했다.
연구팀이 개발한 진단 센서를 활용해 혈액 내에 존재하는 베타-아밀로이드 및 타우 단백질 등 알츠하이머병과 관련한 4종의 바이오마커 농도를 측정·비교하면 민감도는 90%, 정확도 88.6%로 중증 알츠하이머 환자를 구별해 낼 수 있다.
김가영 박사과정·김민지 석사과정이 공동 1저자로 참여한 이번 연구 결과는 국제 학술지‘네이처 커뮤니케이션스(Nature communications)’1월 8일 자 온라인판에 게재됐다. (논문명: Clinically accurate diagnosis of Alzheimer’s disease via multiplexed sensing of core biomarkers in human plasma)
알츠하이머병은 치매의 약 70%를 차지하는 대표적인 치매 질환이다. 현재 전 세계 65세 이상 인구 중 10% 이상이 이 질병으로 인해 고통을 받고 있다. 하지만 현재의 진단 방법은 고가의 양전자 단층촬영(PET) 또는 자기공명영상진단(MRI) 장비를 사용해야만 하기에 많은 환자를 진단하기 위해서는 저렴하면서도 정확한 진단 기술개발의 필요성이 제기돼 왔다.
연구팀은 랑뮤어 블라젯(Langmuir-blodgett)이라는 기술을 이용해 고밀도로 정렬한 탄소 나노튜브(Carbon nanotube)를 기반으로 한 고민감성의 저항 센서를 개발했다. 탄소 나노튜브를 고밀도로 정렬하게 되면 무작위의 방향성을 가질 때 생성되는 접합 저항(Tube-to-tube junction resistance)을 최소화할 수 있어 분석물을 더 민감하게 검출할 수 있다.
실제로 고밀도로 정렬된 탄소 나노튜브를 이용한 저항 센서는 기존에 개발된 탄소 나노튜브 기반의 바이오센서들 대비 100배 이상의 높은 민감도를 보였다.
연구팀은 고밀도로 정렬된 탄소 나노튜브를 이용해 혈액에 존재하는 알츠하이머병의 바이오마커 4종류를 동시에 측정할 수 있는 저항 센서 칩을 제작했다. 알츠하이머병의 대표적인 바이오마커인 베타-아밀로이드 42 (β-amyloid42,), 베타-아밀로이드 40 (β-amyloid40), 총-타우 단백질 (Total tau proteins) 및 과인산화된 타우 단백질 (Phosphorylated tau proteins)은 그 양이 알츠하이머병의 병리와 직접적인 상관관계를 가지기 때문에 알츠하이머병 환자를 구별해 내는 데 매우 유용하다.
고밀도로 정렬된 탄소 나노튜브 기반 센서 칩을 이용해 실제 알츠하이머 환자와 정상인의 혈액 샘플 내에 존재하는 4종의 바이오마커 농도를 측정 하고 비교한 결과, 민감도와 선택성은 각각 90%, 그리고 88.6%의 정확도를 지녀 중증 알츠하이머 환자를 상당히 정확하게 진단할 수 있음을 확인했다. 연구팀이 개발한 고밀도로 정렬된 탄소 나노튜브 센서는 측정방식이 간편하고, 제작비용도 저렴하다.
박찬범 교수는“본 연구는 알츠하이머병으로 이미 확정된 중증환자들을 대상으로 진행하였다. 향후 실제 진료 환경에 활용하기 위해서는 경도인지장애 (Mild cognitive impairment) 환자의 진단 가능성을 테스트하는 것이 필요하다”며“이를 위하여 경도인지장애 코호트, 치매 코호트 등의 범국가적인 인프라 구축이 필수적이며, 국가 공공기관의 적극적인 연구 네트워크 구축 및 지원의 장기성 보장이 요구된다”고 강조했다.
한편 이번 연구는 과학기술정보통신부 리더연구자 지원사업과 충남대병원 및 충북대병원 인체자원은행의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 혈액 내에 존재하는 총 4종의 바이오마커 농도를 측정해 알츠하이머병 환자를 구별하는 고밀도로 정렬된 카본 나노튜브 기반 저항 센서의 모식도
그림 2. 진단 센서 성능
2020.01.15 조회수 22682 -
 임미희 교수, 손상된 뇌 신경교세포 회복 물질 개발
우리 대학 화학과 임미희 교수 연구팀이 손상된 뇌의 신경교세포를 회복시키는 저분자 화합물(Small molecule)을 발견했다.
연구팀의 이번 연구는 기억력 등 인지기능이 저하돼 일상생활의 장애를 유발하는 알츠하이머 등 만성질환의 치료 가능성을 제시할 수 있을 것으로 기대된다.
경북대 의대 박민희 교수가 1 저자로 참여하고 경북대 배재성, 진희경 교수가 공동 교신저자로 참여한 이번 연구는 미국 국립과학원에서 발행하는 국제 학술지 ‘PNAS’ 11월 4일 자 온라인판에 게재됐다.
퇴행성 뇌 질환인 치매의 일종인 알츠하이머병은 다양한 원인에 의해 발생된다. 이 질병을 치료하기 위해서 병의 원인을 정확히 파악하고 그에 맞는 치료제들을 개발하는 것이 무엇보다 중요하다.
아밀로이드-베타 펩타이드는 알츠하이머병과 밀접한 관계가 있다고 알려져 있다. 또한, 뇌의 신경 세포이며 면역 세포인 신경교세포는 신경염증 반응에 중추적인 역할을 한다. 최근 들어, 아밀로이드-베타 펩타이드와 신경교세포의 신경염증 반응 사이의 상관관계가 알츠하이머병을 일으킬 수 있는 주요한 원인으로 주목받고 있다.
신경교세포는 뇌에서 면역기능을 담당하는 신경세포의 일종으로, 탐식기능 및 식세포 작용을 통해 노폐물을 처리하는 역할을 한다.
연구팀은 알츠하이머 동물 모델들에게 저분자 화합물을 주입한 후, 동물들의 인지능력과 뇌 속에 존재하는 베타 아밀로이드의 양을 관찰해 알츠하이머 치료제로서 어떠한 유효한 효과가 있는지 실험했다.
이를 통해 ‘저분자 화합물’이 주입된 동물들은 손상된 신경교세포가 회복돼 뇌 속에 존재하는 베타 아밀로이드 단백질이 감소하는 등 인지능력이 향상된다는 사실을 발견했다.
임미희 교수는 “이 연구는 마이크로글리아의 식세포 작용 손상을 복구시켜 알츠하이머병을 치료할 수 있다는 것을 증명했다”라며 “발견된 합성 분자를 바탕으로 다양한 퇴행성 뇌질환의 치료제 개발에 더욱 박차를 가할 것이다”라고 말했다.
이번 연구는 한국보건산업진흥원, 한국연구재단, KAIST, 그리고 국가과학기술연구회 지원으로 수행됐다.
2019.11.25 조회수 12329
임미희 교수, 손상된 뇌 신경교세포 회복 물질 개발
우리 대학 화학과 임미희 교수 연구팀이 손상된 뇌의 신경교세포를 회복시키는 저분자 화합물(Small molecule)을 발견했다.
연구팀의 이번 연구는 기억력 등 인지기능이 저하돼 일상생활의 장애를 유발하는 알츠하이머 등 만성질환의 치료 가능성을 제시할 수 있을 것으로 기대된다.
경북대 의대 박민희 교수가 1 저자로 참여하고 경북대 배재성, 진희경 교수가 공동 교신저자로 참여한 이번 연구는 미국 국립과학원에서 발행하는 국제 학술지 ‘PNAS’ 11월 4일 자 온라인판에 게재됐다.
퇴행성 뇌 질환인 치매의 일종인 알츠하이머병은 다양한 원인에 의해 발생된다. 이 질병을 치료하기 위해서 병의 원인을 정확히 파악하고 그에 맞는 치료제들을 개발하는 것이 무엇보다 중요하다.
아밀로이드-베타 펩타이드는 알츠하이머병과 밀접한 관계가 있다고 알려져 있다. 또한, 뇌의 신경 세포이며 면역 세포인 신경교세포는 신경염증 반응에 중추적인 역할을 한다. 최근 들어, 아밀로이드-베타 펩타이드와 신경교세포의 신경염증 반응 사이의 상관관계가 알츠하이머병을 일으킬 수 있는 주요한 원인으로 주목받고 있다.
신경교세포는 뇌에서 면역기능을 담당하는 신경세포의 일종으로, 탐식기능 및 식세포 작용을 통해 노폐물을 처리하는 역할을 한다.
연구팀은 알츠하이머 동물 모델들에게 저분자 화합물을 주입한 후, 동물들의 인지능력과 뇌 속에 존재하는 베타 아밀로이드의 양을 관찰해 알츠하이머 치료제로서 어떠한 유효한 효과가 있는지 실험했다.
이를 통해 ‘저분자 화합물’이 주입된 동물들은 손상된 신경교세포가 회복돼 뇌 속에 존재하는 베타 아밀로이드 단백질이 감소하는 등 인지능력이 향상된다는 사실을 발견했다.
임미희 교수는 “이 연구는 마이크로글리아의 식세포 작용 손상을 복구시켜 알츠하이머병을 치료할 수 있다는 것을 증명했다”라며 “발견된 합성 분자를 바탕으로 다양한 퇴행성 뇌질환의 치료제 개발에 더욱 박차를 가할 것이다”라고 말했다.
이번 연구는 한국보건산업진흥원, 한국연구재단, KAIST, 그리고 국가과학기술연구회 지원으로 수행됐다.
2019.11.25 조회수 12329 -
 정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
2019.09.24 조회수 12718
정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
2019.09.24 조회수 12718 -
 박준성 연구원, 알츠하이머병의 새로운 원인 규명
〈 박준성 박사 〉
우리 대학 의과학대학원 박준성 박사(지도교수 : 이정호 교수), KISTI(한국과학기술정보연구원) 국가슈퍼컴퓨팅본부 유석종 박사 공동 연구팀이 노화 과정에서 발생하는 후천적 뇌 돌연변이가 알츠하이머병의 새 원인이 될 수 있다는 이론을 제시했다.
연구팀은 52명의 알츠하이머병 환자에게 얻은 사후 뇌 조직에서 전장 엑솜 유전체 서열(whole-exome sequencing) 데이터 분석을 통해 알츠하이머병에 존재하는 뇌 체성 유전변이를 찾아냈다. 또한, 뇌 체성 돌연변이가 알츠하이머병의 중요 원인으로 알려진 신경섬유다발 형성을 비정상적으로 증가시킴을 확인했다.
박준성 박사와 KISTI 이준학 박사가 공동 1 저자로 참여한 이번 연구는 국제 학술지 네이처 커뮤니케이션(Nature Communications) 7월 12일자 온라인판에 게재됐다. (논문명 : Brain somatic mutations observed in Alzheimer's disease associated with aging and dysregulation of tau phosphorylation)
노인성 치매의 가장 흔한 원인으로 알려진 알츠하이머병은 전 세계 GDP의 1%를 차지할 정도로 사회, 경제적 소모비용이 큰 질환이다. 하지만 여전히 알츠하이머병을 일으키는 분자 유전학적 원인은 명확하게 규명되지 않고 있다.
기존의 알츠하이머병 유전체 연구는 주로 환자의 말초조직인 혈액에서 전장유전체 연관분석(Genome-wide association study)을 하거나, 이미 가족력이 있는 환자에서 발견된 일부 유전자들(e.g., APP, PSEN1/2)에 대한 유전자 패널 분석 등이 주를 이루었다.
연구팀은 산발성 알츠하이머병 환자들에게 내후각피질에서 신경섬유다발이 공통으로 나타나는 현상에 주목해 알츠하이머병 환자의 뇌 조직에서 직접 엑솜 유전체 데이터를 생성해 알츠하이머병 뇌-특이적 체성 유전변이를 발굴했다.
연구팀은 알츠하이머병 환자와 정상인의 해마 형성체 부위를 레이저 현미 해부법을 통해 정밀하게 오려냈고, 저빈도의 체성 유전변이(Somatic mutation)를 정확하게 찾아내기 위해 대용량 고심도 엑솜 시퀀싱 데이터를 생성하고 저빈도 체성 유전변이 분석에 특화된 분석 파이프라인을 독자적으로 구축했다.
이러한 새 방법론을 통해 실제로 알츠하이머병 환자의 뇌에 체성 유전변이가 실제로 존재함을 체계적으로 규명함과 동시에 체성 유전변이의 누적속도 및 신경섬유다발 형성과의 관련성도 함께 밝혀냈다.
연구팀의 발견은 알츠하이머병의 발병에 체성 유전변이가 주요한 역할을 할 수 있음을 강력하게 시사하는 것으로, 알츠하이머병 유전체 연구에 대한 새로운 틀을 제시함과 동시에 향후 다른 신경퇴행성뇌질환의 연구에도 기여할 수 있을 것으로 기대된다.
연구팀은 이번 연구 결과를 바탕으로 교원 창업 기업(소바젠, 대표 김병태)을 통해 알츠하이머 질환의 진단과 치료제 개발에 나설 예정이다.
KISTI 유석종 박사는 연구팀이 구축한 저빈도 체성 유전변이 분석 파이프라인 및 빅데이터 분석을 위한 슈퍼컴퓨팅 기술을 통해 알츠하이머병의 새로운 발병 원리를 밝혀냈다라며 타 유전체 기반 연구에 활용할 수 있는 기반을 마련했다라고 말했다.
이번 연구는 서경배 과학재단, 보건복지부 및 한국과학기술정보연구원의 지원을 받아 수행됐고, 신속한 유전체 빅데이터 분석을 위해 KISTI의 슈퍼컴퓨터 5호기 누리온 시스템이 활용됐다.
□ 그림 설명
그림1. 본 연구에서 사용된 체성 유전변이 분석 파이프라인
그림2. 신경섬유성다발 형성에 관여하는 체성 유전변이
그림3. PIN1 유전자에 발생한 병원성 뇌 체성유전변이와 신경섬유다발 형성과의 관계 규명
2019.07.17 조회수 19779
박준성 연구원, 알츠하이머병의 새로운 원인 규명
〈 박준성 박사 〉
우리 대학 의과학대학원 박준성 박사(지도교수 : 이정호 교수), KISTI(한국과학기술정보연구원) 국가슈퍼컴퓨팅본부 유석종 박사 공동 연구팀이 노화 과정에서 발생하는 후천적 뇌 돌연변이가 알츠하이머병의 새 원인이 될 수 있다는 이론을 제시했다.
연구팀은 52명의 알츠하이머병 환자에게 얻은 사후 뇌 조직에서 전장 엑솜 유전체 서열(whole-exome sequencing) 데이터 분석을 통해 알츠하이머병에 존재하는 뇌 체성 유전변이를 찾아냈다. 또한, 뇌 체성 돌연변이가 알츠하이머병의 중요 원인으로 알려진 신경섬유다발 형성을 비정상적으로 증가시킴을 확인했다.
박준성 박사와 KISTI 이준학 박사가 공동 1 저자로 참여한 이번 연구는 국제 학술지 네이처 커뮤니케이션(Nature Communications) 7월 12일자 온라인판에 게재됐다. (논문명 : Brain somatic mutations observed in Alzheimer's disease associated with aging and dysregulation of tau phosphorylation)
노인성 치매의 가장 흔한 원인으로 알려진 알츠하이머병은 전 세계 GDP의 1%를 차지할 정도로 사회, 경제적 소모비용이 큰 질환이다. 하지만 여전히 알츠하이머병을 일으키는 분자 유전학적 원인은 명확하게 규명되지 않고 있다.
기존의 알츠하이머병 유전체 연구는 주로 환자의 말초조직인 혈액에서 전장유전체 연관분석(Genome-wide association study)을 하거나, 이미 가족력이 있는 환자에서 발견된 일부 유전자들(e.g., APP, PSEN1/2)에 대한 유전자 패널 분석 등이 주를 이루었다.
연구팀은 산발성 알츠하이머병 환자들에게 내후각피질에서 신경섬유다발이 공통으로 나타나는 현상에 주목해 알츠하이머병 환자의 뇌 조직에서 직접 엑솜 유전체 데이터를 생성해 알츠하이머병 뇌-특이적 체성 유전변이를 발굴했다.
연구팀은 알츠하이머병 환자와 정상인의 해마 형성체 부위를 레이저 현미 해부법을 통해 정밀하게 오려냈고, 저빈도의 체성 유전변이(Somatic mutation)를 정확하게 찾아내기 위해 대용량 고심도 엑솜 시퀀싱 데이터를 생성하고 저빈도 체성 유전변이 분석에 특화된 분석 파이프라인을 독자적으로 구축했다.
이러한 새 방법론을 통해 실제로 알츠하이머병 환자의 뇌에 체성 유전변이가 실제로 존재함을 체계적으로 규명함과 동시에 체성 유전변이의 누적속도 및 신경섬유다발 형성과의 관련성도 함께 밝혀냈다.
연구팀의 발견은 알츠하이머병의 발병에 체성 유전변이가 주요한 역할을 할 수 있음을 강력하게 시사하는 것으로, 알츠하이머병 유전체 연구에 대한 새로운 틀을 제시함과 동시에 향후 다른 신경퇴행성뇌질환의 연구에도 기여할 수 있을 것으로 기대된다.
연구팀은 이번 연구 결과를 바탕으로 교원 창업 기업(소바젠, 대표 김병태)을 통해 알츠하이머 질환의 진단과 치료제 개발에 나설 예정이다.
KISTI 유석종 박사는 연구팀이 구축한 저빈도 체성 유전변이 분석 파이프라인 및 빅데이터 분석을 위한 슈퍼컴퓨팅 기술을 통해 알츠하이머병의 새로운 발병 원리를 밝혀냈다라며 타 유전체 기반 연구에 활용할 수 있는 기반을 마련했다라고 말했다.
이번 연구는 서경배 과학재단, 보건복지부 및 한국과학기술정보연구원의 지원을 받아 수행됐고, 신속한 유전체 빅데이터 분석을 위해 KISTI의 슈퍼컴퓨터 5호기 누리온 시스템이 활용됐다.
□ 그림 설명
그림1. 본 연구에서 사용된 체성 유전변이 분석 파이프라인
그림2. 신경섬유성다발 형성에 관여하는 체성 유전변이
그림3. PIN1 유전자에 발생한 병원성 뇌 체성유전변이와 신경섬유다발 형성과의 관계 규명
2019.07.17 조회수 19779 -
 이진우 교수, 그래핀 기반의 자연 효소 모방물질 개발
〈 이진우 교수 〉
우리 대학 생명화학공학과 이진우 교수 연구팀이 그래핀을 기반으로 해 과산화효소의 선택성과 활성을 모방한 나노단위 크기의 무기 소재(나노자임, Nanozyme)를 합성하는 데 성공했다.
연구팀은 이 무기 소재를 이용하면 알츠하이머병 조기 진단과 관련된 신경전달물질인 아세틸콜린을 자연 효소를 이용했을 때보다 더 민감하게 검출할 수 있음을 확인했다.
가천대학교 바이오나노학과 김문일 교수, UNIST 에너지화학공학부 곽상규 교수팀과 공동으로 연구하고 김민수 박사가 1 저자로 참여한 이번 연구는 재료 분야 국제 학술지 ‘에이씨에스 나노(ACS Nano)’ 3월 25일자에 게재됐다. (논문명 : N and B Codoped Graphene: A Strong Candidate To Replace Natural Peroxidase in Sensitive and Selective Bioassays , 질소와 붕소가 동시에 도핑된 그래핀: 민감하고 선택성이 있는 바이오에세이에 사용되는 자연의 과산화효소를 대체할 수 있는 강력한 후보)
효소는 우리의 몸 속 다양한 화학 반응에 촉매로 참여하고 있다. 각각의 효소는 구조가 매우 복잡해 체내에서 특정 온도와 환경에서 원하는 특정 반응에만 촉매 역할을 할 수 있다.
특히 과산화효소는 과산화수소와 반응하면 푸른 색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있다. 이를 이용해 산화 과정에서 아세틸콜린을 포함한 과산화수소를 배출하는 다양한 물질을 시각적으로 검출할 수 있다는 장점이 있다.
대신 효소는 안정성, 생산성이 낮고 가격이 비싸다는 단점이 있다. 단백질로 이뤄진 효소와 달리 무기물질로 합성된 효소 모방 물질은 기존 효소의 단점을 해소할 수 있어 효소의 역할인 질병의 검출 및 진단 시스템에 활용할 수 있다. 따라서 효소의 활성을 정확히 모방하는 나노물질의 필요성이 커지고 있다.
그러나 효소를 모방하는 나노물질은 활성을 모방하는 것이 가능하지만 원하지 않은 다른 부가적인 반응을 일으킬 수 있다는 단점이 있어 효소를 대체하는 데 어려움이 있다. 특히 기존의 과산화효소 활성이 높은 물질은 과산화수소가 없는 상황에서도 색이 변하기 때문에 검출 물질이 없어도 발색이 되는 단점이 있다.
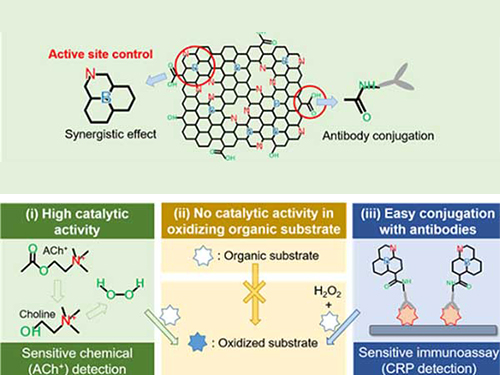
문제 해결을 위해 연구팀은 과산화효소 활성만을 선택적으로 모방하는 질소와 붕소가 동시에 도핑된 그래핀을 합성했다. 이 그래핀의 경우 과산화수소 활성은 폭발적으로 증가하지만 다른 효소 활성은 거의 증가하지 않아 과산화효소를 정확하게 모방할 수 있다.
연구팀은 실험적 내용을 계산화학을 통해 증명했으며 새롭게 개발한 물질을 이용해 중요 신경전달 물질인 아세틸콜린을 시각적으로 검출하는 데 성공했다.
아세틸콜린은 알츠하이머병의 조기 진단과 관련이 높아 연구팀의 효소모방 물질을 이용하면 향후 질병 진단 및 치료에 기여할 수 있을 것으로 예상된다.
이 교수는 “효소 모방 물질은 오래되지 않은 분야이지만 기존 효소를 대체할 수 있다는 잠재성 때문에 관심이 폭발적으로 커지고 있다”라며 “이번 연구를 통해 효소의 높은 활성 뿐 아니라 선택성까지 가질 수 있는 물질을 합성하고 알츠하이머의 진단 마커인 아세틸콜린을 효과적으로 시각적 검출할 수 있는 기술을 확보했다”라고 말했다.
이번 연구는 한국연구재단의 이공분야 기초연구사업 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. 촉매의 과산화효소와 산화효소 활성을 시각적으로 확인할 수 있는 사진
그림2. 질소와 붕소가 동시에 도핑된 그래핀의 바이오 에세이 적용
2019.04.23 조회수 20867
이진우 교수, 그래핀 기반의 자연 효소 모방물질 개발
〈 이진우 교수 〉
우리 대학 생명화학공학과 이진우 교수 연구팀이 그래핀을 기반으로 해 과산화효소의 선택성과 활성을 모방한 나노단위 크기의 무기 소재(나노자임, Nanozyme)를 합성하는 데 성공했다.
연구팀은 이 무기 소재를 이용하면 알츠하이머병 조기 진단과 관련된 신경전달물질인 아세틸콜린을 자연 효소를 이용했을 때보다 더 민감하게 검출할 수 있음을 확인했다.
가천대학교 바이오나노학과 김문일 교수, UNIST 에너지화학공학부 곽상규 교수팀과 공동으로 연구하고 김민수 박사가 1 저자로 참여한 이번 연구는 재료 분야 국제 학술지 ‘에이씨에스 나노(ACS Nano)’ 3월 25일자에 게재됐다. (논문명 : N and B Codoped Graphene: A Strong Candidate To Replace Natural Peroxidase in Sensitive and Selective Bioassays , 질소와 붕소가 동시에 도핑된 그래핀: 민감하고 선택성이 있는 바이오에세이에 사용되는 자연의 과산화효소를 대체할 수 있는 강력한 후보)
효소는 우리의 몸 속 다양한 화학 반응에 촉매로 참여하고 있다. 각각의 효소는 구조가 매우 복잡해 체내에서 특정 온도와 환경에서 원하는 특정 반응에만 촉매 역할을 할 수 있다.
특히 과산화효소는 과산화수소와 반응하면 푸른 색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있다. 이를 이용해 산화 과정에서 아세틸콜린을 포함한 과산화수소를 배출하는 다양한 물질을 시각적으로 검출할 수 있다는 장점이 있다.
대신 효소는 안정성, 생산성이 낮고 가격이 비싸다는 단점이 있다. 단백질로 이뤄진 효소와 달리 무기물질로 합성된 효소 모방 물질은 기존 효소의 단점을 해소할 수 있어 효소의 역할인 질병의 검출 및 진단 시스템에 활용할 수 있다. 따라서 효소의 활성을 정확히 모방하는 나노물질의 필요성이 커지고 있다.
그러나 효소를 모방하는 나노물질은 활성을 모방하는 것이 가능하지만 원하지 않은 다른 부가적인 반응을 일으킬 수 있다는 단점이 있어 효소를 대체하는 데 어려움이 있다. 특히 기존의 과산화효소 활성이 높은 물질은 과산화수소가 없는 상황에서도 색이 변하기 때문에 검출 물질이 없어도 발색이 되는 단점이 있다.
문제 해결을 위해 연구팀은 과산화효소 활성만을 선택적으로 모방하는 질소와 붕소가 동시에 도핑된 그래핀을 합성했다. 이 그래핀의 경우 과산화수소 활성은 폭발적으로 증가하지만 다른 효소 활성은 거의 증가하지 않아 과산화효소를 정확하게 모방할 수 있다.
연구팀은 실험적 내용을 계산화학을 통해 증명했으며 새롭게 개발한 물질을 이용해 중요 신경전달 물질인 아세틸콜린을 시각적으로 검출하는 데 성공했다.
아세틸콜린은 알츠하이머병의 조기 진단과 관련이 높아 연구팀의 효소모방 물질을 이용하면 향후 질병 진단 및 치료에 기여할 수 있을 것으로 예상된다.
이 교수는 “효소 모방 물질은 오래되지 않은 분야이지만 기존 효소를 대체할 수 있다는 잠재성 때문에 관심이 폭발적으로 커지고 있다”라며 “이번 연구를 통해 효소의 높은 활성 뿐 아니라 선택성까지 가질 수 있는 물질을 합성하고 알츠하이머의 진단 마커인 아세틸콜린을 효과적으로 시각적 검출할 수 있는 기술을 확보했다”라고 말했다.
이번 연구는 한국연구재단의 이공분야 기초연구사업 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. 촉매의 과산화효소와 산화효소 활성을 시각적으로 확인할 수 있는 사진
그림2. 질소와 붕소가 동시에 도핑된 그래핀의 바이오 에세이 적용
2019.04.23 조회수 20867 -
 박용근, 정용 교수, 알츠하이머 정량화 가능한 홀로그래피영상 기술 개발
우리 대학 물리학과 박용근 교수와 바이오및뇌공학과 정용 교수(KI 헬스사이언스 연구소) 공동 연구팀이 홀로그래피 영상 기술을 이용해 알츠하이머 질환을 정량적으로 연구할 수 있는 광학 기술을 개발했다.
이무성 연구원과 이익성 박사가 공동 1저자로 참여한 이번 연구 결과는 네이처 자매지 ‘사이언티픽 리포트(Scientific Reports)’ 8월 3일자 온라인 판에 게재됐다.
뇌의 구조는 뇌 기능 및 질병과 밀접한 관련을 갖고 있다. 특히 알츠하이머에 걸린 뇌는 회백질 및 해마에 아밀로이드 반점이나 신경 섬유 엉킴과 같은 비정상적 구조를 갖기 때문에 뇌 영상 촬영 기술 신경과학에서 꼭 필요한 기술이다.
뇌 관련 질병의 치료를 위해 자기공명영상(MRI)이나 양전자 단층 촬영(PET)과 같은 기존 영상 촬영 기술들을 많이 활용하고 있지만 0.1밀리미터 이하의 세밀한 구조는 관찰하기 힘들다는 한계를 갖는다.
이를 보완하기 위해 조직 병리학 기법을 이용해 뇌의 단면 구조를 관찰했지만, 뇌 조직이 투명하기 때문에 촬영을 위해선 염색 과정을 거쳐야 한다. 이 과정에서 왜곡이 발생할 수 있다.
또한 조직 병리로 얻은 정보는 정성적 정보가 대부분이기 때문에 질병 진단에 필요한 정량적, 객관적 기준을 제공하기 어려웠다.
문제 해결을 위해 연구팀은 먼저 홀로그래피 현미경 기술을 통해 뇌 구조의 정보를 정량적으로 분석했다.
연구팀의 홀로그래피 현미경은 빛의 간섭을 이용해 별도의 염색 과정 없이 조직의 굴절률 분포 수치 영상을 계산할 수 있다.
조직 샘플을 투과한 빛은 굴절률 분포에 따라 특정한 산란 과정을 겪는다. 위에서 얻은 굴절률 분포를 토대로 연구팀은 뇌 조직 내에서 빛이 산란되는 평균 거리와 산란광이 퍼지는 방향성을 정량화했다.
연구팀은 산란 평균 거리와 방향성 분포를 이용해 알츠하이머 인자를 가진 쥐의 뇌 조직에서 발생하는 구조 변화 및 정도를 정량적으로 수치화했다.
그 결과 알츠하이머 모델의 해마 및 회백질의 산란 평균 거리와 방향성이 정상 모델에 비해 더 낮아지는 것을 확인했다. 특히 해마 내 산란되는 평균 거리는 약 40%가 감소했다. 이는 해마와 회백질 구조가 알츠하이머병에 의해 손상되고 불균일해지기 때문으로 해석된다.
연구팀은 이번 연구가 알츠하이머 뿐 아니라 파킨슨 병 등 다른 질병 연구에도 광범위하게 활용될 수 있을 것이라고 내다봤다.
박 교수는 “최근 창업한 Tomocube(토모큐브) 사의 제품을 이용해 관련 연구자들이 보다 쉽게 새로운 방법을 적용시켜 다양한 조직 병리 연구에 활용할 수 있을 것으로 기대된다” 고 말했다.
□ 그림 설명
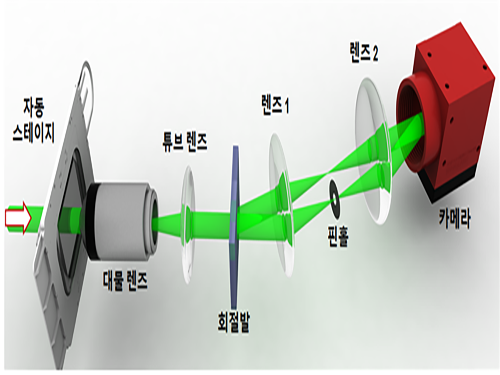
그림1. 홀로그래피 현미경 모식도
그림2. 기존 현미경과 홀로그래피 현미경 성능 비교
그림3. 정상 모델과 알츠하이머병 모델의 뇌 조직의 산란 계수, 이방성 분포
2016.08.17 조회수 12899
박용근, 정용 교수, 알츠하이머 정량화 가능한 홀로그래피영상 기술 개발
우리 대학 물리학과 박용근 교수와 바이오및뇌공학과 정용 교수(KI 헬스사이언스 연구소) 공동 연구팀이 홀로그래피 영상 기술을 이용해 알츠하이머 질환을 정량적으로 연구할 수 있는 광학 기술을 개발했다.
이무성 연구원과 이익성 박사가 공동 1저자로 참여한 이번 연구 결과는 네이처 자매지 ‘사이언티픽 리포트(Scientific Reports)’ 8월 3일자 온라인 판에 게재됐다.
뇌의 구조는 뇌 기능 및 질병과 밀접한 관련을 갖고 있다. 특히 알츠하이머에 걸린 뇌는 회백질 및 해마에 아밀로이드 반점이나 신경 섬유 엉킴과 같은 비정상적 구조를 갖기 때문에 뇌 영상 촬영 기술 신경과학에서 꼭 필요한 기술이다.
뇌 관련 질병의 치료를 위해 자기공명영상(MRI)이나 양전자 단층 촬영(PET)과 같은 기존 영상 촬영 기술들을 많이 활용하고 있지만 0.1밀리미터 이하의 세밀한 구조는 관찰하기 힘들다는 한계를 갖는다.
이를 보완하기 위해 조직 병리학 기법을 이용해 뇌의 단면 구조를 관찰했지만, 뇌 조직이 투명하기 때문에 촬영을 위해선 염색 과정을 거쳐야 한다. 이 과정에서 왜곡이 발생할 수 있다.
또한 조직 병리로 얻은 정보는 정성적 정보가 대부분이기 때문에 질병 진단에 필요한 정량적, 객관적 기준을 제공하기 어려웠다.
문제 해결을 위해 연구팀은 먼저 홀로그래피 현미경 기술을 통해 뇌 구조의 정보를 정량적으로 분석했다.
연구팀의 홀로그래피 현미경은 빛의 간섭을 이용해 별도의 염색 과정 없이 조직의 굴절률 분포 수치 영상을 계산할 수 있다.
조직 샘플을 투과한 빛은 굴절률 분포에 따라 특정한 산란 과정을 겪는다. 위에서 얻은 굴절률 분포를 토대로 연구팀은 뇌 조직 내에서 빛이 산란되는 평균 거리와 산란광이 퍼지는 방향성을 정량화했다.
연구팀은 산란 평균 거리와 방향성 분포를 이용해 알츠하이머 인자를 가진 쥐의 뇌 조직에서 발생하는 구조 변화 및 정도를 정량적으로 수치화했다.
그 결과 알츠하이머 모델의 해마 및 회백질의 산란 평균 거리와 방향성이 정상 모델에 비해 더 낮아지는 것을 확인했다. 특히 해마 내 산란되는 평균 거리는 약 40%가 감소했다. 이는 해마와 회백질 구조가 알츠하이머병에 의해 손상되고 불균일해지기 때문으로 해석된다.
연구팀은 이번 연구가 알츠하이머 뿐 아니라 파킨슨 병 등 다른 질병 연구에도 광범위하게 활용될 수 있을 것이라고 내다봤다.
박 교수는 “최근 창업한 Tomocube(토모큐브) 사의 제품을 이용해 관련 연구자들이 보다 쉽게 새로운 방법을 적용시켜 다양한 조직 병리 연구에 활용할 수 있을 것으로 기대된다” 고 말했다.
□ 그림 설명
그림1. 홀로그래피 현미경 모식도
그림2. 기존 현미경과 홀로그래피 현미경 성능 비교
그림3. 정상 모델과 알츠하이머병 모델의 뇌 조직의 산란 계수, 이방성 분포
2016.08.17 조회수 12899 -
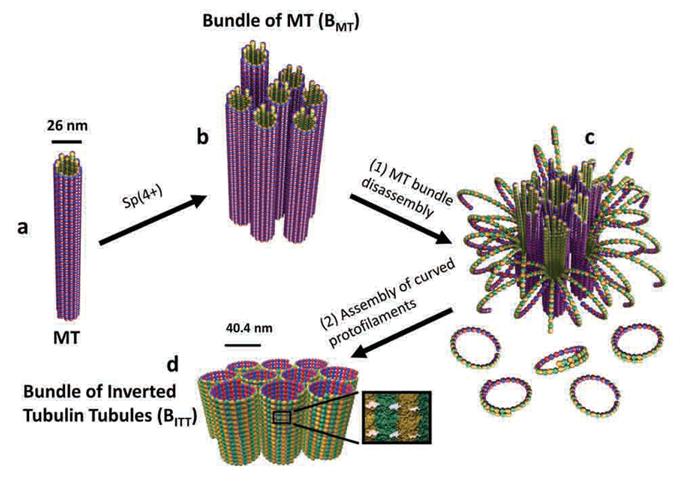 단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25796
단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25796 -
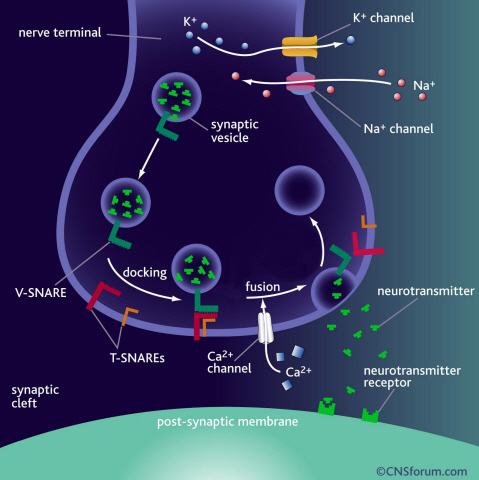 뇌신경전달 단백질의 구조와 작동원리 규명
- 생체막 융합 단백질의 구조변화 실시간 측정 -- 퇴행성 뇌질환 연구에 실마리 제공 -
우리 학교 물리학과 윤태영 교수 연구팀이 자기력 나노집게를 이용해 뇌신경세포사이의 신경물질전달에 가장 중추적인 역할을 하는 스네어(SNARE) 단백질의 숨겨진 구조와 작동원리를 단분자 수준에서 밝히는데 성공했다.
스네어 단백질의 세포막 융합기능은 알츠하이머병 같은 퇴행성 뇌질환이나 신경질환과 밀접하게 연관되어 있어 이 같은 질병의 예방과 치료법 개발에 새로운 실마리가 될 것으로 기대된다.
뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 가장 핵심적인 역할을 하는 세포막 융합 단백질이다.
지금까지 학계에서는 스네어 단백질이 신경물질을 주고받는 과정을 조절할 것이라고 추정해 왔지만 그 구조와 기능을 명확하게 밝혀내지 못했다.
연구팀은 자기력 나노집게를 이용해 피코 뉴턴(pN, 1조분의 1뉴턴) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하는 실험기법을 개발했다.
이를 통해 스네어 단백질에 숨겨진 중간구조가 존재하며, 이 구조에 대한 정밀한 측정결과 중간상태가 어떤 구조를 갖는지 정확하게 예측했다.
이와 함께 생체막 사이에 있는 스네어 단백질의 중간구조가 생체막이 서로 밀어내는 힘을 견디고 유지하면서 신경물질을 주고받는 과정을 조절하는 역할을 할 수 있음을 밝혔다.
윤태영 교수는 “생체단백질이 갖는 숨겨진 구조와 작동원리를 힘을 정교하게 조절하는 실험만으로 직접 관찰하는 것과 동일한 획기적 연구 결과를 일궈냈다”며 “이 기술은 생물학의 연구대상을 물리학적인 방법 연구하는데 매우 중요한 기술로 향후 학제적 융합연구에 매우 중요한 기반이 될 것”이라고 말했다.
한편, 이번 연구는 KAIST 물리학과 윤태영 교수와 김기범 연구교수의 주도 아래 KIST 의공학연구소 신연균 교수와 공동연구로 진행됐고, KAIST 물리학과 조용훈 교수, 민두영 박사과정, KIAS 계산과학부 현창봉 교수가 참여했으며, 이번 세계적 과학학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 4월 16일자에 게재됐다.
(a) 뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 핵심적인 역할을 한다.
(b) 자기력 나노집게를 이용하여 단분자 수준에서 단백질 구조 변화를 실시간으로 측정방법의 개략도. 피코 뉴톤(pN) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하여 생체막 융합 단백질의 숨겨진 중간구조와 작동원리를 단분자 수준에서 관찰한다.
2013.05.09 조회수 19710
뇌신경전달 단백질의 구조와 작동원리 규명
- 생체막 융합 단백질의 구조변화 실시간 측정 -- 퇴행성 뇌질환 연구에 실마리 제공 -
우리 학교 물리학과 윤태영 교수 연구팀이 자기력 나노집게를 이용해 뇌신경세포사이의 신경물질전달에 가장 중추적인 역할을 하는 스네어(SNARE) 단백질의 숨겨진 구조와 작동원리를 단분자 수준에서 밝히는데 성공했다.
스네어 단백질의 세포막 융합기능은 알츠하이머병 같은 퇴행성 뇌질환이나 신경질환과 밀접하게 연관되어 있어 이 같은 질병의 예방과 치료법 개발에 새로운 실마리가 될 것으로 기대된다.
뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 가장 핵심적인 역할을 하는 세포막 융합 단백질이다.
지금까지 학계에서는 스네어 단백질이 신경물질을 주고받는 과정을 조절할 것이라고 추정해 왔지만 그 구조와 기능을 명확하게 밝혀내지 못했다.
연구팀은 자기력 나노집게를 이용해 피코 뉴턴(pN, 1조분의 1뉴턴) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하는 실험기법을 개발했다.
이를 통해 스네어 단백질에 숨겨진 중간구조가 존재하며, 이 구조에 대한 정밀한 측정결과 중간상태가 어떤 구조를 갖는지 정확하게 예측했다.
이와 함께 생체막 사이에 있는 스네어 단백질의 중간구조가 생체막이 서로 밀어내는 힘을 견디고 유지하면서 신경물질을 주고받는 과정을 조절하는 역할을 할 수 있음을 밝혔다.
윤태영 교수는 “생체단백질이 갖는 숨겨진 구조와 작동원리를 힘을 정교하게 조절하는 실험만으로 직접 관찰하는 것과 동일한 획기적 연구 결과를 일궈냈다”며 “이 기술은 생물학의 연구대상을 물리학적인 방법 연구하는데 매우 중요한 기술로 향후 학제적 융합연구에 매우 중요한 기반이 될 것”이라고 말했다.
한편, 이번 연구는 KAIST 물리학과 윤태영 교수와 김기범 연구교수의 주도 아래 KIST 의공학연구소 신연균 교수와 공동연구로 진행됐고, KAIST 물리학과 조용훈 교수, 민두영 박사과정, KIAS 계산과학부 현창봉 교수가 참여했으며, 이번 세계적 과학학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 4월 16일자에 게재됐다.
(a) 뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 핵심적인 역할을 한다.
(b) 자기력 나노집게를 이용하여 단분자 수준에서 단백질 구조 변화를 실시간으로 측정방법의 개략도. 피코 뉴톤(pN) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하여 생체막 융합 단백질의 숨겨진 중간구조와 작동원리를 단분자 수준에서 관찰한다.
2013.05.09 조회수 19710