%EC%83%9D%EB%AC%BC%ED%95%99
-
 생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 17478
생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 17478 -
 김재경 교수, 수학적 모델링 통해 신약 개발 걸림돌 해소
〈 김대욱 박사과정, 김재경 교수 〉
우리 대학 수리과학과 김재경 교수와 글로벌 제약회사 화이자(Pfizer)의 장 청(Cheng Chang) 박사 공동연구팀이 수학적 모델을 기반으로 동물 실험과 임상 시험 간 차이가 발생하는 원인을 밝히고 그 해결책을 제시했다.
연구팀은 일주기 리듬 수면 장애 신약을 개발하는 과정에서 동물 실험과 임상 시험 간 발생하는 차이 문제를 수학적 모델을 이용해 해결함으로써 신약 개발의 가능성을 높였다. 또한, 동물과 사람 간 차이 뿐 아니라 사람마다 발생하는 약효의 차이 발생 원인도 밝혀냈다.
김대욱 박사과정이 1 저자로 참여한 이번 연구결과는 국제 학술지 ‘분자 시스템 생물학 (Molecular Systems Biology)’ 7월 8일자 온라인판에 게재됐고, 우수성을 인정받아 7월호 표지논문으로 선정됐다. (논문명 : Systems approach reveals photosensitivity and PER2 level as determinants of clock-modulator efficacy)
신약을 개발하기 위해 임상 시험 전 단계로 쥐 등의 동물을 대상으로 전임상 실험을 하게 된다. 이 과정에서 동물에서 보였던 효과가 사람에게선 보이지 않을 때가 종종 있고 사람마다 효과가 다르게 나타나기도 한다. 이러한 약효의 차이가 발생하는 원인을 찾지 못하면 신약 개발에 큰 걸림돌이 된다.
수면 장애는 맞춤형 치료 분야에서 개발이 가장 더딘 질병 중 하나이다. 쥐는 사람과 달리 수면시간이 반대인 야행성 동물이다 보니 수면시간을 조절할 수 있는 치료제가 실험 쥐에게는 효과가 있어도 사람에게는 무효한 경우가 많았다. 하지만 그 원인이 알려지지 않아 신약 개발에 어려움이 있었다.
연구팀은 이러한 차이의 원인을 미분방정식을 이용한 가상실험과 실제 실험을 결합해 연구했고, 주행성인 사람은 야행성인 쥐에 비해 빛 노출 때문에 약효가 더 많이 반감되는 것이 원인임을 밝혔다. 이는 빛 노출 조절을 통해 그동안 사람에게 보이지 않던 약효가 발현되게 할 수 있음을 뜻한다.
수면 장애 치료 약물의 약효가 사람마다 큰 차이를 보이는 것도 신약 개발의 걸림돌이었다. 연구팀은 증상이 비슷해도 환자마다 약효 차이가 나타나는 원인을 밝히기 위해 수리 모델링을 이용한 가상환자를 이용했다.
이를 통해 약효가 달라지는 원인은 수면시간을 결정하는 핵심 역할을 하는 생체시계 단백질인 PER2의 발현량이 달라서임을 규명했다.
또한, PER2의 양이 낮에는 증가하고 밤에는 감소하기 때문에 하루 중 언제 투약하느냐에 따라 약효가 바뀜을 이용해 환자마다 적절한 투약 시간을 찾아 최적의 치료 효과를 가져오는 시간요법(Chronotherapy)를 개발했다.
김재경 교수는 “수학이 실제 의약학 분야에 이바지해 우리가 좀 더 건강하고 행복한 삶을 살 수 있는데 도울 수 있어 행복한 연구였다”라며 “이번 성과를 통해 국내에선 아직은 부족한 의약학과 수학의 교류가 활발해지길 기대한다”라고 말했다.
□ 그림 설명
그림1. 김재경 교수 연구팀 성과 개념도
그림2. 맞춤형 시간 치료법 (Chronotherapy) 개념도
2019.07.09 조회수 17583
김재경 교수, 수학적 모델링 통해 신약 개발 걸림돌 해소
〈 김대욱 박사과정, 김재경 교수 〉
우리 대학 수리과학과 김재경 교수와 글로벌 제약회사 화이자(Pfizer)의 장 청(Cheng Chang) 박사 공동연구팀이 수학적 모델을 기반으로 동물 실험과 임상 시험 간 차이가 발생하는 원인을 밝히고 그 해결책을 제시했다.
연구팀은 일주기 리듬 수면 장애 신약을 개발하는 과정에서 동물 실험과 임상 시험 간 발생하는 차이 문제를 수학적 모델을 이용해 해결함으로써 신약 개발의 가능성을 높였다. 또한, 동물과 사람 간 차이 뿐 아니라 사람마다 발생하는 약효의 차이 발생 원인도 밝혀냈다.
김대욱 박사과정이 1 저자로 참여한 이번 연구결과는 국제 학술지 ‘분자 시스템 생물학 (Molecular Systems Biology)’ 7월 8일자 온라인판에 게재됐고, 우수성을 인정받아 7월호 표지논문으로 선정됐다. (논문명 : Systems approach reveals photosensitivity and PER2 level as determinants of clock-modulator efficacy)
신약을 개발하기 위해 임상 시험 전 단계로 쥐 등의 동물을 대상으로 전임상 실험을 하게 된다. 이 과정에서 동물에서 보였던 효과가 사람에게선 보이지 않을 때가 종종 있고 사람마다 효과가 다르게 나타나기도 한다. 이러한 약효의 차이가 발생하는 원인을 찾지 못하면 신약 개발에 큰 걸림돌이 된다.
수면 장애는 맞춤형 치료 분야에서 개발이 가장 더딘 질병 중 하나이다. 쥐는 사람과 달리 수면시간이 반대인 야행성 동물이다 보니 수면시간을 조절할 수 있는 치료제가 실험 쥐에게는 효과가 있어도 사람에게는 무효한 경우가 많았다. 하지만 그 원인이 알려지지 않아 신약 개발에 어려움이 있었다.
연구팀은 이러한 차이의 원인을 미분방정식을 이용한 가상실험과 실제 실험을 결합해 연구했고, 주행성인 사람은 야행성인 쥐에 비해 빛 노출 때문에 약효가 더 많이 반감되는 것이 원인임을 밝혔다. 이는 빛 노출 조절을 통해 그동안 사람에게 보이지 않던 약효가 발현되게 할 수 있음을 뜻한다.
수면 장애 치료 약물의 약효가 사람마다 큰 차이를 보이는 것도 신약 개발의 걸림돌이었다. 연구팀은 증상이 비슷해도 환자마다 약효 차이가 나타나는 원인을 밝히기 위해 수리 모델링을 이용한 가상환자를 이용했다.
이를 통해 약효가 달라지는 원인은 수면시간을 결정하는 핵심 역할을 하는 생체시계 단백질인 PER2의 발현량이 달라서임을 규명했다.
또한, PER2의 양이 낮에는 증가하고 밤에는 감소하기 때문에 하루 중 언제 투약하느냐에 따라 약효가 바뀜을 이용해 환자마다 적절한 투약 시간을 찾아 최적의 치료 효과를 가져오는 시간요법(Chronotherapy)를 개발했다.
김재경 교수는 “수학이 실제 의약학 분야에 이바지해 우리가 좀 더 건강하고 행복한 삶을 살 수 있는데 도울 수 있어 행복한 연구였다”라며 “이번 성과를 통해 국내에선 아직은 부족한 의약학과 수학의 교류가 활발해지길 기대한다”라고 말했다.
□ 그림 설명
그림1. 김재경 교수 연구팀 성과 개념도
그림2. 맞춤형 시간 치료법 (Chronotherapy) 개념도
2019.07.09 조회수 17583 -
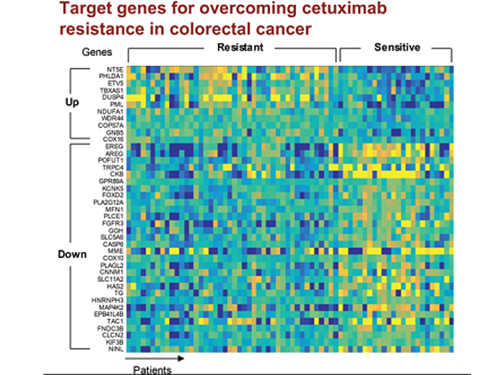 조광현 교수, 대장암 항암제 내성 극복할 병용 치료타겟 발굴
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암의 항암제 내성을 극복할 수 있는 새로운 병용치료 타겟을 발굴하는 데 성공했다.
연구팀은 암세포의 복잡한 생체데이터를 분자 네트워크 관점에서 분석하는 시스템생물학 접근법의 중요성을 제시했다. 이 방법을 통해 암세포가 가지는 약제 내성의 원리를 시스템 차원에서 파악하고, 새로운 약물 타겟을 체계적으로 발굴할 수 있을 것으로 기대된다.
박상민 박사과정, 황채영 박사 등이 참여한 이번 연구결과는 국제학술지 ‘유럽생화학회저널(FEBS Journal)’의 4월호 표지논문으로 게재됐다. (논문명 : Systems analysis identifies potential target genes to overcome cetuximab resistance in colorectal cancer cells)
암은 흔하게 발생하는 대표적인 난치병으로 특히 대장암은 전 세계적으로 환자 수가 100만 명을 넘어섰고, 국내의 경우 서구화된 식습관과 비만 등으로 인해 발병률 증가 속도가 10년간 가장 높게 나타났다. 최근 급격한 고령화에 따라 대장암 환자의 발생률 및 사망률이 가파르게 증가할 것으로 예상되고 있다.
최근 암세포의 특정 분자만을 표적으로 하는 표적항암제가 개발돼 부작용을 크게 줄이고 효과를 높일 수 있지만, 여전히 약물에 반응하는 환자가 매우 제한적이며 그나마 반응을 보이더라도 표적 항암치료 후 약물에 대한 내성이 생겨 암이 재발하는 문제를 안고 있다.
또한, 환자별로 항암제에 대한 반응이 매우 달라 환자의 암 조직 내 유전자 변이의 특징에 따라 적합한 치료를 선택하는 정밀의학의 필요성이 커지고 있다. 대장암 역시 약물의 효과를 예측할 수 있는 유전자 바이오마커의 여부에 따라 적합한 표적항암제를 처방하는 시도가 이뤄지고 있다.
FDA 승인을 받은 대표적인 대장암 치료제인 세툭시맙(cetuximab)의 경우 약물 반응성을 예측하는 바이오마커로 KRAS 유전자 돌연변이의 유무가 활용되고 있는데 이 유전자 돌연변이가 없는 환자에게 처방을 권고하고 있다.
그러나 KRAS 돌연변이가 없는 환자도 세툭시맙 반응률은 절반 정도에 불과하고 기존 항암 화학요법 단독시행과 비교해도 평균 5개월의 수명을 연장하는 데 그치고 있다. 오히려 KRAS 돌연변이가 있는 환자에게서 반응성이 있는 경우가 보고되고 있다.
따라서 KRAS 돌연변이 유무 이외의 새 바이오마커가 요구되고 있으며 KRAS 돌연변이가 존재해도 내성을 극복할 수 있는 병용치료 타겟의 발굴이 필요하다.
조 교수 연구팀은 유전체 데이터 분석, 수학 모델링, 컴퓨터 시뮬레이션 분석과 암 세포주 실험을 융합한 시스템생물학 연구를 통해 세툭시맙 반응성에 대한 바이오마커로 다섯 개의 새로운 유전자(DUSP4, ETV5, GNB5, NT5E, PHLDA1)를 찾아냈다.
그리고 대장암세포에서 각 유전자를 실험적으로 억제한 결과 KRAS 정상 세포에서 발생하는 세툭시맙 내성을 모두 극복할 수 있었다.
특히 GNB5를 억제하면 KRAS 돌연변이가 있는 세포주에서도 세툭시맙 처리에 따른 약물내성을 극복할 수 있음을 밝혔다. 따라서 GNB5의 억제를 통해 대장암 환자의 KRAS 돌연변이 유무와 관계없이 세툭시맙에 대한 내성을 극복할 수 있어 GNB5가 효과적인 병용치료 분자 타겟이 될 수 있음을 증명했다.
연구팀이 제시한 유전자를 바이오마커로 활용하면 세툭시맙에 잘 반응할 수 있는 민감 환자군을 미리 선별해 치료할 수 있는 정밀의학의 실현을 앞당길 수 있다.
또한, 발굴된 유전자들을 표적화하는 신약개발을 통해 내성을 가지는 환자군에 대해서도 새로운 치료전략을 제시할 수 있다. 특히 세툭시맙 치료 대상에서 제외됐던 KRAS 돌연변이가 있는 환자군에 대해서도 GNB5의 억제를 통해 치료 효과를 가져올 수 있을 것으로 기대된다.
조 교수는 “지금껏 GNB5 유전자 조절을 대장암의 조합치료에 활용한 예는 없었다”라며 “시스템생물학으로 암세포가 가지는 약제 내성의 원리를 밝히고, 내성 환자군에 대한 바이오마커 동정 및 내성 극복을 위한 병행치료 타겟 발굴을 통해 정밀의학을 실현할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유럽생화학회저널 4월 표지
2019.05.07 조회수 16336
조광현 교수, 대장암 항암제 내성 극복할 병용 치료타겟 발굴
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암의 항암제 내성을 극복할 수 있는 새로운 병용치료 타겟을 발굴하는 데 성공했다.
연구팀은 암세포의 복잡한 생체데이터를 분자 네트워크 관점에서 분석하는 시스템생물학 접근법의 중요성을 제시했다. 이 방법을 통해 암세포가 가지는 약제 내성의 원리를 시스템 차원에서 파악하고, 새로운 약물 타겟을 체계적으로 발굴할 수 있을 것으로 기대된다.
박상민 박사과정, 황채영 박사 등이 참여한 이번 연구결과는 국제학술지 ‘유럽생화학회저널(FEBS Journal)’의 4월호 표지논문으로 게재됐다. (논문명 : Systems analysis identifies potential target genes to overcome cetuximab resistance in colorectal cancer cells)
암은 흔하게 발생하는 대표적인 난치병으로 특히 대장암은 전 세계적으로 환자 수가 100만 명을 넘어섰고, 국내의 경우 서구화된 식습관과 비만 등으로 인해 발병률 증가 속도가 10년간 가장 높게 나타났다. 최근 급격한 고령화에 따라 대장암 환자의 발생률 및 사망률이 가파르게 증가할 것으로 예상되고 있다.
최근 암세포의 특정 분자만을 표적으로 하는 표적항암제가 개발돼 부작용을 크게 줄이고 효과를 높일 수 있지만, 여전히 약물에 반응하는 환자가 매우 제한적이며 그나마 반응을 보이더라도 표적 항암치료 후 약물에 대한 내성이 생겨 암이 재발하는 문제를 안고 있다.
또한, 환자별로 항암제에 대한 반응이 매우 달라 환자의 암 조직 내 유전자 변이의 특징에 따라 적합한 치료를 선택하는 정밀의학의 필요성이 커지고 있다. 대장암 역시 약물의 효과를 예측할 수 있는 유전자 바이오마커의 여부에 따라 적합한 표적항암제를 처방하는 시도가 이뤄지고 있다.
FDA 승인을 받은 대표적인 대장암 치료제인 세툭시맙(cetuximab)의 경우 약물 반응성을 예측하는 바이오마커로 KRAS 유전자 돌연변이의 유무가 활용되고 있는데 이 유전자 돌연변이가 없는 환자에게 처방을 권고하고 있다.
그러나 KRAS 돌연변이가 없는 환자도 세툭시맙 반응률은 절반 정도에 불과하고 기존 항암 화학요법 단독시행과 비교해도 평균 5개월의 수명을 연장하는 데 그치고 있다. 오히려 KRAS 돌연변이가 있는 환자에게서 반응성이 있는 경우가 보고되고 있다.
따라서 KRAS 돌연변이 유무 이외의 새 바이오마커가 요구되고 있으며 KRAS 돌연변이가 존재해도 내성을 극복할 수 있는 병용치료 타겟의 발굴이 필요하다.
조 교수 연구팀은 유전체 데이터 분석, 수학 모델링, 컴퓨터 시뮬레이션 분석과 암 세포주 실험을 융합한 시스템생물학 연구를 통해 세툭시맙 반응성에 대한 바이오마커로 다섯 개의 새로운 유전자(DUSP4, ETV5, GNB5, NT5E, PHLDA1)를 찾아냈다.
그리고 대장암세포에서 각 유전자를 실험적으로 억제한 결과 KRAS 정상 세포에서 발생하는 세툭시맙 내성을 모두 극복할 수 있었다.
특히 GNB5를 억제하면 KRAS 돌연변이가 있는 세포주에서도 세툭시맙 처리에 따른 약물내성을 극복할 수 있음을 밝혔다. 따라서 GNB5의 억제를 통해 대장암 환자의 KRAS 돌연변이 유무와 관계없이 세툭시맙에 대한 내성을 극복할 수 있어 GNB5가 효과적인 병용치료 분자 타겟이 될 수 있음을 증명했다.
연구팀이 제시한 유전자를 바이오마커로 활용하면 세툭시맙에 잘 반응할 수 있는 민감 환자군을 미리 선별해 치료할 수 있는 정밀의학의 실현을 앞당길 수 있다.
또한, 발굴된 유전자들을 표적화하는 신약개발을 통해 내성을 가지는 환자군에 대해서도 새로운 치료전략을 제시할 수 있다. 특히 세툭시맙 치료 대상에서 제외됐던 KRAS 돌연변이가 있는 환자군에 대해서도 GNB5의 억제를 통해 치료 효과를 가져올 수 있을 것으로 기대된다.
조 교수는 “지금껏 GNB5 유전자 조절을 대장암의 조합치료에 활용한 예는 없었다”라며 “시스템생물학으로 암세포가 가지는 약제 내성의 원리를 밝히고, 내성 환자군에 대한 바이오마커 동정 및 내성 극복을 위한 병행치료 타겟 발굴을 통해 정밀의학을 실현할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유럽생화학회저널 4월 표지
2019.05.07 조회수 16336 -
 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 15842
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 15842 -
 조광현 교수, 뇌파 생성, 변조 담당하는 신경회로 원리 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌파의 생성 및 변조를 담당하는 핵심 신경회로를 규명하는 데 성공했다.
이를 통해 뇌의 동작원리를 밝힐 뿐 아니라 향후 여러 뇌질환 환자에게서 발생하는 비정상적 뇌파활동을 신경세포 네트워크 수준에서 규명하는 데 활용 가능할 것으로 기대된다. 이번 연구는 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명했다는 의미를 갖는다.
이병욱 박사과정, 신동관 박사, 스티븐 그로스 박사가 함께 참여한 이번 연구는 국제 학술지 ‘셀 리포트(Cell Reports)’ 11월 6일자 온라인 판에 게재됐다.
뇌의 다양한 기능은 신경세포(뉴런) 사이의 복잡한 상호작용을 통해 이뤄진다. 특히 뉴런들의 동시다발적인 발화에 의해 형성되는 뇌파는 뇌의 활동 상태를 측정하는 가장 중요한 지표이며, 특정 기능을 수행하기 위해 영역 간 선택적 통신의 매개체 역할을 하는 것으로 알려져 있다.
또한 뇌파의 비정상적인 생성 및 변조 현상은 다양한 뇌질환과 밀접한 관계를 갖는 것으로 밝혀지고 있다. 이에 따라 전 세계 신경생물학 연구자들은 뇌파의 생성 및 변조 원리를 파악하기 위해 노력해 왔다.
그러나 뇌파의 생성 및 변조는 수많은 뉴런 사이의 복잡한 상호작용을 통해 발생하는 예측할 수 없는 창발적 특성(emergent property)을 갖기 때문에 기존의 신경 생물학 실험을 통해 그 원리를 규명하기에는 한계가 있었다.
조 교수 연구팀은 시스템생물학 기반의 연구방법을 통해 뇌파의 생성 및 변조 원리를 분석했다. 연구팀은 여러 뇌 영역 중 특히 감각 피질(sensory cortex)에 주목했다. 감각 피질은 외부 감각 정보를 처리하고 통합, 조절하는 핵심 영역으로 여러 주파수 대역의 뇌파와 변조를 관측할 수 있다.
연구팀은 최근 커넥토믹스 (connectomics) 연구를 통해 밝혀진 쥐의 감각피질 내 뉴런의 종류 및 뉴런 간 연결성 정보를 이용해 감각피질을 구성하는 뉴런들과 이들을 연결하는 시냅스를 수학 모델을 통해 표현하고 이로부터 신경회로를 구축해 뇌파의 생성 및 변조 과정을 분석했다.
연구팀은 대규모 컴퓨터 시뮬레이션 분석을 통해 흥분성 뉴런과 억제성 뉴런으로 구성된 양성피드백과 음성피드백의 중첩된 구조(interlinked positive and negative feedback)가 뇌파의 생성 및 주파수 변조 현상의 핵심회로임을 최초로 규명했다.
특히 연구팀은 기존의 전기생리학 실험을 통해 측정된 뉴런 간 시냅스의 특정 연결강도가 신경회로의 뇌파 생성 및 변조 기능을 극대화시킬 수 있는 최적의 조합임을 밝혀냈다.
이번에 개발한 수학모형을 활용하면 전통적 생물학 실험을 통해 파악이 어려웠던 뉴런들 간의 다양한 상호작용을 이해하고 신경회로의 복잡한 설계원리를 파악할 수 있을 것으로 기대된다.
또한 여러 뇌질환 환자의 뇌에서 관측되는 비정상적인 뇌파 활동을 신경네트워크 차원에서 분석하고 규명할 수 있을 것으로 예상된다.
시스템생물학 접근을 통한 신경회로의 구조 및 기능 분석은 인공지능의 발전에도 기여할 것으로 기대된다. 두뇌 신경회로의 작동원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다. 자폐증이나 집중력 조절장애 등과 관련된 신경회로 규명, 두뇌 치료 기술 개발 등의 원천 의료기술 개발에도 혁신으로 이어질 수 있다.
조 교수는 “지금껏 뇌파의 생성 및 변조를 담당하는 핵심 신경회로가 밝혀진 바가 없었다”며 “이번 연구에서는 최근 커넥토믹스 (connectomcis) 연구를 통해 점차 밝혀지고 있는 뉴런간의 복잡한 연결성에 숨겨진 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작원리를 파악할 수 있는 새로운 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, 그리고 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뉴런 간 연결 강도에 내제된 기능적 설계원리 파악
그림2. 뇌파의 생성 및 변조를 담당하는 핵심 신경회로
2018.11.14 조회수 14223
조광현 교수, 뇌파 생성, 변조 담당하는 신경회로 원리 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌파의 생성 및 변조를 담당하는 핵심 신경회로를 규명하는 데 성공했다.
이를 통해 뇌의 동작원리를 밝힐 뿐 아니라 향후 여러 뇌질환 환자에게서 발생하는 비정상적 뇌파활동을 신경세포 네트워크 수준에서 규명하는 데 활용 가능할 것으로 기대된다. 이번 연구는 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명했다는 의미를 갖는다.
이병욱 박사과정, 신동관 박사, 스티븐 그로스 박사가 함께 참여한 이번 연구는 국제 학술지 ‘셀 리포트(Cell Reports)’ 11월 6일자 온라인 판에 게재됐다.
뇌의 다양한 기능은 신경세포(뉴런) 사이의 복잡한 상호작용을 통해 이뤄진다. 특히 뉴런들의 동시다발적인 발화에 의해 형성되는 뇌파는 뇌의 활동 상태를 측정하는 가장 중요한 지표이며, 특정 기능을 수행하기 위해 영역 간 선택적 통신의 매개체 역할을 하는 것으로 알려져 있다.
또한 뇌파의 비정상적인 생성 및 변조 현상은 다양한 뇌질환과 밀접한 관계를 갖는 것으로 밝혀지고 있다. 이에 따라 전 세계 신경생물학 연구자들은 뇌파의 생성 및 변조 원리를 파악하기 위해 노력해 왔다.
그러나 뇌파의 생성 및 변조는 수많은 뉴런 사이의 복잡한 상호작용을 통해 발생하는 예측할 수 없는 창발적 특성(emergent property)을 갖기 때문에 기존의 신경 생물학 실험을 통해 그 원리를 규명하기에는 한계가 있었다.
조 교수 연구팀은 시스템생물학 기반의 연구방법을 통해 뇌파의 생성 및 변조 원리를 분석했다. 연구팀은 여러 뇌 영역 중 특히 감각 피질(sensory cortex)에 주목했다. 감각 피질은 외부 감각 정보를 처리하고 통합, 조절하는 핵심 영역으로 여러 주파수 대역의 뇌파와 변조를 관측할 수 있다.
연구팀은 최근 커넥토믹스 (connectomics) 연구를 통해 밝혀진 쥐의 감각피질 내 뉴런의 종류 및 뉴런 간 연결성 정보를 이용해 감각피질을 구성하는 뉴런들과 이들을 연결하는 시냅스를 수학 모델을 통해 표현하고 이로부터 신경회로를 구축해 뇌파의 생성 및 변조 과정을 분석했다.
연구팀은 대규모 컴퓨터 시뮬레이션 분석을 통해 흥분성 뉴런과 억제성 뉴런으로 구성된 양성피드백과 음성피드백의 중첩된 구조(interlinked positive and negative feedback)가 뇌파의 생성 및 주파수 변조 현상의 핵심회로임을 최초로 규명했다.
특히 연구팀은 기존의 전기생리학 실험을 통해 측정된 뉴런 간 시냅스의 특정 연결강도가 신경회로의 뇌파 생성 및 변조 기능을 극대화시킬 수 있는 최적의 조합임을 밝혀냈다.
이번에 개발한 수학모형을 활용하면 전통적 생물학 실험을 통해 파악이 어려웠던 뉴런들 간의 다양한 상호작용을 이해하고 신경회로의 복잡한 설계원리를 파악할 수 있을 것으로 기대된다.
또한 여러 뇌질환 환자의 뇌에서 관측되는 비정상적인 뇌파 활동을 신경네트워크 차원에서 분석하고 규명할 수 있을 것으로 예상된다.
시스템생물학 접근을 통한 신경회로의 구조 및 기능 분석은 인공지능의 발전에도 기여할 것으로 기대된다. 두뇌 신경회로의 작동원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다. 자폐증이나 집중력 조절장애 등과 관련된 신경회로 규명, 두뇌 치료 기술 개발 등의 원천 의료기술 개발에도 혁신으로 이어질 수 있다.
조 교수는 “지금껏 뇌파의 생성 및 변조를 담당하는 핵심 신경회로가 밝혀진 바가 없었다”며 “이번 연구에서는 최근 커넥토믹스 (connectomcis) 연구를 통해 점차 밝혀지고 있는 뉴런간의 복잡한 연결성에 숨겨진 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작원리를 파악할 수 있는 새로운 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, 그리고 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뉴런 간 연결 강도에 내제된 기능적 설계원리 파악
그림2. 뇌파의 생성 및 변조를 담당하는 핵심 신경회로
2018.11.14 조회수 14223 -
 조광현 교수, 섬유아세포 과활성 유발 분자피드백 회로 규명
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 삼성병원 김석형 교수 연구팀과 공동연구를 통해 섬유증 및 암 악성화의 원인이 되는 섬유아세포 과활성을 유발하는 분자피드백 회로를 최초로 규명했다.
신동관 박사와 안수균 학생 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 8월 1일자 온라인 판에 게재됐다.
( https://www.nature.com/articles/s41467-018-05274-6 )
인간의 섬유아세포는 대부분의 정상조직에 비활성화된 상태로 존재하다가 상처회복을 위해 필요할 때 급진적으로 활성화된다. 하지만 이러한 급진적 활성화가 유발되는 원리는 아직 밝혀지지 않았다.
조광현 교수 연구팀은 삼성병원 김석형 교수팀과 공동연구를 통해 Twist1, Prrx1, TNC 분자들이 연쇄적으로 활성을 유발하는 양성피드백회로를 구성함으로서 그와 같은 급진적인 섬유아세포의 활성을 유발한다는 것을 분자생물학실험과 수학모델링, 컴퓨터시뮬레이션 분석, 그리고 동물실험과 임상데이터 분석을 통해 밝혔다.
활성화된 섬유아세포는 상처가 치유된 뒤 다시 비활성화된 상태로 전환돼야 하는데 이 때 피드백회로가 계속 작동하면 섬유증의 발생이나 암 악성화의 원인이 된다.
따라서 이번에 밝혀낸 Twist1-Prrx1-TNC 분자피드백회로는 섬유증과 암의 새로운 치료 타겟으로 활용될 수 있을 것으로 기대된다.
□ 그림 설명
그림1. 섬유아세포의 급진적 활성화를 유발하는 Twist1-Prrx1-TNC 분자피드백회로 규명 과정
그림2. 정상적인 섬유아세포의 활성화 조절과 피드백회로의 비가역적 활성화에 따른 비정상적인 섬유아세포 활성화 조절과정의 비교
2018.08.10 조회수 9788
조광현 교수, 섬유아세포 과활성 유발 분자피드백 회로 규명
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 삼성병원 김석형 교수 연구팀과 공동연구를 통해 섬유증 및 암 악성화의 원인이 되는 섬유아세포 과활성을 유발하는 분자피드백 회로를 최초로 규명했다.
신동관 박사와 안수균 학생 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 8월 1일자 온라인 판에 게재됐다.
( https://www.nature.com/articles/s41467-018-05274-6 )
인간의 섬유아세포는 대부분의 정상조직에 비활성화된 상태로 존재하다가 상처회복을 위해 필요할 때 급진적으로 활성화된다. 하지만 이러한 급진적 활성화가 유발되는 원리는 아직 밝혀지지 않았다.
조광현 교수 연구팀은 삼성병원 김석형 교수팀과 공동연구를 통해 Twist1, Prrx1, TNC 분자들이 연쇄적으로 활성을 유발하는 양성피드백회로를 구성함으로서 그와 같은 급진적인 섬유아세포의 활성을 유발한다는 것을 분자생물학실험과 수학모델링, 컴퓨터시뮬레이션 분석, 그리고 동물실험과 임상데이터 분석을 통해 밝혔다.
활성화된 섬유아세포는 상처가 치유된 뒤 다시 비활성화된 상태로 전환돼야 하는데 이 때 피드백회로가 계속 작동하면 섬유증의 발생이나 암 악성화의 원인이 된다.
따라서 이번에 밝혀낸 Twist1-Prrx1-TNC 분자피드백회로는 섬유증과 암의 새로운 치료 타겟으로 활용될 수 있을 것으로 기대된다.
□ 그림 설명
그림1. 섬유아세포의 급진적 활성화를 유발하는 Twist1-Prrx1-TNC 분자피드백회로 규명 과정
그림2. 정상적인 섬유아세포의 활성화 조절과 피드백회로의 비가역적 활성화에 따른 비정상적인 섬유아세포 활성화 조절과정의 비교
2018.08.10 조회수 9788 -
 고규영 특훈교수, 호암상금 1억원 기부
우리 대학 의과학대학원 고규영 특훈교수가 호암상 상금 1억원을 KAIST 발전기금으로 쾌척했다.
혈관생물학 분야의 세계적인 권위자인 고규영 교수는 지난 1일 호암아트홀에서 열린 ‘제28회 호암상’ 시상식에서 의학상을 수상했다. 고 교수는 암 혈관을 제거하는 대신 정상화시키는 역발상 접근으로 항암제 전달 효율성을 높여 암의 성장과 전이를 줄일 수 있는 새 패러다임을 제시한 공을 인정받았다.
고 교수는 “기초의학자로서 연구 성과를 인정받아 호암상을 수상하게 되어 큰 영광이다”며 “지속적 발전을 위해 더욱 연구에 박차를 다해 갈 것이다”이라며 수상금의 일부를 연구의 원동력이 된 의과학대학원에 기부했다.
특히 고 교수는 지난 2012년에는 제5회 아산의학상을, 2011년에는 제7회 경암상을, 2007년에는 제17회 분쉬의학상 수상한 바 있으며, 수상시마다 매번 상금을 의과학대학원 발전기금으로 기부해 오고 있다.
신성철 총장은 “의미 있는 수상금을 의과학대학원 발전기금으로 흔쾌히 쾌척해주셔서 감사드린다”며 “고 교수의 기부금은 세계적인 의과학자를 키우고 있는 의과학대학원 발전에 큰 도움이 될 것”이라고 밝혔다.
고 교수는 전북대 의대에서 박사 학위를 받고 미국 코넬대학과 인디애나 주립대에서 박사후 과정을 거친 뒤 전북대 의대 교수, 포스텍 교수를 역임하고 현재 KAIST 의과학대학원 특훈 교수와 기초과학연구원 혈관 연구단장으로 재직 중이다.
2018.06.19 조회수 10505
고규영 특훈교수, 호암상금 1억원 기부
우리 대학 의과학대학원 고규영 특훈교수가 호암상 상금 1억원을 KAIST 발전기금으로 쾌척했다.
혈관생물학 분야의 세계적인 권위자인 고규영 교수는 지난 1일 호암아트홀에서 열린 ‘제28회 호암상’ 시상식에서 의학상을 수상했다. 고 교수는 암 혈관을 제거하는 대신 정상화시키는 역발상 접근으로 항암제 전달 효율성을 높여 암의 성장과 전이를 줄일 수 있는 새 패러다임을 제시한 공을 인정받았다.
고 교수는 “기초의학자로서 연구 성과를 인정받아 호암상을 수상하게 되어 큰 영광이다”며 “지속적 발전을 위해 더욱 연구에 박차를 다해 갈 것이다”이라며 수상금의 일부를 연구의 원동력이 된 의과학대학원에 기부했다.
특히 고 교수는 지난 2012년에는 제5회 아산의학상을, 2011년에는 제7회 경암상을, 2007년에는 제17회 분쉬의학상 수상한 바 있으며, 수상시마다 매번 상금을 의과학대학원 발전기금으로 기부해 오고 있다.
신성철 총장은 “의미 있는 수상금을 의과학대학원 발전기금으로 흔쾌히 쾌척해주셔서 감사드린다”며 “고 교수의 기부금은 세계적인 의과학자를 키우고 있는 의과학대학원 발전에 큰 도움이 될 것”이라고 밝혔다.
고 교수는 전북대 의대에서 박사 학위를 받고 미국 코넬대학과 인디애나 주립대에서 박사후 과정을 거친 뒤 전북대 의대 교수, 포스텍 교수를 역임하고 현재 KAIST 의과학대학원 특훈 교수와 기초과학연구원 혈관 연구단장으로 재직 중이다.
2018.06.19 조회수 10505 -
 이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 12609
이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 12609 -
 성단근, 조용훈, 조광현 교수, 2018년도 한국과학기술한림원 신입 정회원 선정
〈 성 단 근 교수 〉
〈 조 용 훈 교수 〉
〈 조 광 현 교수 〉
우리 대학 조용훈, 성단근, 조광현 교수가 지난 12일 성남 한림원회관에서 열린 한국과학기술한림원 2018년도 신년하례식에서 정회원에 선출됐다.
올해 선출된 정회원은 총 24명으로 조용훈 교수는 이학부, 성단근, 조광현 교수는 공학부 정회원으로 선정됐다.
조용훈 교수는 고체 상태에서 양자 광학적인 연구를 가능하게 하는 저차원 반도체 기반의 양자 포토닉스 분야를 개척했으며, 국제적으로 이 분야 연구를 선도한 공을 인정받았다.
성단근 교수는 네트워크 프로토콜 및 에너지 ICT와 관련된 다양한 연구를 수행하고, KAIST의 인공위성연구센터를 설립해 우리별 1, 2, 3호를 성공적으로 발사 및 운영하는 데에 크게 기여한 공을 인정받았다.
조광현 교수는 시스템 생물학 분야에서 IT와 BT를 융합한 독창적인 연구를 수행하고 특히 복잡한 생명 시스템에 대한 전자공학적 모델링 및 컴퓨터 시뮬레이션 분석기법을 처음으로 개발하고 이를 복잡한 생명과학문제에 적용하여 우수한 연구 성과를 도출한 공을 인정받았다.
특히 조 교수는 이번에 선출된 2018년도 정회원 중 최연소 교수로서 현재 한림원 정회원 중 유일한 1970년대 생이다.
한국과학기술한림원의 정회원 임기는 만 70세에 도달한 연도 말일까지이면 정원 500명으로 구성됐다.
2018.01.16 조회수 9626
성단근, 조용훈, 조광현 교수, 2018년도 한국과학기술한림원 신입 정회원 선정
〈 성 단 근 교수 〉
〈 조 용 훈 교수 〉
〈 조 광 현 교수 〉
우리 대학 조용훈, 성단근, 조광현 교수가 지난 12일 성남 한림원회관에서 열린 한국과학기술한림원 2018년도 신년하례식에서 정회원에 선출됐다.
올해 선출된 정회원은 총 24명으로 조용훈 교수는 이학부, 성단근, 조광현 교수는 공학부 정회원으로 선정됐다.
조용훈 교수는 고체 상태에서 양자 광학적인 연구를 가능하게 하는 저차원 반도체 기반의 양자 포토닉스 분야를 개척했으며, 국제적으로 이 분야 연구를 선도한 공을 인정받았다.
성단근 교수는 네트워크 프로토콜 및 에너지 ICT와 관련된 다양한 연구를 수행하고, KAIST의 인공위성연구센터를 설립해 우리별 1, 2, 3호를 성공적으로 발사 및 운영하는 데에 크게 기여한 공을 인정받았다.
조광현 교수는 시스템 생물학 분야에서 IT와 BT를 융합한 독창적인 연구를 수행하고 특히 복잡한 생명 시스템에 대한 전자공학적 모델링 및 컴퓨터 시뮬레이션 분석기법을 처음으로 개발하고 이를 복잡한 생명과학문제에 적용하여 우수한 연구 성과를 도출한 공을 인정받았다.
특히 조 교수는 이번에 선출된 2018년도 정회원 중 최연소 교수로서 현재 한림원 정회원 중 유일한 1970년대 생이다.
한국과학기술한림원의 정회원 임기는 만 70세에 도달한 연도 말일까지이면 정원 500명으로 구성됐다.
2018.01.16 조회수 9626 -
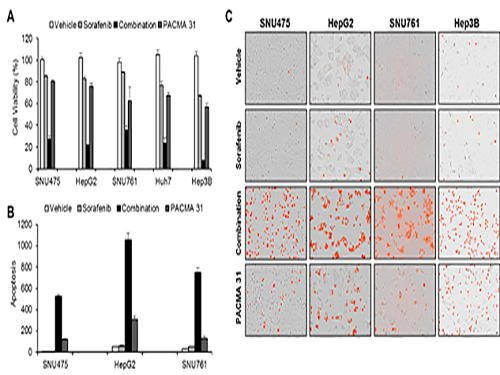 조광현 교수, 간암 표적 치료제 내성 극복 위한 최적 약물조합 발견
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 간암 약물 치료의 효과를 높이는 새로운 방법을 찾아냈다. 특히 이번 연구는 바이오분야의 4차 산업혁명을 견인하고 있는 IT와 BT의 융합연구인 시스템생물학(Systems Biology) 연구로 이뤄졌다.
서울대병원 내과 윤정환 교수팀과 공동연구를 통해 이루어낸 이번 연구 결과는 국제 간 전문지인 헤파톨로지(Hepatology)에 게재됐다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업과 중견연구자지원사업의 지원을 받아 수행됐다.
간암은 전 세계적으로 남성에게는 다섯 번째, 여성에게는 일곱 번째로 발생률이 높은 암이며 암 사망원인의 두 번째를 차지한다. 특히 우리나라의 간암 사망률은 인구 10만 명 당 28.4명으로 경제협력개발기구(OECD) 국가 중 압도적인 1위이며 2위인 일본의 2배에 이르고 있다.
우리나라에서만 간암 환자가 매년 평균 1만 6000명이 새로 발생하고 있지만 5년 생존율이 12%에 미치지 못한다. 국가암정보센터에 따르면 지난해 암으로 사망한 사람 가운데 폐암이 1만 7399명으로 가장 많았고 간암은 1만 1311명으로 그 뒤를 이었다.
간암은 우리나라의 암 가운데 사회적 비용이 1위인 암이다. 그 이유는 다른 암에 비해 사망자가 많고 더 젊은 나이(40, 50대)에 사망하기 때문이다. 이에 부작용이 적고 생존율을 높여줄 수 있는 새로운 치료법 개발이 시급한 실정이다.
간암의 치료로는 수술 및 색전술, 약물 치료가 있지만 수술이 어려운 진행성 간암에서는 치료 방법이 극히 제한적이다.
진행성 간암의 표적 항암제로 소라페닙(Sorafenib)이 유일하게 승인돼 임상에서 쓰이고 있는데 국내에서만 매년 200억 원 이상 처방되고 있지만 일부 환자에서만 효능을 나타내며 또한 대부분의 경우 약제 내성이 발생한다.
소라페닙은 말기 간암 환자의 생존 기간을 약 3개월 정도 밖에 늘리지 못하지만 다국적 제약회사에 의해 개발된 많은 후발주자 약물들이 그 효과를 뛰어 넘는데 실패했다.
소라페닙은 다중타겟을 치료표적으로 하여 그 작용 기전이 모호하고 따라서 약제의 내성기전 또한 아직 잘 알려져 있지 않다.
조광현 교수가 이끈 융합 연구팀은 소라페닙 작용 및 내성 기전을 규명하기 위해 소라페닙을 간암 세포에 처리하였을 때 세포내 분자 발현이 변화하는 것을 분석했다.
이를 통해 암세포가 소라페닙에 대항하는 기전을 알아냈고 시스템생물학적 분석을 실시하여 암세포내 단백질 이황화 이성질화 효소(protein disulfide isomerase, PDI)가 암세포가 소라페닙에 대항하는데 핵심적 역할을 하는 것을 발견했으며 이 효소를 차단했을 때 소라페닙의 효능이 훨씬 증가함을 관찰했다.
공동연구를 수행한 서울대병원 내과 윤정환 교수 연구팀은 쥐를 이용한 동물실험에서 소라페닙과 단백질 이황화 이성질화 효소 차단제를 같이 처리하면 간암 증식 억제에 시너지가 있음을 관찰하였고 소라페닙에 저항성을 가진 간암 환자의 조직에서 이 효소가 증가되어 있음을 관찰하여, 향후 임상 적용을 위한 가능성을 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 IT와 BT의 융합연구인 시스템생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암에 대한 표적 치료제 작용을 네트워크 차원에서 분석하여 내성을 극복할 수 있는 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 말했다.
□ 사진 설명
사진1. 간암세포를 이용한 세포실험을 이용해 시뮬레이션 결과를 확인
사진2. 구축된 ER stress 네트워크를 이용한 네트워크 분석 및 컴퓨터 시뮬레이션 결과
사진3. 간암 세포가 소라페닙에 반응할 때 전사체 변화를 분석하여 ER stress 반응이 주요하게 나타남을 발견하게 된 ER stress 네트워크 모델
2017.08.24 조회수 15393
조광현 교수, 간암 표적 치료제 내성 극복 위한 최적 약물조합 발견
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 간암 약물 치료의 효과를 높이는 새로운 방법을 찾아냈다. 특히 이번 연구는 바이오분야의 4차 산업혁명을 견인하고 있는 IT와 BT의 융합연구인 시스템생물학(Systems Biology) 연구로 이뤄졌다.
서울대병원 내과 윤정환 교수팀과 공동연구를 통해 이루어낸 이번 연구 결과는 국제 간 전문지인 헤파톨로지(Hepatology)에 게재됐다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업과 중견연구자지원사업의 지원을 받아 수행됐다.
간암은 전 세계적으로 남성에게는 다섯 번째, 여성에게는 일곱 번째로 발생률이 높은 암이며 암 사망원인의 두 번째를 차지한다. 특히 우리나라의 간암 사망률은 인구 10만 명 당 28.4명으로 경제협력개발기구(OECD) 국가 중 압도적인 1위이며 2위인 일본의 2배에 이르고 있다.
우리나라에서만 간암 환자가 매년 평균 1만 6000명이 새로 발생하고 있지만 5년 생존율이 12%에 미치지 못한다. 국가암정보센터에 따르면 지난해 암으로 사망한 사람 가운데 폐암이 1만 7399명으로 가장 많았고 간암은 1만 1311명으로 그 뒤를 이었다.
간암은 우리나라의 암 가운데 사회적 비용이 1위인 암이다. 그 이유는 다른 암에 비해 사망자가 많고 더 젊은 나이(40, 50대)에 사망하기 때문이다. 이에 부작용이 적고 생존율을 높여줄 수 있는 새로운 치료법 개발이 시급한 실정이다.
간암의 치료로는 수술 및 색전술, 약물 치료가 있지만 수술이 어려운 진행성 간암에서는 치료 방법이 극히 제한적이다.
진행성 간암의 표적 항암제로 소라페닙(Sorafenib)이 유일하게 승인돼 임상에서 쓰이고 있는데 국내에서만 매년 200억 원 이상 처방되고 있지만 일부 환자에서만 효능을 나타내며 또한 대부분의 경우 약제 내성이 발생한다.
소라페닙은 말기 간암 환자의 생존 기간을 약 3개월 정도 밖에 늘리지 못하지만 다국적 제약회사에 의해 개발된 많은 후발주자 약물들이 그 효과를 뛰어 넘는데 실패했다.
소라페닙은 다중타겟을 치료표적으로 하여 그 작용 기전이 모호하고 따라서 약제의 내성기전 또한 아직 잘 알려져 있지 않다.
조광현 교수가 이끈 융합 연구팀은 소라페닙 작용 및 내성 기전을 규명하기 위해 소라페닙을 간암 세포에 처리하였을 때 세포내 분자 발현이 변화하는 것을 분석했다.
이를 통해 암세포가 소라페닙에 대항하는 기전을 알아냈고 시스템생물학적 분석을 실시하여 암세포내 단백질 이황화 이성질화 효소(protein disulfide isomerase, PDI)가 암세포가 소라페닙에 대항하는데 핵심적 역할을 하는 것을 발견했으며 이 효소를 차단했을 때 소라페닙의 효능이 훨씬 증가함을 관찰했다.
공동연구를 수행한 서울대병원 내과 윤정환 교수 연구팀은 쥐를 이용한 동물실험에서 소라페닙과 단백질 이황화 이성질화 효소 차단제를 같이 처리하면 간암 증식 억제에 시너지가 있음을 관찰하였고 소라페닙에 저항성을 가진 간암 환자의 조직에서 이 효소가 증가되어 있음을 관찰하여, 향후 임상 적용을 위한 가능성을 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 IT와 BT의 융합연구인 시스템생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암에 대한 표적 치료제 작용을 네트워크 차원에서 분석하여 내성을 극복할 수 있는 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 말했다.
□ 사진 설명
사진1. 간암세포를 이용한 세포실험을 이용해 시뮬레이션 결과를 확인
사진2. 구축된 ER stress 네트워크를 이용한 네트워크 분석 및 컴퓨터 시뮬레이션 결과
사진3. 간암 세포가 소라페닙에 반응할 때 전사체 변화를 분석하여 ER stress 반응이 주요하게 나타남을 발견하게 된 ER stress 네트워크 모델
2017.08.24 조회수 15393 -
 김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
2017.07.11 조회수 14971
김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
2017.07.11 조회수 14971 -
 KAIST, 2017 하계 다보스 포럼에 참가해 융합연구 성과 적극 홍보
우리대학이 국내대학 중 유일하게 오는 6월 27일부터 29일까지 중국 다롄시 국제컨퍼런스센터에서 열리는 2017 세계경제포럼(WEF) 하계대회(이하 하계 다보스 포럼)에 초청받아 신 총장 등 참가교수들이 세션 운영과 패널 참여를 통해 첨단 융합연구 사례를 적극 홍보하는 한편 창의적 인재양성과 세계적인 빅 이슈에 대해 다양한 해법 등을 제시할 예정이다. 정식명칭이 “새로운 챔피언들의 연차총회”라고 불리는 하계 다보스 포럼은 중국이 스위스 다보스 포럼과 같이 세계 경제와 글로벌 이슈를 주도하기 위해 2007년부터 세계경제포럼(WEF)과 매년 공동으로 개최해오는 국제회의다. 인공지능·빅데이터 등으로 대표되는 4차 산업혁명 물결이 전 세계를 휩쓸고 있는 가운데 열리는 올해 포럼에는 리커창 중국 국무원 총리를 포함, 화웨이의 궈핑 최고경영자, 로봇·자율주행차 등 다양한 분야에서 기술 혁신에 나서고 있는 바이두의 장야친 총재 등 90여 개국에서 2,000여명의 정치계·관계·재계·학계 인사가 참가한다.
‘제4차 산업혁명시대에 포용적 성장을 이루기(Achieving inclusive growth in the fourth industrial revolution)’라는 주제로 열리는 이번 포럼에서 과학기술 전문가 등 전 세계 90여 개국의 참가자들은 다양한 세션에 참여해 4차 산업혁명시대에 관한 글로벌 혁신이슈와 과학기술, 그리고 포용적 성장에 관해 심도 있는 발표와 토론을 벌일 예정이다. 우리대학은 전 세계 리더들을 대상으로 최신의 연구동향을 소개하고 함께 토론하는 자리인 ‘아이디어스랩(IdeasLab)’을 국내대학 중 유일하게 운영할 계획이다. 우리대학이 아이디어스랩을 운영하는 것은 올해가 6번째다.
올해 아이디어스랩은 ‘미래 소재 (Materials of the Future)’를 주제로 열리는데 우리대학에서 개발한 제4차 산업혁명을 이끌 소재들에 대한 발표와 함께 토론이 진행된다. 회의는 세션 위원장을 맡은 신성철 총장이 우리대학 현황과 아이디어스랩을 소개한 뒤 우리대학 교수진의 최첨단 융합연구 결과에 대한 발표가 이어진다. 신성철 총장은 이와 함께 글로벌대학리더스포럼(GULF)이 주관하는 다양한 세션에 토론리더로 참여해 우리대학 연구원이 수행 중인 제4차 산업혁명시대의 융합연구 사례들과 창의적 교육혁신 등을 주제로 발표와 토론을 진행한다.
신 총장은 국내 유일의 세계경제포럼 산하 전 세계 27개 선도대학 총장들의 모임인 GULF의 멤버다. 이 모임에는 우리대학외에 영국 옥스퍼드대와 캠브리지대를 비롯, 미국 MIT·하버드대·스탠포드대·콜롬비아대와 일본 동경대, 중국 북경대 총장들이 회원으로 참여하고 있다. 신 총장은 이밖에 4차 산업혁명시대의 포용적 성장을 위한 전략세션에도 참여하는 한편 세계경제포럼 이사진과의 회의 등에도 참석하는 등 다양한 활동을 하게 된다.
다보스 포럼과 하계 다보스 포럼에 15년 이상 초청을 받아 온 이상엽 연구원장(생명화학공학과·특훈교수)은 ‘삶의 미래: 의약(Future of Life: Medicine)’세션에서 발표자로 나서 시스템생물학에 의한 전통의약의 선진화와 마이크로바이움(장내 미생물) 등에 대한 연구내용과 미래전망 등에 관해 소개한다. 이 교수는 또 세계경제포럼 바이오텍 글로벌 퓨처카운슬 의장과 4차 산업혁명 카운슬 위원자격으로 다양한 바이오 세션들과 4차 산업혁명 만찬세션에도 참가해서 혁신 융합연구 사례와 4차 산업혁명 속 포용적 성장을 위한 전략 등을 주제로 토론을 진행한다.
신성철 총장은 “KAIST는 그동안 아이디어스랩 운영을 통해 거둔 세계적인 연구 성과를 다보스 포럼에 참석한 전 세계 지도자들에게 발표하고 공유함으로써 좋은 평가를 받아왔다”며 “이번 포럼은 4차 산업혁명 시대가 가져 올 기술변화와 인간중심의 발전방안 등에 대해 심층 논의하는 한편 그동안 KAIST가 추진해 온 혁신적 연구 및 융합연구 성과를 적극 소개하는 자리가 될 것”이라고 강조했다.
2017.06.21 조회수 13907
KAIST, 2017 하계 다보스 포럼에 참가해 융합연구 성과 적극 홍보
우리대학이 국내대학 중 유일하게 오는 6월 27일부터 29일까지 중국 다롄시 국제컨퍼런스센터에서 열리는 2017 세계경제포럼(WEF) 하계대회(이하 하계 다보스 포럼)에 초청받아 신 총장 등 참가교수들이 세션 운영과 패널 참여를 통해 첨단 융합연구 사례를 적극 홍보하는 한편 창의적 인재양성과 세계적인 빅 이슈에 대해 다양한 해법 등을 제시할 예정이다. 정식명칭이 “새로운 챔피언들의 연차총회”라고 불리는 하계 다보스 포럼은 중국이 스위스 다보스 포럼과 같이 세계 경제와 글로벌 이슈를 주도하기 위해 2007년부터 세계경제포럼(WEF)과 매년 공동으로 개최해오는 국제회의다. 인공지능·빅데이터 등으로 대표되는 4차 산업혁명 물결이 전 세계를 휩쓸고 있는 가운데 열리는 올해 포럼에는 리커창 중국 국무원 총리를 포함, 화웨이의 궈핑 최고경영자, 로봇·자율주행차 등 다양한 분야에서 기술 혁신에 나서고 있는 바이두의 장야친 총재 등 90여 개국에서 2,000여명의 정치계·관계·재계·학계 인사가 참가한다.
‘제4차 산업혁명시대에 포용적 성장을 이루기(Achieving inclusive growth in the fourth industrial revolution)’라는 주제로 열리는 이번 포럼에서 과학기술 전문가 등 전 세계 90여 개국의 참가자들은 다양한 세션에 참여해 4차 산업혁명시대에 관한 글로벌 혁신이슈와 과학기술, 그리고 포용적 성장에 관해 심도 있는 발표와 토론을 벌일 예정이다. 우리대학은 전 세계 리더들을 대상으로 최신의 연구동향을 소개하고 함께 토론하는 자리인 ‘아이디어스랩(IdeasLab)’을 국내대학 중 유일하게 운영할 계획이다. 우리대학이 아이디어스랩을 운영하는 것은 올해가 6번째다.
올해 아이디어스랩은 ‘미래 소재 (Materials of the Future)’를 주제로 열리는데 우리대학에서 개발한 제4차 산업혁명을 이끌 소재들에 대한 발표와 함께 토론이 진행된다. 회의는 세션 위원장을 맡은 신성철 총장이 우리대학 현황과 아이디어스랩을 소개한 뒤 우리대학 교수진의 최첨단 융합연구 결과에 대한 발표가 이어진다. 신성철 총장은 이와 함께 글로벌대학리더스포럼(GULF)이 주관하는 다양한 세션에 토론리더로 참여해 우리대학 연구원이 수행 중인 제4차 산업혁명시대의 융합연구 사례들과 창의적 교육혁신 등을 주제로 발표와 토론을 진행한다.
신 총장은 국내 유일의 세계경제포럼 산하 전 세계 27개 선도대학 총장들의 모임인 GULF의 멤버다. 이 모임에는 우리대학외에 영국 옥스퍼드대와 캠브리지대를 비롯, 미국 MIT·하버드대·스탠포드대·콜롬비아대와 일본 동경대, 중국 북경대 총장들이 회원으로 참여하고 있다. 신 총장은 이밖에 4차 산업혁명시대의 포용적 성장을 위한 전략세션에도 참여하는 한편 세계경제포럼 이사진과의 회의 등에도 참석하는 등 다양한 활동을 하게 된다.
다보스 포럼과 하계 다보스 포럼에 15년 이상 초청을 받아 온 이상엽 연구원장(생명화학공학과·특훈교수)은 ‘삶의 미래: 의약(Future of Life: Medicine)’세션에서 발표자로 나서 시스템생물학에 의한 전통의약의 선진화와 마이크로바이움(장내 미생물) 등에 대한 연구내용과 미래전망 등에 관해 소개한다. 이 교수는 또 세계경제포럼 바이오텍 글로벌 퓨처카운슬 의장과 4차 산업혁명 카운슬 위원자격으로 다양한 바이오 세션들과 4차 산업혁명 만찬세션에도 참가해서 혁신 융합연구 사례와 4차 산업혁명 속 포용적 성장을 위한 전략 등을 주제로 토론을 진행한다.
신성철 총장은 “KAIST는 그동안 아이디어스랩 운영을 통해 거둔 세계적인 연구 성과를 다보스 포럼에 참석한 전 세계 지도자들에게 발표하고 공유함으로써 좋은 평가를 받아왔다”며 “이번 포럼은 4차 산업혁명 시대가 가져 올 기술변화와 인간중심의 발전방안 등에 대해 심층 논의하는 한편 그동안 KAIST가 추진해 온 혁신적 연구 및 융합연구 성과를 적극 소개하는 자리가 될 것”이라고 강조했다.
2017.06.21 조회수 13907