-
 김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
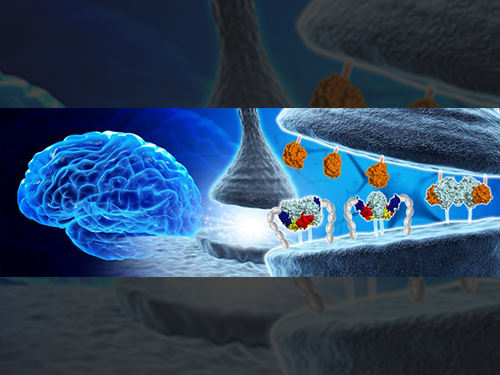
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
2017.07.11
조회수 14075
-
 항공우주공학과, NASA임무설계대회 최우수상 수상
〈 KAIST 팀 학생들, 왼쪽부터 이주성, 고재열, 최석민, 서종은, 이은광 〉
〈 안재명 지도교수 〉
우리 대학 항공우주공학과 학생 팀이 美 항공우주국(NASA)이 주관하는 항공우주 임무 설계 경연대회인 라스칼(RASCAL : Revolutionary Aerospace Systems Concepts Academic Linkage) 대회에서 달 탐사 시스템 설계 분야 최우수상(Best in Theme Award)을 수상했다.
항공우주공학과 안재명 교수의 지도하에 고재열, 서종은, 이주성, 최석민, 이은광 학생으로 구성된 KAIST 팀은 미국 학교가 반드시 포함돼야 하는 대회 규정에 따라 텍사스 공대(Texas Tech University), 왕립 멜버른 공대(Royal Melbourne Institute of Technology)와 함께 연합 팀으로 출전했다.
연합 팀은 두 차례의 예선을 거쳐 최종 14팀에 선정돼 5월 30일부터 6월 3일까지 플로리다에서 열린 본선에서 발표회를 가졌다. 총 4개 분야 중 ‘장기간 유인 달 탐사를 위한 물자 전송 시스템 설계’ 에 참여한 연합 팀은 해당 부문 1등상을 수상했다.
NASA 주관 하에 2002년부터 개최된 라스칼은 혁신적인 항공우주 시스템 및 임무를 주제로 학생들의 설계 역량을 겨루는 대회로 세계 최고 수준 학교 및 학생들이 참가하고 있다.
올해 대회 분야는 ▲우주인을 위한 경량 체력단련 모듈 설계(Lightweight Exercise Suite) ▲우주인의 선외 활동을 위한 에어록 모듈 설계(Airlock Design) ▲지구저궤도 및 화성에서 사용 가능한 상용 우주인 거주 모듈 설계(Commercially Enabled LEO/Mars Habitable Module) ▲장기간 유인 달 탐사를 위한 물자 전송 시스템 설계(Logistics Delivery System)로 구분된다.
달 탐사를 위해서는 많은 시간과 물자가 필요하다. KAIST 팀은 장기 유인 달 탐사를 위한 우주 물자이동시스템 설계를 위해 작년부터 약 8개월 간 연합 팀과의 회의를 통해 연구를 해왔다.
특히 장기 유인 달 탐사 임무에는 초기 계획 수립 시 예측할 수 없는 돌발 상황이 발생할 수 있다. KAIST 팀은 이와 같은 임무 불확실성에 대응하기 위해 유연성을 극대화하는 시스템과 운용 개념을 도출, 물자 수송에 소요되는 비용 효용성을 극대화했다.
구체적으로 우주선을 기능에 따라 추진 모듈과 배송 모듈로 나누어 설계했고 달 기지의 수요에 맞춰 배송 모듈을 교환할 수 있게 했다. 또한 다양한 출발 지점을 활용했다
항공우주공학과는 시스템 중심적 사고를 기반으로 한 항공 우주 연구에 초점을 맞춰왔고, 이를 통해 첫 참가임에도 NASA 주관 대회에서 우수한 성적을 거둘 수 있었다.
지도를 맡은 안재명 교수는 “멀리 떨어진 국제연합팀을 리드하며 훌륭한 결과를 만든 학생들이 자랑스럽다”며 “학과가 지속적으로 노력한 시스템-설계 중심 교육의 결실이라고 생각하고 향후 설계교육 분야의 국제협력을 통해 양질의 교육과 다양한 기회를 제공하겠다.”고 말했다.
항공우주공학과, NASA임무설계대회 최우수상 수상
〈 KAIST 팀 학생들, 왼쪽부터 이주성, 고재열, 최석민, 서종은, 이은광 〉
〈 안재명 지도교수 〉
우리 대학 항공우주공학과 학생 팀이 美 항공우주국(NASA)이 주관하는 항공우주 임무 설계 경연대회인 라스칼(RASCAL : Revolutionary Aerospace Systems Concepts Academic Linkage) 대회에서 달 탐사 시스템 설계 분야 최우수상(Best in Theme Award)을 수상했다.
항공우주공학과 안재명 교수의 지도하에 고재열, 서종은, 이주성, 최석민, 이은광 학생으로 구성된 KAIST 팀은 미국 학교가 반드시 포함돼야 하는 대회 규정에 따라 텍사스 공대(Texas Tech University), 왕립 멜버른 공대(Royal Melbourne Institute of Technology)와 함께 연합 팀으로 출전했다.
연합 팀은 두 차례의 예선을 거쳐 최종 14팀에 선정돼 5월 30일부터 6월 3일까지 플로리다에서 열린 본선에서 발표회를 가졌다. 총 4개 분야 중 ‘장기간 유인 달 탐사를 위한 물자 전송 시스템 설계’ 에 참여한 연합 팀은 해당 부문 1등상을 수상했다.
NASA 주관 하에 2002년부터 개최된 라스칼은 혁신적인 항공우주 시스템 및 임무를 주제로 학생들의 설계 역량을 겨루는 대회로 세계 최고 수준 학교 및 학생들이 참가하고 있다.
올해 대회 분야는 ▲우주인을 위한 경량 체력단련 모듈 설계(Lightweight Exercise Suite) ▲우주인의 선외 활동을 위한 에어록 모듈 설계(Airlock Design) ▲지구저궤도 및 화성에서 사용 가능한 상용 우주인 거주 모듈 설계(Commercially Enabled LEO/Mars Habitable Module) ▲장기간 유인 달 탐사를 위한 물자 전송 시스템 설계(Logistics Delivery System)로 구분된다.
달 탐사를 위해서는 많은 시간과 물자가 필요하다. KAIST 팀은 장기 유인 달 탐사를 위한 우주 물자이동시스템 설계를 위해 작년부터 약 8개월 간 연합 팀과의 회의를 통해 연구를 해왔다.
특히 장기 유인 달 탐사 임무에는 초기 계획 수립 시 예측할 수 없는 돌발 상황이 발생할 수 있다. KAIST 팀은 이와 같은 임무 불확실성에 대응하기 위해 유연성을 극대화하는 시스템과 운용 개념을 도출, 물자 수송에 소요되는 비용 효용성을 극대화했다.
구체적으로 우주선을 기능에 따라 추진 모듈과 배송 모듈로 나누어 설계했고 달 기지의 수요에 맞춰 배송 모듈을 교환할 수 있게 했다. 또한 다양한 출발 지점을 활용했다
항공우주공학과는 시스템 중심적 사고를 기반으로 한 항공 우주 연구에 초점을 맞춰왔고, 이를 통해 첫 참가임에도 NASA 주관 대회에서 우수한 성적을 거둘 수 있었다.
지도를 맡은 안재명 교수는 “멀리 떨어진 국제연합팀을 리드하며 훌륭한 결과를 만든 학생들이 자랑스럽다”며 “학과가 지속적으로 노력한 시스템-설계 중심 교육의 결실이라고 생각하고 향후 설계교육 분야의 국제협력을 통해 양질의 교육과 다양한 기회를 제공하겠다.”고 말했다.
2017.06.20
조회수 16013
-
 국제대학생프로그래밍 대회에서 동메달 수상
〈 한태숙 교수와 참가 학생들 〉
우리 대학 전산학부와 수리과학과 학부생 팀이 국제 대학생 프로그래밍 대회인 ACM ICPC 월드 파이널에서 동메달 및 First Problem Solver 상을 수상했다.
지난 5월 25일 미국 사우스다코다 주 래피드시티에서 열린 제 41회 국제 대학생 프로그래밍 대회는 미국 컴퓨터 협회(ACM)가 주최하고 IBM이 후원한다.
1977년 처음 개최돼 전 세계 대학생을 대상으로 열리는 권위 있는 행사로 지역대회에는 103개국 2천 900여 개 대학에서 총 5만 여 명이 참가했고 본선 대회에서는 400여 명의 대학생들이 경쟁을 벌였다.
대회는 3명이 한 팀이 돼 12문제를 해결하는 방식으로 진행되며 우리 대학에서는 신성용 전산학부 명예교수, 한태숙 교수가 코치를 맡았고, 전산학부 고지훈, 강한필 학생과 수리과학과 이종원 학생이 참가했다.
우리 대학 대표팀은 9위를 기록해 동메달과 3천 달러의 상금을 차지했고 전 참가팀 중에서 처음으로 문제를 풀어 First Problem Solver 상을 수상했다.
자세한 스코어 정보는 https://icpc.baylor.edu/scoreboard/ 를 통해 확인 가능하다.
국제대학생프로그래밍 대회에서 동메달 수상
〈 한태숙 교수와 참가 학생들 〉
우리 대학 전산학부와 수리과학과 학부생 팀이 국제 대학생 프로그래밍 대회인 ACM ICPC 월드 파이널에서 동메달 및 First Problem Solver 상을 수상했다.
지난 5월 25일 미국 사우스다코다 주 래피드시티에서 열린 제 41회 국제 대학생 프로그래밍 대회는 미국 컴퓨터 협회(ACM)가 주최하고 IBM이 후원한다.
1977년 처음 개최돼 전 세계 대학생을 대상으로 열리는 권위 있는 행사로 지역대회에는 103개국 2천 900여 개 대학에서 총 5만 여 명이 참가했고 본선 대회에서는 400여 명의 대학생들이 경쟁을 벌였다.
대회는 3명이 한 팀이 돼 12문제를 해결하는 방식으로 진행되며 우리 대학에서는 신성용 전산학부 명예교수, 한태숙 교수가 코치를 맡았고, 전산학부 고지훈, 강한필 학생과 수리과학과 이종원 학생이 참가했다.
우리 대학 대표팀은 9위를 기록해 동메달과 3천 달러의 상금을 차지했고 전 참가팀 중에서 처음으로 문제를 풀어 First Problem Solver 상을 수상했다.
자세한 스코어 정보는 https://icpc.baylor.edu/scoreboard/ 를 통해 확인 가능하다.
2017.06.02
조회수 10566
-
 김세윤 교수, 이노시톨 대사효소에 의한 패혈증 유발 염증전달신호 규명
우리 대학 생명과학과 김세윤 교수 연구팀이 이노시톨 생합성 대사의 핵심효소인 IPMK (Inositol polyphosphate multikinase)에 의해 패혈증 등의 선천성 면역반응을 매개하는 신호전달네트워크가 정교하게 조절되는 현상을 규명했다.
김은하 박사과정이 제1저자로 참여한 이번 연구 결과는 서울대학교 성노현 교수 연구팀과 공동으로 진행됐고 사이언스 어드밴시스(Science Advances)지 4월 21일자에 게재됐다.
김세윤 교수 연구팀은 이노시톨 대사체 및 생합성 대사를 수 년 간 연구했고 이노시톨 다인산 멀티키나아제 효소(IPMK)에 의한 세포 성장 및 에너지 대사조절 기능을 다각적으로 규명한 바 있다.
이번 연구에서는 대식세포(macrophage) 특이적으로 IPMK 효소가 결핍된 생쥐에서 패혈성 쇼크를 유발시켰을 때 염증수준이 현저히 저하되고 또한 높은 생존율을 보이는 것을 확인했다. 이는 선천성 면역의 핵심인 염증반응이 강력히 저해되는 것을 의미한다.
IPMK 효소가 면역신호조절물질인 TRAF6 단백질과 직접 결합해 TRAF6 단백질의 분해를 조절하는 유비퀴틴화를 억제함을 규명했고, IPMK효소와 TRAF6단백질간 결합력을 저해할 수 있는 펩타이드를 활용함으로써 내독소에 의한 염증반응을 낮출 수 있음을 다각적으로 검증했다.
이번 연구는 미생물 감염 등에 의한 패혈증 발병의 원리를 규명함과 동시에 최근 급증하는 선천 면역 질환 (ex. 신경계 염증질환 및 당뇨)에 대한 이해를 넓히고 새로운 치료기술개발에 필요한 학문적 토대를 제공했다는 의의를 갖는다.
이번 연구는 미래창조과학부 뇌과학원천기술개발사업의 지원을 받아 이뤄졌다.
□ 그림 설명
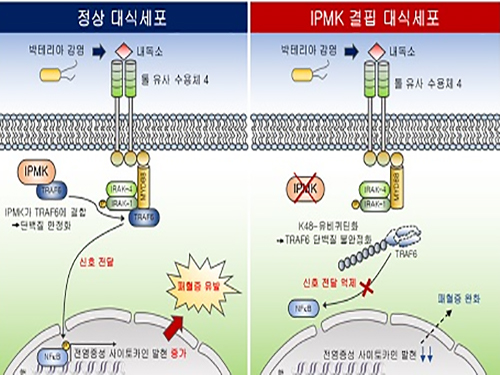
그림1. IPMK 효소의 선천성 면역조절 모식도
김세윤 교수, 이노시톨 대사효소에 의한 패혈증 유발 염증전달신호 규명
우리 대학 생명과학과 김세윤 교수 연구팀이 이노시톨 생합성 대사의 핵심효소인 IPMK (Inositol polyphosphate multikinase)에 의해 패혈증 등의 선천성 면역반응을 매개하는 신호전달네트워크가 정교하게 조절되는 현상을 규명했다.
김은하 박사과정이 제1저자로 참여한 이번 연구 결과는 서울대학교 성노현 교수 연구팀과 공동으로 진행됐고 사이언스 어드밴시스(Science Advances)지 4월 21일자에 게재됐다.
김세윤 교수 연구팀은 이노시톨 대사체 및 생합성 대사를 수 년 간 연구했고 이노시톨 다인산 멀티키나아제 효소(IPMK)에 의한 세포 성장 및 에너지 대사조절 기능을 다각적으로 규명한 바 있다.
이번 연구에서는 대식세포(macrophage) 특이적으로 IPMK 효소가 결핍된 생쥐에서 패혈성 쇼크를 유발시켰을 때 염증수준이 현저히 저하되고 또한 높은 생존율을 보이는 것을 확인했다. 이는 선천성 면역의 핵심인 염증반응이 강력히 저해되는 것을 의미한다.
IPMK 효소가 면역신호조절물질인 TRAF6 단백질과 직접 결합해 TRAF6 단백질의 분해를 조절하는 유비퀴틴화를 억제함을 규명했고, IPMK효소와 TRAF6단백질간 결합력을 저해할 수 있는 펩타이드를 활용함으로써 내독소에 의한 염증반응을 낮출 수 있음을 다각적으로 검증했다.
이번 연구는 미생물 감염 등에 의한 패혈증 발병의 원리를 규명함과 동시에 최근 급증하는 선천 면역 질환 (ex. 신경계 염증질환 및 당뇨)에 대한 이해를 넓히고 새로운 치료기술개발에 필요한 학문적 토대를 제공했다는 의의를 갖는다.
이번 연구는 미래창조과학부 뇌과학원천기술개발사업의 지원을 받아 이뤄졌다.
□ 그림 설명
그림1. IPMK 효소의 선천성 면역조절 모식도
2017.04.25
조회수 16178
-
 기계공학과 학부팀, 휠체어 전동장치로 혁신설계경연대회 우승
〈 수상자 이현주 권도훈 정종호 도학기 학생 〉
우리 대학 기계공학과 학부생 팀이 지난 12일부터 이틀간 일본 오사카에서 열린 아시아 디자인 엔지니어링 워크숍(Asia Design Engineering Workshop : A-DEWS)의 혁신설계경연대회(IDC)에서 우승을 차지했다.
혁신설계경연대회는 혁신적인 제품 및 서비스를 창조하는 엔지니어와 학생들을 응원하기 위해 진행된 행사이다.
한국, 일본, 대만, 말레이시아 등 학부생 또는 대학원생으로 구성된 총 10팀이 참가했고 KAIST 기계공학과 학부생 팀은 우승에 해당하는 혁신설계디자인상을 수상했다.
우리 대학은 ‘창의적 시스템 구현’이라는 과목을 수강하는 학부생 권도훈, 김태현, 도학기, 이현주, 정종호(지도교수 최세범, 조교 정호진) 학생으로 구성됐다.
우리 대학 팀은 수동 휠체어를 위한 탈부착 전동 주행 보조기(Safe Attachable Wheelchair Assistive Device in Capstone Design : SAWADiCap)’를 제작했다. 수동 휠체어에 탈부착이 가능한 동력 전달장치를 설치하는 기술로 전동 휠체어에 비해 훨씬 저렴하고 기존의 탈부착 장치보다 작동 및 설치가 쉽다.
연구팀은 자기 강화효과를 이용한 구동력 향상과 장착 과정 시 사용자의 안전을 고려한 설계를 강점으로 내세워 발표를 진행했다.
권도훈 학생은 “규모가 큰 대회는 아니었지만 처음으로 국제학회에 참석해 다양한 분야의 사람들과 연구를 만나는 귀중한 경험이었고 우승까지 하게 돼 매우 기쁘다”고 말했다.
최세범 지도교수는 “학생들이 견문을 넓히고 자신감을 갖게 돼 기쁘다”며 “경제적으로 힘든 장애인들에게 초저가의 휠체어 전동 장치를 보급해 활동성을 높이는 데 실질적인 도움이 되고 싶다”고 말했다.
2000년에 시작돼 올해로 16회를 맞는 아시아 디자인 엔지니어링 워크숍은 국제설계협회 아시아 지부가 주최한다. 올해는 일본 기계학회(JSME)와 오사카 대학의 주관으로 개최됐다. 최근의 연구 결과 및 경향을 공유할 수 있으며 설계 엔지니어링 분야의 연구원과 실무자를 위한 국제 포럼이다.
기계공학과 학부팀, 휠체어 전동장치로 혁신설계경연대회 우승
〈 수상자 이현주 권도훈 정종호 도학기 학생 〉
우리 대학 기계공학과 학부생 팀이 지난 12일부터 이틀간 일본 오사카에서 열린 아시아 디자인 엔지니어링 워크숍(Asia Design Engineering Workshop : A-DEWS)의 혁신설계경연대회(IDC)에서 우승을 차지했다.
혁신설계경연대회는 혁신적인 제품 및 서비스를 창조하는 엔지니어와 학생들을 응원하기 위해 진행된 행사이다.
한국, 일본, 대만, 말레이시아 등 학부생 또는 대학원생으로 구성된 총 10팀이 참가했고 KAIST 기계공학과 학부생 팀은 우승에 해당하는 혁신설계디자인상을 수상했다.
우리 대학은 ‘창의적 시스템 구현’이라는 과목을 수강하는 학부생 권도훈, 김태현, 도학기, 이현주, 정종호(지도교수 최세범, 조교 정호진) 학생으로 구성됐다.
우리 대학 팀은 수동 휠체어를 위한 탈부착 전동 주행 보조기(Safe Attachable Wheelchair Assistive Device in Capstone Design : SAWADiCap)’를 제작했다. 수동 휠체어에 탈부착이 가능한 동력 전달장치를 설치하는 기술로 전동 휠체어에 비해 훨씬 저렴하고 기존의 탈부착 장치보다 작동 및 설치가 쉽다.
연구팀은 자기 강화효과를 이용한 구동력 향상과 장착 과정 시 사용자의 안전을 고려한 설계를 강점으로 내세워 발표를 진행했다.
권도훈 학생은 “규모가 큰 대회는 아니었지만 처음으로 국제학회에 참석해 다양한 분야의 사람들과 연구를 만나는 귀중한 경험이었고 우승까지 하게 돼 매우 기쁘다”고 말했다.
최세범 지도교수는 “학생들이 견문을 넓히고 자신감을 갖게 돼 기쁘다”며 “경제적으로 힘든 장애인들에게 초저가의 휠체어 전동 장치를 보급해 활동성을 높이는 데 실질적인 도움이 되고 싶다”고 말했다.
2000년에 시작돼 올해로 16회를 맞는 아시아 디자인 엔지니어링 워크숍은 국제설계협회 아시아 지부가 주최한다. 올해는 일본 기계학회(JSME)와 오사카 대학의 주관으로 개최됐다. 최근의 연구 결과 및 경향을 공유할 수 있으며 설계 엔지니어링 분야의 연구원과 실무자를 위한 국제 포럼이다.
2016.12.27
조회수 13820
-
 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
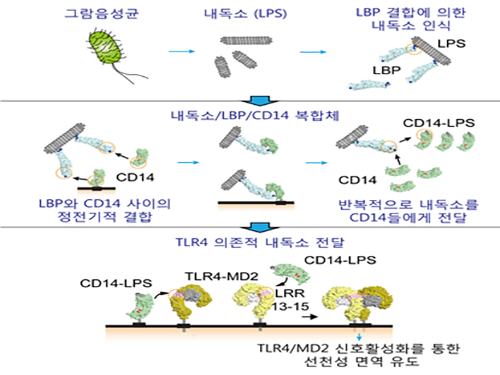
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27
조회수 14732
-
 전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
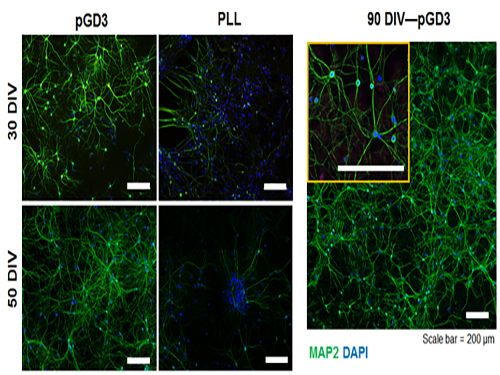
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17
조회수 16735
-
 임우상, 유충국 학생, 2016 구글 PhD 펠로우 선정
〈 임 우 상 학생 〉 〈 유 충 국 학생 〉
우리 대학 전산학부 임우상(지도교수 배두환), 유충국(지도교수 송준화) 박사과정 학생이 2016 구글(Google) PhD 펠로우에 선정됐다.
올해 구글 PhD 펠로우십은 전 세계에서 52명이 선발됐으며 동아시아에서는 6명, 국내 대학에서는 유일하게 우리 대학 학생만이 구글 펠로우에 선정됐다.
구글 PhD 펠로우십은 컴퓨터 과학과 관련된 유망한 연구 분야에서 우수한 활약을 하고 있는 대학원생을 발굴하고 지원하는 프로그램이다.
2009년부터 시작된 이 장학 프로그램은 선정된 학생들에게 1만 달러의 장학금, 구글 각 분야 전문가 멘토들과 일대일 연구 토의 및 피드백 등의 혜택을 제공한다.
임우상 학생은 대규모 행렬(Large-scale Matrix)의 효율적이고 정확한 분해에 관한 연구 성과 및 후속 연구로 기계학습(machine Learning) 분야에서 펠로우로 선정됐다.
기계학습에서 자주 수반되는 PSD (Positive Semi-Definite) 행렬 분해에 대한 오차를 수학적으로 분석해 창의적인 데이터 압축 방법을 제안했고, 이에 기반한 대규모 PSD 행렬 고유분해를 기존 보다 훨씬 높은 효율성으로 정확하게 수행하는 알고리즘을 제안했다.
해당 논문은 기계학습 분야 최고 권위 국제학회 중 하나인 ICML (국제 기계학습 학술대회International Conference on Machine Learning)에 발표됐다. 그 외에도 전국 대학생 수학경시대회 입상, 기계학습 여름학교 (MLSS) 우수 연구 발표자 선정, 국제 기계학습 협회 (IMLS) 에서 장학금 수상 및 우수 국제 학회들에 논문을 출판하면서 활발한 연구 활동을 펼치고 있다.
유충국 학생은 모바일 센서를 활용한 독창적인 서비스 및 지원 시스템에 관한 연구 성과를 인정받아 모바일 컴퓨팅(Mobile Computing) 분야에서 선정됐다.
그는 스마트폰 카메라를 활용한 3차원 공간상에서 물체의 위치를 계산해내는 기술을 개발해 임의의 물체 표면상에서 손가락 상호작용을 가능하게 했다. 이 연구는 IBM 연구소와 공동으로 수행해 인간-컴퓨터 상호작용(CHI) 학회에 발표됐다.
최근에는 군중이 밀집한 환경에서도 정확하고 신속하게 위치를 탐지하는 기술을 개발 중이다. 관련 미국 특허만 5개를 출원하는 등 활발한 연구 활동을 수행하고 있다.
또한 스마트폰을 통해 일상 대화 중 비언어적인 특성을 분석해 언어발달 지체를 겪고 있는 아동을 위한 가족 언어습관 교정 훈련 서비스에 관한 연구도 진행 중이다. 소셜 컴퓨팅 분야 최정상 학회인 CSCW(컴퓨터 기반 협업 및 소셜 컴퓨팅 학술대회)에서 한국 기관 소속으로는 최초로 최우수 논문상을 수상하는 등 연구 독창성을 인정받고 있다.
임우상, 유충국 학생, 2016 구글 PhD 펠로우 선정
〈 임 우 상 학생 〉 〈 유 충 국 학생 〉
우리 대학 전산학부 임우상(지도교수 배두환), 유충국(지도교수 송준화) 박사과정 학생이 2016 구글(Google) PhD 펠로우에 선정됐다.
올해 구글 PhD 펠로우십은 전 세계에서 52명이 선발됐으며 동아시아에서는 6명, 국내 대학에서는 유일하게 우리 대학 학생만이 구글 펠로우에 선정됐다.
구글 PhD 펠로우십은 컴퓨터 과학과 관련된 유망한 연구 분야에서 우수한 활약을 하고 있는 대학원생을 발굴하고 지원하는 프로그램이다.
2009년부터 시작된 이 장학 프로그램은 선정된 학생들에게 1만 달러의 장학금, 구글 각 분야 전문가 멘토들과 일대일 연구 토의 및 피드백 등의 혜택을 제공한다.
임우상 학생은 대규모 행렬(Large-scale Matrix)의 효율적이고 정확한 분해에 관한 연구 성과 및 후속 연구로 기계학습(machine Learning) 분야에서 펠로우로 선정됐다.
기계학습에서 자주 수반되는 PSD (Positive Semi-Definite) 행렬 분해에 대한 오차를 수학적으로 분석해 창의적인 데이터 압축 방법을 제안했고, 이에 기반한 대규모 PSD 행렬 고유분해를 기존 보다 훨씬 높은 효율성으로 정확하게 수행하는 알고리즘을 제안했다.
해당 논문은 기계학습 분야 최고 권위 국제학회 중 하나인 ICML (국제 기계학습 학술대회International Conference on Machine Learning)에 발표됐다. 그 외에도 전국 대학생 수학경시대회 입상, 기계학습 여름학교 (MLSS) 우수 연구 발표자 선정, 국제 기계학습 협회 (IMLS) 에서 장학금 수상 및 우수 국제 학회들에 논문을 출판하면서 활발한 연구 활동을 펼치고 있다.
유충국 학생은 모바일 센서를 활용한 독창적인 서비스 및 지원 시스템에 관한 연구 성과를 인정받아 모바일 컴퓨팅(Mobile Computing) 분야에서 선정됐다.
그는 스마트폰 카메라를 활용한 3차원 공간상에서 물체의 위치를 계산해내는 기술을 개발해 임의의 물체 표면상에서 손가락 상호작용을 가능하게 했다. 이 연구는 IBM 연구소와 공동으로 수행해 인간-컴퓨터 상호작용(CHI) 학회에 발표됐다.
최근에는 군중이 밀집한 환경에서도 정확하고 신속하게 위치를 탐지하는 기술을 개발 중이다. 관련 미국 특허만 5개를 출원하는 등 활발한 연구 활동을 수행하고 있다.
또한 스마트폰을 통해 일상 대화 중 비언어적인 특성을 분석해 언어발달 지체를 겪고 있는 아동을 위한 가족 언어습관 교정 훈련 서비스에 관한 연구도 진행 중이다. 소셜 컴퓨팅 분야 최정상 학회인 CSCW(컴퓨터 기반 협업 및 소셜 컴퓨팅 학술대회)에서 한국 기관 소속으로는 최초로 최우수 논문상을 수상하는 등 연구 독창성을 인정받고 있다.
2016.09.20
조회수 10757
-
 전상용 교수, 황달 유발 물질 이용해 암 표적치료 기술개발
우리 대학 생명과학과 전상용 교수, 이용현 박사 연구팀이 몸속에서 황달을 유발하는 물질인 빌리루빈을 항암약물 전달체로 이용하는 기술을 개발했다.
이 연구는 동물실험에서의 높은 생체적합성과 우수한 항암 효능을 보여 기존 암 치료법의 새로운 대안이 될 것으로 기대된다.
이번 연구 성과는 응용화학분야 학술지 ‘앙케반테 케미(Angewandte chemie)’의 에디터 선정 가장 주목받는 화제의 논문(Hot Paper)으로 선정돼 8월 3일자 온라인 판에 게재됐다.
약물전달시스템은 환부와 정상조직에서의 pH, 활성산소 등의 병태생리학적 차이를 분석해 빛, 자기장, 초음파 등 외부자극을 국소적으로 조사하는 방법이다. 이를 통해 효과적으로 선택적으로 표적에만 약물을 방출할 수 있다.
약물전달시스템은 기존 합성의약품 기반의 항암 치료제에 비해 독성을 크게 낮출 수 있기 때문에 자극감응성 약물전달체에 대한 개발이 활발하게 이뤄지고 있다.
하지만 고분자, 무기 나노입자같은 인공소재 기반의 자극감응성 약물전달체는 공정이 복잡해 상용화가 어렵고, 잠재적 독성을 유발할 가능성이 높다.
연구팀은 문제 해결을 위해 몸속 물질인 빌리루빈을 이용했다. 연구팀은 지난 5월 빌리루빈은 황달을 일으킬 수 있지만 적절하게 조절된다면 심혈관 질환이나 암 발병 가능성이 현저히 낮아져 난치성 염증을 치료할 수 있다는 연구결과를 발표했었다.
빌리루빈은 노란 색소로 혈중 농도가 높아지면 황달의 원인이 된다. 특히 신생아의 경우 간 기능이 미성숙하고 뇌혈관장벽이 미성숙하기 때문에 황달 치료를 위해 추가적 외부요법이 필요하다.
이것이 임상에서 널리 이용되는 광선치료인데 빌리루빈에 빛을 조사하면 친수성(親水性)이 강해져 빌리루빈 조직이 해체되고 배설이 촉진된다. 또한 빌리루빈은 강한 항산화작용 특성을 갖고 있어 빌리루빈이 산화될 때 친수성이 큰 빌리버딘이라는 물질로 전환되거나 작은 빌리루빈 산화물질로 깨져 역시 배설이 촉진된다.
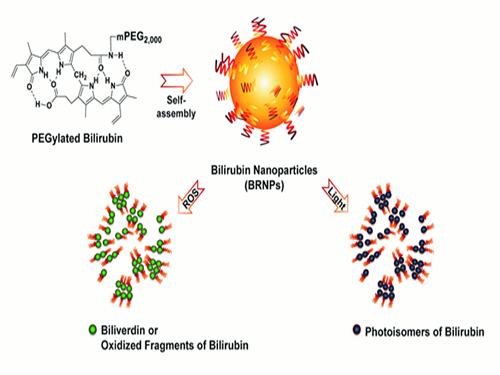
연구팀은 위와 같은 빌리루빈의 특성을 이용했다. 우선 지난 5월의 연구를 토대로 빌리루빈의 배설이 잘 이뤄지도록 친수성을 갖는 물질과 결합시켜 나노입자로 만든 후 항암제인 독소루비신을(Doxorubicin) 선적시켰다.
그 후 암 부위에 빛을 노출시키면 빛에 의해 빌리루빈이 와해돼 선적된 항암제가 암 조직을 공격하는 원리이다.
연구팀은 이 시스템이 인간 폐암 동물모델에서 기존 항암치료 그룹에 비해 우수한 치료 효능을 보이는 것을 규명했다. 빛으로 암 부위를 국소적으로 조사했을 때 더 향상된 치료 효능이 나타났고, 운반체인 빌리루빈 나노입자 자체도 일정량의 항암효과를 나타냄을 확인했다.
이 기술은 최초로 빌리루빈을 활용한 항암치료용 다중자극감응형 약물전달시스템을 개발함으로써 원천기술 확보했다는 의의를 갖는다.
전 교수는 “물체 유래 천연 물질 빌리루빈을 사용해 독성이 없고 간단한 시스템으로 구성된 약물전달시스템을 개발해 상업화에 큰 장점을 가질 것이다”고 말했다.
이용현 박사는 “향후 임상 연구와 적용 가능성을 평가해 궁극적으로 암을 치료하는 새 방안으로 개발되길 기대한다”고 말했다.
이번 연구는 한국연구재단 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 빌리루빈 나노입자가 빛과 활성산소에 의하여 와해됨을 보여주는 결과
그림2. 인간 폐암 동물모델에서 약물이 로딩된 빌리루빈 나노입자가 실제 작용하는 모식도
전상용 교수, 황달 유발 물질 이용해 암 표적치료 기술개발
우리 대학 생명과학과 전상용 교수, 이용현 박사 연구팀이 몸속에서 황달을 유발하는 물질인 빌리루빈을 항암약물 전달체로 이용하는 기술을 개발했다.
이 연구는 동물실험에서의 높은 생체적합성과 우수한 항암 효능을 보여 기존 암 치료법의 새로운 대안이 될 것으로 기대된다.
이번 연구 성과는 응용화학분야 학술지 ‘앙케반테 케미(Angewandte chemie)’의 에디터 선정 가장 주목받는 화제의 논문(Hot Paper)으로 선정돼 8월 3일자 온라인 판에 게재됐다.
약물전달시스템은 환부와 정상조직에서의 pH, 활성산소 등의 병태생리학적 차이를 분석해 빛, 자기장, 초음파 등 외부자극을 국소적으로 조사하는 방법이다. 이를 통해 효과적으로 선택적으로 표적에만 약물을 방출할 수 있다.
약물전달시스템은 기존 합성의약품 기반의 항암 치료제에 비해 독성을 크게 낮출 수 있기 때문에 자극감응성 약물전달체에 대한 개발이 활발하게 이뤄지고 있다.
하지만 고분자, 무기 나노입자같은 인공소재 기반의 자극감응성 약물전달체는 공정이 복잡해 상용화가 어렵고, 잠재적 독성을 유발할 가능성이 높다.
연구팀은 문제 해결을 위해 몸속 물질인 빌리루빈을 이용했다. 연구팀은 지난 5월 빌리루빈은 황달을 일으킬 수 있지만 적절하게 조절된다면 심혈관 질환이나 암 발병 가능성이 현저히 낮아져 난치성 염증을 치료할 수 있다는 연구결과를 발표했었다.
빌리루빈은 노란 색소로 혈중 농도가 높아지면 황달의 원인이 된다. 특히 신생아의 경우 간 기능이 미성숙하고 뇌혈관장벽이 미성숙하기 때문에 황달 치료를 위해 추가적 외부요법이 필요하다.
이것이 임상에서 널리 이용되는 광선치료인데 빌리루빈에 빛을 조사하면 친수성(親水性)이 강해져 빌리루빈 조직이 해체되고 배설이 촉진된다. 또한 빌리루빈은 강한 항산화작용 특성을 갖고 있어 빌리루빈이 산화될 때 친수성이 큰 빌리버딘이라는 물질로 전환되거나 작은 빌리루빈 산화물질로 깨져 역시 배설이 촉진된다.
연구팀은 위와 같은 빌리루빈의 특성을 이용했다. 우선 지난 5월의 연구를 토대로 빌리루빈의 배설이 잘 이뤄지도록 친수성을 갖는 물질과 결합시켜 나노입자로 만든 후 항암제인 독소루비신을(Doxorubicin) 선적시켰다.
그 후 암 부위에 빛을 노출시키면 빛에 의해 빌리루빈이 와해돼 선적된 항암제가 암 조직을 공격하는 원리이다.
연구팀은 이 시스템이 인간 폐암 동물모델에서 기존 항암치료 그룹에 비해 우수한 치료 효능을 보이는 것을 규명했다. 빛으로 암 부위를 국소적으로 조사했을 때 더 향상된 치료 효능이 나타났고, 운반체인 빌리루빈 나노입자 자체도 일정량의 항암효과를 나타냄을 확인했다.
이 기술은 최초로 빌리루빈을 활용한 항암치료용 다중자극감응형 약물전달시스템을 개발함으로써 원천기술 확보했다는 의의를 갖는다.
전 교수는 “물체 유래 천연 물질 빌리루빈을 사용해 독성이 없고 간단한 시스템으로 구성된 약물전달시스템을 개발해 상업화에 큰 장점을 가질 것이다”고 말했다.
이용현 박사는 “향후 임상 연구와 적용 가능성을 평가해 궁극적으로 암을 치료하는 새 방안으로 개발되길 기대한다”고 말했다.
이번 연구는 한국연구재단 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 빌리루빈 나노입자가 빛과 활성산소에 의하여 와해됨을 보여주는 결과
그림2. 인간 폐암 동물모델에서 약물이 로딩된 빌리루빈 나노입자가 실제 작용하는 모식도
2016.08.18
조회수 13081
-
 최철희, 최경선 교수, 빛을 이용한 치료용 단백질 전달시스템 개발
우리 대학 바이오및뇌공학과 최철희 교수, 최경선 교수 공동 연구팀이 빛을 이용해 치료용 단백질을 체내로 정확하고 안전하게 전달할 수 있는 기술을 개발했다.
이는 체내 세포에서 자연적으로 생산되는 나노입자인 엑소솜과 단백질 약물이 빛을 받으면 자석처럼 서로 결합하는 기술로 우수한 기능과 안전성이 확보됐다는 의의를 갖는다.
이번 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communicaitons)’ 7월 22일자 온라인 판에 게재됐다.
최근 바이오 신약의 중요성이 커지면서 바이오 신약의 대부분을 차지하는 단백질 의약을 효과적으로 신체 내 표적 세포에 전달할 수 있는 약물전달시스템 개발이 활발히 이뤄지고 있다.
특히 나노입자는 그 특성 상 종양으로 더 많은 양이 침투할 수 있다는 장점이 있다. 따라서 새로운 물리, 화학 및 광학적 특성을 갖는 나노소재의 입자를 이용해 단백질 등의 바이오 신약을 전달하려는 시도가 진행 중이다.
하지만 현재 기술은 표적 세포에 이르기까지 생체 단백질 활성을 유지시키기 어렵고 면역 반응의 발생을 억제시켜야 하는 문제 등의 한계를 갖는다. 또한 치료용 단백질은 그 크기가 매우 커 기존 방법으로는 실용화가 매우 어렵다. 무엇보다도 가장 큰 문제는 독성 발생 가능성 등 인체 안전성이 해결되지 않았다는 않다는 점이다.
연구팀은 문제 해결을 위해 인간의 세포에서 자연적으로 발생하는 나노입자인 엑소솜(세포외 소낭)을 단백질 약물의 운송 수단으로 사용했고, 빛을 받으면 서로 결합하는 특징을 갖는 CRY2와 CIBN 단백질(CRY2, CIBN : 애기식물장대에서 유래한 서로 결합하는 특성을 갖는 단백질)을 이용했다.
엑소솜에는 CIBN을, 단백질 약물에는 CRY2를 융합시킨 뒤 450~490nm 파장의 푸른빛을 쏘면 CIBN과 CRY의 결합하는 특성으로 인해 자연스럽게 엑소솜에 단백질 약물의 탑재가 유도된다.
이 기술은 기존의 수동적인 탑재에 비해 두 가지 장점을 갖는다. 우선 세포 바깥에서 정제된 단백질을 엑소솜에 넣는 기술에 비해 치료용 단백질의 적재율이 천배 가까이 높아졌다. 그리고 단백질을 정제할 필요가 없어져 효율성, 성공률은 높아지고 비용은 적어진다.
연구팀은 기존보다 낮은 비용으로 보다 쉽게 치료용 단백질이 탑재된 엑소솜을 생산하면서 효율 및 안정성이 향상된 치료용 단백질 전달시스템을 개발했다.
이 기술은 기존 단백질 약물이 세포 외부에서만 작용한다는 한계를 극복함으로써 향후 바이오의약 분야의 새로운 패러다임을 제시하는 원천 기술이 될 것으로 기대된다.
연구팀은 현재 다양한 난치성 질환 치료를 위한 표적 단백질이 탑재된 치료용 엑소솜을 개발 중이며 효능 및 임상 적용 가능성을 검증하고 있다.
최철희 교수는 “이번 기술은 생체에서 만들어지는 나노입자인 엑소솜에 치료용 단백질을 효율적으로 탑재시켰다”며 “안전하고 기능이 우수한 단백질 약물을 대량 생산할 수 있는 획기적인 원천기술이다”고 말했다.
이 기술은 KAIST 교원창업기업인 ㈜셀렉스라이프사이언스 사에 기술이전 돼 엑소솜 약물 제조 기술의 최적화 및 전, 임상 시험을 위한 개발 단계 중이다.
□ 그림 설명
그림1. 엑소솜 내부에 치료용 단백질이 함유된 것을 묘사한 개념도
그림2. 개발한 기술의 개념도
최철희, 최경선 교수, 빛을 이용한 치료용 단백질 전달시스템 개발
우리 대학 바이오및뇌공학과 최철희 교수, 최경선 교수 공동 연구팀이 빛을 이용해 치료용 단백질을 체내로 정확하고 안전하게 전달할 수 있는 기술을 개발했다.
이는 체내 세포에서 자연적으로 생산되는 나노입자인 엑소솜과 단백질 약물이 빛을 받으면 자석처럼 서로 결합하는 기술로 우수한 기능과 안전성이 확보됐다는 의의를 갖는다.
이번 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communicaitons)’ 7월 22일자 온라인 판에 게재됐다.
최근 바이오 신약의 중요성이 커지면서 바이오 신약의 대부분을 차지하는 단백질 의약을 효과적으로 신체 내 표적 세포에 전달할 수 있는 약물전달시스템 개발이 활발히 이뤄지고 있다.
특히 나노입자는 그 특성 상 종양으로 더 많은 양이 침투할 수 있다는 장점이 있다. 따라서 새로운 물리, 화학 및 광학적 특성을 갖는 나노소재의 입자를 이용해 단백질 등의 바이오 신약을 전달하려는 시도가 진행 중이다.
하지만 현재 기술은 표적 세포에 이르기까지 생체 단백질 활성을 유지시키기 어렵고 면역 반응의 발생을 억제시켜야 하는 문제 등의 한계를 갖는다. 또한 치료용 단백질은 그 크기가 매우 커 기존 방법으로는 실용화가 매우 어렵다. 무엇보다도 가장 큰 문제는 독성 발생 가능성 등 인체 안전성이 해결되지 않았다는 않다는 점이다.
연구팀은 문제 해결을 위해 인간의 세포에서 자연적으로 발생하는 나노입자인 엑소솜(세포외 소낭)을 단백질 약물의 운송 수단으로 사용했고, 빛을 받으면 서로 결합하는 특징을 갖는 CRY2와 CIBN 단백질(CRY2, CIBN : 애기식물장대에서 유래한 서로 결합하는 특성을 갖는 단백질)을 이용했다.
엑소솜에는 CIBN을, 단백질 약물에는 CRY2를 융합시킨 뒤 450~490nm 파장의 푸른빛을 쏘면 CIBN과 CRY의 결합하는 특성으로 인해 자연스럽게 엑소솜에 단백질 약물의 탑재가 유도된다.
이 기술은 기존의 수동적인 탑재에 비해 두 가지 장점을 갖는다. 우선 세포 바깥에서 정제된 단백질을 엑소솜에 넣는 기술에 비해 치료용 단백질의 적재율이 천배 가까이 높아졌다. 그리고 단백질을 정제할 필요가 없어져 효율성, 성공률은 높아지고 비용은 적어진다.
연구팀은 기존보다 낮은 비용으로 보다 쉽게 치료용 단백질이 탑재된 엑소솜을 생산하면서 효율 및 안정성이 향상된 치료용 단백질 전달시스템을 개발했다.
이 기술은 기존 단백질 약물이 세포 외부에서만 작용한다는 한계를 극복함으로써 향후 바이오의약 분야의 새로운 패러다임을 제시하는 원천 기술이 될 것으로 기대된다.
연구팀은 현재 다양한 난치성 질환 치료를 위한 표적 단백질이 탑재된 치료용 엑소솜을 개발 중이며 효능 및 임상 적용 가능성을 검증하고 있다.
최철희 교수는 “이번 기술은 생체에서 만들어지는 나노입자인 엑소솜에 치료용 단백질을 효율적으로 탑재시켰다”며 “안전하고 기능이 우수한 단백질 약물을 대량 생산할 수 있는 획기적인 원천기술이다”고 말했다.
이 기술은 KAIST 교원창업기업인 ㈜셀렉스라이프사이언스 사에 기술이전 돼 엑소솜 약물 제조 기술의 최적화 및 전, 임상 시험을 위한 개발 단계 중이다.
□ 그림 설명
그림1. 엑소솜 내부에 치료용 단백질이 함유된 것을 묘사한 개념도
그림2. 개발한 기술의 개념도
2016.08.09
조회수 11647
-
 백승욱 교수, 국제 복사 열전달 학회 기여업적상 수상
〈 백 승 욱 교수 〉
우리 대학 항공우주공학과 백승욱 교수가 지난 6월 9일 터키 카파도키아에서 열린 국제 복사 열전달 학회에서 기여업적상(Achievement award of the significant contribution to radiation transfer)을 수상했다.
국제 복사 연전달 학회는 전 세계 연구자들이 복사 열전달 분야의 연구 결과를 발표하고 토론하는 국제 학회이다.
국제 열‧물질 전달센터(ICHMT)가 주최하는 이 학회는 1968년 시작돼 지금까지 이어지고 있으며 열 및 물질 전달을 연구하는 과학자와 공학자들이 모여 우수한 성과를 사회에 환원하기 위한 다양한 노력을 수행한다.
기여업적상은 국제 복사 열전달 학회에서 관련 분야의 전체 연구자를 대상으로 연구 활동의 파급력, 학계 발전 기여도, 후학 양성 등을 종합해 4년에 한 번 수상자를 배출한다.
백 교수는 1985년 우리 대학에 부임 후 30년 간 국제학술지 논문 150편, 국제학회 논문 176편, 국내학술지 논문 100편, 국내학회 논문 136편을 발표했다. 이를 통해 복사 열전달 분야의 연구 역량과 수준을 높이면서 외연확장을 위한 선도적 역할을 수행한 공을 인정받았다.
백 교수의 주요 연구주제로는 고체 입자 또는 기체가 복사 특성에 미치는 영향, 재연소 과정에서의 복사 열전달, 복사에 의한 점화 및 화염 확산 과정 등이 있고, 역해석 기법을 활용한 복사 열전달 연구로 양질의 논문을 발표했다.
이번 학회에서는 ‘연소 현상의 열복사 특성’이라는 제목으로 지금까지의 연구 성과를 발표하는 기조 연설자로도 선정됐다.
백승욱 교수, 국제 복사 열전달 학회 기여업적상 수상
〈 백 승 욱 교수 〉
우리 대학 항공우주공학과 백승욱 교수가 지난 6월 9일 터키 카파도키아에서 열린 국제 복사 열전달 학회에서 기여업적상(Achievement award of the significant contribution to radiation transfer)을 수상했다.
국제 복사 연전달 학회는 전 세계 연구자들이 복사 열전달 분야의 연구 결과를 발표하고 토론하는 국제 학회이다.
국제 열‧물질 전달센터(ICHMT)가 주최하는 이 학회는 1968년 시작돼 지금까지 이어지고 있으며 열 및 물질 전달을 연구하는 과학자와 공학자들이 모여 우수한 성과를 사회에 환원하기 위한 다양한 노력을 수행한다.
기여업적상은 국제 복사 열전달 학회에서 관련 분야의 전체 연구자를 대상으로 연구 활동의 파급력, 학계 발전 기여도, 후학 양성 등을 종합해 4년에 한 번 수상자를 배출한다.
백 교수는 1985년 우리 대학에 부임 후 30년 간 국제학술지 논문 150편, 국제학회 논문 176편, 국내학술지 논문 100편, 국내학회 논문 136편을 발표했다. 이를 통해 복사 열전달 분야의 연구 역량과 수준을 높이면서 외연확장을 위한 선도적 역할을 수행한 공을 인정받았다.
백 교수의 주요 연구주제로는 고체 입자 또는 기체가 복사 특성에 미치는 영향, 재연소 과정에서의 복사 열전달, 복사에 의한 점화 및 화염 확산 과정 등이 있고, 역해석 기법을 활용한 복사 열전달 연구로 양질의 논문을 발표했다.
이번 학회에서는 ‘연소 현상의 열복사 특성’이라는 제목으로 지금까지의 연구 성과를 발표하는 기조 연설자로도 선정됐다.
2016.07.07
조회수 9122
-
 최광욱 교수, 신체 세포조직의 성장 원리 규명
우리 대학 생명과학과 최광욱 교수 연구팀이 신호전달체계에 존재하는 ‘14-3-3’ 단백질이 신체 기관 발달 및 세포 조직 성장에 새롭게 관여함을 규명했다.
이번 연구는 네이처의 자매지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 6일자 온라인 판에 게재됐다. (논문명: 14-3-3 proteins regulate Tctp-Rheb interaction for organ growth in Drosophila)
우리 신체에는 토르 신호(Tor signaling)라고 불리는 신호전달체계가 존재한다. 이 신호전달체계는 단백질 합성을 늘려 세포 크기를 키우거나 세포 숫자를 늘리는 역할을 한다. 토르 신호가 너무 많으면 암을 유발하기도 하고, 반대로 너무 적으면 신체 기관이 제대로 성장을 할 수 없게 된다.
이와 같이 토르 신호는 세포 조직의 성장과 밀접한 관련이 있다. 이 토르 신호를 조절하는데 Tctp(Translationally controlled tumor protein)와 Rheb 단백질이중요한 역할을 한다.
최 교수 연구팀은 과거 연구에서 토르 신호전달체계에서 Tctp 단백질이 Rheb 단백질의 기능 조절에 영향을 끼친다는 것을 밝혔다. 하지만 Tctp와 Rheb이 어떤 방식으로 조절되는지, 중간에 어떤 매개체가 필요한지 등은 밝혀내지 못했다.
연구팀은 문제를 해결하기 위해 초파리를 이용한 유전적 상호작용 분석 실험을 수행했다. 그리고 14-3-3 단백질이 Tctp와 Rheb 사이의 다리 역할을 해 두 단백질이 상호작용할 수 있음을 밝혔다.
초파리 체내에는 두 개의 14-3-3 동종형 유전자가 존재한다. 따라서 두 개 중 하나가 없어도 현저한 성장 장애는 나타나지 않는다. 그러나 연구팀은 Tctp 또는 Rheb의 기능이 부분적으로 손상된 상태에서 14-3-3의 결핍이 발생하면 기관 성장에 심각한 문제가 생기는 것을 확인했다.
이러한 상승효과의 원리를 통해 14-3-3 단백질이 Tctp와 Rheb 단백질 사이의 결합을 직접적으로 조절해 성장에 관여함을 규명했다.
이번 연구에 기초해 향후 고등 동물에서도 유사한 조절 기작이 존재하는지 확인하기 위한 연구가 진행될 것으로 예상된다. 고등 동물에서의 연구도 성공적으로 이뤄진다면 향후 암 조직의 조절이나 기관 발달 촉진 등의 효과도 얻을 수 있을 것으로 기대된다.
연구팀은 14-3-3 유전자가 초파리 뿐 아니라 인체에도 존재하기 때문에 토르 신호전달체계의 문제로 인한 종양의 원인 규명 및 치료법 예방에 중요한 역할을 할 것으로 전망했다.
최 교수는 “인체에는 유전자 중복으로 인해 기능이 밝혀지지 않은 질병 관련 유전자들이 많다”며 “초파리 모델 동물이 질병 관련 유전자들의 생체 내 작용을 규명하는 데 기여할 것이다”고 말했다.
생명과학과 르 풍 타오 학생이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
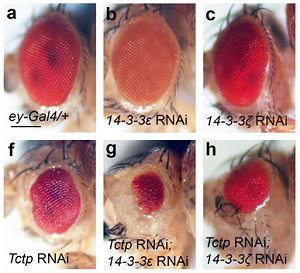
□ 사진 설명
사진1. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 눈이 소실된 사진
사진2. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 날개가 소실된 그림
사진3. 14-3-3 결핍으로 인한 초파리의 두뇌부가 상실된 사진
최광욱 교수, 신체 세포조직의 성장 원리 규명
우리 대학 생명과학과 최광욱 교수 연구팀이 신호전달체계에 존재하는 ‘14-3-3’ 단백질이 신체 기관 발달 및 세포 조직 성장에 새롭게 관여함을 규명했다.
이번 연구는 네이처의 자매지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 6일자 온라인 판에 게재됐다. (논문명: 14-3-3 proteins regulate Tctp-Rheb interaction for organ growth in Drosophila)
우리 신체에는 토르 신호(Tor signaling)라고 불리는 신호전달체계가 존재한다. 이 신호전달체계는 단백질 합성을 늘려 세포 크기를 키우거나 세포 숫자를 늘리는 역할을 한다. 토르 신호가 너무 많으면 암을 유발하기도 하고, 반대로 너무 적으면 신체 기관이 제대로 성장을 할 수 없게 된다.
이와 같이 토르 신호는 세포 조직의 성장과 밀접한 관련이 있다. 이 토르 신호를 조절하는데 Tctp(Translationally controlled tumor protein)와 Rheb 단백질이중요한 역할을 한다.
최 교수 연구팀은 과거 연구에서 토르 신호전달체계에서 Tctp 단백질이 Rheb 단백질의 기능 조절에 영향을 끼친다는 것을 밝혔다. 하지만 Tctp와 Rheb이 어떤 방식으로 조절되는지, 중간에 어떤 매개체가 필요한지 등은 밝혀내지 못했다.
연구팀은 문제를 해결하기 위해 초파리를 이용한 유전적 상호작용 분석 실험을 수행했다. 그리고 14-3-3 단백질이 Tctp와 Rheb 사이의 다리 역할을 해 두 단백질이 상호작용할 수 있음을 밝혔다.
초파리 체내에는 두 개의 14-3-3 동종형 유전자가 존재한다. 따라서 두 개 중 하나가 없어도 현저한 성장 장애는 나타나지 않는다. 그러나 연구팀은 Tctp 또는 Rheb의 기능이 부분적으로 손상된 상태에서 14-3-3의 결핍이 발생하면 기관 성장에 심각한 문제가 생기는 것을 확인했다.
이러한 상승효과의 원리를 통해 14-3-3 단백질이 Tctp와 Rheb 단백질 사이의 결합을 직접적으로 조절해 성장에 관여함을 규명했다.
이번 연구에 기초해 향후 고등 동물에서도 유사한 조절 기작이 존재하는지 확인하기 위한 연구가 진행될 것으로 예상된다. 고등 동물에서의 연구도 성공적으로 이뤄진다면 향후 암 조직의 조절이나 기관 발달 촉진 등의 효과도 얻을 수 있을 것으로 기대된다.
연구팀은 14-3-3 유전자가 초파리 뿐 아니라 인체에도 존재하기 때문에 토르 신호전달체계의 문제로 인한 종양의 원인 규명 및 치료법 예방에 중요한 역할을 할 것으로 전망했다.
최 교수는 “인체에는 유전자 중복으로 인해 기능이 밝혀지지 않은 질병 관련 유전자들이 많다”며 “초파리 모델 동물이 질병 관련 유전자들의 생체 내 작용을 규명하는 데 기여할 것이다”고 말했다.
생명과학과 르 풍 타오 학생이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 사진 설명
사진1. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 눈이 소실된 사진
사진2. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 날개가 소실된 그림
사진3. 14-3-3 결핍으로 인한 초파리의 두뇌부가 상실된 사진
2016.05.18
조회수 11396
 김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
2017.07.11 조회수 14075
김호민 교수, 뇌의 시냅스 구조 및 기능 조절 단백질 구조 규명
< 김 호 민 교수 〉
우리 대학 의과학대학원 김호민 교수와 DGIST 고재원 교수 공동 연구팀이 신경세포 연결을 조절하는 핵심단백질인 MDGA1의 3차원 구조를 최초로 규명해 시냅스 발달을 조절하는 원리를 제시했다.
이번 연구 내용은 신경생물학 분야 국제학술지 ‘뉴런(Neuron)’ 6월 21일자 Issue Highlight에 게재됐다.
뇌는 많은 신경세포로 이뤄져 있고 두 신경세포가 연접하면서 형성되는 시냅스라는 구조를 통해 신호를 전달하면서 그 기능을 수행한다.
대표적인 시냅스 접착 단백질로 알려진 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)은 상호작용을 통해 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)의 발달 및 기능을 유지한다.
연구팀은 뉴롤리진(Neuroligin)과 뉴렉신(Neurexin)의 결합을 조절하는 MDGA1의 3차원 구조와 억제성시냅스(inhibitory synapse)의 형성을 저해하는 원리를 최초로 규명했다.
김 교수는 “단백질 구조생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 규명했다는데 의미가 있다”며 “시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해하는 밑거름이 될 것이다. 향후 뇌신경·뇌정신질환 치료제 개발에 활용될 수 있을 것으로 기대된다.”고 말했다.
이번 연구는 미래창조과학부 기초연구지원사업(개인연구)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 시냅스 조절하는 핵심단백질 구조 최초 규명
그림2. 시냅스 단백질 MDGA1에 의해 조절되는 억제성 시냅스 형성 분자 메커니즘
2017.07.11 조회수 14075 항공우주공학과, NASA임무설계대회 최우수상 수상
〈 KAIST 팀 학생들, 왼쪽부터 이주성, 고재열, 최석민, 서종은, 이은광 〉
〈 안재명 지도교수 〉
우리 대학 항공우주공학과 학생 팀이 美 항공우주국(NASA)이 주관하는 항공우주 임무 설계 경연대회인 라스칼(RASCAL : Revolutionary Aerospace Systems Concepts Academic Linkage) 대회에서 달 탐사 시스템 설계 분야 최우수상(Best in Theme Award)을 수상했다.
항공우주공학과 안재명 교수의 지도하에 고재열, 서종은, 이주성, 최석민, 이은광 학생으로 구성된 KAIST 팀은 미국 학교가 반드시 포함돼야 하는 대회 규정에 따라 텍사스 공대(Texas Tech University), 왕립 멜버른 공대(Royal Melbourne Institute of Technology)와 함께 연합 팀으로 출전했다.
연합 팀은 두 차례의 예선을 거쳐 최종 14팀에 선정돼 5월 30일부터 6월 3일까지 플로리다에서 열린 본선에서 발표회를 가졌다. 총 4개 분야 중 ‘장기간 유인 달 탐사를 위한 물자 전송 시스템 설계’ 에 참여한 연합 팀은 해당 부문 1등상을 수상했다.
NASA 주관 하에 2002년부터 개최된 라스칼은 혁신적인 항공우주 시스템 및 임무를 주제로 학생들의 설계 역량을 겨루는 대회로 세계 최고 수준 학교 및 학생들이 참가하고 있다.
올해 대회 분야는 ▲우주인을 위한 경량 체력단련 모듈 설계(Lightweight Exercise Suite) ▲우주인의 선외 활동을 위한 에어록 모듈 설계(Airlock Design) ▲지구저궤도 및 화성에서 사용 가능한 상용 우주인 거주 모듈 설계(Commercially Enabled LEO/Mars Habitable Module) ▲장기간 유인 달 탐사를 위한 물자 전송 시스템 설계(Logistics Delivery System)로 구분된다.
달 탐사를 위해서는 많은 시간과 물자가 필요하다. KAIST 팀은 장기 유인 달 탐사를 위한 우주 물자이동시스템 설계를 위해 작년부터 약 8개월 간 연합 팀과의 회의를 통해 연구를 해왔다.
특히 장기 유인 달 탐사 임무에는 초기 계획 수립 시 예측할 수 없는 돌발 상황이 발생할 수 있다. KAIST 팀은 이와 같은 임무 불확실성에 대응하기 위해 유연성을 극대화하는 시스템과 운용 개념을 도출, 물자 수송에 소요되는 비용 효용성을 극대화했다.
구체적으로 우주선을 기능에 따라 추진 모듈과 배송 모듈로 나누어 설계했고 달 기지의 수요에 맞춰 배송 모듈을 교환할 수 있게 했다. 또한 다양한 출발 지점을 활용했다
항공우주공학과는 시스템 중심적 사고를 기반으로 한 항공 우주 연구에 초점을 맞춰왔고, 이를 통해 첫 참가임에도 NASA 주관 대회에서 우수한 성적을 거둘 수 있었다.
지도를 맡은 안재명 교수는 “멀리 떨어진 국제연합팀을 리드하며 훌륭한 결과를 만든 학생들이 자랑스럽다”며 “학과가 지속적으로 노력한 시스템-설계 중심 교육의 결실이라고 생각하고 향후 설계교육 분야의 국제협력을 통해 양질의 교육과 다양한 기회를 제공하겠다.”고 말했다.
2017.06.20 조회수 16013
항공우주공학과, NASA임무설계대회 최우수상 수상
〈 KAIST 팀 학생들, 왼쪽부터 이주성, 고재열, 최석민, 서종은, 이은광 〉
〈 안재명 지도교수 〉
우리 대학 항공우주공학과 학생 팀이 美 항공우주국(NASA)이 주관하는 항공우주 임무 설계 경연대회인 라스칼(RASCAL : Revolutionary Aerospace Systems Concepts Academic Linkage) 대회에서 달 탐사 시스템 설계 분야 최우수상(Best in Theme Award)을 수상했다.
항공우주공학과 안재명 교수의 지도하에 고재열, 서종은, 이주성, 최석민, 이은광 학생으로 구성된 KAIST 팀은 미국 학교가 반드시 포함돼야 하는 대회 규정에 따라 텍사스 공대(Texas Tech University), 왕립 멜버른 공대(Royal Melbourne Institute of Technology)와 함께 연합 팀으로 출전했다.
연합 팀은 두 차례의 예선을 거쳐 최종 14팀에 선정돼 5월 30일부터 6월 3일까지 플로리다에서 열린 본선에서 발표회를 가졌다. 총 4개 분야 중 ‘장기간 유인 달 탐사를 위한 물자 전송 시스템 설계’ 에 참여한 연합 팀은 해당 부문 1등상을 수상했다.
NASA 주관 하에 2002년부터 개최된 라스칼은 혁신적인 항공우주 시스템 및 임무를 주제로 학생들의 설계 역량을 겨루는 대회로 세계 최고 수준 학교 및 학생들이 참가하고 있다.
올해 대회 분야는 ▲우주인을 위한 경량 체력단련 모듈 설계(Lightweight Exercise Suite) ▲우주인의 선외 활동을 위한 에어록 모듈 설계(Airlock Design) ▲지구저궤도 및 화성에서 사용 가능한 상용 우주인 거주 모듈 설계(Commercially Enabled LEO/Mars Habitable Module) ▲장기간 유인 달 탐사를 위한 물자 전송 시스템 설계(Logistics Delivery System)로 구분된다.
달 탐사를 위해서는 많은 시간과 물자가 필요하다. KAIST 팀은 장기 유인 달 탐사를 위한 우주 물자이동시스템 설계를 위해 작년부터 약 8개월 간 연합 팀과의 회의를 통해 연구를 해왔다.
특히 장기 유인 달 탐사 임무에는 초기 계획 수립 시 예측할 수 없는 돌발 상황이 발생할 수 있다. KAIST 팀은 이와 같은 임무 불확실성에 대응하기 위해 유연성을 극대화하는 시스템과 운용 개념을 도출, 물자 수송에 소요되는 비용 효용성을 극대화했다.
구체적으로 우주선을 기능에 따라 추진 모듈과 배송 모듈로 나누어 설계했고 달 기지의 수요에 맞춰 배송 모듈을 교환할 수 있게 했다. 또한 다양한 출발 지점을 활용했다
항공우주공학과는 시스템 중심적 사고를 기반으로 한 항공 우주 연구에 초점을 맞춰왔고, 이를 통해 첫 참가임에도 NASA 주관 대회에서 우수한 성적을 거둘 수 있었다.
지도를 맡은 안재명 교수는 “멀리 떨어진 국제연합팀을 리드하며 훌륭한 결과를 만든 학생들이 자랑스럽다”며 “학과가 지속적으로 노력한 시스템-설계 중심 교육의 결실이라고 생각하고 향후 설계교육 분야의 국제협력을 통해 양질의 교육과 다양한 기회를 제공하겠다.”고 말했다.
2017.06.20 조회수 16013 국제대학생프로그래밍 대회에서 동메달 수상
〈 한태숙 교수와 참가 학생들 〉
우리 대학 전산학부와 수리과학과 학부생 팀이 국제 대학생 프로그래밍 대회인 ACM ICPC 월드 파이널에서 동메달 및 First Problem Solver 상을 수상했다.
지난 5월 25일 미국 사우스다코다 주 래피드시티에서 열린 제 41회 국제 대학생 프로그래밍 대회는 미국 컴퓨터 협회(ACM)가 주최하고 IBM이 후원한다.
1977년 처음 개최돼 전 세계 대학생을 대상으로 열리는 권위 있는 행사로 지역대회에는 103개국 2천 900여 개 대학에서 총 5만 여 명이 참가했고 본선 대회에서는 400여 명의 대학생들이 경쟁을 벌였다.
대회는 3명이 한 팀이 돼 12문제를 해결하는 방식으로 진행되며 우리 대학에서는 신성용 전산학부 명예교수, 한태숙 교수가 코치를 맡았고, 전산학부 고지훈, 강한필 학생과 수리과학과 이종원 학생이 참가했다.
우리 대학 대표팀은 9위를 기록해 동메달과 3천 달러의 상금을 차지했고 전 참가팀 중에서 처음으로 문제를 풀어 First Problem Solver 상을 수상했다.
자세한 스코어 정보는 https://icpc.baylor.edu/scoreboard/ 를 통해 확인 가능하다.
2017.06.02 조회수 10566
국제대학생프로그래밍 대회에서 동메달 수상
〈 한태숙 교수와 참가 학생들 〉
우리 대학 전산학부와 수리과학과 학부생 팀이 국제 대학생 프로그래밍 대회인 ACM ICPC 월드 파이널에서 동메달 및 First Problem Solver 상을 수상했다.
지난 5월 25일 미국 사우스다코다 주 래피드시티에서 열린 제 41회 국제 대학생 프로그래밍 대회는 미국 컴퓨터 협회(ACM)가 주최하고 IBM이 후원한다.
1977년 처음 개최돼 전 세계 대학생을 대상으로 열리는 권위 있는 행사로 지역대회에는 103개국 2천 900여 개 대학에서 총 5만 여 명이 참가했고 본선 대회에서는 400여 명의 대학생들이 경쟁을 벌였다.
대회는 3명이 한 팀이 돼 12문제를 해결하는 방식으로 진행되며 우리 대학에서는 신성용 전산학부 명예교수, 한태숙 교수가 코치를 맡았고, 전산학부 고지훈, 강한필 학생과 수리과학과 이종원 학생이 참가했다.
우리 대학 대표팀은 9위를 기록해 동메달과 3천 달러의 상금을 차지했고 전 참가팀 중에서 처음으로 문제를 풀어 First Problem Solver 상을 수상했다.
자세한 스코어 정보는 https://icpc.baylor.edu/scoreboard/ 를 통해 확인 가능하다.
2017.06.02 조회수 10566 김세윤 교수, 이노시톨 대사효소에 의한 패혈증 유발 염증전달신호 규명
우리 대학 생명과학과 김세윤 교수 연구팀이 이노시톨 생합성 대사의 핵심효소인 IPMK (Inositol polyphosphate multikinase)에 의해 패혈증 등의 선천성 면역반응을 매개하는 신호전달네트워크가 정교하게 조절되는 현상을 규명했다.
김은하 박사과정이 제1저자로 참여한 이번 연구 결과는 서울대학교 성노현 교수 연구팀과 공동으로 진행됐고 사이언스 어드밴시스(Science Advances)지 4월 21일자에 게재됐다.
김세윤 교수 연구팀은 이노시톨 대사체 및 생합성 대사를 수 년 간 연구했고 이노시톨 다인산 멀티키나아제 효소(IPMK)에 의한 세포 성장 및 에너지 대사조절 기능을 다각적으로 규명한 바 있다.
이번 연구에서는 대식세포(macrophage) 특이적으로 IPMK 효소가 결핍된 생쥐에서 패혈성 쇼크를 유발시켰을 때 염증수준이 현저히 저하되고 또한 높은 생존율을 보이는 것을 확인했다. 이는 선천성 면역의 핵심인 염증반응이 강력히 저해되는 것을 의미한다.
IPMK 효소가 면역신호조절물질인 TRAF6 단백질과 직접 결합해 TRAF6 단백질의 분해를 조절하는 유비퀴틴화를 억제함을 규명했고, IPMK효소와 TRAF6단백질간 결합력을 저해할 수 있는 펩타이드를 활용함으로써 내독소에 의한 염증반응을 낮출 수 있음을 다각적으로 검증했다.
이번 연구는 미생물 감염 등에 의한 패혈증 발병의 원리를 규명함과 동시에 최근 급증하는 선천 면역 질환 (ex. 신경계 염증질환 및 당뇨)에 대한 이해를 넓히고 새로운 치료기술개발에 필요한 학문적 토대를 제공했다는 의의를 갖는다.
이번 연구는 미래창조과학부 뇌과학원천기술개발사업의 지원을 받아 이뤄졌다.
□ 그림 설명
그림1. IPMK 효소의 선천성 면역조절 모식도
2017.04.25 조회수 16178
김세윤 교수, 이노시톨 대사효소에 의한 패혈증 유발 염증전달신호 규명
우리 대학 생명과학과 김세윤 교수 연구팀이 이노시톨 생합성 대사의 핵심효소인 IPMK (Inositol polyphosphate multikinase)에 의해 패혈증 등의 선천성 면역반응을 매개하는 신호전달네트워크가 정교하게 조절되는 현상을 규명했다.
김은하 박사과정이 제1저자로 참여한 이번 연구 결과는 서울대학교 성노현 교수 연구팀과 공동으로 진행됐고 사이언스 어드밴시스(Science Advances)지 4월 21일자에 게재됐다.
김세윤 교수 연구팀은 이노시톨 대사체 및 생합성 대사를 수 년 간 연구했고 이노시톨 다인산 멀티키나아제 효소(IPMK)에 의한 세포 성장 및 에너지 대사조절 기능을 다각적으로 규명한 바 있다.
이번 연구에서는 대식세포(macrophage) 특이적으로 IPMK 효소가 결핍된 생쥐에서 패혈성 쇼크를 유발시켰을 때 염증수준이 현저히 저하되고 또한 높은 생존율을 보이는 것을 확인했다. 이는 선천성 면역의 핵심인 염증반응이 강력히 저해되는 것을 의미한다.
IPMK 효소가 면역신호조절물질인 TRAF6 단백질과 직접 결합해 TRAF6 단백질의 분해를 조절하는 유비퀴틴화를 억제함을 규명했고, IPMK효소와 TRAF6단백질간 결합력을 저해할 수 있는 펩타이드를 활용함으로써 내독소에 의한 염증반응을 낮출 수 있음을 다각적으로 검증했다.
이번 연구는 미생물 감염 등에 의한 패혈증 발병의 원리를 규명함과 동시에 최근 급증하는 선천 면역 질환 (ex. 신경계 염증질환 및 당뇨)에 대한 이해를 넓히고 새로운 치료기술개발에 필요한 학문적 토대를 제공했다는 의의를 갖는다.
이번 연구는 미래창조과학부 뇌과학원천기술개발사업의 지원을 받아 이뤄졌다.
□ 그림 설명
그림1. IPMK 효소의 선천성 면역조절 모식도
2017.04.25 조회수 16178 기계공학과 학부팀, 휠체어 전동장치로 혁신설계경연대회 우승
〈 수상자 이현주 권도훈 정종호 도학기 학생 〉
우리 대학 기계공학과 학부생 팀이 지난 12일부터 이틀간 일본 오사카에서 열린 아시아 디자인 엔지니어링 워크숍(Asia Design Engineering Workshop : A-DEWS)의 혁신설계경연대회(IDC)에서 우승을 차지했다.
혁신설계경연대회는 혁신적인 제품 및 서비스를 창조하는 엔지니어와 학생들을 응원하기 위해 진행된 행사이다.
한국, 일본, 대만, 말레이시아 등 학부생 또는 대학원생으로 구성된 총 10팀이 참가했고 KAIST 기계공학과 학부생 팀은 우승에 해당하는 혁신설계디자인상을 수상했다.
우리 대학은 ‘창의적 시스템 구현’이라는 과목을 수강하는 학부생 권도훈, 김태현, 도학기, 이현주, 정종호(지도교수 최세범, 조교 정호진) 학생으로 구성됐다.
우리 대학 팀은 수동 휠체어를 위한 탈부착 전동 주행 보조기(Safe Attachable Wheelchair Assistive Device in Capstone Design : SAWADiCap)’를 제작했다. 수동 휠체어에 탈부착이 가능한 동력 전달장치를 설치하는 기술로 전동 휠체어에 비해 훨씬 저렴하고 기존의 탈부착 장치보다 작동 및 설치가 쉽다.
연구팀은 자기 강화효과를 이용한 구동력 향상과 장착 과정 시 사용자의 안전을 고려한 설계를 강점으로 내세워 발표를 진행했다.
권도훈 학생은 “규모가 큰 대회는 아니었지만 처음으로 국제학회에 참석해 다양한 분야의 사람들과 연구를 만나는 귀중한 경험이었고 우승까지 하게 돼 매우 기쁘다”고 말했다.
최세범 지도교수는 “학생들이 견문을 넓히고 자신감을 갖게 돼 기쁘다”며 “경제적으로 힘든 장애인들에게 초저가의 휠체어 전동 장치를 보급해 활동성을 높이는 데 실질적인 도움이 되고 싶다”고 말했다.
2000년에 시작돼 올해로 16회를 맞는 아시아 디자인 엔지니어링 워크숍은 국제설계협회 아시아 지부가 주최한다. 올해는 일본 기계학회(JSME)와 오사카 대학의 주관으로 개최됐다. 최근의 연구 결과 및 경향을 공유할 수 있으며 설계 엔지니어링 분야의 연구원과 실무자를 위한 국제 포럼이다.
2016.12.27 조회수 13820
기계공학과 학부팀, 휠체어 전동장치로 혁신설계경연대회 우승
〈 수상자 이현주 권도훈 정종호 도학기 학생 〉
우리 대학 기계공학과 학부생 팀이 지난 12일부터 이틀간 일본 오사카에서 열린 아시아 디자인 엔지니어링 워크숍(Asia Design Engineering Workshop : A-DEWS)의 혁신설계경연대회(IDC)에서 우승을 차지했다.
혁신설계경연대회는 혁신적인 제품 및 서비스를 창조하는 엔지니어와 학생들을 응원하기 위해 진행된 행사이다.
한국, 일본, 대만, 말레이시아 등 학부생 또는 대학원생으로 구성된 총 10팀이 참가했고 KAIST 기계공학과 학부생 팀은 우승에 해당하는 혁신설계디자인상을 수상했다.
우리 대학은 ‘창의적 시스템 구현’이라는 과목을 수강하는 학부생 권도훈, 김태현, 도학기, 이현주, 정종호(지도교수 최세범, 조교 정호진) 학생으로 구성됐다.
우리 대학 팀은 수동 휠체어를 위한 탈부착 전동 주행 보조기(Safe Attachable Wheelchair Assistive Device in Capstone Design : SAWADiCap)’를 제작했다. 수동 휠체어에 탈부착이 가능한 동력 전달장치를 설치하는 기술로 전동 휠체어에 비해 훨씬 저렴하고 기존의 탈부착 장치보다 작동 및 설치가 쉽다.
연구팀은 자기 강화효과를 이용한 구동력 향상과 장착 과정 시 사용자의 안전을 고려한 설계를 강점으로 내세워 발표를 진행했다.
권도훈 학생은 “규모가 큰 대회는 아니었지만 처음으로 국제학회에 참석해 다양한 분야의 사람들과 연구를 만나는 귀중한 경험이었고 우승까지 하게 돼 매우 기쁘다”고 말했다.
최세범 지도교수는 “학생들이 견문을 넓히고 자신감을 갖게 돼 기쁘다”며 “경제적으로 힘든 장애인들에게 초저가의 휠체어 전동 장치를 보급해 활동성을 높이는 데 실질적인 도움이 되고 싶다”고 말했다.
2000년에 시작돼 올해로 16회를 맞는 아시아 디자인 엔지니어링 워크숍은 국제설계협회 아시아 지부가 주최한다. 올해는 일본 기계학회(JSME)와 오사카 대학의 주관으로 개최됐다. 최근의 연구 결과 및 경향을 공유할 수 있으며 설계 엔지니어링 분야의 연구원과 실무자를 위한 국제 포럼이다.
2016.12.27 조회수 13820 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 14732
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 14732 전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 16735
전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 16735 임우상, 유충국 학생, 2016 구글 PhD 펠로우 선정
〈 임 우 상 학생 〉 〈 유 충 국 학생 〉
우리 대학 전산학부 임우상(지도교수 배두환), 유충국(지도교수 송준화) 박사과정 학생이 2016 구글(Google) PhD 펠로우에 선정됐다.
올해 구글 PhD 펠로우십은 전 세계에서 52명이 선발됐으며 동아시아에서는 6명, 국내 대학에서는 유일하게 우리 대학 학생만이 구글 펠로우에 선정됐다.
구글 PhD 펠로우십은 컴퓨터 과학과 관련된 유망한 연구 분야에서 우수한 활약을 하고 있는 대학원생을 발굴하고 지원하는 프로그램이다.
2009년부터 시작된 이 장학 프로그램은 선정된 학생들에게 1만 달러의 장학금, 구글 각 분야 전문가 멘토들과 일대일 연구 토의 및 피드백 등의 혜택을 제공한다.
임우상 학생은 대규모 행렬(Large-scale Matrix)의 효율적이고 정확한 분해에 관한 연구 성과 및 후속 연구로 기계학습(machine Learning) 분야에서 펠로우로 선정됐다.
기계학습에서 자주 수반되는 PSD (Positive Semi-Definite) 행렬 분해에 대한 오차를 수학적으로 분석해 창의적인 데이터 압축 방법을 제안했고, 이에 기반한 대규모 PSD 행렬 고유분해를 기존 보다 훨씬 높은 효율성으로 정확하게 수행하는 알고리즘을 제안했다.
해당 논문은 기계학습 분야 최고 권위 국제학회 중 하나인 ICML (국제 기계학습 학술대회International Conference on Machine Learning)에 발표됐다. 그 외에도 전국 대학생 수학경시대회 입상, 기계학습 여름학교 (MLSS) 우수 연구 발표자 선정, 국제 기계학습 협회 (IMLS) 에서 장학금 수상 및 우수 국제 학회들에 논문을 출판하면서 활발한 연구 활동을 펼치고 있다.
유충국 학생은 모바일 센서를 활용한 독창적인 서비스 및 지원 시스템에 관한 연구 성과를 인정받아 모바일 컴퓨팅(Mobile Computing) 분야에서 선정됐다.
그는 스마트폰 카메라를 활용한 3차원 공간상에서 물체의 위치를 계산해내는 기술을 개발해 임의의 물체 표면상에서 손가락 상호작용을 가능하게 했다. 이 연구는 IBM 연구소와 공동으로 수행해 인간-컴퓨터 상호작용(CHI) 학회에 발표됐다.
최근에는 군중이 밀집한 환경에서도 정확하고 신속하게 위치를 탐지하는 기술을 개발 중이다. 관련 미국 특허만 5개를 출원하는 등 활발한 연구 활동을 수행하고 있다.
또한 스마트폰을 통해 일상 대화 중 비언어적인 특성을 분석해 언어발달 지체를 겪고 있는 아동을 위한 가족 언어습관 교정 훈련 서비스에 관한 연구도 진행 중이다. 소셜 컴퓨팅 분야 최정상 학회인 CSCW(컴퓨터 기반 협업 및 소셜 컴퓨팅 학술대회)에서 한국 기관 소속으로는 최초로 최우수 논문상을 수상하는 등 연구 독창성을 인정받고 있다.
2016.09.20 조회수 10757
임우상, 유충국 학생, 2016 구글 PhD 펠로우 선정
〈 임 우 상 학생 〉 〈 유 충 국 학생 〉
우리 대학 전산학부 임우상(지도교수 배두환), 유충국(지도교수 송준화) 박사과정 학생이 2016 구글(Google) PhD 펠로우에 선정됐다.
올해 구글 PhD 펠로우십은 전 세계에서 52명이 선발됐으며 동아시아에서는 6명, 국내 대학에서는 유일하게 우리 대학 학생만이 구글 펠로우에 선정됐다.
구글 PhD 펠로우십은 컴퓨터 과학과 관련된 유망한 연구 분야에서 우수한 활약을 하고 있는 대학원생을 발굴하고 지원하는 프로그램이다.
2009년부터 시작된 이 장학 프로그램은 선정된 학생들에게 1만 달러의 장학금, 구글 각 분야 전문가 멘토들과 일대일 연구 토의 및 피드백 등의 혜택을 제공한다.
임우상 학생은 대규모 행렬(Large-scale Matrix)의 효율적이고 정확한 분해에 관한 연구 성과 및 후속 연구로 기계학습(machine Learning) 분야에서 펠로우로 선정됐다.
기계학습에서 자주 수반되는 PSD (Positive Semi-Definite) 행렬 분해에 대한 오차를 수학적으로 분석해 창의적인 데이터 압축 방법을 제안했고, 이에 기반한 대규모 PSD 행렬 고유분해를 기존 보다 훨씬 높은 효율성으로 정확하게 수행하는 알고리즘을 제안했다.
해당 논문은 기계학습 분야 최고 권위 국제학회 중 하나인 ICML (국제 기계학습 학술대회International Conference on Machine Learning)에 발표됐다. 그 외에도 전국 대학생 수학경시대회 입상, 기계학습 여름학교 (MLSS) 우수 연구 발표자 선정, 국제 기계학습 협회 (IMLS) 에서 장학금 수상 및 우수 국제 학회들에 논문을 출판하면서 활발한 연구 활동을 펼치고 있다.
유충국 학생은 모바일 센서를 활용한 독창적인 서비스 및 지원 시스템에 관한 연구 성과를 인정받아 모바일 컴퓨팅(Mobile Computing) 분야에서 선정됐다.
그는 스마트폰 카메라를 활용한 3차원 공간상에서 물체의 위치를 계산해내는 기술을 개발해 임의의 물체 표면상에서 손가락 상호작용을 가능하게 했다. 이 연구는 IBM 연구소와 공동으로 수행해 인간-컴퓨터 상호작용(CHI) 학회에 발표됐다.
최근에는 군중이 밀집한 환경에서도 정확하고 신속하게 위치를 탐지하는 기술을 개발 중이다. 관련 미국 특허만 5개를 출원하는 등 활발한 연구 활동을 수행하고 있다.
또한 스마트폰을 통해 일상 대화 중 비언어적인 특성을 분석해 언어발달 지체를 겪고 있는 아동을 위한 가족 언어습관 교정 훈련 서비스에 관한 연구도 진행 중이다. 소셜 컴퓨팅 분야 최정상 학회인 CSCW(컴퓨터 기반 협업 및 소셜 컴퓨팅 학술대회)에서 한국 기관 소속으로는 최초로 최우수 논문상을 수상하는 등 연구 독창성을 인정받고 있다.
2016.09.20 조회수 10757 전상용 교수, 황달 유발 물질 이용해 암 표적치료 기술개발
우리 대학 생명과학과 전상용 교수, 이용현 박사 연구팀이 몸속에서 황달을 유발하는 물질인 빌리루빈을 항암약물 전달체로 이용하는 기술을 개발했다.
이 연구는 동물실험에서의 높은 생체적합성과 우수한 항암 효능을 보여 기존 암 치료법의 새로운 대안이 될 것으로 기대된다.
이번 연구 성과는 응용화학분야 학술지 ‘앙케반테 케미(Angewandte chemie)’의 에디터 선정 가장 주목받는 화제의 논문(Hot Paper)으로 선정돼 8월 3일자 온라인 판에 게재됐다.
약물전달시스템은 환부와 정상조직에서의 pH, 활성산소 등의 병태생리학적 차이를 분석해 빛, 자기장, 초음파 등 외부자극을 국소적으로 조사하는 방법이다. 이를 통해 효과적으로 선택적으로 표적에만 약물을 방출할 수 있다.
약물전달시스템은 기존 합성의약품 기반의 항암 치료제에 비해 독성을 크게 낮출 수 있기 때문에 자극감응성 약물전달체에 대한 개발이 활발하게 이뤄지고 있다.
하지만 고분자, 무기 나노입자같은 인공소재 기반의 자극감응성 약물전달체는 공정이 복잡해 상용화가 어렵고, 잠재적 독성을 유발할 가능성이 높다.
연구팀은 문제 해결을 위해 몸속 물질인 빌리루빈을 이용했다. 연구팀은 지난 5월 빌리루빈은 황달을 일으킬 수 있지만 적절하게 조절된다면 심혈관 질환이나 암 발병 가능성이 현저히 낮아져 난치성 염증을 치료할 수 있다는 연구결과를 발표했었다.
빌리루빈은 노란 색소로 혈중 농도가 높아지면 황달의 원인이 된다. 특히 신생아의 경우 간 기능이 미성숙하고 뇌혈관장벽이 미성숙하기 때문에 황달 치료를 위해 추가적 외부요법이 필요하다.
이것이 임상에서 널리 이용되는 광선치료인데 빌리루빈에 빛을 조사하면 친수성(親水性)이 강해져 빌리루빈 조직이 해체되고 배설이 촉진된다. 또한 빌리루빈은 강한 항산화작용 특성을 갖고 있어 빌리루빈이 산화될 때 친수성이 큰 빌리버딘이라는 물질로 전환되거나 작은 빌리루빈 산화물질로 깨져 역시 배설이 촉진된다.
연구팀은 위와 같은 빌리루빈의 특성을 이용했다. 우선 지난 5월의 연구를 토대로 빌리루빈의 배설이 잘 이뤄지도록 친수성을 갖는 물질과 결합시켜 나노입자로 만든 후 항암제인 독소루비신을(Doxorubicin) 선적시켰다.
그 후 암 부위에 빛을 노출시키면 빛에 의해 빌리루빈이 와해돼 선적된 항암제가 암 조직을 공격하는 원리이다.
연구팀은 이 시스템이 인간 폐암 동물모델에서 기존 항암치료 그룹에 비해 우수한 치료 효능을 보이는 것을 규명했다. 빛으로 암 부위를 국소적으로 조사했을 때 더 향상된 치료 효능이 나타났고, 운반체인 빌리루빈 나노입자 자체도 일정량의 항암효과를 나타냄을 확인했다.
이 기술은 최초로 빌리루빈을 활용한 항암치료용 다중자극감응형 약물전달시스템을 개발함으로써 원천기술 확보했다는 의의를 갖는다.
전 교수는 “물체 유래 천연 물질 빌리루빈을 사용해 독성이 없고 간단한 시스템으로 구성된 약물전달시스템을 개발해 상업화에 큰 장점을 가질 것이다”고 말했다.
이용현 박사는 “향후 임상 연구와 적용 가능성을 평가해 궁극적으로 암을 치료하는 새 방안으로 개발되길 기대한다”고 말했다.
이번 연구는 한국연구재단 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 빌리루빈 나노입자가 빛과 활성산소에 의하여 와해됨을 보여주는 결과
그림2. 인간 폐암 동물모델에서 약물이 로딩된 빌리루빈 나노입자가 실제 작용하는 모식도
2016.08.18 조회수 13081
전상용 교수, 황달 유발 물질 이용해 암 표적치료 기술개발
우리 대학 생명과학과 전상용 교수, 이용현 박사 연구팀이 몸속에서 황달을 유발하는 물질인 빌리루빈을 항암약물 전달체로 이용하는 기술을 개발했다.
이 연구는 동물실험에서의 높은 생체적합성과 우수한 항암 효능을 보여 기존 암 치료법의 새로운 대안이 될 것으로 기대된다.
이번 연구 성과는 응용화학분야 학술지 ‘앙케반테 케미(Angewandte chemie)’의 에디터 선정 가장 주목받는 화제의 논문(Hot Paper)으로 선정돼 8월 3일자 온라인 판에 게재됐다.
약물전달시스템은 환부와 정상조직에서의 pH, 활성산소 등의 병태생리학적 차이를 분석해 빛, 자기장, 초음파 등 외부자극을 국소적으로 조사하는 방법이다. 이를 통해 효과적으로 선택적으로 표적에만 약물을 방출할 수 있다.
약물전달시스템은 기존 합성의약품 기반의 항암 치료제에 비해 독성을 크게 낮출 수 있기 때문에 자극감응성 약물전달체에 대한 개발이 활발하게 이뤄지고 있다.
하지만 고분자, 무기 나노입자같은 인공소재 기반의 자극감응성 약물전달체는 공정이 복잡해 상용화가 어렵고, 잠재적 독성을 유발할 가능성이 높다.
연구팀은 문제 해결을 위해 몸속 물질인 빌리루빈을 이용했다. 연구팀은 지난 5월 빌리루빈은 황달을 일으킬 수 있지만 적절하게 조절된다면 심혈관 질환이나 암 발병 가능성이 현저히 낮아져 난치성 염증을 치료할 수 있다는 연구결과를 발표했었다.
빌리루빈은 노란 색소로 혈중 농도가 높아지면 황달의 원인이 된다. 특히 신생아의 경우 간 기능이 미성숙하고 뇌혈관장벽이 미성숙하기 때문에 황달 치료를 위해 추가적 외부요법이 필요하다.
이것이 임상에서 널리 이용되는 광선치료인데 빌리루빈에 빛을 조사하면 친수성(親水性)이 강해져 빌리루빈 조직이 해체되고 배설이 촉진된다. 또한 빌리루빈은 강한 항산화작용 특성을 갖고 있어 빌리루빈이 산화될 때 친수성이 큰 빌리버딘이라는 물질로 전환되거나 작은 빌리루빈 산화물질로 깨져 역시 배설이 촉진된다.
연구팀은 위와 같은 빌리루빈의 특성을 이용했다. 우선 지난 5월의 연구를 토대로 빌리루빈의 배설이 잘 이뤄지도록 친수성을 갖는 물질과 결합시켜 나노입자로 만든 후 항암제인 독소루비신을(Doxorubicin) 선적시켰다.
그 후 암 부위에 빛을 노출시키면 빛에 의해 빌리루빈이 와해돼 선적된 항암제가 암 조직을 공격하는 원리이다.
연구팀은 이 시스템이 인간 폐암 동물모델에서 기존 항암치료 그룹에 비해 우수한 치료 효능을 보이는 것을 규명했다. 빛으로 암 부위를 국소적으로 조사했을 때 더 향상된 치료 효능이 나타났고, 운반체인 빌리루빈 나노입자 자체도 일정량의 항암효과를 나타냄을 확인했다.
이 기술은 최초로 빌리루빈을 활용한 항암치료용 다중자극감응형 약물전달시스템을 개발함으로써 원천기술 확보했다는 의의를 갖는다.
전 교수는 “물체 유래 천연 물질 빌리루빈을 사용해 독성이 없고 간단한 시스템으로 구성된 약물전달시스템을 개발해 상업화에 큰 장점을 가질 것이다”고 말했다.
이용현 박사는 “향후 임상 연구와 적용 가능성을 평가해 궁극적으로 암을 치료하는 새 방안으로 개발되길 기대한다”고 말했다.
이번 연구는 한국연구재단 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 빌리루빈 나노입자가 빛과 활성산소에 의하여 와해됨을 보여주는 결과
그림2. 인간 폐암 동물모델에서 약물이 로딩된 빌리루빈 나노입자가 실제 작용하는 모식도
2016.08.18 조회수 13081 최철희, 최경선 교수, 빛을 이용한 치료용 단백질 전달시스템 개발
우리 대학 바이오및뇌공학과 최철희 교수, 최경선 교수 공동 연구팀이 빛을 이용해 치료용 단백질을 체내로 정확하고 안전하게 전달할 수 있는 기술을 개발했다.
이는 체내 세포에서 자연적으로 생산되는 나노입자인 엑소솜과 단백질 약물이 빛을 받으면 자석처럼 서로 결합하는 기술로 우수한 기능과 안전성이 확보됐다는 의의를 갖는다.
이번 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communicaitons)’ 7월 22일자 온라인 판에 게재됐다.
최근 바이오 신약의 중요성이 커지면서 바이오 신약의 대부분을 차지하는 단백질 의약을 효과적으로 신체 내 표적 세포에 전달할 수 있는 약물전달시스템 개발이 활발히 이뤄지고 있다.
특히 나노입자는 그 특성 상 종양으로 더 많은 양이 침투할 수 있다는 장점이 있다. 따라서 새로운 물리, 화학 및 광학적 특성을 갖는 나노소재의 입자를 이용해 단백질 등의 바이오 신약을 전달하려는 시도가 진행 중이다.
하지만 현재 기술은 표적 세포에 이르기까지 생체 단백질 활성을 유지시키기 어렵고 면역 반응의 발생을 억제시켜야 하는 문제 등의 한계를 갖는다. 또한 치료용 단백질은 그 크기가 매우 커 기존 방법으로는 실용화가 매우 어렵다. 무엇보다도 가장 큰 문제는 독성 발생 가능성 등 인체 안전성이 해결되지 않았다는 않다는 점이다.
연구팀은 문제 해결을 위해 인간의 세포에서 자연적으로 발생하는 나노입자인 엑소솜(세포외 소낭)을 단백질 약물의 운송 수단으로 사용했고, 빛을 받으면 서로 결합하는 특징을 갖는 CRY2와 CIBN 단백질(CRY2, CIBN : 애기식물장대에서 유래한 서로 결합하는 특성을 갖는 단백질)을 이용했다.
엑소솜에는 CIBN을, 단백질 약물에는 CRY2를 융합시킨 뒤 450~490nm 파장의 푸른빛을 쏘면 CIBN과 CRY의 결합하는 특성으로 인해 자연스럽게 엑소솜에 단백질 약물의 탑재가 유도된다.
이 기술은 기존의 수동적인 탑재에 비해 두 가지 장점을 갖는다. 우선 세포 바깥에서 정제된 단백질을 엑소솜에 넣는 기술에 비해 치료용 단백질의 적재율이 천배 가까이 높아졌다. 그리고 단백질을 정제할 필요가 없어져 효율성, 성공률은 높아지고 비용은 적어진다.
연구팀은 기존보다 낮은 비용으로 보다 쉽게 치료용 단백질이 탑재된 엑소솜을 생산하면서 효율 및 안정성이 향상된 치료용 단백질 전달시스템을 개발했다.
이 기술은 기존 단백질 약물이 세포 외부에서만 작용한다는 한계를 극복함으로써 향후 바이오의약 분야의 새로운 패러다임을 제시하는 원천 기술이 될 것으로 기대된다.
연구팀은 현재 다양한 난치성 질환 치료를 위한 표적 단백질이 탑재된 치료용 엑소솜을 개발 중이며 효능 및 임상 적용 가능성을 검증하고 있다.
최철희 교수는 “이번 기술은 생체에서 만들어지는 나노입자인 엑소솜에 치료용 단백질을 효율적으로 탑재시켰다”며 “안전하고 기능이 우수한 단백질 약물을 대량 생산할 수 있는 획기적인 원천기술이다”고 말했다.
이 기술은 KAIST 교원창업기업인 ㈜셀렉스라이프사이언스 사에 기술이전 돼 엑소솜 약물 제조 기술의 최적화 및 전, 임상 시험을 위한 개발 단계 중이다.
□ 그림 설명
그림1. 엑소솜 내부에 치료용 단백질이 함유된 것을 묘사한 개념도
그림2. 개발한 기술의 개념도
2016.08.09 조회수 11647
최철희, 최경선 교수, 빛을 이용한 치료용 단백질 전달시스템 개발
우리 대학 바이오및뇌공학과 최철희 교수, 최경선 교수 공동 연구팀이 빛을 이용해 치료용 단백질을 체내로 정확하고 안전하게 전달할 수 있는 기술을 개발했다.
이는 체내 세포에서 자연적으로 생산되는 나노입자인 엑소솜과 단백질 약물이 빛을 받으면 자석처럼 서로 결합하는 기술로 우수한 기능과 안전성이 확보됐다는 의의를 갖는다.
이번 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communicaitons)’ 7월 22일자 온라인 판에 게재됐다.
최근 바이오 신약의 중요성이 커지면서 바이오 신약의 대부분을 차지하는 단백질 의약을 효과적으로 신체 내 표적 세포에 전달할 수 있는 약물전달시스템 개발이 활발히 이뤄지고 있다.
특히 나노입자는 그 특성 상 종양으로 더 많은 양이 침투할 수 있다는 장점이 있다. 따라서 새로운 물리, 화학 및 광학적 특성을 갖는 나노소재의 입자를 이용해 단백질 등의 바이오 신약을 전달하려는 시도가 진행 중이다.
하지만 현재 기술은 표적 세포에 이르기까지 생체 단백질 활성을 유지시키기 어렵고 면역 반응의 발생을 억제시켜야 하는 문제 등의 한계를 갖는다. 또한 치료용 단백질은 그 크기가 매우 커 기존 방법으로는 실용화가 매우 어렵다. 무엇보다도 가장 큰 문제는 독성 발생 가능성 등 인체 안전성이 해결되지 않았다는 않다는 점이다.
연구팀은 문제 해결을 위해 인간의 세포에서 자연적으로 발생하는 나노입자인 엑소솜(세포외 소낭)을 단백질 약물의 운송 수단으로 사용했고, 빛을 받으면 서로 결합하는 특징을 갖는 CRY2와 CIBN 단백질(CRY2, CIBN : 애기식물장대에서 유래한 서로 결합하는 특성을 갖는 단백질)을 이용했다.
엑소솜에는 CIBN을, 단백질 약물에는 CRY2를 융합시킨 뒤 450~490nm 파장의 푸른빛을 쏘면 CIBN과 CRY의 결합하는 특성으로 인해 자연스럽게 엑소솜에 단백질 약물의 탑재가 유도된다.
이 기술은 기존의 수동적인 탑재에 비해 두 가지 장점을 갖는다. 우선 세포 바깥에서 정제된 단백질을 엑소솜에 넣는 기술에 비해 치료용 단백질의 적재율이 천배 가까이 높아졌다. 그리고 단백질을 정제할 필요가 없어져 효율성, 성공률은 높아지고 비용은 적어진다.
연구팀은 기존보다 낮은 비용으로 보다 쉽게 치료용 단백질이 탑재된 엑소솜을 생산하면서 효율 및 안정성이 향상된 치료용 단백질 전달시스템을 개발했다.
이 기술은 기존 단백질 약물이 세포 외부에서만 작용한다는 한계를 극복함으로써 향후 바이오의약 분야의 새로운 패러다임을 제시하는 원천 기술이 될 것으로 기대된다.
연구팀은 현재 다양한 난치성 질환 치료를 위한 표적 단백질이 탑재된 치료용 엑소솜을 개발 중이며 효능 및 임상 적용 가능성을 검증하고 있다.
최철희 교수는 “이번 기술은 생체에서 만들어지는 나노입자인 엑소솜에 치료용 단백질을 효율적으로 탑재시켰다”며 “안전하고 기능이 우수한 단백질 약물을 대량 생산할 수 있는 획기적인 원천기술이다”고 말했다.
이 기술은 KAIST 교원창업기업인 ㈜셀렉스라이프사이언스 사에 기술이전 돼 엑소솜 약물 제조 기술의 최적화 및 전, 임상 시험을 위한 개발 단계 중이다.
□ 그림 설명
그림1. 엑소솜 내부에 치료용 단백질이 함유된 것을 묘사한 개념도
그림2. 개발한 기술의 개념도
2016.08.09 조회수 11647 백승욱 교수, 국제 복사 열전달 학회 기여업적상 수상
〈 백 승 욱 교수 〉
우리 대학 항공우주공학과 백승욱 교수가 지난 6월 9일 터키 카파도키아에서 열린 국제 복사 열전달 학회에서 기여업적상(Achievement award of the significant contribution to radiation transfer)을 수상했다.
국제 복사 연전달 학회는 전 세계 연구자들이 복사 열전달 분야의 연구 결과를 발표하고 토론하는 국제 학회이다.
국제 열‧물질 전달센터(ICHMT)가 주최하는 이 학회는 1968년 시작돼 지금까지 이어지고 있으며 열 및 물질 전달을 연구하는 과학자와 공학자들이 모여 우수한 성과를 사회에 환원하기 위한 다양한 노력을 수행한다.
기여업적상은 국제 복사 열전달 학회에서 관련 분야의 전체 연구자를 대상으로 연구 활동의 파급력, 학계 발전 기여도, 후학 양성 등을 종합해 4년에 한 번 수상자를 배출한다.
백 교수는 1985년 우리 대학에 부임 후 30년 간 국제학술지 논문 150편, 국제학회 논문 176편, 국내학술지 논문 100편, 국내학회 논문 136편을 발표했다. 이를 통해 복사 열전달 분야의 연구 역량과 수준을 높이면서 외연확장을 위한 선도적 역할을 수행한 공을 인정받았다.
백 교수의 주요 연구주제로는 고체 입자 또는 기체가 복사 특성에 미치는 영향, 재연소 과정에서의 복사 열전달, 복사에 의한 점화 및 화염 확산 과정 등이 있고, 역해석 기법을 활용한 복사 열전달 연구로 양질의 논문을 발표했다.
이번 학회에서는 ‘연소 현상의 열복사 특성’이라는 제목으로 지금까지의 연구 성과를 발표하는 기조 연설자로도 선정됐다.
2016.07.07 조회수 9122
백승욱 교수, 국제 복사 열전달 학회 기여업적상 수상
〈 백 승 욱 교수 〉
우리 대학 항공우주공학과 백승욱 교수가 지난 6월 9일 터키 카파도키아에서 열린 국제 복사 열전달 학회에서 기여업적상(Achievement award of the significant contribution to radiation transfer)을 수상했다.
국제 복사 연전달 학회는 전 세계 연구자들이 복사 열전달 분야의 연구 결과를 발표하고 토론하는 국제 학회이다.
국제 열‧물질 전달센터(ICHMT)가 주최하는 이 학회는 1968년 시작돼 지금까지 이어지고 있으며 열 및 물질 전달을 연구하는 과학자와 공학자들이 모여 우수한 성과를 사회에 환원하기 위한 다양한 노력을 수행한다.
기여업적상은 국제 복사 열전달 학회에서 관련 분야의 전체 연구자를 대상으로 연구 활동의 파급력, 학계 발전 기여도, 후학 양성 등을 종합해 4년에 한 번 수상자를 배출한다.
백 교수는 1985년 우리 대학에 부임 후 30년 간 국제학술지 논문 150편, 국제학회 논문 176편, 국내학술지 논문 100편, 국내학회 논문 136편을 발표했다. 이를 통해 복사 열전달 분야의 연구 역량과 수준을 높이면서 외연확장을 위한 선도적 역할을 수행한 공을 인정받았다.
백 교수의 주요 연구주제로는 고체 입자 또는 기체가 복사 특성에 미치는 영향, 재연소 과정에서의 복사 열전달, 복사에 의한 점화 및 화염 확산 과정 등이 있고, 역해석 기법을 활용한 복사 열전달 연구로 양질의 논문을 발표했다.
이번 학회에서는 ‘연소 현상의 열복사 특성’이라는 제목으로 지금까지의 연구 성과를 발표하는 기조 연설자로도 선정됐다.
2016.07.07 조회수 9122 최광욱 교수, 신체 세포조직의 성장 원리 규명
우리 대학 생명과학과 최광욱 교수 연구팀이 신호전달체계에 존재하는 ‘14-3-3’ 단백질이 신체 기관 발달 및 세포 조직 성장에 새롭게 관여함을 규명했다.
이번 연구는 네이처의 자매지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 6일자 온라인 판에 게재됐다. (논문명: 14-3-3 proteins regulate Tctp-Rheb interaction for organ growth in Drosophila)
우리 신체에는 토르 신호(Tor signaling)라고 불리는 신호전달체계가 존재한다. 이 신호전달체계는 단백질 합성을 늘려 세포 크기를 키우거나 세포 숫자를 늘리는 역할을 한다. 토르 신호가 너무 많으면 암을 유발하기도 하고, 반대로 너무 적으면 신체 기관이 제대로 성장을 할 수 없게 된다.
이와 같이 토르 신호는 세포 조직의 성장과 밀접한 관련이 있다. 이 토르 신호를 조절하는데 Tctp(Translationally controlled tumor protein)와 Rheb 단백질이중요한 역할을 한다.
최 교수 연구팀은 과거 연구에서 토르 신호전달체계에서 Tctp 단백질이 Rheb 단백질의 기능 조절에 영향을 끼친다는 것을 밝혔다. 하지만 Tctp와 Rheb이 어떤 방식으로 조절되는지, 중간에 어떤 매개체가 필요한지 등은 밝혀내지 못했다.
연구팀은 문제를 해결하기 위해 초파리를 이용한 유전적 상호작용 분석 실험을 수행했다. 그리고 14-3-3 단백질이 Tctp와 Rheb 사이의 다리 역할을 해 두 단백질이 상호작용할 수 있음을 밝혔다.
초파리 체내에는 두 개의 14-3-3 동종형 유전자가 존재한다. 따라서 두 개 중 하나가 없어도 현저한 성장 장애는 나타나지 않는다. 그러나 연구팀은 Tctp 또는 Rheb의 기능이 부분적으로 손상된 상태에서 14-3-3의 결핍이 발생하면 기관 성장에 심각한 문제가 생기는 것을 확인했다.
이러한 상승효과의 원리를 통해 14-3-3 단백질이 Tctp와 Rheb 단백질 사이의 결합을 직접적으로 조절해 성장에 관여함을 규명했다.
이번 연구에 기초해 향후 고등 동물에서도 유사한 조절 기작이 존재하는지 확인하기 위한 연구가 진행될 것으로 예상된다. 고등 동물에서의 연구도 성공적으로 이뤄진다면 향후 암 조직의 조절이나 기관 발달 촉진 등의 효과도 얻을 수 있을 것으로 기대된다.
연구팀은 14-3-3 유전자가 초파리 뿐 아니라 인체에도 존재하기 때문에 토르 신호전달체계의 문제로 인한 종양의 원인 규명 및 치료법 예방에 중요한 역할을 할 것으로 전망했다.
최 교수는 “인체에는 유전자 중복으로 인해 기능이 밝혀지지 않은 질병 관련 유전자들이 많다”며 “초파리 모델 동물이 질병 관련 유전자들의 생체 내 작용을 규명하는 데 기여할 것이다”고 말했다.
생명과학과 르 풍 타오 학생이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 사진 설명
사진1. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 눈이 소실된 사진
사진2. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 날개가 소실된 그림
사진3. 14-3-3 결핍으로 인한 초파리의 두뇌부가 상실된 사진
2016.05.18 조회수 11396
최광욱 교수, 신체 세포조직의 성장 원리 규명
우리 대학 생명과학과 최광욱 교수 연구팀이 신호전달체계에 존재하는 ‘14-3-3’ 단백질이 신체 기관 발달 및 세포 조직 성장에 새롭게 관여함을 규명했다.
이번 연구는 네이처의 자매지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 6일자 온라인 판에 게재됐다. (논문명: 14-3-3 proteins regulate Tctp-Rheb interaction for organ growth in Drosophila)
우리 신체에는 토르 신호(Tor signaling)라고 불리는 신호전달체계가 존재한다. 이 신호전달체계는 단백질 합성을 늘려 세포 크기를 키우거나 세포 숫자를 늘리는 역할을 한다. 토르 신호가 너무 많으면 암을 유발하기도 하고, 반대로 너무 적으면 신체 기관이 제대로 성장을 할 수 없게 된다.
이와 같이 토르 신호는 세포 조직의 성장과 밀접한 관련이 있다. 이 토르 신호를 조절하는데 Tctp(Translationally controlled tumor protein)와 Rheb 단백질이중요한 역할을 한다.
최 교수 연구팀은 과거 연구에서 토르 신호전달체계에서 Tctp 단백질이 Rheb 단백질의 기능 조절에 영향을 끼친다는 것을 밝혔다. 하지만 Tctp와 Rheb이 어떤 방식으로 조절되는지, 중간에 어떤 매개체가 필요한지 등은 밝혀내지 못했다.
연구팀은 문제를 해결하기 위해 초파리를 이용한 유전적 상호작용 분석 실험을 수행했다. 그리고 14-3-3 단백질이 Tctp와 Rheb 사이의 다리 역할을 해 두 단백질이 상호작용할 수 있음을 밝혔다.
초파리 체내에는 두 개의 14-3-3 동종형 유전자가 존재한다. 따라서 두 개 중 하나가 없어도 현저한 성장 장애는 나타나지 않는다. 그러나 연구팀은 Tctp 또는 Rheb의 기능이 부분적으로 손상된 상태에서 14-3-3의 결핍이 발생하면 기관 성장에 심각한 문제가 생기는 것을 확인했다.
이러한 상승효과의 원리를 통해 14-3-3 단백질이 Tctp와 Rheb 단백질 사이의 결합을 직접적으로 조절해 성장에 관여함을 규명했다.
이번 연구에 기초해 향후 고등 동물에서도 유사한 조절 기작이 존재하는지 확인하기 위한 연구가 진행될 것으로 예상된다. 고등 동물에서의 연구도 성공적으로 이뤄진다면 향후 암 조직의 조절이나 기관 발달 촉진 등의 효과도 얻을 수 있을 것으로 기대된다.
연구팀은 14-3-3 유전자가 초파리 뿐 아니라 인체에도 존재하기 때문에 토르 신호전달체계의 문제로 인한 종양의 원인 규명 및 치료법 예방에 중요한 역할을 할 것으로 전망했다.
최 교수는 “인체에는 유전자 중복으로 인해 기능이 밝혀지지 않은 질병 관련 유전자들이 많다”며 “초파리 모델 동물이 질병 관련 유전자들의 생체 내 작용을 규명하는 데 기여할 것이다”고 말했다.
생명과학과 르 풍 타오 학생이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 사진 설명
사진1. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 눈이 소실된 사진
사진2. 14-3-3과 tctp 단백질 결핍으로 인해 초파리 날개가 소실된 그림
사진3. 14-3-3 결핍으로 인한 초파리의 두뇌부가 상실된 사진
2016.05.18 조회수 11396