%EB%8B%A8%EB%B0%B1%EC%A7%88
-
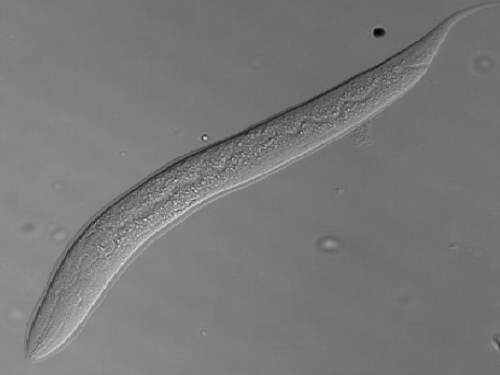 1mm 크기 예쁜꼬마선충에서 노화 늦추는 단백질 찾았다
우리 대학 연구진이 '예쁜꼬마선충'(C. elegans)에서 수명 연장을 돕는 단백질을 찾아냈다.
우리 대학 생명과학과 이승재 교수와 포항공대 김경태 교수 연구팀이 예쁜꼬마선충에서 세포 내 에너지 조절 센서인 'AMPK'를 활성화해 노화를 지연시키는 단백질 'VRK-1'을 발견했다.
예쁜꼬마선충은 몸길이 1㎜ 정도의 선충류다. 배양이 쉽고 사람과 유전 정보 특성이 닮아 실험동물로 널리 활용된다.
한편 에너지 센서라 불리는 AMPK는 공복이나 운동 등으로 에너지 수준이 낮아질 때 활성화돼 세포가 항상성을 유지하도록 돕는다.
예쁜꼬마선충과 생쥐, 초파리 등에서 AMPK가 식이를 제한해 수명 연장을 돕는 역할을 한다는 연구는 그동안 활발히 진행되어 왔지만, AMPK를 자극하는 상위 조절 인자는 알려지지 않았다.
연구팀은 VRK1이 활성화될 때 2만여개의 예쁜꼬마선충 유전자가 단백질로 발현되는 패턴이 AMPK가 활성화될 때의 패턴과 비슷하다는 사실을 발견했다.
VRK1은 AMPK를 인산화시키고, 인산화된 AMPK는 미토콘드리아가 세포에 에너지를 공급하는 데 필수적인 과정인 '전자 전달계'의 기능을 억제함으로써 노화를 늦춘다는 것도 확인했다.
실제 VRK1의 자극에 반응하지 않는 AMPK 돌연변이 예쁜꼬마선충에서는 수명 연장 효과가 나타나지 않았다.
생명과학과 이승재 교수는 "이번 연구 결과는 AMPK 이상으로 인한 대사질환 치료와 항노화 약물 개발에 기여할 것"이라고 말했다.
한편, 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스'(Science Advances) 7월 2일 자에 실렸다.
2020.07.16 조회수 29731
1mm 크기 예쁜꼬마선충에서 노화 늦추는 단백질 찾았다
우리 대학 연구진이 '예쁜꼬마선충'(C. elegans)에서 수명 연장을 돕는 단백질을 찾아냈다.
우리 대학 생명과학과 이승재 교수와 포항공대 김경태 교수 연구팀이 예쁜꼬마선충에서 세포 내 에너지 조절 센서인 'AMPK'를 활성화해 노화를 지연시키는 단백질 'VRK-1'을 발견했다.
예쁜꼬마선충은 몸길이 1㎜ 정도의 선충류다. 배양이 쉽고 사람과 유전 정보 특성이 닮아 실험동물로 널리 활용된다.
한편 에너지 센서라 불리는 AMPK는 공복이나 운동 등으로 에너지 수준이 낮아질 때 활성화돼 세포가 항상성을 유지하도록 돕는다.
예쁜꼬마선충과 생쥐, 초파리 등에서 AMPK가 식이를 제한해 수명 연장을 돕는 역할을 한다는 연구는 그동안 활발히 진행되어 왔지만, AMPK를 자극하는 상위 조절 인자는 알려지지 않았다.
연구팀은 VRK1이 활성화될 때 2만여개의 예쁜꼬마선충 유전자가 단백질로 발현되는 패턴이 AMPK가 활성화될 때의 패턴과 비슷하다는 사실을 발견했다.
VRK1은 AMPK를 인산화시키고, 인산화된 AMPK는 미토콘드리아가 세포에 에너지를 공급하는 데 필수적인 과정인 '전자 전달계'의 기능을 억제함으로써 노화를 늦춘다는 것도 확인했다.
실제 VRK1의 자극에 반응하지 않는 AMPK 돌연변이 예쁜꼬마선충에서는 수명 연장 효과가 나타나지 않았다.
생명과학과 이승재 교수는 "이번 연구 결과는 AMPK 이상으로 인한 대사질환 치료와 항노화 약물 개발에 기여할 것"이라고 말했다.
한편, 이번 연구 결과는 국제 학술지 '사이언스 어드밴시스'(Science Advances) 7월 2일 자에 실렸다.
2020.07.16 조회수 29731 -
 단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
2020.07.09 조회수 26680
단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
2020.07.09 조회수 26680 -
 빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
2020.02.21 조회수 20839
빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
2020.02.21 조회수 20839 -
 허원도 교수, 항체를 빛으로 활성화 시키는 항체광유전학 기술 개발
〈 (좌측부터) 허원도 KAIST 생명과학과 교수, 유다슬이 KAIST 생명과학과 석박통학과정〉
빛으로 면역 반응을 조절할 수 있는 길이 열렸다. 우리대학 생명과학과 허원도 교수 연구팀은 항체를 빛으로 활성화시켜 특정 단백질을 억제하도록 만드는 광유전학 광유전학(Optogenetics) 기술을 개발하였다.
감염이나 질병으로부터 우리 몸을 보호하는 방어 체계를 면역이라고 한다. 항체는 Y자 형태의 단백질로, 면역에서 가장 중요한 역할을 하는 물질 중 하나다. 각설탕보다 가루설탕이 물에 더 잘 녹는 것처럼, 긴 항체보다 짧은 항체 조각이 세포 내에서 더 잘 녹는다. 이런 특징 때문에 항체 조각들은 오래전부터 생물학적 도구나 의약품 재료로 사용되어왔다.
연구진은 빛을 이용해 항체의 활성화를 조절하는 옵토바디(Optobody, Optogenetically activated intracellular antibody) 기술을 개발하였다. 녹색형광단백질(GFP)을 인지하는 가장 작은 항체 조각인 ‘GFP 나노바디’에 청색광을 쬐어주면 재결합되어 활성화됨을 관찰하고, 활성화된 항체 조각이 세포 이동에 관여하는 단백질을 억제함을 확인하였다. 또한 옵토바디 기술을 GFP 나노바디 이외에도 기존에 널리 사용 중인 항체 조각들에 다양하게 적용하였다.
〈 항체 조각과 Optobody 모식도〉
또한 연구진은 화학물질을 이용해 항체의 활성화를 조절하는 케모바디(Chemobody, Chemically activated intracellular antibody) 기술을 추가로 개발하였다. 둘로 쪼개져 있던 항체 조각을 라파마이신(Rapamysin) 으로 재결합시켜 활성화됨을 확인하고, 활성화된 항체 조각이 세포 이동에 관여하는 단백질을 억제하는 것을 관찰하였다.
이번 연구는 항체광유전학 기술을 개발하여, 항체 조각이 쪼개지면 비활성화되고 재결합하면 활성화된다는 것을 밝혔다는 데 의의가 있다. 각각의 단백질은 자신만의 기능을 갖는다. 활성화된 항체가 특정 단백질을 억제했을 때 감소되는 기능을 추적하면, 해당 단백질의 기능을 알 수 있다. 또한 활성화된 항체를 단백질의 실시간 활성 및 이동을 관찰하는 바이오센서로도 이용할 수 있다.
기존의 항체 활성을 조절하는 방법은 화학물질을 이용해 항체의 발현을 유도하는 방법에 국한되어 있었으며, 항체 활성을 정밀하게 조절하기 어려웠다. 이번 연구로 빛을 이용하여 항체 활성을 빠른 시간 내에 시공간적으로 세밀하게 조절하는 것이 가능해졌다. 향후 이 기술은 항체광유전학 분야 및 항체의약품에 크게 응용될 것으로 보인다.
허원도 교수는 “이번 연구로 개발한 항체광유전학기술은 빛으로 세포 내 단백질의 기능을 제어하는 연구에 적용할 수 있고, 더 나아가 앞으로 다양한 질병을 치료하는 항체개발과 차세대 면역항암제 개발에 많이 활용되리라 기대한다”고 말했다.
이번 연구는 기초과학연구원(IBS, 원장 대행 김영덕) 인지 및 사회성 연구단(단장 신희섭, 이창준) 산하에서 시행되었으며 연구결과는 세계적 학술지 네이처 메소드(Nature Methods, IF 28.467)에 10월 15일 0시(한국시간)에 게재되었다.
2019.10.15 조회수 17164
허원도 교수, 항체를 빛으로 활성화 시키는 항체광유전학 기술 개발
〈 (좌측부터) 허원도 KAIST 생명과학과 교수, 유다슬이 KAIST 생명과학과 석박통학과정〉
빛으로 면역 반응을 조절할 수 있는 길이 열렸다. 우리대학 생명과학과 허원도 교수 연구팀은 항체를 빛으로 활성화시켜 특정 단백질을 억제하도록 만드는 광유전학 광유전학(Optogenetics) 기술을 개발하였다.
감염이나 질병으로부터 우리 몸을 보호하는 방어 체계를 면역이라고 한다. 항체는 Y자 형태의 단백질로, 면역에서 가장 중요한 역할을 하는 물질 중 하나다. 각설탕보다 가루설탕이 물에 더 잘 녹는 것처럼, 긴 항체보다 짧은 항체 조각이 세포 내에서 더 잘 녹는다. 이런 특징 때문에 항체 조각들은 오래전부터 생물학적 도구나 의약품 재료로 사용되어왔다.
연구진은 빛을 이용해 항체의 활성화를 조절하는 옵토바디(Optobody, Optogenetically activated intracellular antibody) 기술을 개발하였다. 녹색형광단백질(GFP)을 인지하는 가장 작은 항체 조각인 ‘GFP 나노바디’에 청색광을 쬐어주면 재결합되어 활성화됨을 관찰하고, 활성화된 항체 조각이 세포 이동에 관여하는 단백질을 억제함을 확인하였다. 또한 옵토바디 기술을 GFP 나노바디 이외에도 기존에 널리 사용 중인 항체 조각들에 다양하게 적용하였다.
〈 항체 조각과 Optobody 모식도〉
또한 연구진은 화학물질을 이용해 항체의 활성화를 조절하는 케모바디(Chemobody, Chemically activated intracellular antibody) 기술을 추가로 개발하였다. 둘로 쪼개져 있던 항체 조각을 라파마이신(Rapamysin) 으로 재결합시켜 활성화됨을 확인하고, 활성화된 항체 조각이 세포 이동에 관여하는 단백질을 억제하는 것을 관찰하였다.
이번 연구는 항체광유전학 기술을 개발하여, 항체 조각이 쪼개지면 비활성화되고 재결합하면 활성화된다는 것을 밝혔다는 데 의의가 있다. 각각의 단백질은 자신만의 기능을 갖는다. 활성화된 항체가 특정 단백질을 억제했을 때 감소되는 기능을 추적하면, 해당 단백질의 기능을 알 수 있다. 또한 활성화된 항체를 단백질의 실시간 활성 및 이동을 관찰하는 바이오센서로도 이용할 수 있다.
기존의 항체 활성을 조절하는 방법은 화학물질을 이용해 항체의 발현을 유도하는 방법에 국한되어 있었으며, 항체 활성을 정밀하게 조절하기 어려웠다. 이번 연구로 빛을 이용하여 항체 활성을 빠른 시간 내에 시공간적으로 세밀하게 조절하는 것이 가능해졌다. 향후 이 기술은 항체광유전학 분야 및 항체의약품에 크게 응용될 것으로 보인다.
허원도 교수는 “이번 연구로 개발한 항체광유전학기술은 빛으로 세포 내 단백질의 기능을 제어하는 연구에 적용할 수 있고, 더 나아가 앞으로 다양한 질병을 치료하는 항체개발과 차세대 면역항암제 개발에 많이 활용되리라 기대한다”고 말했다.
이번 연구는 기초과학연구원(IBS, 원장 대행 김영덕) 인지 및 사회성 연구단(단장 신희섭, 이창준) 산하에서 시행되었으며 연구결과는 세계적 학술지 네이처 메소드(Nature Methods, IF 28.467)에 10월 15일 0시(한국시간)에 게재되었다.
2019.10.15 조회수 17164 -
 김진우 교수, 발달과정 세포 간 정보전달 원리 규명
우리 대학 생명과학과 김진우 교수 연구팀이 호메오 단백질의 세포 간 이동으로 인해 세포와 세포 사이에서 정보가 전달될 수 있음을 규명했다.
호메오 단백질은 DNA에 결합하는 능력을 가진 전사인자로, 세포가 어떤 신체부위로 발달할지 운명을 결정하는 역할을 한다고 알려져 있다. 따라서 어떤 호메오 단백질을 가지고 있는지에 따라 동일한 DNA를 가진 세포들의 유전자 발현 양상이 달라져, 뇌·심장·피부 등 상이한 특징을 가지는 신체 기관으로의 발달이 가능해진다.
기존 학설에서는 친수성 물질은 소수성인 세포막을 통과하지 못하므로, 친수성인 호메오 단백질도 만들어진 세포 안에서만 작용한 뒤 소멸된다고 여겼다. 그러나 호메오 단백질이 세포막을 자유롭게 통과해 주변 세포로 이동한다는 주장도 있어, 약 30년간 학계의 논란이 되어 왔다.
이은정 박사가 제1 저자로 참여한 연구팀은 기존 세포생물학의 정설을 깨고, 호메오 단백질이 대부분 세포막 밖으로 분비될 수 있음을 입증했다. 연구팀이 인간의 160여 개 호메오 단백질을 분석한 결과 그 중 95%가 세포의 외부로 분비되어 주변 세포로 이동한 것을 확인했다.
그뿐만 아니라 연구팀은 세포의 외부로 분비되기 위한 조건으로써 호메오 단백질 내부에 소수성 아미노산 잔기가 필요하다는 것도 증명했다.
김진우 교수는 "이 연구를 통해 세포 간 이동이 호메오 단백질들이 가지는 일반적인 특성임이 증명됐다ˮ고 말하며, "이 연구가 30년 가까이 이어져 온 호메오 단백질의 세포 간 이동현상 논란에 종지부를 찍는 중요한 전환점이 될 것으로 본다ˮ라고 연구 의의를 설명했다.
이 연구 성과는 과학기술정보통신부․한국연구재단 기초연구사업(중견연구, 선도연구센터, 글로벌연구실) 등의 지원으로 수행되었으며 생명과학 분야의 세계적 학술지인 `셀 리포트(Cell Reports)'에 7월 16일 게재됐다.
□ 그림 설명
(그림 1) 호메오단백질의 세포 분비능 평가 결과
세포 외부로 분비된 호메오단백질을 검출하기 위해 세포 배양액의 호메오단백질 상대량을 조사했다(왼쪽 푸른색 바탕의 검은색 이미지). 3가지 다른 세포주를 이용해 검출하고, 각 결과를 병합해 오른쪽 모식도에 나타냈다(흰색: 3가지 세포주 모두에서 분비된 호메오단백질 / 회색: 3가지 세포주 모두에서 분비되지 않은 호메오단백질)
(그림 2) 호메오단백질의 세포간 이동 모델
호메오단백질의 분비 능력은 호메오도메인의 존재와 더불어 호메오단백질의 3차원 구조(호메오도메인 외부에 존재하는 소수성 아미노산잔기에 따라 정해짐)에 의해 결정된다. 세포 바깥 공간으로 분비된 호메오단백질는 세포 표면에 존재하는 프로테오클리칸의 당사슬과 결합을 통해 축적된 뒤 인접한 세포의 세포막을 침투해 세포 내부로 들어간다. 세포로 침투한 호메오단백질들은 해당세포에서 유전자 및 단백질 발현 등의 과정을 조절함으로써 세포의 발달과 유지에 관여한다.
2019.07.19 조회수 12181
김진우 교수, 발달과정 세포 간 정보전달 원리 규명
우리 대학 생명과학과 김진우 교수 연구팀이 호메오 단백질의 세포 간 이동으로 인해 세포와 세포 사이에서 정보가 전달될 수 있음을 규명했다.
호메오 단백질은 DNA에 결합하는 능력을 가진 전사인자로, 세포가 어떤 신체부위로 발달할지 운명을 결정하는 역할을 한다고 알려져 있다. 따라서 어떤 호메오 단백질을 가지고 있는지에 따라 동일한 DNA를 가진 세포들의 유전자 발현 양상이 달라져, 뇌·심장·피부 등 상이한 특징을 가지는 신체 기관으로의 발달이 가능해진다.
기존 학설에서는 친수성 물질은 소수성인 세포막을 통과하지 못하므로, 친수성인 호메오 단백질도 만들어진 세포 안에서만 작용한 뒤 소멸된다고 여겼다. 그러나 호메오 단백질이 세포막을 자유롭게 통과해 주변 세포로 이동한다는 주장도 있어, 약 30년간 학계의 논란이 되어 왔다.
이은정 박사가 제1 저자로 참여한 연구팀은 기존 세포생물학의 정설을 깨고, 호메오 단백질이 대부분 세포막 밖으로 분비될 수 있음을 입증했다. 연구팀이 인간의 160여 개 호메오 단백질을 분석한 결과 그 중 95%가 세포의 외부로 분비되어 주변 세포로 이동한 것을 확인했다.
그뿐만 아니라 연구팀은 세포의 외부로 분비되기 위한 조건으로써 호메오 단백질 내부에 소수성 아미노산 잔기가 필요하다는 것도 증명했다.
김진우 교수는 "이 연구를 통해 세포 간 이동이 호메오 단백질들이 가지는 일반적인 특성임이 증명됐다ˮ고 말하며, "이 연구가 30년 가까이 이어져 온 호메오 단백질의 세포 간 이동현상 논란에 종지부를 찍는 중요한 전환점이 될 것으로 본다ˮ라고 연구 의의를 설명했다.
이 연구 성과는 과학기술정보통신부․한국연구재단 기초연구사업(중견연구, 선도연구센터, 글로벌연구실) 등의 지원으로 수행되었으며 생명과학 분야의 세계적 학술지인 `셀 리포트(Cell Reports)'에 7월 16일 게재됐다.
□ 그림 설명
(그림 1) 호메오단백질의 세포 분비능 평가 결과
세포 외부로 분비된 호메오단백질을 검출하기 위해 세포 배양액의 호메오단백질 상대량을 조사했다(왼쪽 푸른색 바탕의 검은색 이미지). 3가지 다른 세포주를 이용해 검출하고, 각 결과를 병합해 오른쪽 모식도에 나타냈다(흰색: 3가지 세포주 모두에서 분비된 호메오단백질 / 회색: 3가지 세포주 모두에서 분비되지 않은 호메오단백질)
(그림 2) 호메오단백질의 세포간 이동 모델
호메오단백질의 분비 능력은 호메오도메인의 존재와 더불어 호메오단백질의 3차원 구조(호메오도메인 외부에 존재하는 소수성 아미노산잔기에 따라 정해짐)에 의해 결정된다. 세포 바깥 공간으로 분비된 호메오단백질는 세포 표면에 존재하는 프로테오클리칸의 당사슬과 결합을 통해 축적된 뒤 인접한 세포의 세포막을 침투해 세포 내부로 들어간다. 세포로 침투한 호메오단백질들은 해당세포에서 유전자 및 단백질 발현 등의 과정을 조절함으로써 세포의 발달과 유지에 관여한다.
2019.07.19 조회수 12181 -
 김학성 교수, 세포 내 단백질 전달 효율 높이는 DNA 기반 나노구조체 개발
우리 대학 생명과학과 김학성 교수, 류이슬 박사 연구팀이 강원대 이중재 교수, 한국원자력연구원 강정애 박사와의 공동 연구를 통해 DNA를 기반으로 나노 구조체를 개발해 세포 속으로의 단백질 전달 효율을 높이는 기술을 개발했다.
이번 연구 결과는 국제 학술지 ‘스몰(Small)’에 2018년 12월 28일일자 표지논문으로 게재됐다.
단백질 치료제는 저분자 화합물에 비해 반응 부위를 구별해내는 특이성이 우수해 차세대 의약품으로 활발히 개발되고 있다. 단백질 치료제가 탁월한 효과를 내기 위해서는 치료용 단백질이 세포 내로 효율적으로 전달되는 기술이 선행돼야 한다.
지금까지는 화학적 합성법 등으로 단백질 전달체를 제작해 왔지만 생체 독성, 낮은 전달 효율, 복잡한 제조공정과 효과가 일관적이지 않은 재현성 등이 해결돼야 할 과제로 남아있다.
연구팀은 생체 분자인 DNA를 기반으로 나노 구조체를 제작해 생체 친화적이면서 특정 세포로의 높은 전달 효율을 보였다. 특히 다양한 단백질을 전달할 수 있는 범용적인 기술로서 폐암 동물 모델에서도 항암 물질을 전달해 높은 항암 효과를 입증했다.
제조공정도 복잡하지 않다. 먼저 금 나노입자 표면에 DNA를 부착한다. 다음으로 징크 핑거를 이용해 각 DNA 가닥에 암세포를 표적하는 생체 분자와 항암 단백질을 결합해 제작했다.
DNA와 징크 핑거 간의 상호작용을 이용하므로 DNA 서열과 길이를 조절해 나노 구조체에 탑재되는 단백질의 양을 손쉽게 조절할 수 있다.
김학성 교수는 “생체 적합한 소재인 DNA와 단백질의 상호작용을 이용해 세포 내로 단백질을 효율적으로 전달하는 새로운 나노 구조체를 개발한 것이다”라며, “세포 내 단백질 치료제의 전달뿐 아니라 동반 진단용으로 광범위하게 활용될 것으로 기대된다”라고 말했다.
이번 연구 성과는 과학기술정보통신부‧한국연구재단 기초연구사업(글로벌연구실, 중견연구, 생애첫연구) 지원으로 수행됐다.
□ 그림 설명
그림1. small 표지
그림2. 나노 구조체 제조 과정 모식도
그림3. 나노 구조체의 세포 내 단백질 전달 효과
그림4. 나노 구조체의 현미경 관찰 사진
2019.01.21 조회수 14934
김학성 교수, 세포 내 단백질 전달 효율 높이는 DNA 기반 나노구조체 개발
우리 대학 생명과학과 김학성 교수, 류이슬 박사 연구팀이 강원대 이중재 교수, 한국원자력연구원 강정애 박사와의 공동 연구를 통해 DNA를 기반으로 나노 구조체를 개발해 세포 속으로의 단백질 전달 효율을 높이는 기술을 개발했다.
이번 연구 결과는 국제 학술지 ‘스몰(Small)’에 2018년 12월 28일일자 표지논문으로 게재됐다.
단백질 치료제는 저분자 화합물에 비해 반응 부위를 구별해내는 특이성이 우수해 차세대 의약품으로 활발히 개발되고 있다. 단백질 치료제가 탁월한 효과를 내기 위해서는 치료용 단백질이 세포 내로 효율적으로 전달되는 기술이 선행돼야 한다.
지금까지는 화학적 합성법 등으로 단백질 전달체를 제작해 왔지만 생체 독성, 낮은 전달 효율, 복잡한 제조공정과 효과가 일관적이지 않은 재현성 등이 해결돼야 할 과제로 남아있다.
연구팀은 생체 분자인 DNA를 기반으로 나노 구조체를 제작해 생체 친화적이면서 특정 세포로의 높은 전달 효율을 보였다. 특히 다양한 단백질을 전달할 수 있는 범용적인 기술로서 폐암 동물 모델에서도 항암 물질을 전달해 높은 항암 효과를 입증했다.
제조공정도 복잡하지 않다. 먼저 금 나노입자 표면에 DNA를 부착한다. 다음으로 징크 핑거를 이용해 각 DNA 가닥에 암세포를 표적하는 생체 분자와 항암 단백질을 결합해 제작했다.
DNA와 징크 핑거 간의 상호작용을 이용하므로 DNA 서열과 길이를 조절해 나노 구조체에 탑재되는 단백질의 양을 손쉽게 조절할 수 있다.
김학성 교수는 “생체 적합한 소재인 DNA와 단백질의 상호작용을 이용해 세포 내로 단백질을 효율적으로 전달하는 새로운 나노 구조체를 개발한 것이다”라며, “세포 내 단백질 치료제의 전달뿐 아니라 동반 진단용으로 광범위하게 활용될 것으로 기대된다”라고 말했다.
이번 연구 성과는 과학기술정보통신부‧한국연구재단 기초연구사업(글로벌연구실, 중견연구, 생애첫연구) 지원으로 수행됐다.
□ 그림 설명
그림1. small 표지
그림2. 나노 구조체 제조 과정 모식도
그림3. 나노 구조체의 세포 내 단백질 전달 효과
그림4. 나노 구조체의 현미경 관찰 사진
2019.01.21 조회수 14934 -
 허원도 교수, 빛만 비춰도 유전자 발현 조절하는 효소 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 살아있는 생쥐의 머리에 빛만 비춰도 생쥐 뇌 유전자 발현을 제어할 수 있는 시스템을 개발했다.
매우 약한 빛에도 반응하도록 유전자 재조합 효소를 설계해 원하는 위치와 타이밍에 효소를 활성화할 수 있다. 많은 시간과 재원이 소요되는 유전자 변형 실험 모델을 만들지 않아도 특정 유전자 발현을 유도할 수 있어 활용이 매우 클 것으로 기대된다.
이번 연구결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 1월 19일자 온라인 판에 게재됐다.
연구팀이 개발한 Flp 유전자 재조합 효소는 빛에 민감하게 반응해 활성화된다. 수술이 아닌 LED 빛을 쏘는 비침습성(non-invasive) 방식만으로도 유전자의 발현을 유도할 수 있어 물리적․화학적 손상에 의한 부작용도 최소화할 수 있다.
Flp 유전자 재조합 효소는 말 그대로 유전자를 자르고 재조합하는 기능을 지녀 유전자 형질 전환 실험모델을 만드는 등 다방면으로 활용됐다. 광유전학 기술에 응용하려는 시도가 있었으나 빛 없이도 스스로 조립(auto-assembly)돼버려 제어가 어려웠다. 뇌 속으로 빛을 직접 전달하려면 광섬유를 집어넣는 수술 과정도 필요했다.
연구팀이 개발한 광활성 Flp 유전자 재조합 효소(이하 PA-Flp 단백질)는 비활성화 상태에서도 빛을 받으면 결합되면서 활성화된다. 연구진은 단백질 공학을 통해 기존에는 잘 알려지지 않았던 Flp 재조합 효소를 활성화하는 위치를 찾는 힌트를 얻어 PA-Flp 단백질을 설계했다. PA-Flp 단백질의 발현 정도는 적색 형광단백질을 붙여 쉽게 알아볼 수 있도록 만들었다.
PA-Flp 단백질은 매우 적은 양으로도 반응하는 민감도를 지녔다. 연구진은 기억을 관장하는 쥐의 뇌 해마 부위에 PA-Flp 단백질을 넣은 뒤 약 30초 동안 LED를 머리 부분에 비추는 실험을 진행했다. 그 결과 생쥐 뇌의 깊은 조직 영역에 도달하는 매우 적은 양의 빛으로도 PA-Flp 단백질이 활성화된 것을 확인했다.
생쥐에게 쏜 빛은 1-2mW/mm2로 실생활에서 사용하는 휴대폰의 손전등 혹은 발표 시 이용하는 레이저 포인터 정도의 세기다. 연구진은 물리적 손상을 전혀 일으키지 않는 비침습성 방식으로도 유전자 발현을 조절하는데 성공한 것이다.
또한 연구진은 행동을 재현하고 검증하는 실험에 나섰다. 해마보다 더 깊숙한 곳에 있는 내측 중격(~3.5mm) 뇌 내측 중격(medial septum): 기억의 중추 역할을 담당하는 해마와 연결된 부위에는 칼슘 채널이 존재하는데 이 칼슘 채널의 발현이 억제되면 물체를 탐색하는 능력이 증가한다는 기존의 연구에 착안하여 실험을 설계했다.
연구진은 내측 중격에 PA-Flp 단백질을 도입하고 LED 빛을 쏘자 칼슘 채널의 발현이 억제됨을 확인했다. 실제 PA-Flp 단백질이 활성화된 실험군은 물체를 탐색하는 능력이 대조군에 비해 훨씬 커져 물체 주변으로 더 많은 움직임을 기록했다.
이번 연구는 빛으로 원하는 타이밍에 유전자를 자르고 재조합하는 효소를 개발해 향후 광유전학에 응용가치가 클 것으로 기대된다. 특정 유전자가 변형된 실험모델을 제작하는데 오랜 시일과 연구비가 투입되는데 반해 이 기술을 활용하면 빛만 쏘는 방식으로도 원하는 유전자를 쉽고 빠르게 조절할 수 있기 때문이다. 또한 광섬유를 심는 별도의 수술 없이도 연구자가 사용하기 간편하고 비용도 저렴하다.
허원도 교수는 “실험쥐의 생리학적 현상에 영향을 줄 수 있는 물리적, 화학적 자극이 거의 없이 LED로 원하는 특정 유전자 발현을 조절할 수 있는 것이 큰 장점이다”라며 “향후 다양한 뇌 영역을 탐구하는데 널리 활용될 것으로 기대한다”고 밝혔다.
□ 그림 설명
그림1. PA-Flp 단백질 작동원리 및 발현
그림2. 물체 탐색 능력이 증가함을 실험으로 확인
2019.01.21 조회수 10944
허원도 교수, 빛만 비춰도 유전자 발현 조절하는 효소 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 살아있는 생쥐의 머리에 빛만 비춰도 생쥐 뇌 유전자 발현을 제어할 수 있는 시스템을 개발했다.
매우 약한 빛에도 반응하도록 유전자 재조합 효소를 설계해 원하는 위치와 타이밍에 효소를 활성화할 수 있다. 많은 시간과 재원이 소요되는 유전자 변형 실험 모델을 만들지 않아도 특정 유전자 발현을 유도할 수 있어 활용이 매우 클 것으로 기대된다.
이번 연구결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 1월 19일자 온라인 판에 게재됐다.
연구팀이 개발한 Flp 유전자 재조합 효소는 빛에 민감하게 반응해 활성화된다. 수술이 아닌 LED 빛을 쏘는 비침습성(non-invasive) 방식만으로도 유전자의 발현을 유도할 수 있어 물리적․화학적 손상에 의한 부작용도 최소화할 수 있다.
Flp 유전자 재조합 효소는 말 그대로 유전자를 자르고 재조합하는 기능을 지녀 유전자 형질 전환 실험모델을 만드는 등 다방면으로 활용됐다. 광유전학 기술에 응용하려는 시도가 있었으나 빛 없이도 스스로 조립(auto-assembly)돼버려 제어가 어려웠다. 뇌 속으로 빛을 직접 전달하려면 광섬유를 집어넣는 수술 과정도 필요했다.
연구팀이 개발한 광활성 Flp 유전자 재조합 효소(이하 PA-Flp 단백질)는 비활성화 상태에서도 빛을 받으면 결합되면서 활성화된다. 연구진은 단백질 공학을 통해 기존에는 잘 알려지지 않았던 Flp 재조합 효소를 활성화하는 위치를 찾는 힌트를 얻어 PA-Flp 단백질을 설계했다. PA-Flp 단백질의 발현 정도는 적색 형광단백질을 붙여 쉽게 알아볼 수 있도록 만들었다.
PA-Flp 단백질은 매우 적은 양으로도 반응하는 민감도를 지녔다. 연구진은 기억을 관장하는 쥐의 뇌 해마 부위에 PA-Flp 단백질을 넣은 뒤 약 30초 동안 LED를 머리 부분에 비추는 실험을 진행했다. 그 결과 생쥐 뇌의 깊은 조직 영역에 도달하는 매우 적은 양의 빛으로도 PA-Flp 단백질이 활성화된 것을 확인했다.
생쥐에게 쏜 빛은 1-2mW/mm2로 실생활에서 사용하는 휴대폰의 손전등 혹은 발표 시 이용하는 레이저 포인터 정도의 세기다. 연구진은 물리적 손상을 전혀 일으키지 않는 비침습성 방식으로도 유전자 발현을 조절하는데 성공한 것이다.
또한 연구진은 행동을 재현하고 검증하는 실험에 나섰다. 해마보다 더 깊숙한 곳에 있는 내측 중격(~3.5mm) 뇌 내측 중격(medial septum): 기억의 중추 역할을 담당하는 해마와 연결된 부위에는 칼슘 채널이 존재하는데 이 칼슘 채널의 발현이 억제되면 물체를 탐색하는 능력이 증가한다는 기존의 연구에 착안하여 실험을 설계했다.
연구진은 내측 중격에 PA-Flp 단백질을 도입하고 LED 빛을 쏘자 칼슘 채널의 발현이 억제됨을 확인했다. 실제 PA-Flp 단백질이 활성화된 실험군은 물체를 탐색하는 능력이 대조군에 비해 훨씬 커져 물체 주변으로 더 많은 움직임을 기록했다.
이번 연구는 빛으로 원하는 타이밍에 유전자를 자르고 재조합하는 효소를 개발해 향후 광유전학에 응용가치가 클 것으로 기대된다. 특정 유전자가 변형된 실험모델을 제작하는데 오랜 시일과 연구비가 투입되는데 반해 이 기술을 활용하면 빛만 쏘는 방식으로도 원하는 유전자를 쉽고 빠르게 조절할 수 있기 때문이다. 또한 광섬유를 심는 별도의 수술 없이도 연구자가 사용하기 간편하고 비용도 저렴하다.
허원도 교수는 “실험쥐의 생리학적 현상에 영향을 줄 수 있는 물리적, 화학적 자극이 거의 없이 LED로 원하는 특정 유전자 발현을 조절할 수 있는 것이 큰 장점이다”라며 “향후 다양한 뇌 영역을 탐구하는데 널리 활용될 것으로 기대한다”고 밝혔다.
□ 그림 설명
그림1. PA-Flp 단백질 작동원리 및 발현
그림2. 물체 탐색 능력이 증가함을 실험으로 확인
2019.01.21 조회수 10944 -
 허원도 교수, 변화무쌍 스위치 단백질 관찰하는 바이오센서 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 신호전달 스위치단백질의 활성을 모니터링하는 새로운‘바이오센서’를 개발하고 살아있는 생쥐의 신경세포 활성화를 관찰하는데 성공했다.
이번 연구를 통해 암세포의 이동과 신경세포 활성화 등 다양한 세포 기능에 관여하는 신호전달 스위치 단백질의 변화무쌍한 과정을 실시간으로 볼 수 있을 것으로 기대된다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈’(Nature Communications)에 1월 14일자 온라인 판에 게재됐다.
세포의 신호전달 스위치 단백질은 스위치가 켜지면 기계가 작동하듯 활성화 여부로 세포의 기능을 제어한다. 대표적인 신호전달 스위치단백질인 small GTPase은 세포의 이동, 분열, 사멸과 유전자 발현 등에 관여한다. 핵심 단백질인 small GTPase를 제어할 수 있다면 세포의 기능도 조절할 수 있어 많은 연구팀들이 연구주제로 삼고 있다.
허원도 교수 연구팀이 그간 연구 노하우를 바탕으로 개발한 새로운 바이오센서는 small GTPase 활성의 모든 변화 과정을 실시간으로 볼 수 있는 도구다. 광유전학과 결합해 다양한 방식으로 관찰이 가능하고 민감도가 커 생체 내 두꺼운 조직 안에서 벌어지는 수 나노미터(nm) 크기의 변화까지도 정밀하게 볼 수 있다는 게 특징이다. 고감도 성능을 이용하면 살아있는 동물의 암세포 전이 및 뇌 속 신경세포의 구조변화를 관찰할 수 있어 향후 강력한 이미징 기술이 될 것으로 기대된다.
일반적으로 small GTPase의 활성을 관찰하는 데엔 형광 공명 에너지전달(FRET) 방식을 이용했다. 하지만 FRET 방식은 광유전학과 광 파장이 겹쳐 정작 관찰해야 할 세포신호의 변화는 보기가 어려웠다. 또 민감도가 낮아 동물 모델에 적용하는 것도 제한적이었다.
연구팀은 단백질 공학 기술로 5가지 종류의 small GTPase 단백질의 바이오센서를 개발하고 두 가지 파장(488nm, 561nm)에서 관찰이 가능한 바이오센서를 개발, 이를 동시에 분석하는데 성공했다. 연구진이 개발한 바이오센서는 기존 바이오센서가 청색광을 활용하는 광유전학 기법의 파장과 겹치는 문제를 효과적으로 극복해 세포의 이동방향을 살피면서 동시에 공간적 기능도 분석할 수 있는 장점이 있다.
연구팀은 유방암 전이 암세포에 바이오센서를 발현시키고, 광유전학 기술로 암세포 이동 방향을 조절하자 small GTPase 단백질이 활성화됨을 확인했다. 이 과정에서 암세포의 이동 방향이 변할 때, 세포 내 small GTPase가 이리저리 움직이며 활성화하는 모습을 실시간 이미징하는데 성공했다. 연구진은 small GTPase의 활성을 실시간으로 탐지해 추후 암치료물질을 탐색하는 등 다방면의 기술 접목이 가능할 것으로 전망한다.
더 나아가 IBS 연구진은 미국 막스 플랑크 플로리다 연구소(Max Plank Florida Institute)의 권형배 박사 연구팀과 공동연구를 진행했다. 연구진은 공 위를 달리는 실험으로 깨어있는 생쥐인 실험군과 마취된 대조군의 뇌 영역의 운동 피질의 신경세포에서의 small GTPase단백질의 활성을 비교하는데 성공했다. 살아있는 쥐에서 수 나노미터 단위의 신경세포 수상돌기 가시 수상돌기 가시에서 실시간으로 변화하는 small GTPase 단백질의 활성을 관찰한 것은 이번이 처음이다.
이번에 개발된 바이오센서는 시냅스처럼 수 마이크로미터 단위의 미세한 구조에서도 목표한 단백질을 관찰할 수 있을 만큼 민감도가 크다. 실험쥐의 운동행동과 같은 생리학적 현상에 지장을 주지 않는 자연스러운 상태에서 뇌 영역을 바로 실시간으로 관찰할 수 있어 뇌 관련 연구에도 다양하게 적용될 수 있다.
연구를 이끈 허원도 교수는 “이번 연구는 small GTPase 단백질을 생체 내에서 관찰하기 위한 기존의 바이오센서들의 기술적 한계를 극복하는데 성공했다”며 “특히 청색 빛을 활용한 광유전학 기술과 동시에 적용할 수 있어 다양한 세포막 수용체와 관련된 광범위한 세포신호전달연구와 뇌인지과학연구에 접목이 가능할 것으로 기대된다”고 말했다.
□ 그림 설명
그림1. small GTPase 바이오센서 개발
그림2. small GTPase 바이오센서를 이용해 유방암 전이 암세포 관찰
그림3. 운동 행동 중인 생쥐 실시간 관찰
2019.01.15 조회수 13325
허원도 교수, 변화무쌍 스위치 단백질 관찰하는 바이오센서 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀(기초과학연구원 인지 및 사회성 연구단)이 신호전달 스위치단백질의 활성을 모니터링하는 새로운‘바이오센서’를 개발하고 살아있는 생쥐의 신경세포 활성화를 관찰하는데 성공했다.
이번 연구를 통해 암세포의 이동과 신경세포 활성화 등 다양한 세포 기능에 관여하는 신호전달 스위치 단백질의 변화무쌍한 과정을 실시간으로 볼 수 있을 것으로 기대된다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈’(Nature Communications)에 1월 14일자 온라인 판에 게재됐다.
세포의 신호전달 스위치 단백질은 스위치가 켜지면 기계가 작동하듯 활성화 여부로 세포의 기능을 제어한다. 대표적인 신호전달 스위치단백질인 small GTPase은 세포의 이동, 분열, 사멸과 유전자 발현 등에 관여한다. 핵심 단백질인 small GTPase를 제어할 수 있다면 세포의 기능도 조절할 수 있어 많은 연구팀들이 연구주제로 삼고 있다.
허원도 교수 연구팀이 그간 연구 노하우를 바탕으로 개발한 새로운 바이오센서는 small GTPase 활성의 모든 변화 과정을 실시간으로 볼 수 있는 도구다. 광유전학과 결합해 다양한 방식으로 관찰이 가능하고 민감도가 커 생체 내 두꺼운 조직 안에서 벌어지는 수 나노미터(nm) 크기의 변화까지도 정밀하게 볼 수 있다는 게 특징이다. 고감도 성능을 이용하면 살아있는 동물의 암세포 전이 및 뇌 속 신경세포의 구조변화를 관찰할 수 있어 향후 강력한 이미징 기술이 될 것으로 기대된다.
일반적으로 small GTPase의 활성을 관찰하는 데엔 형광 공명 에너지전달(FRET) 방식을 이용했다. 하지만 FRET 방식은 광유전학과 광 파장이 겹쳐 정작 관찰해야 할 세포신호의 변화는 보기가 어려웠다. 또 민감도가 낮아 동물 모델에 적용하는 것도 제한적이었다.
연구팀은 단백질 공학 기술로 5가지 종류의 small GTPase 단백질의 바이오센서를 개발하고 두 가지 파장(488nm, 561nm)에서 관찰이 가능한 바이오센서를 개발, 이를 동시에 분석하는데 성공했다. 연구진이 개발한 바이오센서는 기존 바이오센서가 청색광을 활용하는 광유전학 기법의 파장과 겹치는 문제를 효과적으로 극복해 세포의 이동방향을 살피면서 동시에 공간적 기능도 분석할 수 있는 장점이 있다.
연구팀은 유방암 전이 암세포에 바이오센서를 발현시키고, 광유전학 기술로 암세포 이동 방향을 조절하자 small GTPase 단백질이 활성화됨을 확인했다. 이 과정에서 암세포의 이동 방향이 변할 때, 세포 내 small GTPase가 이리저리 움직이며 활성화하는 모습을 실시간 이미징하는데 성공했다. 연구진은 small GTPase의 활성을 실시간으로 탐지해 추후 암치료물질을 탐색하는 등 다방면의 기술 접목이 가능할 것으로 전망한다.
더 나아가 IBS 연구진은 미국 막스 플랑크 플로리다 연구소(Max Plank Florida Institute)의 권형배 박사 연구팀과 공동연구를 진행했다. 연구진은 공 위를 달리는 실험으로 깨어있는 생쥐인 실험군과 마취된 대조군의 뇌 영역의 운동 피질의 신경세포에서의 small GTPase단백질의 활성을 비교하는데 성공했다. 살아있는 쥐에서 수 나노미터 단위의 신경세포 수상돌기 가시 수상돌기 가시에서 실시간으로 변화하는 small GTPase 단백질의 활성을 관찰한 것은 이번이 처음이다.
이번에 개발된 바이오센서는 시냅스처럼 수 마이크로미터 단위의 미세한 구조에서도 목표한 단백질을 관찰할 수 있을 만큼 민감도가 크다. 실험쥐의 운동행동과 같은 생리학적 현상에 지장을 주지 않는 자연스러운 상태에서 뇌 영역을 바로 실시간으로 관찰할 수 있어 뇌 관련 연구에도 다양하게 적용될 수 있다.
연구를 이끈 허원도 교수는 “이번 연구는 small GTPase 단백질을 생체 내에서 관찰하기 위한 기존의 바이오센서들의 기술적 한계를 극복하는데 성공했다”며 “특히 청색 빛을 활용한 광유전학 기술과 동시에 적용할 수 있어 다양한 세포막 수용체와 관련된 광범위한 세포신호전달연구와 뇌인지과학연구에 접목이 가능할 것으로 기대된다”고 말했다.
□ 그림 설명
그림1. small GTPase 바이오센서 개발
그림2. small GTPase 바이오센서를 이용해 유방암 전이 암세포 관찰
그림3. 운동 행동 중인 생쥐 실시간 관찰
2019.01.15 조회수 13325 -
 김학성 교수, 빛에 의해 스위치처럼 작동하는 단백질 개발
〈 김 학 성 교수 〉
우리 대학 생명과학과 김학성 교수 연구팀이 빛으로 결합력을 제어할 수 있는 결합 단백질을 개발해 빛을 이용한 세포 신호전달 제어에 새 방법을 제시했다.
이는 제한적이었던 기존 광 제어 기술의 한계를 극복해 다양한 세포신호 전달 제어에 활용할 수 있을 것으로 기대된다.
허우성, 최정민 박사가 주도한 이번 연구는 앙케반테 케미(Angewandte Chemie) 6월 27일자 온라인 판에 게재됐다.
빛을 이용한 세포의 신호전달 조절은 물리, 화학적 방법보다 비 침습적이고 빠르기 때문에 신호전달 연구에 효과적으로 활용 가능하다.
그러나 지금까지는 자연에 존재하는 광 스위치 단백질에 의존했기 때문에 이 단백질들을 각각의 신호전달 조절에 맞도록 다시 설계해야 하는 복잡하고 힘든 과정으로 인해 응용이 극히 제한됐다.
최근에는 합성된 광스위치 분자를 단백질에 결합시켜 빛에 따라 그 기능을 조절하려는 연구가 진행됐다. 그러나 이 경우 빛에 따라 스위치처럼 작동하는 단백질의 설계방법이 단백질 종류에 따라 다르고 복잡하다는 한계가 있었다.
연구팀은 LRR(Leucine-rich repeat) 단백질을 기반으로 아조벤젠 유래 광 스위치 분자를 합리적 방법으로 단백질 모듈에 결합시켰다. 이를 통해 빛으로 단백질의 구조변화를 유도해 표적에 대한 결합력을 조절했다.
또한 빛에 의한 상피세포 성장인자 수용체(EGFR, epithelial growth factor receptor)에 대한 결합력 조절이 가능한 단백질을 개발하고, 이를 이용해 세포 내 EGFR 신호 전달을 빛으로 조절할 수 있음을 증명했다.
연구팀은 LRR 모듈로 구성된 단백질의 구조 특성을 기반으로 광스위치 분자를 반복 모듈 사이에 결합시켜 빛으로 표적에 대한 결합력이 효과적으로 조절되는 단백질의 합리적 설계 방법을 개발했다.
이는 다양한 표적에 대해 결합하는 LRR 단백질에 광범위하게 적용할 수 있는 기반 기술로, 빛을 이용한 세포 내 다양한 신호 전달 조절에 활용할 수 있는 새로운 단백질 창출 방법을 제시한 것이다.
이번 연구는 한국연구재단의 글로벌연구실사업(GRL)과 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. LRR 단백질 기반으로 합리적 설계를 통해 광스위치 단백질 개발 및 이를 이용한 세포 신호전달 조절
2018.08.13 조회수 13711
김학성 교수, 빛에 의해 스위치처럼 작동하는 단백질 개발
〈 김 학 성 교수 〉
우리 대학 생명과학과 김학성 교수 연구팀이 빛으로 결합력을 제어할 수 있는 결합 단백질을 개발해 빛을 이용한 세포 신호전달 제어에 새 방법을 제시했다.
이는 제한적이었던 기존 광 제어 기술의 한계를 극복해 다양한 세포신호 전달 제어에 활용할 수 있을 것으로 기대된다.
허우성, 최정민 박사가 주도한 이번 연구는 앙케반테 케미(Angewandte Chemie) 6월 27일자 온라인 판에 게재됐다.
빛을 이용한 세포의 신호전달 조절은 물리, 화학적 방법보다 비 침습적이고 빠르기 때문에 신호전달 연구에 효과적으로 활용 가능하다.
그러나 지금까지는 자연에 존재하는 광 스위치 단백질에 의존했기 때문에 이 단백질들을 각각의 신호전달 조절에 맞도록 다시 설계해야 하는 복잡하고 힘든 과정으로 인해 응용이 극히 제한됐다.
최근에는 합성된 광스위치 분자를 단백질에 결합시켜 빛에 따라 그 기능을 조절하려는 연구가 진행됐다. 그러나 이 경우 빛에 따라 스위치처럼 작동하는 단백질의 설계방법이 단백질 종류에 따라 다르고 복잡하다는 한계가 있었다.
연구팀은 LRR(Leucine-rich repeat) 단백질을 기반으로 아조벤젠 유래 광 스위치 분자를 합리적 방법으로 단백질 모듈에 결합시켰다. 이를 통해 빛으로 단백질의 구조변화를 유도해 표적에 대한 결합력을 조절했다.
또한 빛에 의한 상피세포 성장인자 수용체(EGFR, epithelial growth factor receptor)에 대한 결합력 조절이 가능한 단백질을 개발하고, 이를 이용해 세포 내 EGFR 신호 전달을 빛으로 조절할 수 있음을 증명했다.
연구팀은 LRR 모듈로 구성된 단백질의 구조 특성을 기반으로 광스위치 분자를 반복 모듈 사이에 결합시켜 빛으로 표적에 대한 결합력이 효과적으로 조절되는 단백질의 합리적 설계 방법을 개발했다.
이는 다양한 표적에 대해 결합하는 LRR 단백질에 광범위하게 적용할 수 있는 기반 기술로, 빛을 이용한 세포 내 다양한 신호 전달 조절에 활용할 수 있는 새로운 단백질 창출 방법을 제시한 것이다.
이번 연구는 한국연구재단의 글로벌연구실사업(GRL)과 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. LRR 단백질 기반으로 합리적 설계를 통해 광스위치 단백질 개발 및 이를 이용한 세포 신호전달 조절
2018.08.13 조회수 13711 -
 이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 17520
이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 17520 -
 박희성 교수, 이달의 과학기술인상 5월 수상자 선정
〈 박 희 성 교수 〉
우리 대학 화학과 박희성 교수가 ‘이달의 과학기술인상’ 5월 수상자로 선정됐다.
이달의 과학기술인상은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구 개발자를 매월 1명씩 선정하는 상으로 과학기술정보통신부 장관상과 상금 1천만 원을 수여한다.
과학기술정보통신부와 한국연구재단은 선정 배경에 대해 박희성 교수가 암, 치매 등 각종 질병 유발에 관여하는 단백질 변형을 인위적으로 제어할 수 있는 ‘맞춤형 단백질 변형기술’을 개발해 질병의 원인 규명과 신약 개발 연구의 단초를 마련한 공로가 높이 평가됐다고 밝혔다.
우리 몸의 단백질은 인산화, 당화, 아세틸화, 메틸화 등 200여 종의 다양한 변형(post-translational modification)을 통해 생체 신호를 전달하고 세포의 성장·분열 같은 신진대사를 조절한다. 하지만 유전적·환경적 요인으로 인한 비정상적 단백질 변형은 암, 치매, 당뇨 등 각종 퇴행성 질환과 만성질환의 원인이 된다.
많은 학자들이 단백질 변형에 따른 세포내 기능 연구와 질병의 연관성을 밝히기 위해 맞춤형 단백질 개발 연구를 진행했지만 기존 기술로는 원하는 변형을 갖는 단백질을 제조하는 것이 불가능했다.
박희성 교수는 박테리아의 생합성 경로를 재설계하고 비천연 아미노산을 표적단백질에 위치 특이적으로 첨가하는 방법으로 2011년 단백질 변형 중 가장 광범위한 단백질 인산화 제어에 성공했다.
이후 후속연구를 통해 비천연 아미노산의 특이적인 화학 반응성을 이용해 단백질 표면에서 탄소-탄소 결합을 일으켜 당화, 메틸화 등 200여 종의 맞춤형 단백질을 제조할 수 있는 기술을 최초로 개발했다.
박 교수팀은 퇴행성 신경질환의 원인중 하나로 알려진 비정상적 단백질 아세틸화를 실험용 쥐를 이용한 동물 모델에서 직접 구현했다.
이를 통해 실험용 쥐의 특정 발달 단계나 시기에 표적 단백질의 특정 위치에서 아세틸화 변형을 조절할 수 있었다. 또 다른 조직에 영향을 주지 않고 간이나 콩팥 등 특정 조직이나 기관에서만 표적 단백질이 아세틸화 변형 제어가 가능한 것도 확인했다.
박희성 교수는 “이 연구는 단백질 표면에서 선택적으로 탄소 간 결합을 일으켜 맞춤형으로 변형을 유발시키는 획기적인 단백질 변형 방법으로 암, 치매 등 단백질의 비정상적인 변형으로 유발되는 다양한 질병들에 대한 원인 규명과 치료제 개발에 돌파구를 마련하는 연구 결과이다” 고 말했다.
2018.05.03 조회수 16046
박희성 교수, 이달의 과학기술인상 5월 수상자 선정
〈 박 희 성 교수 〉
우리 대학 화학과 박희성 교수가 ‘이달의 과학기술인상’ 5월 수상자로 선정됐다.
이달의 과학기술인상은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구 개발자를 매월 1명씩 선정하는 상으로 과학기술정보통신부 장관상과 상금 1천만 원을 수여한다.
과학기술정보통신부와 한국연구재단은 선정 배경에 대해 박희성 교수가 암, 치매 등 각종 질병 유발에 관여하는 단백질 변형을 인위적으로 제어할 수 있는 ‘맞춤형 단백질 변형기술’을 개발해 질병의 원인 규명과 신약 개발 연구의 단초를 마련한 공로가 높이 평가됐다고 밝혔다.
우리 몸의 단백질은 인산화, 당화, 아세틸화, 메틸화 등 200여 종의 다양한 변형(post-translational modification)을 통해 생체 신호를 전달하고 세포의 성장·분열 같은 신진대사를 조절한다. 하지만 유전적·환경적 요인으로 인한 비정상적 단백질 변형은 암, 치매, 당뇨 등 각종 퇴행성 질환과 만성질환의 원인이 된다.
많은 학자들이 단백질 변형에 따른 세포내 기능 연구와 질병의 연관성을 밝히기 위해 맞춤형 단백질 개발 연구를 진행했지만 기존 기술로는 원하는 변형을 갖는 단백질을 제조하는 것이 불가능했다.
박희성 교수는 박테리아의 생합성 경로를 재설계하고 비천연 아미노산을 표적단백질에 위치 특이적으로 첨가하는 방법으로 2011년 단백질 변형 중 가장 광범위한 단백질 인산화 제어에 성공했다.
이후 후속연구를 통해 비천연 아미노산의 특이적인 화학 반응성을 이용해 단백질 표면에서 탄소-탄소 결합을 일으켜 당화, 메틸화 등 200여 종의 맞춤형 단백질을 제조할 수 있는 기술을 최초로 개발했다.
박 교수팀은 퇴행성 신경질환의 원인중 하나로 알려진 비정상적 단백질 아세틸화를 실험용 쥐를 이용한 동물 모델에서 직접 구현했다.
이를 통해 실험용 쥐의 특정 발달 단계나 시기에 표적 단백질의 특정 위치에서 아세틸화 변형을 조절할 수 있었다. 또 다른 조직에 영향을 주지 않고 간이나 콩팥 등 특정 조직이나 기관에서만 표적 단백질이 아세틸화 변형 제어가 가능한 것도 확인했다.
박희성 교수는 “이 연구는 단백질 표면에서 선택적으로 탄소 간 결합을 일으켜 맞춤형으로 변형을 유발시키는 획기적인 단백질 변형 방법으로 암, 치매 등 단백질의 비정상적인 변형으로 유발되는 다양한 질병들에 대한 원인 규명과 치료제 개발에 돌파구를 마련하는 연구 결과이다” 고 말했다.
2018.05.03 조회수 16046 -
 김필한 교수, 초고속 레이저 생체현미경 개발
〈 김 필 한 교수 〉
우리 대학 나노과학기술대학원 김필한 교수 연구팀이 개발한 초고속 생체현미경(IVM: IntraVital Microscopy)을 통해 미래 글로벌 바이오헬스 시장을 겨냥한 상용화에 나선다.
김 교수는 (재)의약바이오컨버젼스연구단, 서울대학교 김성훈 교수와의 공동 연구를 통해 개발한 최첨단 초고속 레이저스캐닝 3차원 생체현미경 기술을 토대로 아이빔테크놀로지(주)(IVIM Technology, Inc)를 창업했다.
이 생체현미경(IntraVital Microscopy : IVM)은 수많은 세포들 간 상호작용을 통해 나타나는 생명 현상을 탐구하고 여러 질환의 복잡한 발생 과정을 밝힘으로써 기초 의생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
연구팀의 기술은 살아있는 생체 내부조직을 구성하는 세포의 움직임을 직접 관찰할 수 있다. MRI나 CT 등 기존 생체영상 기술로는 불가능한 신체 다양한 장기 내부의 수많은 세포 하나하나를 구별하고 각 세포들의 움직임을 3차원으로 즉시 확인 가능하다.
이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 초고속 생체현미경 기술은 여러 색의 레이저 빔을 이용해 기존의 조직분석 기술로는 불가능했던 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화할 수 있다.
이를 활용하면 생체 외부에서 수집한 데이터로 수립한 가정을 실제 살아있는 생체 내 환경에서 세포 단위로 검증하고 분석할 수 있다.
생체현미경은 바이오제약 분야에서도 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
연구팀의 생체현미경은 동물실험에서 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 동영상으로 관찰할 수 있다. 현재 (재)의약바이오컨버젼스연구단과 함께 차세대 신약개발을 위한 핵심기술로 발전시키기 위해 노력 중이다.
김 교수가 창업한 회사는 시장성과 성장가능성을 높게 평가받아 벤처기업으로서는 이례적으로 빠르게 창업 3개월 만에 LB인베스트먼트와 에이티넘인베스트먼트로부터 총 30억 원의 투자를 유치했다.
김 교수는 “이 기술은 다양한 생명 현상을 보다 정밀하게 종합 분석하기 위한 원천기술이다”며 “고령화 사회의 도래와 함께 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술의 발전을 가속화할 핵심 기술이 될 것으로 확신한다”고 말했다.
김 교수 연구팀의 연구는 창업원의 엔드런(End-Run) 사업과 과학기술정보통신부가 추진하는 글로벌프론티어사업의 혁신형의약바이오컨버전스사업의 지원을 받아 수행됐다.
□ 사진 설명
사진1. 초고속 레이저 생체현미경 (IVM) 사진1
사진2. 초고속 레이저 생체현미경 (IVM) 사진2
사진3. 생체 내부 세포수준 변화의 IVM 영상 결과
사진4. 생체 내부 다양한 장기의 세포수준 IVM 영상 결과
2017.11.21 조회수 25472
김필한 교수, 초고속 레이저 생체현미경 개발
〈 김 필 한 교수 〉
우리 대학 나노과학기술대학원 김필한 교수 연구팀이 개발한 초고속 생체현미경(IVM: IntraVital Microscopy)을 통해 미래 글로벌 바이오헬스 시장을 겨냥한 상용화에 나선다.
김 교수는 (재)의약바이오컨버젼스연구단, 서울대학교 김성훈 교수와의 공동 연구를 통해 개발한 최첨단 초고속 레이저스캐닝 3차원 생체현미경 기술을 토대로 아이빔테크놀로지(주)(IVIM Technology, Inc)를 창업했다.
이 생체현미경(IntraVital Microscopy : IVM)은 수많은 세포들 간 상호작용을 통해 나타나는 생명 현상을 탐구하고 여러 질환의 복잡한 발생 과정을 밝힘으로써 기초 의생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
연구팀의 기술은 살아있는 생체 내부조직을 구성하는 세포의 움직임을 직접 관찰할 수 있다. MRI나 CT 등 기존 생체영상 기술로는 불가능한 신체 다양한 장기 내부의 수많은 세포 하나하나를 구별하고 각 세포들의 움직임을 3차원으로 즉시 확인 가능하다.
이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 초고속 생체현미경 기술은 여러 색의 레이저 빔을 이용해 기존의 조직분석 기술로는 불가능했던 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화할 수 있다.
이를 활용하면 생체 외부에서 수집한 데이터로 수립한 가정을 실제 살아있는 생체 내 환경에서 세포 단위로 검증하고 분석할 수 있다.
생체현미경은 바이오제약 분야에서도 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
연구팀의 생체현미경은 동물실험에서 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 동영상으로 관찰할 수 있다. 현재 (재)의약바이오컨버젼스연구단과 함께 차세대 신약개발을 위한 핵심기술로 발전시키기 위해 노력 중이다.
김 교수가 창업한 회사는 시장성과 성장가능성을 높게 평가받아 벤처기업으로서는 이례적으로 빠르게 창업 3개월 만에 LB인베스트먼트와 에이티넘인베스트먼트로부터 총 30억 원의 투자를 유치했다.
김 교수는 “이 기술은 다양한 생명 현상을 보다 정밀하게 종합 분석하기 위한 원천기술이다”며 “고령화 사회의 도래와 함께 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술의 발전을 가속화할 핵심 기술이 될 것으로 확신한다”고 말했다.
김 교수 연구팀의 연구는 창업원의 엔드런(End-Run) 사업과 과학기술정보통신부가 추진하는 글로벌프론티어사업의 혁신형의약바이오컨버전스사업의 지원을 받아 수행됐다.
□ 사진 설명
사진1. 초고속 레이저 생체현미경 (IVM) 사진1
사진2. 초고속 레이저 생체현미경 (IVM) 사진2
사진3. 생체 내부 세포수준 변화의 IVM 영상 결과
사진4. 생체 내부 다양한 장기의 세포수준 IVM 영상 결과
2017.11.21 조회수 25472