-
 김정원 교수, 이달의 과학기술인상 10월 수상자 선정
우리 대학 기계공학과 김정원 교수가 이달의 과학기술인상 10월 수상자에 선정됐다.
과학기술정보통신부와 한국연구재단은 김정원 교수가 초고속, 고분해능, 다기능성 센서기술을 개발하여 기초정밀 공학의 지평을 넓힌 공로를 높이 평가했다고 선정 배경을 설명했다.
'이달의 과학기술인상'은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구개발자를 매월 1명씩 선정해 과기정통부 장관상과 상금 1천만 원을 수여하는 상이다. 세종대왕이 길이와 부피의 측정체계를 확립한 10월 26일을 기념하는 ‘계량측정의 날’을 맞아 김정원 교수가 이달의 수상자로 선정됐다.
레이저를 이용한 초정밀 거리 측정기술은 비접촉, 비파괴 등의 장점을 앞세워 중력파 검출부터 산업용 센서까지 다양한 분야에서 활약해 왔다. 하지만 대표적인 레이저 측정기술 중 하나인 펄스비행시간(time-of-flight, TOF) 기술은 긴 거리 측정은 가능하지만 분해능이 떨어지며, 레이저 간섭계 기술은 분해능은 우수하지만 측정 범위가 마이크로미터에 불과하다. 또한 두 기술 모두 측정 속도가 느리며, 거리·분해능·시간 중 한 가지 성능을 향상하면 나머지 성능이 저하되는 한계가 있었다.
김 교수는 레이저에서 발생한 빛 펄스와 광다이오드로 생성한 전류 펄스사이의 시간 차가 100 아토초(10-16초, 1경분의 1초) 이하로 작다는 사실을 발견하고, 전광샘플링하는 방법으로 한 번에 여러 지점을 동시 측정할 수 있는 독창적인 초고속·초정밀·다기능 TOF센서를 개발했다. 측정속도 100메가헤르츠(1초에1억번 진동), 분해능 180피코미터(55억분의 1미터), 동적범위 150데시벨의 성능으로 기존 TOF와 간섭계 기술의 한계를 동시에 극복했다는 평이다. 연구결과는 네이처 포토닉스(Nature Photonics) 2020년 2월 10일자에 게재됐다.
김정원 교수는 "함께 열정적으로 연구한 대학원생들과 연구에 전념할 수 있는 환경을 만들어준 학교에 감사드린다"라며 "향후 마이크로 소자 내에서의 역학현상 탐구나 첨단제조를 위한 초정밀 형상측정 등 새롭고 다양한 기계·제조 분야에서 활용이 기대된다"라고 수상 소감을 밝혔다.
김정원 교수, 이달의 과학기술인상 10월 수상자 선정
우리 대학 기계공학과 김정원 교수가 이달의 과학기술인상 10월 수상자에 선정됐다.
과학기술정보통신부와 한국연구재단은 김정원 교수가 초고속, 고분해능, 다기능성 센서기술을 개발하여 기초정밀 공학의 지평을 넓힌 공로를 높이 평가했다고 선정 배경을 설명했다.
'이달의 과학기술인상'은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구개발자를 매월 1명씩 선정해 과기정통부 장관상과 상금 1천만 원을 수여하는 상이다. 세종대왕이 길이와 부피의 측정체계를 확립한 10월 26일을 기념하는 ‘계량측정의 날’을 맞아 김정원 교수가 이달의 수상자로 선정됐다.
레이저를 이용한 초정밀 거리 측정기술은 비접촉, 비파괴 등의 장점을 앞세워 중력파 검출부터 산업용 센서까지 다양한 분야에서 활약해 왔다. 하지만 대표적인 레이저 측정기술 중 하나인 펄스비행시간(time-of-flight, TOF) 기술은 긴 거리 측정은 가능하지만 분해능이 떨어지며, 레이저 간섭계 기술은 분해능은 우수하지만 측정 범위가 마이크로미터에 불과하다. 또한 두 기술 모두 측정 속도가 느리며, 거리·분해능·시간 중 한 가지 성능을 향상하면 나머지 성능이 저하되는 한계가 있었다.
김 교수는 레이저에서 발생한 빛 펄스와 광다이오드로 생성한 전류 펄스사이의 시간 차가 100 아토초(10-16초, 1경분의 1초) 이하로 작다는 사실을 발견하고, 전광샘플링하는 방법으로 한 번에 여러 지점을 동시 측정할 수 있는 독창적인 초고속·초정밀·다기능 TOF센서를 개발했다. 측정속도 100메가헤르츠(1초에1억번 진동), 분해능 180피코미터(55억분의 1미터), 동적범위 150데시벨의 성능으로 기존 TOF와 간섭계 기술의 한계를 동시에 극복했다는 평이다. 연구결과는 네이처 포토닉스(Nature Photonics) 2020년 2월 10일자에 게재됐다.
김정원 교수는 "함께 열정적으로 연구한 대학원생들과 연구에 전념할 수 있는 환경을 만들어준 학교에 감사드린다"라며 "향후 마이크로 소자 내에서의 역학현상 탐구나 첨단제조를 위한 초정밀 형상측정 등 새롭고 다양한 기계·제조 분야에서 활용이 기대된다"라고 수상 소감을 밝혔다.
2020.10.08
조회수 22387
-
 생명과학과 조원기 교수, 서경배과학재단 2020년 신진과학자 선정
우리 대학 생명과학과 조원기 교수가 서경배과학재단 2020년 신진 과학자로 선정됐다.
아모레퍼시픽그룹 서경배 회장은 2016년 사재 3000억원을 출연해 서경배과학재단을 설립했다. 재단은 '생명과학 연구자의 혁신적인 발견을 지원해 인류에 공헌한다'는 비전 아래 매년 국내외 생명과학분야에서 새로운 연구 영역을 개척하고 있는 한국인 신진 과학자를 선정하고 있다.
서경배과학재단은 2017년부터 올해까지 17명의 생명과학분야 신진 과학자를 선정했으며, 이들에게는 1인당 매년 최대 5억원을 5년 동안 지급해 총 425억원의 연구비를 지원한다.
서 이사장은 “오랜 기간 많은 분들의 관심과 사랑을 받아왔다”며 “생명과학·바이오 분야를 장기적으로 지원해 인류에 공헌하는 것이 제가 받은 사랑을 사회에 환원할 수 있는 방법”이라고 밝히며 서경배과학재단을 통한 장기적 지원을 다짐했다.
올해는 1월 연구제안서 공모를 시작해 임용 5년 미만의 생명과학분야 신진 과학자에게 총 67건의 연구제안서를 접수받았다. 국내외 석학으로 구성된 심사위원단은 본 심사에 오른 20개 제안서를 7월까지 서면 심사하고 9월에는 12개 제안서의 발표 평가를 통해 최종 3명을 선정했다.
이에 우리 대학 조원기 교수는 살아있는 단일 세포핵 내에서 초고해상도 이미징을 통해 시시각각으로 변화하는 염색질의 단위체들과 핵내 구조체들의 4차원 상호작용을 실시간으로 관찰할 수 있는 연구를 제안했다. 이 연구는 생물학 연구의 오랜 숙제인 전사 조절 과정에 대한 이해를 크게 높일 수 있는 것으로 평가받았다.
조원기 교수와 함께 선정된 서울대학교 노성훈 교수는 현대 구조생물학 연구방법의 한계 극복을 위해 초저온 전자현미경(Cryo-EM) 기반 세포 및 분자 이미징 플랫폼을 개발하고 이를 통해 세포 노화와 질병 발생 기전을 연구하는 선도적인 주제를 제안했다. 또한 함께 선정된 캠브리지대학교 이주현 교수는 폐섬유화증 환자로부터 만들어낸 폐 오가노이드(유사 장기) 모델을 이용해 만성 폐질환으로 손상된 폐 재생 복구 기작을 이해하고자 하는 도전적이고 혁신적인 연구를 보여줬다.
앞서 뽑힌 우리 대학 과학자들의 연구성과도 국내외 학계에서 주목 받고 있다. 특히 코로나19 등 감염병 예방·치료에 기여한 정인경 교수(생명과학과, 2018년 선정)와 주영석 교수(의과학대학원, 2018년 선정)의 연구는 서경배과학재단이 강조하는 공익을 위한 생명과학분야 지원의 중요성을 다시 한 번 확인시켰다.
생명과학과 조원기 교수, 서경배과학재단 2020년 신진과학자 선정
우리 대학 생명과학과 조원기 교수가 서경배과학재단 2020년 신진 과학자로 선정됐다.
아모레퍼시픽그룹 서경배 회장은 2016년 사재 3000억원을 출연해 서경배과학재단을 설립했다. 재단은 '생명과학 연구자의 혁신적인 발견을 지원해 인류에 공헌한다'는 비전 아래 매년 국내외 생명과학분야에서 새로운 연구 영역을 개척하고 있는 한국인 신진 과학자를 선정하고 있다.
서경배과학재단은 2017년부터 올해까지 17명의 생명과학분야 신진 과학자를 선정했으며, 이들에게는 1인당 매년 최대 5억원을 5년 동안 지급해 총 425억원의 연구비를 지원한다.
서 이사장은 “오랜 기간 많은 분들의 관심과 사랑을 받아왔다”며 “생명과학·바이오 분야를 장기적으로 지원해 인류에 공헌하는 것이 제가 받은 사랑을 사회에 환원할 수 있는 방법”이라고 밝히며 서경배과학재단을 통한 장기적 지원을 다짐했다.
올해는 1월 연구제안서 공모를 시작해 임용 5년 미만의 생명과학분야 신진 과학자에게 총 67건의 연구제안서를 접수받았다. 국내외 석학으로 구성된 심사위원단은 본 심사에 오른 20개 제안서를 7월까지 서면 심사하고 9월에는 12개 제안서의 발표 평가를 통해 최종 3명을 선정했다.
이에 우리 대학 조원기 교수는 살아있는 단일 세포핵 내에서 초고해상도 이미징을 통해 시시각각으로 변화하는 염색질의 단위체들과 핵내 구조체들의 4차원 상호작용을 실시간으로 관찰할 수 있는 연구를 제안했다. 이 연구는 생물학 연구의 오랜 숙제인 전사 조절 과정에 대한 이해를 크게 높일 수 있는 것으로 평가받았다.
조원기 교수와 함께 선정된 서울대학교 노성훈 교수는 현대 구조생물학 연구방법의 한계 극복을 위해 초저온 전자현미경(Cryo-EM) 기반 세포 및 분자 이미징 플랫폼을 개발하고 이를 통해 세포 노화와 질병 발생 기전을 연구하는 선도적인 주제를 제안했다. 또한 함께 선정된 캠브리지대학교 이주현 교수는 폐섬유화증 환자로부터 만들어낸 폐 오가노이드(유사 장기) 모델을 이용해 만성 폐질환으로 손상된 폐 재생 복구 기작을 이해하고자 하는 도전적이고 혁신적인 연구를 보여줬다.
앞서 뽑힌 우리 대학 과학자들의 연구성과도 국내외 학계에서 주목 받고 있다. 특히 코로나19 등 감염병 예방·치료에 기여한 정인경 교수(생명과학과, 2018년 선정)와 주영석 교수(의과학대학원, 2018년 선정)의 연구는 서경배과학재단이 강조하는 공익을 위한 생명과학분야 지원의 중요성을 다시 한 번 확인시켰다.
2020.09.16
조회수 21921
-
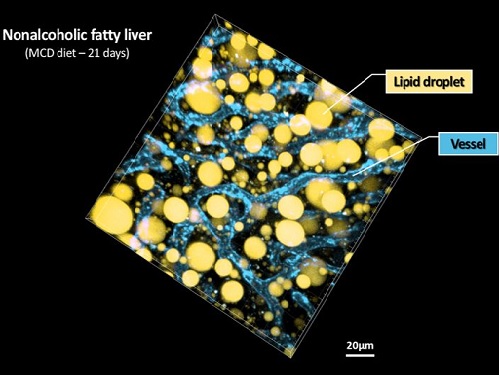 비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
2020.09.14
조회수 24002
-
 항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25
조회수 26392
-
 최재혁 교수, IEEE-IEIE가 공동 선정한 2020년 올해의 'IT 젊은 공학자상' 수상
우리 대학 전기및전자공학부 최재혁(사진) 교수가 국제전기전자학회[IEEE, 회장 토시오 후쿠다(Toshio Fukuda)]와 대한전자공학회(IEIE, 회장 임혜숙 교수·이화여대)가 공동 주관하고 해동과학문화재단(이사장 김영재)이 후원하는 'IT 젊은 공학자상' 수상자로 20일 선정됐다. 시상식은 8월 20일 오후 6시 제주 롯데호텔에서 개최됐다.
2006년부터 시작해 올해 15회째 진행되는 'IT 젊은 공학자상'은 국제전자전기학회(IEEE)와 대한전자공학회(IEIE)가 공동으로 시상하는 국제적인 상이다. 국내‧외 전문가들의 엄격한 심사를 거쳐 IT분야에서 기술과 학문 발전에 크게 기여한 만 40세 미만의 젊은 과학‧기술자를 매년 1명 선정해 시상하고 있다.
올해의 수상자로 선정된 최 교수는 5G 통신을 비롯한 초고속 통신시스템을 위한 고성능 반도체 회로 설계 분야 연구를 진행했다. 특히 차세대 유무선 통신 및 메모리 시스템의 핵심 기술로 꼽히는 '초(超)저잡음 고주파 신호 생성'분야에서 세계 최고 기술을 보유하고 있으며 SCI 저널논문 및 국제학회 논문 64편을 발표했고 25건의 국내‧국제특허를 출원 및 등록했다.
최 교수는 이와 함께 반도체회로 분야 최고 학술대회인 '국제반도체회로 학술대회 (ISSCC, International Solid-State Circuits)'와 '유럽반도체회로 학술대회(ESSCIRC, European Solid-State Circuit Conference)'의 기술프로그램위원 (Technical Program Committee)로 활동 중이며 특히 올해부터는 '국제전기전자학회 산하 반도체회로소사이어티(SSCS, IEEE Solid-State Circuit Society)'에서 `저명연구자(Distinguished Lecturer)' 선정돼 활발히 활동하고 있다.
최재혁 교수, IEEE-IEIE가 공동 선정한 2020년 올해의 'IT 젊은 공학자상' 수상
우리 대학 전기및전자공학부 최재혁(사진) 교수가 국제전기전자학회[IEEE, 회장 토시오 후쿠다(Toshio Fukuda)]와 대한전자공학회(IEIE, 회장 임혜숙 교수·이화여대)가 공동 주관하고 해동과학문화재단(이사장 김영재)이 후원하는 'IT 젊은 공학자상' 수상자로 20일 선정됐다. 시상식은 8월 20일 오후 6시 제주 롯데호텔에서 개최됐다.
2006년부터 시작해 올해 15회째 진행되는 'IT 젊은 공학자상'은 국제전자전기학회(IEEE)와 대한전자공학회(IEIE)가 공동으로 시상하는 국제적인 상이다. 국내‧외 전문가들의 엄격한 심사를 거쳐 IT분야에서 기술과 학문 발전에 크게 기여한 만 40세 미만의 젊은 과학‧기술자를 매년 1명 선정해 시상하고 있다.
올해의 수상자로 선정된 최 교수는 5G 통신을 비롯한 초고속 통신시스템을 위한 고성능 반도체 회로 설계 분야 연구를 진행했다. 특히 차세대 유무선 통신 및 메모리 시스템의 핵심 기술로 꼽히는 '초(超)저잡음 고주파 신호 생성'분야에서 세계 최고 기술을 보유하고 있으며 SCI 저널논문 및 국제학회 논문 64편을 발표했고 25건의 국내‧국제특허를 출원 및 등록했다.
최 교수는 이와 함께 반도체회로 분야 최고 학술대회인 '국제반도체회로 학술대회 (ISSCC, International Solid-State Circuits)'와 '유럽반도체회로 학술대회(ESSCIRC, European Solid-State Circuit Conference)'의 기술프로그램위원 (Technical Program Committee)로 활동 중이며 특히 올해부터는 '국제전기전자학회 산하 반도체회로소사이어티(SSCS, IEEE Solid-State Circuit Society)'에서 `저명연구자(Distinguished Lecturer)' 선정돼 활발히 활동하고 있다.
2020.08.23
조회수 20914
-
 6G 테라헤르츠 기술 선도를 위한 LG전자, KRISS와 R&D 협력 MoU
우리 대학이 LG전자, 한국표준과학연구원(KRISS)와 함께 차세대 이동통신 개발에 발 빠르게 대응한다.
우리 대학은 12일 대전 유성구에 위치한 한국표준과학연구원에서 LG-KAIST 6G 연구센터 조동호 센터장, 한국표준과학연구원 박현민 원장, LG전자 C&M표준연구소 김병훈 소장 등이 참석한 가운데 3자 업무협약(MOU)을 맺었다.
이번 협약으로 참여기관 3곳은 6G 기술에 대한 원천기술 개발부터 기술 검증까지 6G 연구개발 프로세스를 구축하는 계기를 마련했다.
협약 참여기관은 올해 하반기부터 6G 테라헤르츠(THz)와 관련한 원천 기술 개발, 기술 검증, 인프라 구축 및 운영, 주파수 발굴, 채널 특성 분석 등을 진행해 글로벌 기술 리더십을 확보할 계획이다.
6G는 2029년 상용화가 예상되는 차세대 이동통신 기술로 6G 시대에는 사람, 사물, 공간 등이 유기적으로 연결된 만물지능인터넷(AloE: Ambient IoE) 환경이 인공지능(AI)과 결합, 조성될 것으로 예상된다.
테라헤르츠 무선 송수신 기술은 6G 이동통신의 핵심이다. 이 기술은 0.1 테라헤르츠에서 수(數) 테라헤르츠에 이르는 주파수 대역을 활용하여 초당 최대 1테라비트(1Tbps)의 데이터 전송 속도를 가능하게 하는 기술이다.
앞서 우리 대학은 지난해 1월 LG전자와 LG-KAIST 6G 연구센터를 국내 최초로 설립하고 6G 이동통신 핵심 기술에 대한 선행 연구, 개발 등을 진행하고 있다. 특히 LG-KAIST 6G 연구센터는 현재까지 테라헤르츠 무선 송수신 원천 기술을 포함해 다수의 6G 핵심 기술 개발을 추진하고 있다.
조동호 센터장은 “우리나라가 5G 세계 최초 상용화에 이어 6G 이동통신의 연구개발을 주도하기 위해 국내 최고 산학연 기관들이 모여 4차 산업혁명 후 미래사회 인프라의 불확실성을 최소화하고 미래산업을 위한 기술 초석을 마련하는 것은 큰 의미가 있을 것”이라고 말했다.
한편 한국표준과학연구원은 1975년 설립된 국가측정표준 기관이다. 통신, 반도체, 자동차 등 국가 주력산업의 제품 품질 향상에 공헌하고 있다. 특히 연구원 내 전자파 표준그룹은 전자파 전 분야 측정표준을 확립해 국내외에 보급하고 있다. 또 6G 테라헤르츠에 활용될 220 GHz까지 주파수 대역의 원천 측정기술, 기술 검증 인프라 등을 확보하고 있다.
한국표준과학연구원 박현민 원장은 “한국표준과학연구원에서 개발하는 전자파분야 원천 측정기술이 우리나라 기업의 6G 연구개발 분야 글로벌 경쟁력 확보에 초석이 되기를 바란다”며 “산학연 간 긴밀하고 지속적인 연구협력으로 국내외 측정표준 분야에서 선도적인 역할을 기대한다”고 말했다.
LG전자 C&M표준연구소 김병훈 소장은 “차세대 이동통신 기술 선점 경쟁이 치열하다. LG전자는 이번 협약을 통해 6G 핵심 후보 기술인 테라헤르츠 무선 송수신에 대한 연구를 고도화 하고 글로벌 기술 리더십을 견고하게 구축하길 기대한다”며 “협약 기관들의 역량 강화를 넘어 국가 기술 경쟁력의 강화와 연구개발 협력 활성화에 기여하도록 노력해 나가겠다”고 강조했다.
6G 테라헤르츠 기술 선도를 위한 LG전자, KRISS와 R&D 협력 MoU
우리 대학이 LG전자, 한국표준과학연구원(KRISS)와 함께 차세대 이동통신 개발에 발 빠르게 대응한다.
우리 대학은 12일 대전 유성구에 위치한 한국표준과학연구원에서 LG-KAIST 6G 연구센터 조동호 센터장, 한국표준과학연구원 박현민 원장, LG전자 C&M표준연구소 김병훈 소장 등이 참석한 가운데 3자 업무협약(MOU)을 맺었다.
이번 협약으로 참여기관 3곳은 6G 기술에 대한 원천기술 개발부터 기술 검증까지 6G 연구개발 프로세스를 구축하는 계기를 마련했다.
협약 참여기관은 올해 하반기부터 6G 테라헤르츠(THz)와 관련한 원천 기술 개발, 기술 검증, 인프라 구축 및 운영, 주파수 발굴, 채널 특성 분석 등을 진행해 글로벌 기술 리더십을 확보할 계획이다.
6G는 2029년 상용화가 예상되는 차세대 이동통신 기술로 6G 시대에는 사람, 사물, 공간 등이 유기적으로 연결된 만물지능인터넷(AloE: Ambient IoE) 환경이 인공지능(AI)과 결합, 조성될 것으로 예상된다.
테라헤르츠 무선 송수신 기술은 6G 이동통신의 핵심이다. 이 기술은 0.1 테라헤르츠에서 수(數) 테라헤르츠에 이르는 주파수 대역을 활용하여 초당 최대 1테라비트(1Tbps)의 데이터 전송 속도를 가능하게 하는 기술이다.
앞서 우리 대학은 지난해 1월 LG전자와 LG-KAIST 6G 연구센터를 국내 최초로 설립하고 6G 이동통신 핵심 기술에 대한 선행 연구, 개발 등을 진행하고 있다. 특히 LG-KAIST 6G 연구센터는 현재까지 테라헤르츠 무선 송수신 원천 기술을 포함해 다수의 6G 핵심 기술 개발을 추진하고 있다.
조동호 센터장은 “우리나라가 5G 세계 최초 상용화에 이어 6G 이동통신의 연구개발을 주도하기 위해 국내 최고 산학연 기관들이 모여 4차 산업혁명 후 미래사회 인프라의 불확실성을 최소화하고 미래산업을 위한 기술 초석을 마련하는 것은 큰 의미가 있을 것”이라고 말했다.
한편 한국표준과학연구원은 1975년 설립된 국가측정표준 기관이다. 통신, 반도체, 자동차 등 국가 주력산업의 제품 품질 향상에 공헌하고 있다. 특히 연구원 내 전자파 표준그룹은 전자파 전 분야 측정표준을 확립해 국내외에 보급하고 있다. 또 6G 테라헤르츠에 활용될 220 GHz까지 주파수 대역의 원천 측정기술, 기술 검증 인프라 등을 확보하고 있다.
한국표준과학연구원 박현민 원장은 “한국표준과학연구원에서 개발하는 전자파분야 원천 측정기술이 우리나라 기업의 6G 연구개발 분야 글로벌 경쟁력 확보에 초석이 되기를 바란다”며 “산학연 간 긴밀하고 지속적인 연구협력으로 국내외 측정표준 분야에서 선도적인 역할을 기대한다”고 말했다.
LG전자 C&M표준연구소 김병훈 소장은 “차세대 이동통신 기술 선점 경쟁이 치열하다. LG전자는 이번 협약을 통해 6G 핵심 후보 기술인 테라헤르츠 무선 송수신에 대한 연구를 고도화 하고 글로벌 기술 리더십을 견고하게 구축하길 기대한다”며 “협약 기관들의 역량 강화를 넘어 국가 기술 경쟁력의 강화와 연구개발 협력 활성화에 기여하도록 노력해 나가겠다”고 강조했다.
2020.08.13
조회수 19473
-
 이수영 광원산업 회장, 노벨상 연구 지원 위해 676억 원 기부
"KAIST에서 우리나라 최초의 과학 분야 노벨상 수상자가 반드시 나와야 합니다ˮ
이수영 회장(83세·現 KAIST 발전재단 이사장, 광원산업 회장)이 23일 오후 2시 우리 대학 학술문화관(E9) 스카이라운지에서 열린 기부 약정식을 통해 평생을 일궈 모은 676억 원 상당의 부동산을 출연해 `이수영 과학교육재단'을 설립하기로 했다.
이수영 과학교육재단'의 수익금은 'KAIST 싱귤래러티(Singularity) 교수' 지원을 통한 노벨상 연구 기금으로 사용된다. 이번 이 회장의 기부는 지난 2012년 미국의 80억여 원 상당의 부동산과 2016년 또 한 차례에 걸쳐 10억여 원 상당의 미국 부동산을 유증한 것에 이은 세 번째 기부로 총 기부액은 KAIST 개교 이래 최고액인 766억 원을 기록했다.
지난 2012년 첫 기부를 시작으로 KAIST와 인연을 맺은 뒤, 이듬해인 2013년부터 현재까지 발전재단 이사장으로 재임 중인 이수영 광원산업 회장은 "오랫동안 가까운 자리에서 지켜본 결과 KAIST는 우리나라 발전은 물론 인류와 사회에 공헌할 수 있는 최고의 대학이라는 믿음을 갖게 되었다ˮ라고 기부 배경을 밝혔다.
이 회장은 이어 "우리나라 대표기업인 삼성전자의 경우 반도체 석·박사 연구인력의 25%가 KAIST 출신ˮ이라며 "2019년 314조 원의 매출로 국내 GDP의 16.4%를 차지할 정도로 국가 경제 성장에 가장 크게 기여하고 있는 삼성전자를 세계적인 기업으로 성장시킬 수 있었던 것은 세계적인 과학기술 인재를 양성하고 있는 KAIST 덕분ˮ이라고 말했다.
이 회장은 이와 함께 "세상만사는 사람으로 시작해서 사람으로 끝나기 때문에 KAIST는 사명감을 가지고 대한민국을 이끌어나갈 영재를 키워야 한다ˮ고 강조하면서 "어느 대학도 해내지 못한 탁월한 성취를 이뤄내 대한민국의 이름을 세계에 드높이는 일에 이 기부가 뜻깊게 활용되기를 바란다ˮ고 덧붙였다.
KAIST는 이수영 회장의 이번 기부를 바탕으로 설립되는 `이수영 과학교육재단'의 지원을 받아 `KAIST 싱귤래러티 교수'를 육성할 계획이다.
'KAIST 싱귤래러티 교수' 제도는 과학 지식의 패러다임을 바꾸거나 새로운 분야를 개척할 수 있는 교수, 인류 난제를 해결하고 독창적인 과학 지식과 이론을 정립할 수 있는 교수를 선발해 지원하는 제도다.
미래 과학기술 및 산업 발전을 선도할 혁신기술과 학문적 독창성을 창출할 수 있는 우수 연구 인력을 확보하고 기술적 특이점 도래에 대비하기 위해 장기간의 연구 수행을 지원하는 것이 특징이다. KAIST는 '이수영 과학교육재단' 지원으로 세계 최정상급 과학자 배출을 위한 지속 가능하고 안정적인 연구 환경을 조성하고 이를 통해 교내 연구진의 노벨상 수상 가능성을 높이겠다는 계획이다.
싱귤래러티 교수로 선정되면 10년간의 임용기간 동안 연구비를 지원받고, 논문·특허 중심의 연차 실적 평가가 유예된다. 임용기간 종료 시 연구 진행 과정 및 특이점 기술 역량 확보 등 평가에 따라 지원 기간을 추가로 10년까지 연장할 수 있다.
이수영 회장은 "우리나라의 미래를 위해 가진 것을 나눌 수 있어서 기쁘다ˮ고 기부 소감을 밝히면서 "대한민국의 미래와 나라를 위하는 뜻을 가진 분들이 기부 문화 활성화를 위해 더 많이 동참해주기를 바란다ˮ고 당부했다.
KAIST 신성철 총장은 "평생의 피땀으로 일궈낸 재산을 아낌없이 내놓은 이수영 회장님의 결단에 경의를 표한다ˮ라고 감사 인사를 전하면서 "대한민국의 과학기술 발전을 이끌고 있는 KAIST의 역할과 임무에 대한 사명감을 항상 마음에 새기고 이수영 이사장님의 뜻을 반드시 이룰 수 있도록 모든 구성원들이 최선을 다할 것ˮ이라고 밝혔다.
이수영 KAIST 발전재단 이사장은 경기여고와 서울대 법대를 졸업하고 1963년 서울신문에 입사해 기자 생활을 시작했다. 1980년까지 한국경제신문과 서울경제신문 등의 언론사에서 취재 현장을 누볐다. 기자로 재직하던 시절인 1971년에 광원목장을 설립해 축산업을 시작했고, 1988년 부동산 전문기업인 광원산업을 창업해 현재까지 회장을 맡고 있다. 2012년 KAIST 명예박사를 받았으며, 2018년에는 국민훈장 목련장을 수훈했다.
한편, KAIST에는 그간 이수영 이사장을 포함해 대한민국 1호 한의학박사인 故 류근철 박사(578억 원), 정문술 前 미래산업 회장(515억 원), 김병호 前 서전농업 회장(350억 원), 故 김영한 여사(340억 원) 등의 기부자들이 KAIST에 고액의 발전기금을 기탁했다.
이수영 광원산업 회장, 노벨상 연구 지원 위해 676억 원 기부
"KAIST에서 우리나라 최초의 과학 분야 노벨상 수상자가 반드시 나와야 합니다ˮ
이수영 회장(83세·現 KAIST 발전재단 이사장, 광원산업 회장)이 23일 오후 2시 우리 대학 학술문화관(E9) 스카이라운지에서 열린 기부 약정식을 통해 평생을 일궈 모은 676억 원 상당의 부동산을 출연해 `이수영 과학교육재단'을 설립하기로 했다.
이수영 과학교육재단'의 수익금은 'KAIST 싱귤래러티(Singularity) 교수' 지원을 통한 노벨상 연구 기금으로 사용된다. 이번 이 회장의 기부는 지난 2012년 미국의 80억여 원 상당의 부동산과 2016년 또 한 차례에 걸쳐 10억여 원 상당의 미국 부동산을 유증한 것에 이은 세 번째 기부로 총 기부액은 KAIST 개교 이래 최고액인 766억 원을 기록했다.
지난 2012년 첫 기부를 시작으로 KAIST와 인연을 맺은 뒤, 이듬해인 2013년부터 현재까지 발전재단 이사장으로 재임 중인 이수영 광원산업 회장은 "오랫동안 가까운 자리에서 지켜본 결과 KAIST는 우리나라 발전은 물론 인류와 사회에 공헌할 수 있는 최고의 대학이라는 믿음을 갖게 되었다ˮ라고 기부 배경을 밝혔다.
이 회장은 이어 "우리나라 대표기업인 삼성전자의 경우 반도체 석·박사 연구인력의 25%가 KAIST 출신ˮ이라며 "2019년 314조 원의 매출로 국내 GDP의 16.4%를 차지할 정도로 국가 경제 성장에 가장 크게 기여하고 있는 삼성전자를 세계적인 기업으로 성장시킬 수 있었던 것은 세계적인 과학기술 인재를 양성하고 있는 KAIST 덕분ˮ이라고 말했다.
이 회장은 이와 함께 "세상만사는 사람으로 시작해서 사람으로 끝나기 때문에 KAIST는 사명감을 가지고 대한민국을 이끌어나갈 영재를 키워야 한다ˮ고 강조하면서 "어느 대학도 해내지 못한 탁월한 성취를 이뤄내 대한민국의 이름을 세계에 드높이는 일에 이 기부가 뜻깊게 활용되기를 바란다ˮ고 덧붙였다.
KAIST는 이수영 회장의 이번 기부를 바탕으로 설립되는 `이수영 과학교육재단'의 지원을 받아 `KAIST 싱귤래러티 교수'를 육성할 계획이다.
'KAIST 싱귤래러티 교수' 제도는 과학 지식의 패러다임을 바꾸거나 새로운 분야를 개척할 수 있는 교수, 인류 난제를 해결하고 독창적인 과학 지식과 이론을 정립할 수 있는 교수를 선발해 지원하는 제도다.
미래 과학기술 및 산업 발전을 선도할 혁신기술과 학문적 독창성을 창출할 수 있는 우수 연구 인력을 확보하고 기술적 특이점 도래에 대비하기 위해 장기간의 연구 수행을 지원하는 것이 특징이다. KAIST는 '이수영 과학교육재단' 지원으로 세계 최정상급 과학자 배출을 위한 지속 가능하고 안정적인 연구 환경을 조성하고 이를 통해 교내 연구진의 노벨상 수상 가능성을 높이겠다는 계획이다.
싱귤래러티 교수로 선정되면 10년간의 임용기간 동안 연구비를 지원받고, 논문·특허 중심의 연차 실적 평가가 유예된다. 임용기간 종료 시 연구 진행 과정 및 특이점 기술 역량 확보 등 평가에 따라 지원 기간을 추가로 10년까지 연장할 수 있다.
이수영 회장은 "우리나라의 미래를 위해 가진 것을 나눌 수 있어서 기쁘다ˮ고 기부 소감을 밝히면서 "대한민국의 미래와 나라를 위하는 뜻을 가진 분들이 기부 문화 활성화를 위해 더 많이 동참해주기를 바란다ˮ고 당부했다.
KAIST 신성철 총장은 "평생의 피땀으로 일궈낸 재산을 아낌없이 내놓은 이수영 회장님의 결단에 경의를 표한다ˮ라고 감사 인사를 전하면서 "대한민국의 과학기술 발전을 이끌고 있는 KAIST의 역할과 임무에 대한 사명감을 항상 마음에 새기고 이수영 이사장님의 뜻을 반드시 이룰 수 있도록 모든 구성원들이 최선을 다할 것ˮ이라고 밝혔다.
이수영 KAIST 발전재단 이사장은 경기여고와 서울대 법대를 졸업하고 1963년 서울신문에 입사해 기자 생활을 시작했다. 1980년까지 한국경제신문과 서울경제신문 등의 언론사에서 취재 현장을 누볐다. 기자로 재직하던 시절인 1971년에 광원목장을 설립해 축산업을 시작했고, 1988년 부동산 전문기업인 광원산업을 창업해 현재까지 회장을 맡고 있다. 2012년 KAIST 명예박사를 받았으며, 2018년에는 국민훈장 목련장을 수훈했다.
한편, KAIST에는 그간 이수영 이사장을 포함해 대한민국 1호 한의학박사인 故 류근철 박사(578억 원), 정문술 前 미래산업 회장(515억 원), 김병호 前 서전농업 회장(350억 원), 故 김영한 여사(340억 원) 등의 기부자들이 KAIST에 고액의 발전기금을 기탁했다.
2020.07.23
조회수 24728
-
 중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14
조회수 24926
-
 이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
2020.07.09
조회수 20524
-
 단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
2020.07.09
조회수 19788
-
 김종환 교수, 제33회 정보문화의달 기념 유공자 대통령 표창 수상
우리 대학 전기및전자공학부 김종환 교수는 지난 6월 22일, 과학기술정보통신부와 한국정보화진흥원이 개최한 「제33회 정보문화의 달」 기념식에서 2020년 정보문화 유공 정부포상 '대통령 표창'을 수상하였다.
본 포상은 디지털 정보격차 해소, 디지털 역기능 대응 등에 기여한 유공자를 발굴·포상하여 디지털 포용사회 구현과 정보문화 창달에 기여한 자에게 수상되는 상으로, KAIST에 부임한 이래로 '로봇축구와 국제로봇올림피아드 및 AI 월드컵'을 창시하여 정보화 수준 향상과 건전정보문화 조성 및 디지털 정보격차 해소에 기여한 점을 높이 평가받아 수상하게 되었다.
'디지털로 하나 되는 대한민국, 다 함께 누리는 디지털 포용세상'을 주제로 열린 본 행사에는 최기영 과기정통부 장관, 허욱 방송통신위원회 상임위원 등이 참석하였다.
김종환 교수, 제33회 정보문화의달 기념 유공자 대통령 표창 수상
우리 대학 전기및전자공학부 김종환 교수는 지난 6월 22일, 과학기술정보통신부와 한국정보화진흥원이 개최한 「제33회 정보문화의 달」 기념식에서 2020년 정보문화 유공 정부포상 '대통령 표창'을 수상하였다.
본 포상은 디지털 정보격차 해소, 디지털 역기능 대응 등에 기여한 유공자를 발굴·포상하여 디지털 포용사회 구현과 정보문화 창달에 기여한 자에게 수상되는 상으로, KAIST에 부임한 이래로 '로봇축구와 국제로봇올림피아드 및 AI 월드컵'을 창시하여 정보화 수준 향상과 건전정보문화 조성 및 디지털 정보격차 해소에 기여한 점을 높이 평가받아 수상하게 되었다.
'디지털로 하나 되는 대한민국, 다 함께 누리는 디지털 포용세상'을 주제로 열린 본 행사에는 최기영 과기정통부 장관, 허욱 방송통신위원회 상임위원 등이 참석하였다.
2020.07.02
조회수 18254
-
 문수복 교수, 국가과학기술자문회의 심의위원 선임
우리대학 전산학부 문수복 교수가 국가과학기술자문회의 제3기 심의위원으로 선임됐다.
국가과학기술자문회의는 국가기술 정책의 기본 방향과 주요 의제에 대한 정책 자문을 수행하는 헌법기구로서 대통령이 의장을 맡는다. 문 교수는 김인수 광주과학기술원(GIST) 지구환경공학부 교수, 윤희숙 재료연구소 실장, 이정원 과학기술정책연구원(STEPI) 선임 연구위원, 조정우 SK바이오팜 대표이사와 함께 현 정부 3기 심의위원으로 위촉됐다.
국가과학기술자문회의는 “과학기술 분야에서의 전문성 및 연구성과, 정책경험, 산·학·연 구성 비율 등 요소를 고려해 선정했다”며 선정 이유를 밝혔으며, 임기는 이달 27일부터 내년 6월 26일까지 1년이다.
문수복 교수, 국가과학기술자문회의 심의위원 선임
우리대학 전산학부 문수복 교수가 국가과학기술자문회의 제3기 심의위원으로 선임됐다.
국가과학기술자문회의는 국가기술 정책의 기본 방향과 주요 의제에 대한 정책 자문을 수행하는 헌법기구로서 대통령이 의장을 맡는다. 문 교수는 김인수 광주과학기술원(GIST) 지구환경공학부 교수, 윤희숙 재료연구소 실장, 이정원 과학기술정책연구원(STEPI) 선임 연구위원, 조정우 SK바이오팜 대표이사와 함께 현 정부 3기 심의위원으로 위촉됐다.
국가과학기술자문회의는 “과학기술 분야에서의 전문성 및 연구성과, 정책경험, 산·학·연 구성 비율 등 요소를 고려해 선정했다”며 선정 이유를 밝혔으며, 임기는 이달 27일부터 내년 6월 26일까지 1년이다.
2020.06.29
조회수 16872
 김정원 교수, 이달의 과학기술인상 10월 수상자 선정
우리 대학 기계공학과 김정원 교수가 이달의 과학기술인상 10월 수상자에 선정됐다.
과학기술정보통신부와 한국연구재단은 김정원 교수가 초고속, 고분해능, 다기능성 센서기술을 개발하여 기초정밀 공학의 지평을 넓힌 공로를 높이 평가했다고 선정 배경을 설명했다.
'이달의 과학기술인상'은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구개발자를 매월 1명씩 선정해 과기정통부 장관상과 상금 1천만 원을 수여하는 상이다. 세종대왕이 길이와 부피의 측정체계를 확립한 10월 26일을 기념하는 ‘계량측정의 날’을 맞아 김정원 교수가 이달의 수상자로 선정됐다.
레이저를 이용한 초정밀 거리 측정기술은 비접촉, 비파괴 등의 장점을 앞세워 중력파 검출부터 산업용 센서까지 다양한 분야에서 활약해 왔다. 하지만 대표적인 레이저 측정기술 중 하나인 펄스비행시간(time-of-flight, TOF) 기술은 긴 거리 측정은 가능하지만 분해능이 떨어지며, 레이저 간섭계 기술은 분해능은 우수하지만 측정 범위가 마이크로미터에 불과하다. 또한 두 기술 모두 측정 속도가 느리며, 거리·분해능·시간 중 한 가지 성능을 향상하면 나머지 성능이 저하되는 한계가 있었다.
김 교수는 레이저에서 발생한 빛 펄스와 광다이오드로 생성한 전류 펄스사이의 시간 차가 100 아토초(10-16초, 1경분의 1초) 이하로 작다는 사실을 발견하고, 전광샘플링하는 방법으로 한 번에 여러 지점을 동시 측정할 수 있는 독창적인 초고속·초정밀·다기능 TOF센서를 개발했다. 측정속도 100메가헤르츠(1초에1억번 진동), 분해능 180피코미터(55억분의 1미터), 동적범위 150데시벨의 성능으로 기존 TOF와 간섭계 기술의 한계를 동시에 극복했다는 평이다. 연구결과는 네이처 포토닉스(Nature Photonics) 2020년 2월 10일자에 게재됐다.
김정원 교수는 "함께 열정적으로 연구한 대학원생들과 연구에 전념할 수 있는 환경을 만들어준 학교에 감사드린다"라며 "향후 마이크로 소자 내에서의 역학현상 탐구나 첨단제조를 위한 초정밀 형상측정 등 새롭고 다양한 기계·제조 분야에서 활용이 기대된다"라고 수상 소감을 밝혔다.
2020.10.08 조회수 22387
김정원 교수, 이달의 과학기술인상 10월 수상자 선정
우리 대학 기계공학과 김정원 교수가 이달의 과학기술인상 10월 수상자에 선정됐다.
과학기술정보통신부와 한국연구재단은 김정원 교수가 초고속, 고분해능, 다기능성 센서기술을 개발하여 기초정밀 공학의 지평을 넓힌 공로를 높이 평가했다고 선정 배경을 설명했다.
'이달의 과학기술인상'은 우수한 연구개발 성과로 과학기술 발전에 공헌한 연구개발자를 매월 1명씩 선정해 과기정통부 장관상과 상금 1천만 원을 수여하는 상이다. 세종대왕이 길이와 부피의 측정체계를 확립한 10월 26일을 기념하는 ‘계량측정의 날’을 맞아 김정원 교수가 이달의 수상자로 선정됐다.
레이저를 이용한 초정밀 거리 측정기술은 비접촉, 비파괴 등의 장점을 앞세워 중력파 검출부터 산업용 센서까지 다양한 분야에서 활약해 왔다. 하지만 대표적인 레이저 측정기술 중 하나인 펄스비행시간(time-of-flight, TOF) 기술은 긴 거리 측정은 가능하지만 분해능이 떨어지며, 레이저 간섭계 기술은 분해능은 우수하지만 측정 범위가 마이크로미터에 불과하다. 또한 두 기술 모두 측정 속도가 느리며, 거리·분해능·시간 중 한 가지 성능을 향상하면 나머지 성능이 저하되는 한계가 있었다.
김 교수는 레이저에서 발생한 빛 펄스와 광다이오드로 생성한 전류 펄스사이의 시간 차가 100 아토초(10-16초, 1경분의 1초) 이하로 작다는 사실을 발견하고, 전광샘플링하는 방법으로 한 번에 여러 지점을 동시 측정할 수 있는 독창적인 초고속·초정밀·다기능 TOF센서를 개발했다. 측정속도 100메가헤르츠(1초에1억번 진동), 분해능 180피코미터(55억분의 1미터), 동적범위 150데시벨의 성능으로 기존 TOF와 간섭계 기술의 한계를 동시에 극복했다는 평이다. 연구결과는 네이처 포토닉스(Nature Photonics) 2020년 2월 10일자에 게재됐다.
김정원 교수는 "함께 열정적으로 연구한 대학원생들과 연구에 전념할 수 있는 환경을 만들어준 학교에 감사드린다"라며 "향후 마이크로 소자 내에서의 역학현상 탐구나 첨단제조를 위한 초정밀 형상측정 등 새롭고 다양한 기계·제조 분야에서 활용이 기대된다"라고 수상 소감을 밝혔다.
2020.10.08 조회수 22387 생명과학과 조원기 교수, 서경배과학재단 2020년 신진과학자 선정
우리 대학 생명과학과 조원기 교수가 서경배과학재단 2020년 신진 과학자로 선정됐다.
아모레퍼시픽그룹 서경배 회장은 2016년 사재 3000억원을 출연해 서경배과학재단을 설립했다. 재단은 '생명과학 연구자의 혁신적인 발견을 지원해 인류에 공헌한다'는 비전 아래 매년 국내외 생명과학분야에서 새로운 연구 영역을 개척하고 있는 한국인 신진 과학자를 선정하고 있다.
서경배과학재단은 2017년부터 올해까지 17명의 생명과학분야 신진 과학자를 선정했으며, 이들에게는 1인당 매년 최대 5억원을 5년 동안 지급해 총 425억원의 연구비를 지원한다.
서 이사장은 “오랜 기간 많은 분들의 관심과 사랑을 받아왔다”며 “생명과학·바이오 분야를 장기적으로 지원해 인류에 공헌하는 것이 제가 받은 사랑을 사회에 환원할 수 있는 방법”이라고 밝히며 서경배과학재단을 통한 장기적 지원을 다짐했다.
올해는 1월 연구제안서 공모를 시작해 임용 5년 미만의 생명과학분야 신진 과학자에게 총 67건의 연구제안서를 접수받았다. 국내외 석학으로 구성된 심사위원단은 본 심사에 오른 20개 제안서를 7월까지 서면 심사하고 9월에는 12개 제안서의 발표 평가를 통해 최종 3명을 선정했다.
이에 우리 대학 조원기 교수는 살아있는 단일 세포핵 내에서 초고해상도 이미징을 통해 시시각각으로 변화하는 염색질의 단위체들과 핵내 구조체들의 4차원 상호작용을 실시간으로 관찰할 수 있는 연구를 제안했다. 이 연구는 생물학 연구의 오랜 숙제인 전사 조절 과정에 대한 이해를 크게 높일 수 있는 것으로 평가받았다.
조원기 교수와 함께 선정된 서울대학교 노성훈 교수는 현대 구조생물학 연구방법의 한계 극복을 위해 초저온 전자현미경(Cryo-EM) 기반 세포 및 분자 이미징 플랫폼을 개발하고 이를 통해 세포 노화와 질병 발생 기전을 연구하는 선도적인 주제를 제안했다. 또한 함께 선정된 캠브리지대학교 이주현 교수는 폐섬유화증 환자로부터 만들어낸 폐 오가노이드(유사 장기) 모델을 이용해 만성 폐질환으로 손상된 폐 재생 복구 기작을 이해하고자 하는 도전적이고 혁신적인 연구를 보여줬다.
앞서 뽑힌 우리 대학 과학자들의 연구성과도 국내외 학계에서 주목 받고 있다. 특히 코로나19 등 감염병 예방·치료에 기여한 정인경 교수(생명과학과, 2018년 선정)와 주영석 교수(의과학대학원, 2018년 선정)의 연구는 서경배과학재단이 강조하는 공익을 위한 생명과학분야 지원의 중요성을 다시 한 번 확인시켰다.
2020.09.16 조회수 21921
생명과학과 조원기 교수, 서경배과학재단 2020년 신진과학자 선정
우리 대학 생명과학과 조원기 교수가 서경배과학재단 2020년 신진 과학자로 선정됐다.
아모레퍼시픽그룹 서경배 회장은 2016년 사재 3000억원을 출연해 서경배과학재단을 설립했다. 재단은 '생명과학 연구자의 혁신적인 발견을 지원해 인류에 공헌한다'는 비전 아래 매년 국내외 생명과학분야에서 새로운 연구 영역을 개척하고 있는 한국인 신진 과학자를 선정하고 있다.
서경배과학재단은 2017년부터 올해까지 17명의 생명과학분야 신진 과학자를 선정했으며, 이들에게는 1인당 매년 최대 5억원을 5년 동안 지급해 총 425억원의 연구비를 지원한다.
서 이사장은 “오랜 기간 많은 분들의 관심과 사랑을 받아왔다”며 “생명과학·바이오 분야를 장기적으로 지원해 인류에 공헌하는 것이 제가 받은 사랑을 사회에 환원할 수 있는 방법”이라고 밝히며 서경배과학재단을 통한 장기적 지원을 다짐했다.
올해는 1월 연구제안서 공모를 시작해 임용 5년 미만의 생명과학분야 신진 과학자에게 총 67건의 연구제안서를 접수받았다. 국내외 석학으로 구성된 심사위원단은 본 심사에 오른 20개 제안서를 7월까지 서면 심사하고 9월에는 12개 제안서의 발표 평가를 통해 최종 3명을 선정했다.
이에 우리 대학 조원기 교수는 살아있는 단일 세포핵 내에서 초고해상도 이미징을 통해 시시각각으로 변화하는 염색질의 단위체들과 핵내 구조체들의 4차원 상호작용을 실시간으로 관찰할 수 있는 연구를 제안했다. 이 연구는 생물학 연구의 오랜 숙제인 전사 조절 과정에 대한 이해를 크게 높일 수 있는 것으로 평가받았다.
조원기 교수와 함께 선정된 서울대학교 노성훈 교수는 현대 구조생물학 연구방법의 한계 극복을 위해 초저온 전자현미경(Cryo-EM) 기반 세포 및 분자 이미징 플랫폼을 개발하고 이를 통해 세포 노화와 질병 발생 기전을 연구하는 선도적인 주제를 제안했다. 또한 함께 선정된 캠브리지대학교 이주현 교수는 폐섬유화증 환자로부터 만들어낸 폐 오가노이드(유사 장기) 모델을 이용해 만성 폐질환으로 손상된 폐 재생 복구 기작을 이해하고자 하는 도전적이고 혁신적인 연구를 보여줬다.
앞서 뽑힌 우리 대학 과학자들의 연구성과도 국내외 학계에서 주목 받고 있다. 특히 코로나19 등 감염병 예방·치료에 기여한 정인경 교수(생명과학과, 2018년 선정)와 주영석 교수(의과학대학원, 2018년 선정)의 연구는 서경배과학재단이 강조하는 공익을 위한 생명과학분야 지원의 중요성을 다시 한 번 확인시켰다.
2020.09.16 조회수 21921 비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
2020.09.14 조회수 24002
비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
2020.09.14 조회수 24002 항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25 조회수 26392
항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25 조회수 26392 최재혁 교수, IEEE-IEIE가 공동 선정한 2020년 올해의 'IT 젊은 공학자상' 수상
우리 대학 전기및전자공학부 최재혁(사진) 교수가 국제전기전자학회[IEEE, 회장 토시오 후쿠다(Toshio Fukuda)]와 대한전자공학회(IEIE, 회장 임혜숙 교수·이화여대)가 공동 주관하고 해동과학문화재단(이사장 김영재)이 후원하는 'IT 젊은 공학자상' 수상자로 20일 선정됐다. 시상식은 8월 20일 오후 6시 제주 롯데호텔에서 개최됐다.
2006년부터 시작해 올해 15회째 진행되는 'IT 젊은 공학자상'은 국제전자전기학회(IEEE)와 대한전자공학회(IEIE)가 공동으로 시상하는 국제적인 상이다. 국내‧외 전문가들의 엄격한 심사를 거쳐 IT분야에서 기술과 학문 발전에 크게 기여한 만 40세 미만의 젊은 과학‧기술자를 매년 1명 선정해 시상하고 있다.
올해의 수상자로 선정된 최 교수는 5G 통신을 비롯한 초고속 통신시스템을 위한 고성능 반도체 회로 설계 분야 연구를 진행했다. 특히 차세대 유무선 통신 및 메모리 시스템의 핵심 기술로 꼽히는 '초(超)저잡음 고주파 신호 생성'분야에서 세계 최고 기술을 보유하고 있으며 SCI 저널논문 및 국제학회 논문 64편을 발표했고 25건의 국내‧국제특허를 출원 및 등록했다.
최 교수는 이와 함께 반도체회로 분야 최고 학술대회인 '국제반도체회로 학술대회 (ISSCC, International Solid-State Circuits)'와 '유럽반도체회로 학술대회(ESSCIRC, European Solid-State Circuit Conference)'의 기술프로그램위원 (Technical Program Committee)로 활동 중이며 특히 올해부터는 '국제전기전자학회 산하 반도체회로소사이어티(SSCS, IEEE Solid-State Circuit Society)'에서 `저명연구자(Distinguished Lecturer)' 선정돼 활발히 활동하고 있다.
2020.08.23 조회수 20914
최재혁 교수, IEEE-IEIE가 공동 선정한 2020년 올해의 'IT 젊은 공학자상' 수상
우리 대학 전기및전자공학부 최재혁(사진) 교수가 국제전기전자학회[IEEE, 회장 토시오 후쿠다(Toshio Fukuda)]와 대한전자공학회(IEIE, 회장 임혜숙 교수·이화여대)가 공동 주관하고 해동과학문화재단(이사장 김영재)이 후원하는 'IT 젊은 공학자상' 수상자로 20일 선정됐다. 시상식은 8월 20일 오후 6시 제주 롯데호텔에서 개최됐다.
2006년부터 시작해 올해 15회째 진행되는 'IT 젊은 공학자상'은 국제전자전기학회(IEEE)와 대한전자공학회(IEIE)가 공동으로 시상하는 국제적인 상이다. 국내‧외 전문가들의 엄격한 심사를 거쳐 IT분야에서 기술과 학문 발전에 크게 기여한 만 40세 미만의 젊은 과학‧기술자를 매년 1명 선정해 시상하고 있다.
올해의 수상자로 선정된 최 교수는 5G 통신을 비롯한 초고속 통신시스템을 위한 고성능 반도체 회로 설계 분야 연구를 진행했다. 특히 차세대 유무선 통신 및 메모리 시스템의 핵심 기술로 꼽히는 '초(超)저잡음 고주파 신호 생성'분야에서 세계 최고 기술을 보유하고 있으며 SCI 저널논문 및 국제학회 논문 64편을 발표했고 25건의 국내‧국제특허를 출원 및 등록했다.
최 교수는 이와 함께 반도체회로 분야 최고 학술대회인 '국제반도체회로 학술대회 (ISSCC, International Solid-State Circuits)'와 '유럽반도체회로 학술대회(ESSCIRC, European Solid-State Circuit Conference)'의 기술프로그램위원 (Technical Program Committee)로 활동 중이며 특히 올해부터는 '국제전기전자학회 산하 반도체회로소사이어티(SSCS, IEEE Solid-State Circuit Society)'에서 `저명연구자(Distinguished Lecturer)' 선정돼 활발히 활동하고 있다.
2020.08.23 조회수 20914 6G 테라헤르츠 기술 선도를 위한 LG전자, KRISS와 R&D 협력 MoU
우리 대학이 LG전자, 한국표준과학연구원(KRISS)와 함께 차세대 이동통신 개발에 발 빠르게 대응한다.
우리 대학은 12일 대전 유성구에 위치한 한국표준과학연구원에서 LG-KAIST 6G 연구센터 조동호 센터장, 한국표준과학연구원 박현민 원장, LG전자 C&M표준연구소 김병훈 소장 등이 참석한 가운데 3자 업무협약(MOU)을 맺었다.
이번 협약으로 참여기관 3곳은 6G 기술에 대한 원천기술 개발부터 기술 검증까지 6G 연구개발 프로세스를 구축하는 계기를 마련했다.
협약 참여기관은 올해 하반기부터 6G 테라헤르츠(THz)와 관련한 원천 기술 개발, 기술 검증, 인프라 구축 및 운영, 주파수 발굴, 채널 특성 분석 등을 진행해 글로벌 기술 리더십을 확보할 계획이다.
6G는 2029년 상용화가 예상되는 차세대 이동통신 기술로 6G 시대에는 사람, 사물, 공간 등이 유기적으로 연결된 만물지능인터넷(AloE: Ambient IoE) 환경이 인공지능(AI)과 결합, 조성될 것으로 예상된다.
테라헤르츠 무선 송수신 기술은 6G 이동통신의 핵심이다. 이 기술은 0.1 테라헤르츠에서 수(數) 테라헤르츠에 이르는 주파수 대역을 활용하여 초당 최대 1테라비트(1Tbps)의 데이터 전송 속도를 가능하게 하는 기술이다.
앞서 우리 대학은 지난해 1월 LG전자와 LG-KAIST 6G 연구센터를 국내 최초로 설립하고 6G 이동통신 핵심 기술에 대한 선행 연구, 개발 등을 진행하고 있다. 특히 LG-KAIST 6G 연구센터는 현재까지 테라헤르츠 무선 송수신 원천 기술을 포함해 다수의 6G 핵심 기술 개발을 추진하고 있다.
조동호 센터장은 “우리나라가 5G 세계 최초 상용화에 이어 6G 이동통신의 연구개발을 주도하기 위해 국내 최고 산학연 기관들이 모여 4차 산업혁명 후 미래사회 인프라의 불확실성을 최소화하고 미래산업을 위한 기술 초석을 마련하는 것은 큰 의미가 있을 것”이라고 말했다.
한편 한국표준과학연구원은 1975년 설립된 국가측정표준 기관이다. 통신, 반도체, 자동차 등 국가 주력산업의 제품 품질 향상에 공헌하고 있다. 특히 연구원 내 전자파 표준그룹은 전자파 전 분야 측정표준을 확립해 국내외에 보급하고 있다. 또 6G 테라헤르츠에 활용될 220 GHz까지 주파수 대역의 원천 측정기술, 기술 검증 인프라 등을 확보하고 있다.
한국표준과학연구원 박현민 원장은 “한국표준과학연구원에서 개발하는 전자파분야 원천 측정기술이 우리나라 기업의 6G 연구개발 분야 글로벌 경쟁력 확보에 초석이 되기를 바란다”며 “산학연 간 긴밀하고 지속적인 연구협력으로 국내외 측정표준 분야에서 선도적인 역할을 기대한다”고 말했다.
LG전자 C&M표준연구소 김병훈 소장은 “차세대 이동통신 기술 선점 경쟁이 치열하다. LG전자는 이번 협약을 통해 6G 핵심 후보 기술인 테라헤르츠 무선 송수신에 대한 연구를 고도화 하고 글로벌 기술 리더십을 견고하게 구축하길 기대한다”며 “협약 기관들의 역량 강화를 넘어 국가 기술 경쟁력의 강화와 연구개발 협력 활성화에 기여하도록 노력해 나가겠다”고 강조했다.
2020.08.13 조회수 19473
6G 테라헤르츠 기술 선도를 위한 LG전자, KRISS와 R&D 협력 MoU
우리 대학이 LG전자, 한국표준과학연구원(KRISS)와 함께 차세대 이동통신 개발에 발 빠르게 대응한다.
우리 대학은 12일 대전 유성구에 위치한 한국표준과학연구원에서 LG-KAIST 6G 연구센터 조동호 센터장, 한국표준과학연구원 박현민 원장, LG전자 C&M표준연구소 김병훈 소장 등이 참석한 가운데 3자 업무협약(MOU)을 맺었다.
이번 협약으로 참여기관 3곳은 6G 기술에 대한 원천기술 개발부터 기술 검증까지 6G 연구개발 프로세스를 구축하는 계기를 마련했다.
협약 참여기관은 올해 하반기부터 6G 테라헤르츠(THz)와 관련한 원천 기술 개발, 기술 검증, 인프라 구축 및 운영, 주파수 발굴, 채널 특성 분석 등을 진행해 글로벌 기술 리더십을 확보할 계획이다.
6G는 2029년 상용화가 예상되는 차세대 이동통신 기술로 6G 시대에는 사람, 사물, 공간 등이 유기적으로 연결된 만물지능인터넷(AloE: Ambient IoE) 환경이 인공지능(AI)과 결합, 조성될 것으로 예상된다.
테라헤르츠 무선 송수신 기술은 6G 이동통신의 핵심이다. 이 기술은 0.1 테라헤르츠에서 수(數) 테라헤르츠에 이르는 주파수 대역을 활용하여 초당 최대 1테라비트(1Tbps)의 데이터 전송 속도를 가능하게 하는 기술이다.
앞서 우리 대학은 지난해 1월 LG전자와 LG-KAIST 6G 연구센터를 국내 최초로 설립하고 6G 이동통신 핵심 기술에 대한 선행 연구, 개발 등을 진행하고 있다. 특히 LG-KAIST 6G 연구센터는 현재까지 테라헤르츠 무선 송수신 원천 기술을 포함해 다수의 6G 핵심 기술 개발을 추진하고 있다.
조동호 센터장은 “우리나라가 5G 세계 최초 상용화에 이어 6G 이동통신의 연구개발을 주도하기 위해 국내 최고 산학연 기관들이 모여 4차 산업혁명 후 미래사회 인프라의 불확실성을 최소화하고 미래산업을 위한 기술 초석을 마련하는 것은 큰 의미가 있을 것”이라고 말했다.
한편 한국표준과학연구원은 1975년 설립된 국가측정표준 기관이다. 통신, 반도체, 자동차 등 국가 주력산업의 제품 품질 향상에 공헌하고 있다. 특히 연구원 내 전자파 표준그룹은 전자파 전 분야 측정표준을 확립해 국내외에 보급하고 있다. 또 6G 테라헤르츠에 활용될 220 GHz까지 주파수 대역의 원천 측정기술, 기술 검증 인프라 등을 확보하고 있다.
한국표준과학연구원 박현민 원장은 “한국표준과학연구원에서 개발하는 전자파분야 원천 측정기술이 우리나라 기업의 6G 연구개발 분야 글로벌 경쟁력 확보에 초석이 되기를 바란다”며 “산학연 간 긴밀하고 지속적인 연구협력으로 국내외 측정표준 분야에서 선도적인 역할을 기대한다”고 말했다.
LG전자 C&M표준연구소 김병훈 소장은 “차세대 이동통신 기술 선점 경쟁이 치열하다. LG전자는 이번 협약을 통해 6G 핵심 후보 기술인 테라헤르츠 무선 송수신에 대한 연구를 고도화 하고 글로벌 기술 리더십을 견고하게 구축하길 기대한다”며 “협약 기관들의 역량 강화를 넘어 국가 기술 경쟁력의 강화와 연구개발 협력 활성화에 기여하도록 노력해 나가겠다”고 강조했다.
2020.08.13 조회수 19473 이수영 광원산업 회장, 노벨상 연구 지원 위해 676억 원 기부
"KAIST에서 우리나라 최초의 과학 분야 노벨상 수상자가 반드시 나와야 합니다ˮ
이수영 회장(83세·現 KAIST 발전재단 이사장, 광원산업 회장)이 23일 오후 2시 우리 대학 학술문화관(E9) 스카이라운지에서 열린 기부 약정식을 통해 평생을 일궈 모은 676억 원 상당의 부동산을 출연해 `이수영 과학교육재단'을 설립하기로 했다.
이수영 과학교육재단'의 수익금은 'KAIST 싱귤래러티(Singularity) 교수' 지원을 통한 노벨상 연구 기금으로 사용된다. 이번 이 회장의 기부는 지난 2012년 미국의 80억여 원 상당의 부동산과 2016년 또 한 차례에 걸쳐 10억여 원 상당의 미국 부동산을 유증한 것에 이은 세 번째 기부로 총 기부액은 KAIST 개교 이래 최고액인 766억 원을 기록했다.
지난 2012년 첫 기부를 시작으로 KAIST와 인연을 맺은 뒤, 이듬해인 2013년부터 현재까지 발전재단 이사장으로 재임 중인 이수영 광원산업 회장은 "오랫동안 가까운 자리에서 지켜본 결과 KAIST는 우리나라 발전은 물론 인류와 사회에 공헌할 수 있는 최고의 대학이라는 믿음을 갖게 되었다ˮ라고 기부 배경을 밝혔다.
이 회장은 이어 "우리나라 대표기업인 삼성전자의 경우 반도체 석·박사 연구인력의 25%가 KAIST 출신ˮ이라며 "2019년 314조 원의 매출로 국내 GDP의 16.4%를 차지할 정도로 국가 경제 성장에 가장 크게 기여하고 있는 삼성전자를 세계적인 기업으로 성장시킬 수 있었던 것은 세계적인 과학기술 인재를 양성하고 있는 KAIST 덕분ˮ이라고 말했다.
이 회장은 이와 함께 "세상만사는 사람으로 시작해서 사람으로 끝나기 때문에 KAIST는 사명감을 가지고 대한민국을 이끌어나갈 영재를 키워야 한다ˮ고 강조하면서 "어느 대학도 해내지 못한 탁월한 성취를 이뤄내 대한민국의 이름을 세계에 드높이는 일에 이 기부가 뜻깊게 활용되기를 바란다ˮ고 덧붙였다.
KAIST는 이수영 회장의 이번 기부를 바탕으로 설립되는 `이수영 과학교육재단'의 지원을 받아 `KAIST 싱귤래러티 교수'를 육성할 계획이다.
'KAIST 싱귤래러티 교수' 제도는 과학 지식의 패러다임을 바꾸거나 새로운 분야를 개척할 수 있는 교수, 인류 난제를 해결하고 독창적인 과학 지식과 이론을 정립할 수 있는 교수를 선발해 지원하는 제도다.
미래 과학기술 및 산업 발전을 선도할 혁신기술과 학문적 독창성을 창출할 수 있는 우수 연구 인력을 확보하고 기술적 특이점 도래에 대비하기 위해 장기간의 연구 수행을 지원하는 것이 특징이다. KAIST는 '이수영 과학교육재단' 지원으로 세계 최정상급 과학자 배출을 위한 지속 가능하고 안정적인 연구 환경을 조성하고 이를 통해 교내 연구진의 노벨상 수상 가능성을 높이겠다는 계획이다.
싱귤래러티 교수로 선정되면 10년간의 임용기간 동안 연구비를 지원받고, 논문·특허 중심의 연차 실적 평가가 유예된다. 임용기간 종료 시 연구 진행 과정 및 특이점 기술 역량 확보 등 평가에 따라 지원 기간을 추가로 10년까지 연장할 수 있다.
이수영 회장은 "우리나라의 미래를 위해 가진 것을 나눌 수 있어서 기쁘다ˮ고 기부 소감을 밝히면서 "대한민국의 미래와 나라를 위하는 뜻을 가진 분들이 기부 문화 활성화를 위해 더 많이 동참해주기를 바란다ˮ고 당부했다.
KAIST 신성철 총장은 "평생의 피땀으로 일궈낸 재산을 아낌없이 내놓은 이수영 회장님의 결단에 경의를 표한다ˮ라고 감사 인사를 전하면서 "대한민국의 과학기술 발전을 이끌고 있는 KAIST의 역할과 임무에 대한 사명감을 항상 마음에 새기고 이수영 이사장님의 뜻을 반드시 이룰 수 있도록 모든 구성원들이 최선을 다할 것ˮ이라고 밝혔다.
이수영 KAIST 발전재단 이사장은 경기여고와 서울대 법대를 졸업하고 1963년 서울신문에 입사해 기자 생활을 시작했다. 1980년까지 한국경제신문과 서울경제신문 등의 언론사에서 취재 현장을 누볐다. 기자로 재직하던 시절인 1971년에 광원목장을 설립해 축산업을 시작했고, 1988년 부동산 전문기업인 광원산업을 창업해 현재까지 회장을 맡고 있다. 2012년 KAIST 명예박사를 받았으며, 2018년에는 국민훈장 목련장을 수훈했다.
한편, KAIST에는 그간 이수영 이사장을 포함해 대한민국 1호 한의학박사인 故 류근철 박사(578억 원), 정문술 前 미래산업 회장(515억 원), 김병호 前 서전농업 회장(350억 원), 故 김영한 여사(340억 원) 등의 기부자들이 KAIST에 고액의 발전기금을 기탁했다.
2020.07.23 조회수 24728
이수영 광원산업 회장, 노벨상 연구 지원 위해 676억 원 기부
"KAIST에서 우리나라 최초의 과학 분야 노벨상 수상자가 반드시 나와야 합니다ˮ
이수영 회장(83세·現 KAIST 발전재단 이사장, 광원산업 회장)이 23일 오후 2시 우리 대학 학술문화관(E9) 스카이라운지에서 열린 기부 약정식을 통해 평생을 일궈 모은 676억 원 상당의 부동산을 출연해 `이수영 과학교육재단'을 설립하기로 했다.
이수영 과학교육재단'의 수익금은 'KAIST 싱귤래러티(Singularity) 교수' 지원을 통한 노벨상 연구 기금으로 사용된다. 이번 이 회장의 기부는 지난 2012년 미국의 80억여 원 상당의 부동산과 2016년 또 한 차례에 걸쳐 10억여 원 상당의 미국 부동산을 유증한 것에 이은 세 번째 기부로 총 기부액은 KAIST 개교 이래 최고액인 766억 원을 기록했다.
지난 2012년 첫 기부를 시작으로 KAIST와 인연을 맺은 뒤, 이듬해인 2013년부터 현재까지 발전재단 이사장으로 재임 중인 이수영 광원산업 회장은 "오랫동안 가까운 자리에서 지켜본 결과 KAIST는 우리나라 발전은 물론 인류와 사회에 공헌할 수 있는 최고의 대학이라는 믿음을 갖게 되었다ˮ라고 기부 배경을 밝혔다.
이 회장은 이어 "우리나라 대표기업인 삼성전자의 경우 반도체 석·박사 연구인력의 25%가 KAIST 출신ˮ이라며 "2019년 314조 원의 매출로 국내 GDP의 16.4%를 차지할 정도로 국가 경제 성장에 가장 크게 기여하고 있는 삼성전자를 세계적인 기업으로 성장시킬 수 있었던 것은 세계적인 과학기술 인재를 양성하고 있는 KAIST 덕분ˮ이라고 말했다.
이 회장은 이와 함께 "세상만사는 사람으로 시작해서 사람으로 끝나기 때문에 KAIST는 사명감을 가지고 대한민국을 이끌어나갈 영재를 키워야 한다ˮ고 강조하면서 "어느 대학도 해내지 못한 탁월한 성취를 이뤄내 대한민국의 이름을 세계에 드높이는 일에 이 기부가 뜻깊게 활용되기를 바란다ˮ고 덧붙였다.
KAIST는 이수영 회장의 이번 기부를 바탕으로 설립되는 `이수영 과학교육재단'의 지원을 받아 `KAIST 싱귤래러티 교수'를 육성할 계획이다.
'KAIST 싱귤래러티 교수' 제도는 과학 지식의 패러다임을 바꾸거나 새로운 분야를 개척할 수 있는 교수, 인류 난제를 해결하고 독창적인 과학 지식과 이론을 정립할 수 있는 교수를 선발해 지원하는 제도다.
미래 과학기술 및 산업 발전을 선도할 혁신기술과 학문적 독창성을 창출할 수 있는 우수 연구 인력을 확보하고 기술적 특이점 도래에 대비하기 위해 장기간의 연구 수행을 지원하는 것이 특징이다. KAIST는 '이수영 과학교육재단' 지원으로 세계 최정상급 과학자 배출을 위한 지속 가능하고 안정적인 연구 환경을 조성하고 이를 통해 교내 연구진의 노벨상 수상 가능성을 높이겠다는 계획이다.
싱귤래러티 교수로 선정되면 10년간의 임용기간 동안 연구비를 지원받고, 논문·특허 중심의 연차 실적 평가가 유예된다. 임용기간 종료 시 연구 진행 과정 및 특이점 기술 역량 확보 등 평가에 따라 지원 기간을 추가로 10년까지 연장할 수 있다.
이수영 회장은 "우리나라의 미래를 위해 가진 것을 나눌 수 있어서 기쁘다ˮ고 기부 소감을 밝히면서 "대한민국의 미래와 나라를 위하는 뜻을 가진 분들이 기부 문화 활성화를 위해 더 많이 동참해주기를 바란다ˮ고 당부했다.
KAIST 신성철 총장은 "평생의 피땀으로 일궈낸 재산을 아낌없이 내놓은 이수영 회장님의 결단에 경의를 표한다ˮ라고 감사 인사를 전하면서 "대한민국의 과학기술 발전을 이끌고 있는 KAIST의 역할과 임무에 대한 사명감을 항상 마음에 새기고 이수영 이사장님의 뜻을 반드시 이룰 수 있도록 모든 구성원들이 최선을 다할 것ˮ이라고 밝혔다.
이수영 KAIST 발전재단 이사장은 경기여고와 서울대 법대를 졸업하고 1963년 서울신문에 입사해 기자 생활을 시작했다. 1980년까지 한국경제신문과 서울경제신문 등의 언론사에서 취재 현장을 누볐다. 기자로 재직하던 시절인 1971년에 광원목장을 설립해 축산업을 시작했고, 1988년 부동산 전문기업인 광원산업을 창업해 현재까지 회장을 맡고 있다. 2012년 KAIST 명예박사를 받았으며, 2018년에는 국민훈장 목련장을 수훈했다.
한편, KAIST에는 그간 이수영 이사장을 포함해 대한민국 1호 한의학박사인 故 류근철 박사(578억 원), 정문술 前 미래산업 회장(515억 원), 김병호 前 서전농업 회장(350억 원), 故 김영한 여사(340억 원) 등의 기부자들이 KAIST에 고액의 발전기금을 기탁했다.
2020.07.23 조회수 24728 중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 24926
중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 24926 이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
2020.07.09 조회수 20524
이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
2020.07.09 조회수 20524 단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
2020.07.09 조회수 19788
단백질 접힘 과정에서의 구조 변화 관측에 성공
우리 대학 화학과 이효철 교수(기초과학연구원 나노물질 및 화학반응 연구단 부연구단장 겸임) 연구팀이 풀려있는 단백질이 접히는 과정을 분자 수준에서 규명하는 데 성공, 단백질 구조기반의 신약 개발을 위한 토대를 마련했다. 획기적인 연구성과를 냈다고 평가받고 있는 이 교수 연구팀은 단백질 접힘 경로에서의 단백질 구조 변화를 실시간으로 관측하는 데 최초로 성공했다고 9일 밝혔다.
이 교수 연구팀에 따르면 풀린 단백질이 접히는 과정을 엑스선 펄스를 이용한 고속 연사 촬영기법을 통해 단백질의 구조 변화를 연속 스냅숏으로 추출했고 이를 통해 일련의 단백질 접힘 과정을 분자 수준에서 밝혀내는 쾌거를 달성했다.
KAIST 화학과 박사과정 졸업생 김태우 연구원이 제1 저자로, KAIST 화학과 이효철, 이영민 교수가 교신저자로 참여한 이번 연구결과는 국제 학술지 `미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the United States of America)' 7월 1일 字에 게재됐다. (논문명 : Protein folding from heterogeneous unfolded state revealed by time-resolved X-ray solution scattering).
잘 접혀있는 단백질이 풀리는 과정은 비교적 쉽게 연구할 수 있어 많은 연구가 이뤄져 왔지만 풀려있는 단백질이 접히는 과정은 연구가 힘들었는데 이효철 교수팀의 이번 연구는 그 과정을 밝혀냈다는데 큰 의미가 있다. 단백질이 접히는 과정을 연구하기 힘든 이유는 풀려있는 단백질이 특정 구조를 가지지 않고 매우 다양한 구조를 갖기 때문이다. 하지만 이 교수 연구팀은 이번 연구에서 엑스선 산란 신호 분석법을 개발, 적용해서 이런 난제를 해결하는 데 성공했다.
단백질의 3차원 구조를 결정하는 고유의 접힘 과정은 가장 중요한 생체 반응이다. 때에 따라 발생하는 잘못 접히는 과정은 단백질의 정상적인 기능을 방해하며, 알츠하이머, 광우병, 파킨슨병 등이 바로 단백질 접힘이 올바르지 않아 발병되는 질병이다.
연구팀은 생체 내 전자전달에 관여하는 사이토크롬 단백질을 풀림 상태에서 접힘 상태로의 전이 과정을 발생시켜, 해당 접힘 과정을 시간 분해 엑스선 산란법을 이용해 연속적으로 움직이는 단백질의 구조 변화를 관측했다. 여기서 주목할만한 점은 이 교수 연구팀은 그간 단백질 접힘에 대한 이론적 모델로만 제시됐던 깔때기꼴 접힘 가설을 사이토크롬 단백질의 접힘 과정을 통해 실험적으로 입증했다는 사실이다.
이와 함께 이 교수팀은 단백질의 구조 변화뿐만 아니라 접히는 과정의 속도가 기존에 알려진 보통의 지수함수 형태가 아니라 늘어진 지수함수 형태임을 밝혀냈다. 이로써 풀린 단백질에서 접힌 상태로 가는 경로가 매우 다양하다는 것을 실험적으로 알아낸 것이다.
제1 저자인 김태우 연구원은 "단백질 접힘은 3차원 단백질 구조가 만들어지는 가장 중요한 생명현상인데, 접힘 과정에 대한 이해는 단백질 구조기반 신약 개발의 기초가 될 것ˮ이라고 기대했다. 공동 교신저자로 참여한 KAIST 화학과 이영민 교수도 "단백질 접힘 이론 모형에 대한 실험적 검증은 이론 생물리학 관점에서 더욱 정확한 계산 방법 개발에 중요한 자산이 될 것ˮ라고 강조했다.
한편 이번 연구는 기초과학연구원, 한국연구재단 등의 지원을 받아 수행됐다.
2020.07.09 조회수 19788 김종환 교수, 제33회 정보문화의달 기념 유공자 대통령 표창 수상
우리 대학 전기및전자공학부 김종환 교수는 지난 6월 22일, 과학기술정보통신부와 한국정보화진흥원이 개최한 「제33회 정보문화의 달」 기념식에서 2020년 정보문화 유공 정부포상 '대통령 표창'을 수상하였다.
본 포상은 디지털 정보격차 해소, 디지털 역기능 대응 등에 기여한 유공자를 발굴·포상하여 디지털 포용사회 구현과 정보문화 창달에 기여한 자에게 수상되는 상으로, KAIST에 부임한 이래로 '로봇축구와 국제로봇올림피아드 및 AI 월드컵'을 창시하여 정보화 수준 향상과 건전정보문화 조성 및 디지털 정보격차 해소에 기여한 점을 높이 평가받아 수상하게 되었다.
'디지털로 하나 되는 대한민국, 다 함께 누리는 디지털 포용세상'을 주제로 열린 본 행사에는 최기영 과기정통부 장관, 허욱 방송통신위원회 상임위원 등이 참석하였다.
2020.07.02 조회수 18254
김종환 교수, 제33회 정보문화의달 기념 유공자 대통령 표창 수상
우리 대학 전기및전자공학부 김종환 교수는 지난 6월 22일, 과학기술정보통신부와 한국정보화진흥원이 개최한 「제33회 정보문화의 달」 기념식에서 2020년 정보문화 유공 정부포상 '대통령 표창'을 수상하였다.
본 포상은 디지털 정보격차 해소, 디지털 역기능 대응 등에 기여한 유공자를 발굴·포상하여 디지털 포용사회 구현과 정보문화 창달에 기여한 자에게 수상되는 상으로, KAIST에 부임한 이래로 '로봇축구와 국제로봇올림피아드 및 AI 월드컵'을 창시하여 정보화 수준 향상과 건전정보문화 조성 및 디지털 정보격차 해소에 기여한 점을 높이 평가받아 수상하게 되었다.
'디지털로 하나 되는 대한민국, 다 함께 누리는 디지털 포용세상'을 주제로 열린 본 행사에는 최기영 과기정통부 장관, 허욱 방송통신위원회 상임위원 등이 참석하였다.
2020.07.02 조회수 18254 문수복 교수, 국가과학기술자문회의 심의위원 선임
우리대학 전산학부 문수복 교수가 국가과학기술자문회의 제3기 심의위원으로 선임됐다.
국가과학기술자문회의는 국가기술 정책의 기본 방향과 주요 의제에 대한 정책 자문을 수행하는 헌법기구로서 대통령이 의장을 맡는다. 문 교수는 김인수 광주과학기술원(GIST) 지구환경공학부 교수, 윤희숙 재료연구소 실장, 이정원 과학기술정책연구원(STEPI) 선임 연구위원, 조정우 SK바이오팜 대표이사와 함께 현 정부 3기 심의위원으로 위촉됐다.
국가과학기술자문회의는 “과학기술 분야에서의 전문성 및 연구성과, 정책경험, 산·학·연 구성 비율 등 요소를 고려해 선정했다”며 선정 이유를 밝혔으며, 임기는 이달 27일부터 내년 6월 26일까지 1년이다.
2020.06.29 조회수 16872
문수복 교수, 국가과학기술자문회의 심의위원 선임
우리대학 전산학부 문수복 교수가 국가과학기술자문회의 제3기 심의위원으로 선임됐다.
국가과학기술자문회의는 국가기술 정책의 기본 방향과 주요 의제에 대한 정책 자문을 수행하는 헌법기구로서 대통령이 의장을 맡는다. 문 교수는 김인수 광주과학기술원(GIST) 지구환경공학부 교수, 윤희숙 재료연구소 실장, 이정원 과학기술정책연구원(STEPI) 선임 연구위원, 조정우 SK바이오팜 대표이사와 함께 현 정부 3기 심의위원으로 위촉됐다.
국가과학기술자문회의는 “과학기술 분야에서의 전문성 및 연구성과, 정책경험, 산·학·연 구성 비율 등 요소를 고려해 선정했다”며 선정 이유를 밝혔으며, 임기는 이달 27일부터 내년 6월 26일까지 1년이다.
2020.06.29 조회수 16872