%EC%9D%98%EA%B3%BC%ED%95%99%EB%8C%80%ED%95%99%EC%9B%90
-
 이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
2020.07.09 조회수 24486
이정호 교수, 다케다제약-뉴욕아카데미 2020 과학혁신가상 수상
우리 대학 의과학대학원 이정호 교수가 다케다제약-미국뉴욕아카데미(NYAS: New York Academy of Sciences) 2020 제3회 과학혁신가상(Innovators in Science Award) 중 신진과학자상(Early-Career Scientist Award)을 수상하게 됐다. 이는 희귀질환 연구분야에서 혁신적인 성과 달성을 위해 헌신해온 연구자에게 수여하는 상이다. 선임과학자상(Senior Scientist Award)과 신진과학자상으로 구성된 이 상의 수상자에게는 각각 상금이 수여된다.
이정호 교수는 희귀 발달성 뇌질환을 유발할 수 있는 뇌 줄기세포 내 유전적 변이에 대한 연구 업적을 인정받아 수상자로 선정됐다. 이 교수는 난치성 간질의 원인을 최초로 찾아냈으며 국소 피질 이형성증, 뇌간의 발달저하가 특징인 주버트 증후군(Joubert syndrome), 뇌의 한쪽 반구가 비정상적으로 비대해지는 편측거대뇌증 등 몇몇 발달성 뇌질환을 유발하는 유전자를 규명하기도 했다. 이 교수는 뇌 체세포 유전변이 국가 연구단(National Creative Research Initiative Center for Brain Somatic Mutations) 단장이자, 저빈도 체세포 유전변이에 의한 난치성 중추신경계 질환을 위한 새로운 치료제 및 진단법 발굴을 모표로 설립된 바이오제약 기업 소바젠(SoVarGen)의 공동창업자 겸 최고기술경영자(CTO, Chief Technology Officer)다.
이 교수는 "개인적으로 존경하는 세계적인 과학 석학으로 구성된 심사위원단으로부터 인정받게 돼 큰 영광이다"라며 "더 중요한 사실은 이번 수상으로 뇌 체세포 유전변이 연구가 치명적인 난치성 신경질환으로 고통받는 환자를 위한 중요한 연구 분야로 인정받게 됐다는 것이다"고 소감을 밝혔다.
시상식은 오는 10월 비대면으로 열리는 '과학혁신가상 시상식 및 심포지엄'에서 진행될 예정이다. 이 행사는 전세계 선도적 연구진, 임상전문가 그리고 저명한 업계의 관계자와 함께 유전성, 신경계, 대사, 자가면역 및 심혈관 관련 희귀질환에 대한 과학적 이해와 치료법에 대한 최신 혁신적 성과를 공유할 수 있는 자리가 될 전망이다.
2020.07.09 조회수 24486 -
 모유 수유가 출산 후 산모의 당뇨병을 예방하는 효과 규명에 성공
우리 대학 의과학대학원 김하일 교수와 분당서울대학교병원 내분비대사내과 장학철 교수 공동연구팀이 모유 수유가 산모의 췌장에 존재하는 베타세포를 건강하게 만듦으로써 출산 후 당뇨병 발생을 억제하는 효과를 규명하는데 성공했다.
KAIST 의과학대학원 졸업생 문준호 박사(서울대학교병원)와 김형석 박사(충남대학교 의과대학)가 공동 1저자로 참여한 이번 연구 성과는 국제학술지‘사이언스 중개의학 (Science Translational Medicine, IF: 17.16)’ 4월 29일자 온라인 판에 게재됐다. (논문명 : Lactation improves pancreatic β cell mass and function through serotonin production)
임신성 당뇨병 및 출산 후 산모의 당뇨병 발병은 여성 평균 출산 연령이 높아짐에 따라 점차 증가하는 추세다. 전체 산모의 10% 이상이 임신성 당뇨병에 걸리고, 그중 절반 이상은 출산 후 당뇨병으로 연결된다. 또한, 임신과 출산을 경험한 여성은 그렇지 않은 여성에 비해 당뇨병 발병률이 더 높다.
당뇨병은 통상 심혈관 및 뇌혈관, 신경, 망막 질환 등의 다양한 합병증을 유발하기 때문에 여성의 건강과 삶의 질을 크게 떨어뜨린다는 게 학계의 정설이다.
모유 수유는 그동안 산모와 아기의 신체적, 정신적 건강에 다양한 이로운 효과가 있고 특히 당뇨병을 예방하는 효과가 있는 것으로 알려졌지만 그 기전에 대해서 정확하게 파악하지 못하는 단점을 안고 있었다.
모유 수유 중인 산모의 뇌하수체는 모유의 생산을 촉진하는 호르몬인 프로락틴을 활발히 분비한다. 프로락틴은 혈당 조절에 관여하는 호르몬인 인슐린을 분비하는 췌장의 베타세포를 자극한다. 이때 합성되는 신경 전달 물질인 세로토닌은 베타세포의 증식을 유발해 베타세포의 양을 증가시키고 베타세포 내부의 활성 산소를 제거하여 산모의 베타세포를 보다 건강한 상태로 만든다. 따라서 모유 수유는 산모의 베타세포를 다양한 대사적 스트레스에 유연하게 반응할 수 있게 만들어 준다.
연구팀은 174명의 임신성 당뇨병 산모들을 출산 후 3년 이상 추적, 관찰한 데이터를 분석한 결과, 수유를 했던 산모들이 수유를 시행하지 않았던 산모에 비해 베타세포의 기능이 개선되고 혈당 수치가 20mg/dL 정도 낮아지는 현상을 확인했다.
공동연구팀을 이끈 KAIST 김하일 교수는“모유 수유에 의한 베타세포의 기능 향상이 임신과 출산을 경험한 여성의 당뇨병 발병 예방에 큰 도움이 된다”면서 “모유 수유가 지닌 효과는 장기간 지속돼 수유가 끝난 후에라도 장기적으로는 당뇨병 예방 효과를 가진다”고 덧붙였다.
이번 연구는 한국연구재단, 국가과학기술연구회, 보건장학회 등의 지원을 받아 수행됐다.
2020.05.04 조회수 13806
모유 수유가 출산 후 산모의 당뇨병을 예방하는 효과 규명에 성공
우리 대학 의과학대학원 김하일 교수와 분당서울대학교병원 내분비대사내과 장학철 교수 공동연구팀이 모유 수유가 산모의 췌장에 존재하는 베타세포를 건강하게 만듦으로써 출산 후 당뇨병 발생을 억제하는 효과를 규명하는데 성공했다.
KAIST 의과학대학원 졸업생 문준호 박사(서울대학교병원)와 김형석 박사(충남대학교 의과대학)가 공동 1저자로 참여한 이번 연구 성과는 국제학술지‘사이언스 중개의학 (Science Translational Medicine, IF: 17.16)’ 4월 29일자 온라인 판에 게재됐다. (논문명 : Lactation improves pancreatic β cell mass and function through serotonin production)
임신성 당뇨병 및 출산 후 산모의 당뇨병 발병은 여성 평균 출산 연령이 높아짐에 따라 점차 증가하는 추세다. 전체 산모의 10% 이상이 임신성 당뇨병에 걸리고, 그중 절반 이상은 출산 후 당뇨병으로 연결된다. 또한, 임신과 출산을 경험한 여성은 그렇지 않은 여성에 비해 당뇨병 발병률이 더 높다.
당뇨병은 통상 심혈관 및 뇌혈관, 신경, 망막 질환 등의 다양한 합병증을 유발하기 때문에 여성의 건강과 삶의 질을 크게 떨어뜨린다는 게 학계의 정설이다.
모유 수유는 그동안 산모와 아기의 신체적, 정신적 건강에 다양한 이로운 효과가 있고 특히 당뇨병을 예방하는 효과가 있는 것으로 알려졌지만 그 기전에 대해서 정확하게 파악하지 못하는 단점을 안고 있었다.
모유 수유 중인 산모의 뇌하수체는 모유의 생산을 촉진하는 호르몬인 프로락틴을 활발히 분비한다. 프로락틴은 혈당 조절에 관여하는 호르몬인 인슐린을 분비하는 췌장의 베타세포를 자극한다. 이때 합성되는 신경 전달 물질인 세로토닌은 베타세포의 증식을 유발해 베타세포의 양을 증가시키고 베타세포 내부의 활성 산소를 제거하여 산모의 베타세포를 보다 건강한 상태로 만든다. 따라서 모유 수유는 산모의 베타세포를 다양한 대사적 스트레스에 유연하게 반응할 수 있게 만들어 준다.
연구팀은 174명의 임신성 당뇨병 산모들을 출산 후 3년 이상 추적, 관찰한 데이터를 분석한 결과, 수유를 했던 산모들이 수유를 시행하지 않았던 산모에 비해 베타세포의 기능이 개선되고 혈당 수치가 20mg/dL 정도 낮아지는 현상을 확인했다.
공동연구팀을 이끈 KAIST 김하일 교수는“모유 수유에 의한 베타세포의 기능 향상이 임신과 출산을 경험한 여성의 당뇨병 발병 예방에 큰 도움이 된다”면서 “모유 수유가 지닌 효과는 장기간 지속돼 수유가 끝난 후에라도 장기적으로는 당뇨병 예방 효과를 가진다”고 덧붙였다.
이번 연구는 한국연구재단, 국가과학기술연구회, 보건장학회 등의 지원을 받아 수행됐다.
2020.05.04 조회수 13806 -
 진원생명과학(주)과의 공동 연구로 C형간염 DNA백신 면역증강 효과 확인
의과학대학원 신의철 교수 연구팀이 기존 치료법이 모두 실패한 만성 C형간염 환자를 대상으로 DNA백신(GLS-6150)을 접종해 심각한 부작용 없이 매우 안전하면서도 C형간염 바이러스에 대한 T세포 면역반응을 높인다는 사실을 임상연구를 통해 밝혔다.
세브란스병원 소화기내과 안상훈 교수, 부산대학교병원 소화기내과 허정 교수, 진원생명과학과 공동으로 진행한 이번 연구에서는 특히 IFNL3라는 사이토카인 면역증강물질 유전자를 백신에 포함했다. 이를 통해 면역반응을 억제하는 조절 T세포(Treg)를 감소시키면서 C형간염 바이러스 면역반응의 핵심 역할을 하는 세포독성 T세포의 기능을 강화할 수 있음을 밝혀냈다.
신의철 교수, 세브란스병원 안상훈 교수, 부산대학교병원 허정 교수가 공동 교신저자로 참여한 이번 연구결과는 간 연구 분야의 국제적 전문 학술지인 ‘저널 오브 헤파톨로지(Journal of Hepatology)’ 2월 20일 자 온라인판에 게재됐다.(논문명: IFNL3-adjuvanted HCV DNA vaccine reduces regulatory T-cell frequency and increases virus-specific T-cell response)
이번 연구를 통해 만성 C형간염 환자, 특히 항바이러스제를 이용하여 치료받은 완치자의 HCV 재감염을 예방하고 만성 C형간염 고위험군의 HCV 감염을 예방하는 백신의 개발 가능성을 확인했다.
이번 임상연구는 지난 2013년 10월 식약처의 임상승인을 받아 세브란스병원과 부산대학교병원에서 기존치료법에 모두 실패한 만성 C형간염 환자 18명을 대상으로 DNA 백신(GLS-6150)의 안전성, 내약성 및 면역원성을 평가하기 위한 다기관·공개·용량 증량·1상 임상시험으로 수행됐다. 이 중 14명을 대상으로 2014년 9월 식약처로부터 추가 임상승인을 받아 2016년에 1상 임상연구를 모두 완료했다. (Clinicaltrials.gov 번호: NCT02027116)
해당 연구팀은 항바이러스제로 치료된 만성 C형간염 완치자를 대상으로 DNA 백신(GLS-6150)의 안전성과 내약성 및 면역원성을 평가하는 임상연구의 승인을 2018년 2월 식약처로부터 받아 현재 세브란스병원과 부산대학교병원에서 세 번째 1상 임상연구를 수행하고 있다. (Clinicaltrials.gov 번호: NCT03674125)
신의철 교수는“이번 연구를 통해 지난 30여 년 동안 실패했던 C형간염 예방백신 개발의 새로운 가능성을 발견했다”라며 “예방백신을 성공적으로 개발하면 가까운 미래에 C형간염 바이러스를 지구상에서 사라지게 할 수도 있을 것이다”라고 말했다.
이번 연구는 진원생명과학(주)의 지원을 받아 C형간염 DNA백신(GLS-6150)을 사용했다.
2020.03.25 조회수 17865
진원생명과학(주)과의 공동 연구로 C형간염 DNA백신 면역증강 효과 확인
의과학대학원 신의철 교수 연구팀이 기존 치료법이 모두 실패한 만성 C형간염 환자를 대상으로 DNA백신(GLS-6150)을 접종해 심각한 부작용 없이 매우 안전하면서도 C형간염 바이러스에 대한 T세포 면역반응을 높인다는 사실을 임상연구를 통해 밝혔다.
세브란스병원 소화기내과 안상훈 교수, 부산대학교병원 소화기내과 허정 교수, 진원생명과학과 공동으로 진행한 이번 연구에서는 특히 IFNL3라는 사이토카인 면역증강물질 유전자를 백신에 포함했다. 이를 통해 면역반응을 억제하는 조절 T세포(Treg)를 감소시키면서 C형간염 바이러스 면역반응의 핵심 역할을 하는 세포독성 T세포의 기능을 강화할 수 있음을 밝혀냈다.
신의철 교수, 세브란스병원 안상훈 교수, 부산대학교병원 허정 교수가 공동 교신저자로 참여한 이번 연구결과는 간 연구 분야의 국제적 전문 학술지인 ‘저널 오브 헤파톨로지(Journal of Hepatology)’ 2월 20일 자 온라인판에 게재됐다.(논문명: IFNL3-adjuvanted HCV DNA vaccine reduces regulatory T-cell frequency and increases virus-specific T-cell response)
이번 연구를 통해 만성 C형간염 환자, 특히 항바이러스제를 이용하여 치료받은 완치자의 HCV 재감염을 예방하고 만성 C형간염 고위험군의 HCV 감염을 예방하는 백신의 개발 가능성을 확인했다.
이번 임상연구는 지난 2013년 10월 식약처의 임상승인을 받아 세브란스병원과 부산대학교병원에서 기존치료법에 모두 실패한 만성 C형간염 환자 18명을 대상으로 DNA 백신(GLS-6150)의 안전성, 내약성 및 면역원성을 평가하기 위한 다기관·공개·용량 증량·1상 임상시험으로 수행됐다. 이 중 14명을 대상으로 2014년 9월 식약처로부터 추가 임상승인을 받아 2016년에 1상 임상연구를 모두 완료했다. (Clinicaltrials.gov 번호: NCT02027116)
해당 연구팀은 항바이러스제로 치료된 만성 C형간염 완치자를 대상으로 DNA 백신(GLS-6150)의 안전성과 내약성 및 면역원성을 평가하는 임상연구의 승인을 2018년 2월 식약처로부터 받아 현재 세브란스병원과 부산대학교병원에서 세 번째 1상 임상연구를 수행하고 있다. (Clinicaltrials.gov 번호: NCT03674125)
신의철 교수는“이번 연구를 통해 지난 30여 년 동안 실패했던 C형간염 예방백신 개발의 새로운 가능성을 발견했다”라며 “예방백신을 성공적으로 개발하면 가까운 미래에 C형간염 바이러스를 지구상에서 사라지게 할 수도 있을 것이다”라고 말했다.
이번 연구는 진원생명과학(주)의 지원을 받아 C형간염 DNA백신(GLS-6150)을 사용했다.
2020.03.25 조회수 17865 -
 신의철 교수, 암세포의 면역세포 억제 핵심원리 규명
〈 신의철 교수, 김창곤 연구원 〉
우리 대학 의과학대학원 신의철 교수, 연세대학교 의과대학 민병소, 김호근 교수 공동 연구팀이 암 환자의 암세포가 면역세포를 억제해 면역반응을 회피하게 만드는 핵심원리를 발견했다.
이번 연구를 통해 최근 유행하는 면역항암제의 치료 효율을 높일 수 있는 효과적인 암 치료 전략을 제시할 수 있을 것으로 기대된다.
김창곤 연구원, 장미 연구교수가 공동 1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 ‘사이언스 면역학(Science Immunology)’ 11월 8일 자 온라인판에 게재됐다 (논문명 : VEGF-A drives TOX-dependent T cell exhaustion in anti–PD-1–resistant microsatellite stable colorectal cancers).
암 환자는 암세포에 대항하는 면역세포, 특히 T세포의 기능이 현저히 약해져 있다. 이렇게 T세포의 기능이 약해지는 주된 이유는 T세포가 PD-1이라는 억제 수용체를 과다하게 발현하기 때문이다.
최근 유행하고 있는 면역항암제도 바로 이 PD-1 억제 수용체의 기능을 차단해 T세포의 기능을 회복시키는 원리로 작동하는 것이다. 하지만 면역항암제는 아직 부족한 부분이 많아 투여받은 암 환자 중 일부에게만 치료 반응이 나타나는 현실이다. 이러한 이유로 많은 연구자가 암 환자의 T세포 기능이 약해지는 다른 이유를 활발히 찾고 있다.
이번 연구에서 공동 연구팀은, 그간 혈관형성인자로만 알려졌던 혈관내피성장인자(vascular endothelial growth factor; VEGF)라는 혈관형성인자 단백질이 암세포에 대항하는 T세포의 기능을 약하게 만드는 주요 원인임을 새롭게 밝혔다.
종양의 지속적인 성장을 위해 암세포는 혈관내피성장인자를 과다 생성하고, 이로 인해 암 조직에는 혈관이 과다 생성된다는 사실은 이미 잘 알려져 있었다. 연구팀은 이번 연구를 통해 혈관내피성장인자가 혈관 형성 이외에도 T세포 억제라는 중요한 작용을 통해 암의 성장을 돕는다는 사실을 새롭게 규명했다.
암세포에서 생성된 혈관내피성장인자는 암세포에 대항하는 T세포 표면에 발현하는 수용체에 결합해 T세포에 톡스(TOX)라 불리는 단백질의 발현을 유도하고, 톡스는 T세포의 기능을 억제하고 약화하는 유전자 발현 프로그램을 작동시킨다는 것이 이번 연구의 핵심이다.
연구팀은 기초적인 발견에 그치지 않고 암 환자의 면역항암제 치료 효율을 높이는 전략을 제시했다. 암 성장을 막을 목적으로 혈관내피성장인자 저해제가 이미 개발됐기 때문에, 연구팀이 새로 발견한 혈관내피성장인자의 T세포 기능 억제작용을 근거로 혈관내피성장인자 저해제를 면역항암제와 함께 사용한다면 치료 효율을 극대화할 수 있을 것으로 기대하고 있다.
실제 이번 연구에서도 면역항암제와 혈관내피성장인자 저해제를 병합 치료하면 우수한 항암 효과가 있음을 동물 모델에서 증명했다.
이번 연구는 연세대학교 의과대학 외과 및 병리학과 연구팀과 KAIST 의과학대학원이 암 환자의 면역학적 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로 중개 연구(translational research)의 주요 성과로 평가받는다.
신 교수는 “암세포와 면역세포 사이에서 어떤 일이 벌어지는지를 상세히 연구함으로써 임상 치료 전략을 제시하게 된 중요한 연구이다”라며 “향후 암 환자의 생존율을 높일 수 있는 새로운 면역기전 연구 및 면역항암제 개발 연구를 계속하겠다”라고 말했다.
이번 연구는 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 신의철 교수 연구팀 연구성과 개념도
2019.11.13 조회수 13095
신의철 교수, 암세포의 면역세포 억제 핵심원리 규명
〈 신의철 교수, 김창곤 연구원 〉
우리 대학 의과학대학원 신의철 교수, 연세대학교 의과대학 민병소, 김호근 교수 공동 연구팀이 암 환자의 암세포가 면역세포를 억제해 면역반응을 회피하게 만드는 핵심원리를 발견했다.
이번 연구를 통해 최근 유행하는 면역항암제의 치료 효율을 높일 수 있는 효과적인 암 치료 전략을 제시할 수 있을 것으로 기대된다.
김창곤 연구원, 장미 연구교수가 공동 1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 ‘사이언스 면역학(Science Immunology)’ 11월 8일 자 온라인판에 게재됐다 (논문명 : VEGF-A drives TOX-dependent T cell exhaustion in anti–PD-1–resistant microsatellite stable colorectal cancers).
암 환자는 암세포에 대항하는 면역세포, 특히 T세포의 기능이 현저히 약해져 있다. 이렇게 T세포의 기능이 약해지는 주된 이유는 T세포가 PD-1이라는 억제 수용체를 과다하게 발현하기 때문이다.
최근 유행하고 있는 면역항암제도 바로 이 PD-1 억제 수용체의 기능을 차단해 T세포의 기능을 회복시키는 원리로 작동하는 것이다. 하지만 면역항암제는 아직 부족한 부분이 많아 투여받은 암 환자 중 일부에게만 치료 반응이 나타나는 현실이다. 이러한 이유로 많은 연구자가 암 환자의 T세포 기능이 약해지는 다른 이유를 활발히 찾고 있다.
이번 연구에서 공동 연구팀은, 그간 혈관형성인자로만 알려졌던 혈관내피성장인자(vascular endothelial growth factor; VEGF)라는 혈관형성인자 단백질이 암세포에 대항하는 T세포의 기능을 약하게 만드는 주요 원인임을 새롭게 밝혔다.
종양의 지속적인 성장을 위해 암세포는 혈관내피성장인자를 과다 생성하고, 이로 인해 암 조직에는 혈관이 과다 생성된다는 사실은 이미 잘 알려져 있었다. 연구팀은 이번 연구를 통해 혈관내피성장인자가 혈관 형성 이외에도 T세포 억제라는 중요한 작용을 통해 암의 성장을 돕는다는 사실을 새롭게 규명했다.
암세포에서 생성된 혈관내피성장인자는 암세포에 대항하는 T세포 표면에 발현하는 수용체에 결합해 T세포에 톡스(TOX)라 불리는 단백질의 발현을 유도하고, 톡스는 T세포의 기능을 억제하고 약화하는 유전자 발현 프로그램을 작동시킨다는 것이 이번 연구의 핵심이다.
연구팀은 기초적인 발견에 그치지 않고 암 환자의 면역항암제 치료 효율을 높이는 전략을 제시했다. 암 성장을 막을 목적으로 혈관내피성장인자 저해제가 이미 개발됐기 때문에, 연구팀이 새로 발견한 혈관내피성장인자의 T세포 기능 억제작용을 근거로 혈관내피성장인자 저해제를 면역항암제와 함께 사용한다면 치료 효율을 극대화할 수 있을 것으로 기대하고 있다.
실제 이번 연구에서도 면역항암제와 혈관내피성장인자 저해제를 병합 치료하면 우수한 항암 효과가 있음을 동물 모델에서 증명했다.
이번 연구는 연세대학교 의과대학 외과 및 병리학과 연구팀과 KAIST 의과학대학원이 암 환자의 면역학적 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로 중개 연구(translational research)의 주요 성과로 평가받는다.
신 교수는 “암세포와 면역세포 사이에서 어떤 일이 벌어지는지를 상세히 연구함으로써 임상 치료 전략을 제시하게 된 중요한 연구이다”라며 “향후 암 환자의 생존율을 높일 수 있는 새로운 면역기전 연구 및 면역항암제 개발 연구를 계속하겠다”라고 말했다.
이번 연구는 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 신의철 교수 연구팀 연구성과 개념도
2019.11.13 조회수 13095 -
 이행기, 이정호 교수, 2019 국가연구개발 우수성과 100선 선정
〈 이행기 교수, 이정호 교수 〉
과학기술정보통신부와 한국과학기술기획평가원이 발표한 ´2019년 국가연구개발 우수성과 100선´에 우리 대학 이행기 교수, 이정호 교수가 선정됐다.
건설및환경공학과 이행기 교수는 기계·소재분야 우수성과에 선정됐다. 이 교수는 나노 및 바이오 기술을 융합한 차세대 건설재료를 개발한 연구 성과를 인정받았다.
의과학대학원 이정호 교수는 생명·해양 분야 우수성과에 선정됐다. 악성 뇌종양, 소아 뇌종양의 근본 원인을 규명하고 혁신적인 치료법을 개발한 공을 인정받았다.
우수성과로 선정된 성과는 과학기술정보통신부장관의 인증서와 현판이 수여된다.
선정된 교수에게는 국가연구개발 성과평가 유공포상(훈·포장, 대통령표창, 국무총리표창 등) 후보자로 추천되고, 신규 연구개발(R&D) 과제 선정에서 우대받게 된다.
2019.10.11 조회수 15895
이행기, 이정호 교수, 2019 국가연구개발 우수성과 100선 선정
〈 이행기 교수, 이정호 교수 〉
과학기술정보통신부와 한국과학기술기획평가원이 발표한 ´2019년 국가연구개발 우수성과 100선´에 우리 대학 이행기 교수, 이정호 교수가 선정됐다.
건설및환경공학과 이행기 교수는 기계·소재분야 우수성과에 선정됐다. 이 교수는 나노 및 바이오 기술을 융합한 차세대 건설재료를 개발한 연구 성과를 인정받았다.
의과학대학원 이정호 교수는 생명·해양 분야 우수성과에 선정됐다. 악성 뇌종양, 소아 뇌종양의 근본 원인을 규명하고 혁신적인 치료법을 개발한 공을 인정받았다.
우수성과로 선정된 성과는 과학기술정보통신부장관의 인증서와 현판이 수여된다.
선정된 교수에게는 국가연구개발 성과평가 유공포상(훈·포장, 대통령표창, 국무총리표창 등) 후보자로 추천되고, 신규 연구개발(R&D) 과제 선정에서 우대받게 된다.
2019.10.11 조회수 15895 -
 박수형 교수, 중증열성혈소판감소증후군 예방 백신 개발
〈 박수형 교수 〉
우리 대학 의과학대학원 박수형 교수 연구팀이 일명 살인진드기병으로 불리는 중증열성혈소판감소증후군(SFTS) 바이러스 감염을 예방하는 백신을 개발했다.
충북대학교 의과대학 최영기 교수와 진원생명과학(주)이 함께 참여한 공동 연구팀은 개발한 백신이 감염 동물모델 실험을 통해 중증열성혈소판감소증후군 바이러스 감염을 완벽하게 억제할 수 있음을 증명했다.
이번 연구를 통해 예방 백신 도출 및 검증 성과뿐 아니라 면역학적 관점에서 백신의 감염 예방 효능을 극대화할 수 있는 항원을 제시함으로써, 추후 중증열성혈소판감소증후군 바이러스에 대한 대응 전략 확립 및 연구에 기여할 것으로 기대된다.
곽정은 박사과정과 충북대학교 김영일 박사가 1 저자로 참여한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 8월 23일 자 온라인판에 게재됐다. (논문명 : Development of a SFTSV DNA vaccine that confers complete protection against lethal infection in ferrets)
흔히 살인진드기병으로 알려진 SFTS는 SFTS 바이러스에 감염된 매개 진드기에 물려 발생하는 신종 감염병으로, 최근 발생 빈도 및 지역의 확산으로 WHO에서도 주의해야 할 10대 신, 변종 바이러스 감염병으로 지정한 질병이다.
일반적으로 6~14일의 잠복기 후 고열(38∼40℃)이 3~10일 이어지고, 혈소판 감소 및 백혈구 감소와 구토, 설사 등 소화기 증상이 발생하며, 일부 사례에서는 중증으로 진행돼 사망에 이르기도 한다.
2013년에 한국에서 처음으로 환자가 발생한 이래 발생 건수가 매년 꾸준히 증가하고 있지만, 진드기 접촉 최소화를 통한 예방이 제시될 뿐 현재까지 예방 백신이 개발되지 않았다.
연구팀은 31종의 서로 다른 SFTS 바이러스의 유전자 서열로부터 공통 서열을 도출해 백신 항원을 설계하고, 진원생명과학의 플랫폼을 이용해 DNA 백신을 제작했다.
DNA 백신 기술은 기존 백신과 달리 바이러스 자체가 아닌 유전자만을 사용해 안전하고 기존 백신 대비 광범위한 면역 반응을 유도할 수 있다는 장점이 있다.
연구팀은 감염 동물모델인 패럿에서 백신이 감염을 완벽하게 억제하며 소화기 증상, 혈소판 및 백혈구 감소, 고열, 간 수치 상승 등 감염 환자에서 발생하는 임상 증상들 역시 관찰되지 않음을 확인했다.
특히 연구팀은 해당 바이러스의 전체 유전자에 대한 5종의 백신을 구상해 SFTS 예방 백신 개발에 대한 전략적 접근법을 제시했다.
연구팀은 수동전달 기법(passive transfer)을 통해 바이러스의 당단백질에 대한 항체 면역 반응이 감염억제에 주요한 역할을 함을 규명했다. 또한, 비-당단백질에 대한 T세포 면역 반응 역시 감염 예방에 기여할 수 있음을 밝혔다.
박 교수는 “이번 연구는 SFTS 바이러스 감염을 완벽하게 방어할 수 있는 백신을 최초로 개발하고, 생쥐 모델이 아닌 환자의 임상 증상과 같게 발생하는 패럿 동물모델에서 완벽한 방어효능을 증명했다는 중요한 의의가 있다”라고 말했다.
최 교수는 “이번 SFTS 바이러스 백신 개발 연구 성과는 국제적으로 SFTS 백신 개발을 위한 기술적 우위를 확보했다는 중요한 의의가 있으며, 연구결과를 바탕으로 지속적인 연구를 통해 SFTS 바이러스 백신의 상용화에 기여할 수 있을 것이다”라고 말했다.
향후 임상개발은 이번 연구에 함께 참여한 DNA 백신 개발 전문기업인 진원생명과학(주)을 통해 진행할 계획이다.
이번 연구는 보건복지부 감염병위기대응기술개발사업의 지원을 받아 수행됐다.
2019.08.28 조회수 19316
박수형 교수, 중증열성혈소판감소증후군 예방 백신 개발
〈 박수형 교수 〉
우리 대학 의과학대학원 박수형 교수 연구팀이 일명 살인진드기병으로 불리는 중증열성혈소판감소증후군(SFTS) 바이러스 감염을 예방하는 백신을 개발했다.
충북대학교 의과대학 최영기 교수와 진원생명과학(주)이 함께 참여한 공동 연구팀은 개발한 백신이 감염 동물모델 실험을 통해 중증열성혈소판감소증후군 바이러스 감염을 완벽하게 억제할 수 있음을 증명했다.
이번 연구를 통해 예방 백신 도출 및 검증 성과뿐 아니라 면역학적 관점에서 백신의 감염 예방 효능을 극대화할 수 있는 항원을 제시함으로써, 추후 중증열성혈소판감소증후군 바이러스에 대한 대응 전략 확립 및 연구에 기여할 것으로 기대된다.
곽정은 박사과정과 충북대학교 김영일 박사가 1 저자로 참여한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 8월 23일 자 온라인판에 게재됐다. (논문명 : Development of a SFTSV DNA vaccine that confers complete protection against lethal infection in ferrets)
흔히 살인진드기병으로 알려진 SFTS는 SFTS 바이러스에 감염된 매개 진드기에 물려 발생하는 신종 감염병으로, 최근 발생 빈도 및 지역의 확산으로 WHO에서도 주의해야 할 10대 신, 변종 바이러스 감염병으로 지정한 질병이다.
일반적으로 6~14일의 잠복기 후 고열(38∼40℃)이 3~10일 이어지고, 혈소판 감소 및 백혈구 감소와 구토, 설사 등 소화기 증상이 발생하며, 일부 사례에서는 중증으로 진행돼 사망에 이르기도 한다.
2013년에 한국에서 처음으로 환자가 발생한 이래 발생 건수가 매년 꾸준히 증가하고 있지만, 진드기 접촉 최소화를 통한 예방이 제시될 뿐 현재까지 예방 백신이 개발되지 않았다.
연구팀은 31종의 서로 다른 SFTS 바이러스의 유전자 서열로부터 공통 서열을 도출해 백신 항원을 설계하고, 진원생명과학의 플랫폼을 이용해 DNA 백신을 제작했다.
DNA 백신 기술은 기존 백신과 달리 바이러스 자체가 아닌 유전자만을 사용해 안전하고 기존 백신 대비 광범위한 면역 반응을 유도할 수 있다는 장점이 있다.
연구팀은 감염 동물모델인 패럿에서 백신이 감염을 완벽하게 억제하며 소화기 증상, 혈소판 및 백혈구 감소, 고열, 간 수치 상승 등 감염 환자에서 발생하는 임상 증상들 역시 관찰되지 않음을 확인했다.
특히 연구팀은 해당 바이러스의 전체 유전자에 대한 5종의 백신을 구상해 SFTS 예방 백신 개발에 대한 전략적 접근법을 제시했다.
연구팀은 수동전달 기법(passive transfer)을 통해 바이러스의 당단백질에 대한 항체 면역 반응이 감염억제에 주요한 역할을 함을 규명했다. 또한, 비-당단백질에 대한 T세포 면역 반응 역시 감염 예방에 기여할 수 있음을 밝혔다.
박 교수는 “이번 연구는 SFTS 바이러스 감염을 완벽하게 방어할 수 있는 백신을 최초로 개발하고, 생쥐 모델이 아닌 환자의 임상 증상과 같게 발생하는 패럿 동물모델에서 완벽한 방어효능을 증명했다는 중요한 의의가 있다”라고 말했다.
최 교수는 “이번 SFTS 바이러스 백신 개발 연구 성과는 국제적으로 SFTS 백신 개발을 위한 기술적 우위를 확보했다는 중요한 의의가 있으며, 연구결과를 바탕으로 지속적인 연구를 통해 SFTS 바이러스 백신의 상용화에 기여할 수 있을 것이다”라고 말했다.
향후 임상개발은 이번 연구에 함께 참여한 DNA 백신 개발 전문기업인 진원생명과학(주)을 통해 진행할 계획이다.
이번 연구는 보건복지부 감염병위기대응기술개발사업의 지원을 받아 수행됐다.
2019.08.28 조회수 19316 -
 심남석 연구원, 난치성 뇌전증의 새로운 유전자 진단법 개발
〈 심남석 연구원 〉
우리 대학 의과학대학원 심남석 박사과정(지도교수 : 이정호 교수), 연세대학교 의료원(의료원장 윤도흠) 세브란스 어린이병원 신경외과 김동석 교수, 소아신경과 강훈철 교수 공동 연구팀이 난치성 뇌전증의 원인 돌연변이를 정확하게 분석할 수 있는 새로운 진단법을 개발했다.
이번 연구를 통해 기초 과학 분야와 임상 진료 영역 간 차이로 환자에게 쉽게 적용하지 못했던 난치성 뇌전증 원인 유전자 진단을 실제 임상 영역에서 시행할 수 있을 것으로 보이며, 이를 통해 환자들에게 더 나은 치료법을 제시할 수 있을 것으로 기대된다.
심남석 박사과정이 1 저자로 참여한 이번 연구는 뇌병리 분야 국제 학술지 ‘악타 뉴로패쏠로지카 (Acta Neuropathologica)’ 8월 3일 자 온라인판에 게재됐다. (논문명 : Precise detection of low-level somatic mutation in resected epilepsy brain tissue)
뇌전증은 전 세계적으로 4번째로 높은 유병률을 보이는 신경학적 질환으로 높은 사회 경제적 비용이 소모된다. 그중 전체 뇌전증의 3~40%를 차지하는 난치성 뇌전증은 약물치료로 조절되지 않고 위험성이 높아 수술 치료가 요구되는 질병이다.
최근 연구팀은 이 난치성 뇌전증이 뇌 체성(사람의 신체적 성질) 돌연변이에 의해 발생한다는 사실을 규명해 새 치료법을 제안한 바 있다. 그러나 뇌 국소 부위에서 발생한 소량의 돌연변이를 찾는 기존 진단법은 정확도가 30% 이하로 매우 낮아 실제 사용에는 어려움이 많다.
연구팀은 세브란스 병원에서 뇌수술을 받은 난치성 뇌전증 환자 232명의 뇌 조직 및 말초 조직(혈액 또는 침)을 분석해 돌연변이가 자주 발생하는 타겟 유전자를 확보했다. 이 타겟 유전자를 대상으로 표적 유전자 복제 염기서열 분석법을 적용해 체성 돌연변이를 분석했다.
연구팀은 고심도 유전체 분석을 통해 최적의 표적 유전자 선별, 고심도 시퀀싱 분석 및 방법의 조합을 찾아 진단 정확도를 50%에서 최대 100%까지 높이는 데 성공했다.
특히 임상에서 쉽게 확보할 수 있는 뇌 조직 절편만으로도 정확도가 100%에 가까운 체성 돌연변이 유전자 진단이 가능함을 확인했다.
1 저자인 심남석 연구원은 “난치성 뇌전증의 유전자 진단은 현재 임상시험 중인 새로운 치료법의 필수적인 과정이다”라며 “높은 효율, 낮은 비용으로 유전자 진단을 할 수 있게 만들어 고통받는 환아들에게 도움을 주고 싶다”라고 말했다.
연구팀은 이번 연구 결과를 바탕으로 교원창업 기업(소바젠, 대표 김병태)을 통해 빠르고 정확한 난치성 뇌전증 원인 유전자 진단 제공할 예정이다.
이번 연구는 서경배 과학재단, 한국연구재단, 보건복지부, 교원창업 기업 소바젠의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 연구에서 발견한 체세포성 돌연변이
2019.08.13 조회수 16995
심남석 연구원, 난치성 뇌전증의 새로운 유전자 진단법 개발
〈 심남석 연구원 〉
우리 대학 의과학대학원 심남석 박사과정(지도교수 : 이정호 교수), 연세대학교 의료원(의료원장 윤도흠) 세브란스 어린이병원 신경외과 김동석 교수, 소아신경과 강훈철 교수 공동 연구팀이 난치성 뇌전증의 원인 돌연변이를 정확하게 분석할 수 있는 새로운 진단법을 개발했다.
이번 연구를 통해 기초 과학 분야와 임상 진료 영역 간 차이로 환자에게 쉽게 적용하지 못했던 난치성 뇌전증 원인 유전자 진단을 실제 임상 영역에서 시행할 수 있을 것으로 보이며, 이를 통해 환자들에게 더 나은 치료법을 제시할 수 있을 것으로 기대된다.
심남석 박사과정이 1 저자로 참여한 이번 연구는 뇌병리 분야 국제 학술지 ‘악타 뉴로패쏠로지카 (Acta Neuropathologica)’ 8월 3일 자 온라인판에 게재됐다. (논문명 : Precise detection of low-level somatic mutation in resected epilepsy brain tissue)
뇌전증은 전 세계적으로 4번째로 높은 유병률을 보이는 신경학적 질환으로 높은 사회 경제적 비용이 소모된다. 그중 전체 뇌전증의 3~40%를 차지하는 난치성 뇌전증은 약물치료로 조절되지 않고 위험성이 높아 수술 치료가 요구되는 질병이다.
최근 연구팀은 이 난치성 뇌전증이 뇌 체성(사람의 신체적 성질) 돌연변이에 의해 발생한다는 사실을 규명해 새 치료법을 제안한 바 있다. 그러나 뇌 국소 부위에서 발생한 소량의 돌연변이를 찾는 기존 진단법은 정확도가 30% 이하로 매우 낮아 실제 사용에는 어려움이 많다.
연구팀은 세브란스 병원에서 뇌수술을 받은 난치성 뇌전증 환자 232명의 뇌 조직 및 말초 조직(혈액 또는 침)을 분석해 돌연변이가 자주 발생하는 타겟 유전자를 확보했다. 이 타겟 유전자를 대상으로 표적 유전자 복제 염기서열 분석법을 적용해 체성 돌연변이를 분석했다.
연구팀은 고심도 유전체 분석을 통해 최적의 표적 유전자 선별, 고심도 시퀀싱 분석 및 방법의 조합을 찾아 진단 정확도를 50%에서 최대 100%까지 높이는 데 성공했다.
특히 임상에서 쉽게 확보할 수 있는 뇌 조직 절편만으로도 정확도가 100%에 가까운 체성 돌연변이 유전자 진단이 가능함을 확인했다.
1 저자인 심남석 연구원은 “난치성 뇌전증의 유전자 진단은 현재 임상시험 중인 새로운 치료법의 필수적인 과정이다”라며 “높은 효율, 낮은 비용으로 유전자 진단을 할 수 있게 만들어 고통받는 환아들에게 도움을 주고 싶다”라고 말했다.
연구팀은 이번 연구 결과를 바탕으로 교원창업 기업(소바젠, 대표 김병태)을 통해 빠르고 정확한 난치성 뇌전증 원인 유전자 진단 제공할 예정이다.
이번 연구는 서경배 과학재단, 한국연구재단, 보건복지부, 교원창업 기업 소바젠의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 연구에서 발견한 체세포성 돌연변이
2019.08.13 조회수 16995 -
 박준성 연구원, 알츠하이머병의 새로운 원인 규명
〈 박준성 박사 〉
우리 대학 의과학대학원 박준성 박사(지도교수 : 이정호 교수), KISTI(한국과학기술정보연구원) 국가슈퍼컴퓨팅본부 유석종 박사 공동 연구팀이 노화 과정에서 발생하는 후천적 뇌 돌연변이가 알츠하이머병의 새 원인이 될 수 있다는 이론을 제시했다.
연구팀은 52명의 알츠하이머병 환자에게 얻은 사후 뇌 조직에서 전장 엑솜 유전체 서열(whole-exome sequencing) 데이터 분석을 통해 알츠하이머병에 존재하는 뇌 체성 유전변이를 찾아냈다. 또한, 뇌 체성 돌연변이가 알츠하이머병의 중요 원인으로 알려진 신경섬유다발 형성을 비정상적으로 증가시킴을 확인했다.
박준성 박사와 KISTI 이준학 박사가 공동 1 저자로 참여한 이번 연구는 국제 학술지 네이처 커뮤니케이션(Nature Communications) 7월 12일자 온라인판에 게재됐다. (논문명 : Brain somatic mutations observed in Alzheimer's disease associated with aging and dysregulation of tau phosphorylation)
노인성 치매의 가장 흔한 원인으로 알려진 알츠하이머병은 전 세계 GDP의 1%를 차지할 정도로 사회, 경제적 소모비용이 큰 질환이다. 하지만 여전히 알츠하이머병을 일으키는 분자 유전학적 원인은 명확하게 규명되지 않고 있다.
기존의 알츠하이머병 유전체 연구는 주로 환자의 말초조직인 혈액에서 전장유전체 연관분석(Genome-wide association study)을 하거나, 이미 가족력이 있는 환자에서 발견된 일부 유전자들(e.g., APP, PSEN1/2)에 대한 유전자 패널 분석 등이 주를 이루었다.
연구팀은 산발성 알츠하이머병 환자들에게 내후각피질에서 신경섬유다발이 공통으로 나타나는 현상에 주목해 알츠하이머병 환자의 뇌 조직에서 직접 엑솜 유전체 데이터를 생성해 알츠하이머병 뇌-특이적 체성 유전변이를 발굴했다.
연구팀은 알츠하이머병 환자와 정상인의 해마 형성체 부위를 레이저 현미 해부법을 통해 정밀하게 오려냈고, 저빈도의 체성 유전변이(Somatic mutation)를 정확하게 찾아내기 위해 대용량 고심도 엑솜 시퀀싱 데이터를 생성하고 저빈도 체성 유전변이 분석에 특화된 분석 파이프라인을 독자적으로 구축했다.
이러한 새 방법론을 통해 실제로 알츠하이머병 환자의 뇌에 체성 유전변이가 실제로 존재함을 체계적으로 규명함과 동시에 체성 유전변이의 누적속도 및 신경섬유다발 형성과의 관련성도 함께 밝혀냈다.
연구팀의 발견은 알츠하이머병의 발병에 체성 유전변이가 주요한 역할을 할 수 있음을 강력하게 시사하는 것으로, 알츠하이머병 유전체 연구에 대한 새로운 틀을 제시함과 동시에 향후 다른 신경퇴행성뇌질환의 연구에도 기여할 수 있을 것으로 기대된다.
연구팀은 이번 연구 결과를 바탕으로 교원 창업 기업(소바젠, 대표 김병태)을 통해 알츠하이머 질환의 진단과 치료제 개발에 나설 예정이다.
KISTI 유석종 박사는 연구팀이 구축한 저빈도 체성 유전변이 분석 파이프라인 및 빅데이터 분석을 위한 슈퍼컴퓨팅 기술을 통해 알츠하이머병의 새로운 발병 원리를 밝혀냈다라며 타 유전체 기반 연구에 활용할 수 있는 기반을 마련했다라고 말했다.
이번 연구는 서경배 과학재단, 보건복지부 및 한국과학기술정보연구원의 지원을 받아 수행됐고, 신속한 유전체 빅데이터 분석을 위해 KISTI의 슈퍼컴퓨터 5호기 누리온 시스템이 활용됐다.
□ 그림 설명
그림1. 본 연구에서 사용된 체성 유전변이 분석 파이프라인
그림2. 신경섬유성다발 형성에 관여하는 체성 유전변이
그림3. PIN1 유전자에 발생한 병원성 뇌 체성유전변이와 신경섬유다발 형성과의 관계 규명
2019.07.17 조회수 19779
박준성 연구원, 알츠하이머병의 새로운 원인 규명
〈 박준성 박사 〉
우리 대학 의과학대학원 박준성 박사(지도교수 : 이정호 교수), KISTI(한국과학기술정보연구원) 국가슈퍼컴퓨팅본부 유석종 박사 공동 연구팀이 노화 과정에서 발생하는 후천적 뇌 돌연변이가 알츠하이머병의 새 원인이 될 수 있다는 이론을 제시했다.
연구팀은 52명의 알츠하이머병 환자에게 얻은 사후 뇌 조직에서 전장 엑솜 유전체 서열(whole-exome sequencing) 데이터 분석을 통해 알츠하이머병에 존재하는 뇌 체성 유전변이를 찾아냈다. 또한, 뇌 체성 돌연변이가 알츠하이머병의 중요 원인으로 알려진 신경섬유다발 형성을 비정상적으로 증가시킴을 확인했다.
박준성 박사와 KISTI 이준학 박사가 공동 1 저자로 참여한 이번 연구는 국제 학술지 네이처 커뮤니케이션(Nature Communications) 7월 12일자 온라인판에 게재됐다. (논문명 : Brain somatic mutations observed in Alzheimer's disease associated with aging and dysregulation of tau phosphorylation)
노인성 치매의 가장 흔한 원인으로 알려진 알츠하이머병은 전 세계 GDP의 1%를 차지할 정도로 사회, 경제적 소모비용이 큰 질환이다. 하지만 여전히 알츠하이머병을 일으키는 분자 유전학적 원인은 명확하게 규명되지 않고 있다.
기존의 알츠하이머병 유전체 연구는 주로 환자의 말초조직인 혈액에서 전장유전체 연관분석(Genome-wide association study)을 하거나, 이미 가족력이 있는 환자에서 발견된 일부 유전자들(e.g., APP, PSEN1/2)에 대한 유전자 패널 분석 등이 주를 이루었다.
연구팀은 산발성 알츠하이머병 환자들에게 내후각피질에서 신경섬유다발이 공통으로 나타나는 현상에 주목해 알츠하이머병 환자의 뇌 조직에서 직접 엑솜 유전체 데이터를 생성해 알츠하이머병 뇌-특이적 체성 유전변이를 발굴했다.
연구팀은 알츠하이머병 환자와 정상인의 해마 형성체 부위를 레이저 현미 해부법을 통해 정밀하게 오려냈고, 저빈도의 체성 유전변이(Somatic mutation)를 정확하게 찾아내기 위해 대용량 고심도 엑솜 시퀀싱 데이터를 생성하고 저빈도 체성 유전변이 분석에 특화된 분석 파이프라인을 독자적으로 구축했다.
이러한 새 방법론을 통해 실제로 알츠하이머병 환자의 뇌에 체성 유전변이가 실제로 존재함을 체계적으로 규명함과 동시에 체성 유전변이의 누적속도 및 신경섬유다발 형성과의 관련성도 함께 밝혀냈다.
연구팀의 발견은 알츠하이머병의 발병에 체성 유전변이가 주요한 역할을 할 수 있음을 강력하게 시사하는 것으로, 알츠하이머병 유전체 연구에 대한 새로운 틀을 제시함과 동시에 향후 다른 신경퇴행성뇌질환의 연구에도 기여할 수 있을 것으로 기대된다.
연구팀은 이번 연구 결과를 바탕으로 교원 창업 기업(소바젠, 대표 김병태)을 통해 알츠하이머 질환의 진단과 치료제 개발에 나설 예정이다.
KISTI 유석종 박사는 연구팀이 구축한 저빈도 체성 유전변이 분석 파이프라인 및 빅데이터 분석을 위한 슈퍼컴퓨팅 기술을 통해 알츠하이머병의 새로운 발병 원리를 밝혀냈다라며 타 유전체 기반 연구에 활용할 수 있는 기반을 마련했다라고 말했다.
이번 연구는 서경배 과학재단, 보건복지부 및 한국과학기술정보연구원의 지원을 받아 수행됐고, 신속한 유전체 빅데이터 분석을 위해 KISTI의 슈퍼컴퓨터 5호기 누리온 시스템이 활용됐다.
□ 그림 설명
그림1. 본 연구에서 사용된 체성 유전변이 분석 파이프라인
그림2. 신경섬유성다발 형성에 관여하는 체성 유전변이
그림3. PIN1 유전자에 발생한 병원성 뇌 체성유전변이와 신경섬유다발 형성과의 관계 규명
2019.07.17 조회수 19779 -
 주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 25767
주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 25767 -
 이흥규 교수, 수지상세포 자식작용의 역할 규명
〈 이흥규 교수 〉
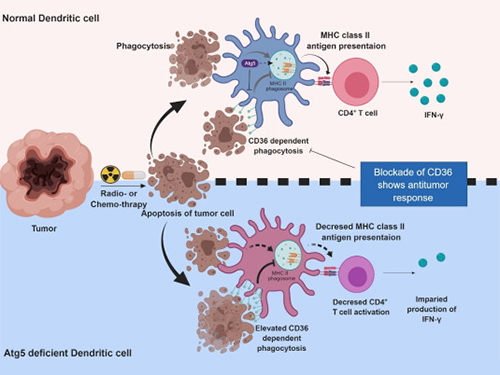
세포 항상성을 유지해주는 ‘자식작용’의 또 다른 기능이 보고됐다. 우리 대학 의과학대학원 이흥규 교수 연구팀이 T세포의 항암 활성이 유도되는 과정에서 수지상세포 자식작용이 기여함을 규명했다.
이번 연구결과는 국제학술지 ‘오토파지(Autophagy)’ 3월 22일 자에 게재됐다.
자식작용은 세포 내 노폐물 및 손상된 세포 소기관을 제거해 세포의 항상성을 유지하는 과정이다.
수지상세포는 병원균이나 암 항원을 인지해 T세포의 면역반응을 유도하는 세포이다. 방사선이나 항암제에 의해 암세포가 사멸하면 수지상세포가 이를 흡수‧제거하고, 자신의 표면에 항원을 제시해 T세포에 전달해주는 기능을 한다.
연구팀은 수지상세포의 자식작용이 T세포 활성화에서 핵심 역할을 한다는 것을 밝히고 항암 효과를 높일 수 있는 원리를 제시했다.
실험결과 자식작용을 일으키는 Atg5 유전자가 결손될 때 수지상세포의 T세포 활성화 기능이 떨어지고 항암 면역반응이 감소했다.
Atg5가 결손되면 수지상세포 표면의 CD36 수용체가 월등히 증가하는데, 이로 인해 식세포작용(암 항원의 흡수)만 과활성되고 항원 제시를 통한 T세포 활성화가 정상적으로 이뤄지지 않는다.
이때 항체를 도입해 CD36 수용체를 다시 억제하면 T세포 면역반응이 많이 증가하고 암의 성장이 억제됐다.
이흥규 교수는 “이번 연구를 통해 자식작용이 T세포의 항암 면역반응에 관여하는 기능을 새롭게 규명했다”라 “향후 CD36 수용체를 활용한 표적 항암치료제 개발의 단초가 되길 기대한다”라고 밝혔다.
이 연구성과는 과학기술정보통신부·한국연구재단 바이오‧의료기술개발사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 수지상세포 자식작용의 기전
그림2. 항원제시에서 수지상세포 자식작용의 기능
2019.04.02 조회수 18156
이흥규 교수, 수지상세포 자식작용의 역할 규명
〈 이흥규 교수 〉
세포 항상성을 유지해주는 ‘자식작용’의 또 다른 기능이 보고됐다. 우리 대학 의과학대학원 이흥규 교수 연구팀이 T세포의 항암 활성이 유도되는 과정에서 수지상세포 자식작용이 기여함을 규명했다.
이번 연구결과는 국제학술지 ‘오토파지(Autophagy)’ 3월 22일 자에 게재됐다.
자식작용은 세포 내 노폐물 및 손상된 세포 소기관을 제거해 세포의 항상성을 유지하는 과정이다.
수지상세포는 병원균이나 암 항원을 인지해 T세포의 면역반응을 유도하는 세포이다. 방사선이나 항암제에 의해 암세포가 사멸하면 수지상세포가 이를 흡수‧제거하고, 자신의 표면에 항원을 제시해 T세포에 전달해주는 기능을 한다.
연구팀은 수지상세포의 자식작용이 T세포 활성화에서 핵심 역할을 한다는 것을 밝히고 항암 효과를 높일 수 있는 원리를 제시했다.
실험결과 자식작용을 일으키는 Atg5 유전자가 결손될 때 수지상세포의 T세포 활성화 기능이 떨어지고 항암 면역반응이 감소했다.
Atg5가 결손되면 수지상세포 표면의 CD36 수용체가 월등히 증가하는데, 이로 인해 식세포작용(암 항원의 흡수)만 과활성되고 항원 제시를 통한 T세포 활성화가 정상적으로 이뤄지지 않는다.
이때 항체를 도입해 CD36 수용체를 다시 억제하면 T세포 면역반응이 많이 증가하고 암의 성장이 억제됐다.
이흥규 교수는 “이번 연구를 통해 자식작용이 T세포의 항암 면역반응에 관여하는 기능을 새롭게 규명했다”라 “향후 CD36 수용체를 활용한 표적 항암치료제 개발의 단초가 되길 기대한다”라고 밝혔다.
이 연구성과는 과학기술정보통신부·한국연구재단 바이오‧의료기술개발사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 수지상세포 자식작용의 기전
그림2. 항원제시에서 수지상세포 자식작용의 기능
2019.04.02 조회수 18156 -
 신의철 교수, 한국과학기술한림원 2019년도 정회원 선정
〈 신 의 철 교수 〉
우리대학 의과학대학원 신의철 교수 등 26명의 국내 과학자가 한국과학기술한림원(원장 이명철) 2019년 신입 정회원으로 선정됐다. 신의철 교수는 네이처 리뷰 면역학에 초청 리뷰논문을 게재한 국내 대표적인 바이러스 면역학자로 꼽힌다.
이밖에 과기한림원은 만 43세 이하 젊은 과학자 중 잠재력과 창의성이 높은 차세대연구자 26명도 선발, 발표했는데 우리대학에서는 이지운 교수(수리과학과)와 임미희 교수(화학과), 김신현 교수(생명화학공학과), 이정률 교수(항공우주공학과), 이현주 교수(생명화학공학과), 정연식 교수(신소재공학과) 등 6명이 학계와 산업계로부터 주목받는 2019년 신입 차세대회원으로 선정됐다.
한국과학기술한림원은 21일 서울 양재동 엘타워에서 2019년도 신년 하례식을 갖고 이들 신입정회원 및 차세대회원을 대상으로 신입회원 회원패 수여식을 가졌다. 이날 하례식에는 이명철 과기한림원장과 문미옥 과학기술정보통신부 제1차관 등 과학기술계 인사 150여명이 같이했다.
2019.01.21 조회수 9817
신의철 교수, 한국과학기술한림원 2019년도 정회원 선정
〈 신 의 철 교수 〉
우리대학 의과학대학원 신의철 교수 등 26명의 국내 과학자가 한국과학기술한림원(원장 이명철) 2019년 신입 정회원으로 선정됐다. 신의철 교수는 네이처 리뷰 면역학에 초청 리뷰논문을 게재한 국내 대표적인 바이러스 면역학자로 꼽힌다.
이밖에 과기한림원은 만 43세 이하 젊은 과학자 중 잠재력과 창의성이 높은 차세대연구자 26명도 선발, 발표했는데 우리대학에서는 이지운 교수(수리과학과)와 임미희 교수(화학과), 김신현 교수(생명화학공학과), 이정률 교수(항공우주공학과), 이현주 교수(생명화학공학과), 정연식 교수(신소재공학과) 등 6명이 학계와 산업계로부터 주목받는 2019년 신입 차세대회원으로 선정됐다.
한국과학기술한림원은 21일 서울 양재동 엘타워에서 2019년도 신년 하례식을 갖고 이들 신입정회원 및 차세대회원을 대상으로 신입회원 회원패 수여식을 가졌다. 이날 하례식에는 이명철 과기한림원장과 문미옥 과학기술정보통신부 제1차관 등 과학기술계 인사 150여명이 같이했다.
2019.01.21 조회수 9817 -
 2018 올해의 KAIST인에 의과학대학원 이정호 교수 선정
〈 이 정 호 교수 〉
우리 대학 의과학대학원 이정호(41) 교수가 ‘2018년 올해의 KAIST인’에 선정됐다.
18회째를 맞는 ‘올해의 KAIST인 상’은 한 해 동안 국내외에서 학교의 발전을 위해 노력하고 탁월한 교육·연구실적을 낸 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
수상자인 이정호 교수는 후천성 뇌 돌연변이에 의한 난치성 뇌전증의 발생 원리와 치료법을 최초로 규명한 연구 성과를 ‘네이처 메디슨(Nature Medicine)지에 2015년, 2018년에 게재했다. 또한 한국인으로서는 최초로 난치성 뇌전증의 유전 병리학적 진단기준을 세우는 세계 뇌전증학회 핵심위원으로 참여해 국제기준을 만드는 공로를 인정받았다.
특히 작년 8월에는 악성 뇌종양인 교모세포종 돌연변이가 암 부위가 아닌 암에서 멀리 떨어진 뇌실하영역에서 발생한다는 사실을 최초로 규명해 국제학술지 ‘네이처(Nature)’에 논문을 게재하기도 했다. 이는 기존의 학설을 뒤집는 연구결과로 국내외 언론으로부터 많은 주목을 받았다.
이 교수는 이 같은 연구 성과를 기반으로 난치성 뇌질환 신약개발 바이오벤처 회사인‘소바젠’(대표이사: 김병태) 설립을 통해 난치성 뇌전증과 교모세포종에 대한 혁신적인 치료제를 개발 중이다.
이정호 교수는“KAIST인이라면 누구나 최고의 명예로 생각하는 상을 받게 돼 개인적으로는 매우 큰 영광이며 동시에 무거운 책임감을 느낀다”라며“각종 난치병에 대한 원인을 규명하고 새로운 치료법을 개발하는 연구를 통해 인류의 건강한 삶을 구현하는 한편 국내외에서 KAIST의 위상을 높이는데 기여하겠다”라고 말했다.
2019.01.02 조회수 10532
2018 올해의 KAIST인에 의과학대학원 이정호 교수 선정
〈 이 정 호 교수 〉
우리 대학 의과학대학원 이정호(41) 교수가 ‘2018년 올해의 KAIST인’에 선정됐다.
18회째를 맞는 ‘올해의 KAIST인 상’은 한 해 동안 국내외에서 학교의 발전을 위해 노력하고 탁월한 교육·연구실적을 낸 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
수상자인 이정호 교수는 후천성 뇌 돌연변이에 의한 난치성 뇌전증의 발생 원리와 치료법을 최초로 규명한 연구 성과를 ‘네이처 메디슨(Nature Medicine)지에 2015년, 2018년에 게재했다. 또한 한국인으로서는 최초로 난치성 뇌전증의 유전 병리학적 진단기준을 세우는 세계 뇌전증학회 핵심위원으로 참여해 국제기준을 만드는 공로를 인정받았다.
특히 작년 8월에는 악성 뇌종양인 교모세포종 돌연변이가 암 부위가 아닌 암에서 멀리 떨어진 뇌실하영역에서 발생한다는 사실을 최초로 규명해 국제학술지 ‘네이처(Nature)’에 논문을 게재하기도 했다. 이는 기존의 학설을 뒤집는 연구결과로 국내외 언론으로부터 많은 주목을 받았다.
이 교수는 이 같은 연구 성과를 기반으로 난치성 뇌질환 신약개발 바이오벤처 회사인‘소바젠’(대표이사: 김병태) 설립을 통해 난치성 뇌전증과 교모세포종에 대한 혁신적인 치료제를 개발 중이다.
이정호 교수는“KAIST인이라면 누구나 최고의 명예로 생각하는 상을 받게 돼 개인적으로는 매우 큰 영광이며 동시에 무거운 책임감을 느낀다”라며“각종 난치병에 대한 원인을 규명하고 새로운 치료법을 개발하는 연구를 통해 인류의 건강한 삶을 구현하는 한편 국내외에서 KAIST의 위상을 높이는데 기여하겠다”라고 말했다.
2019.01.02 조회수 10532