연구

〈 왼쪽 위부터 시계방향으로 이승섭 교수, 이봉재 교수, 임미경 박사, 송재만 박사과정 〉
우리 대학 기계공학과 이봉재 교수와 이승섭 교수 연구팀이 금속-유전체 다층구조 사이의 근접장 복사열전달량을 측정하고 제어하는 데 성공했다.
연구팀의 복사열전달 제어 기술은 차세대 반도체 패키징과 열광전지, 열관리 시스템 등에 적용 가능하고 폐열의 재사용을 통한 에너지 절감, 사물인터넷 센서의 지속적 전력 공급원 등에 응용 가능할 것으로 기대된다.
임미경 박사와 송재만 박사과정이 주도한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 10월 16일자 온라인 판에 게재됐다. (논문명 : Tailoring Near-Field Thermal Radiation between Metallo-Dielectric Multilayers using Coupled Surface Plasmon Polaritons, 표면 플라즈몬 폴라리톤 커플링을 이용한 금속-유전체 다층구조 사이의 근접장 복사열전달 제어)
두 물체 사이의 거리가 나노미터 단위일 때 물체 사이의 복사열전달은 거리가 가까워질수록 매우 크게 증가한다. 그 값은 복사열전달량의 이론적인 최댓값이라 여겨졌던 흑체 복사열전달량보다 1천 배에서 1만 배 이상 커질 수 있다. 이 현상을 근접장 복사열전달이라고 한다.
최근 나노기술의 발전으로 다양한 물질 사이의 근접장 복사열전달을 규명하는 연구가 활발히 진행되고 있다. 특히 나노구조에서 발생하는 표면 폴라리톤 커플링을 이용하면 두 물체 사이의 근접장 복사열전달량을 크게 향상시킬 수 있을 뿐 아니라 파장에 따른 복사열전달 제어가 가능해진다.
이런 이유로 박막, 다층나노구조, 나노와이어 등 나노구조를 도입한 근접장 복사열전달 적용 장치에 대한 이론 연구가 계속 진행되고 있다. 그러나 현재까지 대부분의 연구는 등방성(等方性) 물질 사이의 근접장 복사열전달만을 측정하는 데 초점이 맞춰졌다.
이봉재, 이승섭 교수 공동 연구팀은 커스텀 MEMS 장치 통합 플랫픔과 3축 위치 나노제어 시스템을 이용해 금속-유전체 다층나노구조 사이의 진공 거리에 따른 근접장 복사열전달량을 최초로 측정하는 데 성공했다.
금속-유전체 다층나노구조는 일정한 두께를 갖는 금속과 유전체가 반복적으로 쌓인 구조를 말한다. 금속-유전체 단일 층 쌍을 단위 셀이라 부르며 단위 셀에서 금속 층이 차지하는 두께의 비율을 충전인자라 한다.
연구팀은 다층나노구조의 충전인자와 단위 셀 개수의 변화에 따른 근접장 복사열전달량 측정 결과를 통해 표면 플라즈몬 폴라리톤 커플링으로 근접장 복사열전달량을 크게 향상시켰으며, 나아가 열전달의 파장별 제어가 가능함을 증명했다.
연구를 주도한 이봉재 교수는 “그동안 실험적으로 규명된 등방성 물질은 근접장 복사열전달의 파장별 제어에 한계가 있었다”며 “이번에 밝혀낸 다층나노구조를 사용한 근접장 복사열전달 제어 기술은 열광전지, 다이오드, 복사냉각 등 다양한 근접장 복사열전달 적용 장치 개발에 첫걸음이 될 것으로 기대된다”고 말했다.
이번 연구는 한국연구재단 중견연구자사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 근접장 복사열전달 측정 3차원 개념도와 개발한 장치
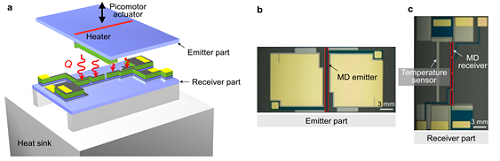
그림2. 금속-유전체 다층나노구조의 충전 인자에 따른 복사 열전달량 분석 결과
-
인물 제30회 삼성휴먼테크논문대상에서 물리학과 정채화 학생 은상 수상
제30회 삼성휴먼테크논문대상에서 우리 대학 물리학과 정채화 학생(지도교수 : 물리학과 양용수 교수)이 기초과학분야 은상을 수상했다. 삼성휴먼테크논문대상은 과학기술 분야의 주역이 될 젊고 우수한 과학자를 발굴하기 위해 1994년부터 시행 중이며 과학기술정보통신부와 중앙일보가 공동 후원하고 있다. 이번 제30회 대회에는 총 1189편의 논문이 접수되었으며, 797명에 달하는 전문가들이 심사를 진행하였다. 정채화 학생은 2000년대 초반 이론적으로만 예측되었으나 20년 이상 풀리지 않았던 난제인 0차원 강유전체에서의 위상학적 분극 정렬을 세계 최초로 실험적으로 규명하였다. 영구자석과 같이 외부의 자기장이 없어도 자화 상태를 스스로 유지할 수 있는 물질들을 강자성체(ferromagnet)라 하고, 강유전체(ferroelectric)는 외부의 전기장 없어도 분극상태를 유지할 수 있는 물질로서 강자성체의 전기(electric) 버전이라고 생각하면 된다. 강자성체(자석)의 경우 나노크
2024-04-04 -
연구 화학물질 없이 식각하는 반도체 기술 최초 개발
차세대 반도체 메모리의 소재로 주목을 받고 있는 강유전체는 차세대 메모리 소자 혹은 작은 물리적 변화를 감지하는 센서로 활용되는 등 그 중요성이 커지고 있다. 이에 반도체의 핵심 소자가 되는 강유전체를 화학물질없이 식각할 수 있는 연구를 성공해 화제다. 우리 대학 신소재공학과 홍승범 교수가 제네바 대학교와 국제공동연구를 통해 강유전체 표면의 비대칭 마멸* 현상을 세계 최초로 관찰 및 규명했고, 이를 활용해 혁신적인 나노 패터닝 기술**을 개발했다고 26일 밝혔다. *마멸: 물체 표면의 재료가 점진적으로 손실 또는 제거되는 현상 **나노 패터닝 기술: 나노스케일로 소재의 표면에 정밀한 패턴을 생성하여 다양한 첨단 기술 분야에서 제품 성능을 향상시키는데 사용되는 기술 연구팀은 강유전체 소재의 표면 특성에 관한 연구에 집중했다. 이들은 원자간력 현미경(Atomic Force Microscopy)을 활용해 다양한 강유전체의 트라이볼로지(Tribology, 마찰 및 마모) 현상
2024-03-26 -
연구 방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다. 우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다. 이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으
2024-02-15 -
연구 정크 DNA가 노화와 발암에 관여한다
인간 유전체 중 일반적인 단백질 생성 유전자는 전체 염기서열의 1% 정도에 불과하며 나머지 99%의 유전체 영역은 그 기능이 뚜렷하게 알려지지 않아 ‘쓸모없는 DNA’라는 뜻으로 ‘정크 DNA’라고 불리고 있다. 정크 DNA 가운데 약 1/6을 차지하는 L1 점핑 유전자는 활성화될 경우 세포의 유전정보를 파괴하거나 교란하는 역할을 할 수 있어 사람의 진화 과정에서 불활성화(화석화) 됐다고 알려져 있었다. 하지만 이번 연구에서 L1 점핑 유전자가 활성화되며, 노화와 발암 과정에 연관이 있음을 처음 확인하였다. 우리 대학 의과학대학원 주영석 교수 연구팀이 서울대학교병원 외과 김민정 교수, 고려대학교 의과대학 권현우 교수팀과의 공동연구로 ‘L1 점핑 유전자’의 활성화에 의한 사람 대장 상피 세포의 유전체 파괴 현상을 규명했다고 15일 밝혔다. 의과학대학원 남창현 박사과정과 육정환 박사(現 서울대병원 내과 임상조교수)
2023-05-15 -
연구 파킨슨병 발병 3차원 게놈 지도 최초 제시
파킨슨병은 60세 이상 인구의 1.2% 이상 발병하는 흔한 퇴행성 뇌 질환으로 급격한 인구 고령화에 따라 전 세계적으로 발병률이 증가하고 있어, 2040년 약 1,420만 명의 환자가 발병할 것으로 예측되고 있다. 현재 파킨슨병의 다양한 발병 원인이 명확하게 규명되지 않은 상황에서, 비정상적으로 발생하는 후성 유전학적 특징들이 파킨슨병 발병에 관여하는 것을 최초로 확인되어 화제다. 우리 대학 생명과학과 정인경 교수 연구팀이 미국 국립보건원(National Institute of Health, NIH) 산하 국립노화연구소(National Institute on Aging, NIA) 엘리에자 매슬리아(Eliezer Masliah) 교수와의 공동연구를 통해 전 세계 최초로 파킨슨병 발병 뇌 조직의 단일세포 3차원 후성유전체 지도를 작성하고, 이를 토대로 656개의 파킨슨병 연관 신규 유전자들을 제시했다고 8일 밝혔다. 이번 연구에서 연구팀은 최신 개발된 단일세포 유전체 기술과
2023-05-08