-
 방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
2024.02.15
조회수 998
-
 100큐비트급 양자컴퓨터 계산데이터 전격 공개
양자컴퓨터는 양자역학의 원리를 활용해 기존의 컴퓨터로는 풀기 어려운 계산을 할 수 있는 컴퓨터다. 양자컴퓨터는 암호 해독, 배터리 소재 개발, 신약 개발 등 다양한 분야에서 그동안 풀지 못한 난제들을 해결할 미래 기술로 주목받고 있다.
우리 대학 물리학과 안재욱 교수 연구팀이 100큐비트급 양자컴퓨터로 조합 최적화 문제를 계산해 계산 결과 데이터베이스와 계산 프로그램을 공개했다고 13일 밝혔다.
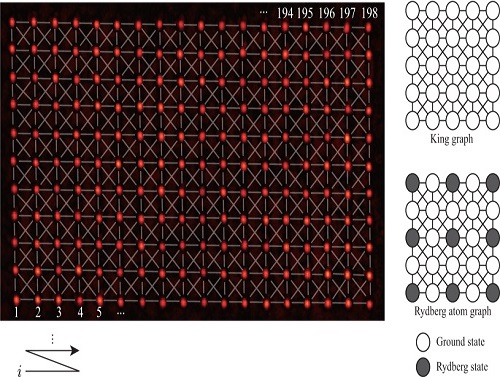
조합 최적화 문제 중 하나인 최대 독립집합 문제(Maximum independent set problem)는 SNS상에서 가장 영향력 있는 인물을 찾는 문제, 전력망을 가장 효율적으로 분배하는 법을 찾는 문제 등 다양한 응용이 가능한 문제다. 지난 2023년 KAIST 연구진은 20큐비트급 리드버그 양자컴퓨터를 이용해 최대 독립집합 문제의 풀이를 시연한 바 있다.
일반적으로 100큐비트급 양자컴퓨터의 데이터를 얻기 위해서는 직접 양자컴퓨터를 제작하거나 클라우드 서비스 업체를 이용할 수밖에 없다. 이번에 KAIST 연구진이 공개한 데이터는 관련 분야 연구자뿐 아니라 양자 컴퓨터에 관심 있는 모든 사람이 무료로 데이터에 접근할 수 있게 되었다는 점에서 중요하다고 할 수 있다. 최대 141큐비트를 활용해 70만 종류 이상의 그래프 최적화를 계산했고, 양자컴퓨터의 계산 결과와 데이터분석 프로그램 일체를 공개했다.
연구를 주도한 안재욱 교수는 “이번 연구를 통해 100큐비트급 양자컴퓨터를 활용한 난제 계산 결과 및 계산 프로그램을 모두 공개하여 그동안 양자컴퓨터에 접근이 어려웠던 연구자를 비롯한 많은 사람이 양자 컴퓨팅 연구에 참여할 수 있을 것으로 기대된다. 아울러, 고성능 양자컴퓨터 개발에 필요한 잡음 분석에도 연구팀이 계산한 데이터베이스가 활용될 수 있을 것이라 생각한다”고 말했다.
우리 대학 물리학과 김강흔, 박주영, 변우정 석박사통합과정, 김민혁 박사(現 고려대 물리학과 교수)가 참여한 해당 연구 결과는 국제 학술지 네이처(Nature) 자매지인 ‘사이언티픽 데이터(Scientific data)’1월 11권에 게재됐다. (논문명: Quantum computing dataset of maximum independent set problem on king lattice of over hundred Rydberg atoms).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
100큐비트급 양자컴퓨터 계산데이터 전격 공개
양자컴퓨터는 양자역학의 원리를 활용해 기존의 컴퓨터로는 풀기 어려운 계산을 할 수 있는 컴퓨터다. 양자컴퓨터는 암호 해독, 배터리 소재 개발, 신약 개발 등 다양한 분야에서 그동안 풀지 못한 난제들을 해결할 미래 기술로 주목받고 있다.
우리 대학 물리학과 안재욱 교수 연구팀이 100큐비트급 양자컴퓨터로 조합 최적화 문제를 계산해 계산 결과 데이터베이스와 계산 프로그램을 공개했다고 13일 밝혔다.
조합 최적화 문제 중 하나인 최대 독립집합 문제(Maximum independent set problem)는 SNS상에서 가장 영향력 있는 인물을 찾는 문제, 전력망을 가장 효율적으로 분배하는 법을 찾는 문제 등 다양한 응용이 가능한 문제다. 지난 2023년 KAIST 연구진은 20큐비트급 리드버그 양자컴퓨터를 이용해 최대 독립집합 문제의 풀이를 시연한 바 있다.
일반적으로 100큐비트급 양자컴퓨터의 데이터를 얻기 위해서는 직접 양자컴퓨터를 제작하거나 클라우드 서비스 업체를 이용할 수밖에 없다. 이번에 KAIST 연구진이 공개한 데이터는 관련 분야 연구자뿐 아니라 양자 컴퓨터에 관심 있는 모든 사람이 무료로 데이터에 접근할 수 있게 되었다는 점에서 중요하다고 할 수 있다. 최대 141큐비트를 활용해 70만 종류 이상의 그래프 최적화를 계산했고, 양자컴퓨터의 계산 결과와 데이터분석 프로그램 일체를 공개했다.
연구를 주도한 안재욱 교수는 “이번 연구를 통해 100큐비트급 양자컴퓨터를 활용한 난제 계산 결과 및 계산 프로그램을 모두 공개하여 그동안 양자컴퓨터에 접근이 어려웠던 연구자를 비롯한 많은 사람이 양자 컴퓨팅 연구에 참여할 수 있을 것으로 기대된다. 아울러, 고성능 양자컴퓨터 개발에 필요한 잡음 분석에도 연구팀이 계산한 데이터베이스가 활용될 수 있을 것이라 생각한다”고 말했다.
우리 대학 물리학과 김강흔, 박주영, 변우정 석박사통합과정, 김민혁 박사(現 고려대 물리학과 교수)가 참여한 해당 연구 결과는 국제 학술지 네이처(Nature) 자매지인 ‘사이언티픽 데이터(Scientific data)’1월 11권에 게재됐다. (논문명: Quantum computing dataset of maximum independent set problem on king lattice of over hundred Rydberg atoms).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.02.13
조회수 1442
-
 RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07
조회수 1562
-
 입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01
조회수 1356
-
 지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30
조회수 1665
-
 양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29
조회수 1472
-
 음악 본능을 인공지능으로 밝혀내다
음악은 세계 공통어로 불릴만큼 문화적 보편 요소로 알려졌다. 그렇다면 어떻게 다양한 문화권의 환경 차이에도 불구하고, ‘음악적 본능’은 어느 정도 공유될 수 있는 것일까?
우리 대학 물리학과 정하웅 교수 연구팀이 인공신경망 모델을 활용해, 사람 뇌에서 특별한 학습 없이도 음악 본능이 나타날 수 있는 원리를 규명했다고 16일 밝혔다.
기존 학자들은 다양한 문화권에 존재하는 음악의 보편성과 차별성을 규명하고, 어떻게 이런 공통성이 나타날 수 있는지에 대해 이해하고자 시도해 왔다. 2019년 세계적인 과학 저널 ‘사이언스’에 게재된 연구를 통해 민족지학적으로 구분된 모든 문화에서 음악을 만들어 내고, 유사한 형태의 박자와 멜로디가 사용된다는 것이 발견됐다. 또한, 신경과학자들은 우리 뇌의 청각 피질(Auditory cortex)에 음악 정보처리를 담당하는 특정한 영역이 존재한다는 것을 밝혀냈다.
연구팀은 인공신경망을 사용해, 음악에 대한 학습 없이도 자연에 대한 소리 정보 학습을 통해 음악 인지 기능이 자발적으로 형성됨을 보였다. (그림2) 연구팀은 구글에서 제공하는 대규모 소리 데이터(AudioSet)를 활용해, 인공신경망이 이러한 다양한 소리 데이터를 인식하도록 학습했다. 흥미롭게도, 연구팀은 네트워크 모델 내에 음악에 선택적으로 반응하는 뉴런(신경계의 단위)이 발생함을 발견했다. 즉, 사람의 말(speech), 동물 소리, 환경 소리, 기계 소리 등의 다양한 소리에는 거의 반응을 보이지 않으나 기악이나 성악 등 다양한 음악에 대해서는 높은 반응을 보이는 뉴런들이 자발적으로 형성된 것이다.
이 인공신경망 뉴런들은 실제 뇌의 음악정보처리 영역의 뉴런들과 유사한 반응 성질을 보였다. 예를 들어, 인공 뉴런은 음악을 시간적으로 잘게 나누어 재배열한 소리에 대해 감소된 반응을 보였다. 이는 자발적으로 나타난 음악 선택성 뉴런들이 음악의 시간적 구조를 부호화하고 있음을 의미한다. 이러한 성질은 특정 장르의 음악에만 국한된 것이 아니라, 클래식, 팝, 락, 재즈, 전자음악 등 25개에 달하는 다양한 장르 각각에 대해서도 공통적으로 나타났다.
심지어, 네트워크에서 음악 선택성 뉴런의 활동을 억제하게 되면, 다른 자연 소리에 대한 인식 정확도를 크게 떨어뜨릴 수 있음을 보였다. 즉, 음악 정보처리 기능이 다른 자연 소리 정보처리에 도움을 주며, 따라서 ‘음악성’이란 자연 소리를 처리하기 위한 진화적 적응에 의해 형성되는 본능일 수 있다는 설명이다.
연구를 주도한 정하웅 교수는 “이러한 결과는 다양한 문화권에서 음악 정보처리의 공통된 기저를 형성하는데, 자연 소리 정보처리를 위한 진화적 압력이 기여했을 수 있음을 시사한다”며, “사람과 유사한 음악성을 인공적으로 구현하여, 음악 생성 AI, 음악 치료, 음악 인지 연구 등에 원천 모델로 활용될 수 있을 것으로 기대한다”고 연구의 의의를 설명했다. 그러나 “현 연구는 음악 학습에 의한 발달 과정을 고려하고 있지 않으며, 발달 초기의 기초적인 음악 정보처리에 대한 논의임을 주의해야 한다”고 연구의 한계를 덧붙였다.
우리 대학 물리학과 김광수 박사(現 MIT 뇌인지과학과)가 제1 저자로, 김동겸 박사(現 IBS)와 함께 진행한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 출판됐다. (논문명: ‘Spontaneous emergence of rudimentary music detectors in deep neural networks’, 국문 번역: ‘심층신경망에서 음악 인지기능의 자발적 발생’)
한편 이번 연구는 한국연구재단의 지원을 통해 수행됐다.
음악 본능을 인공지능으로 밝혀내다
음악은 세계 공통어로 불릴만큼 문화적 보편 요소로 알려졌다. 그렇다면 어떻게 다양한 문화권의 환경 차이에도 불구하고, ‘음악적 본능’은 어느 정도 공유될 수 있는 것일까?
우리 대학 물리학과 정하웅 교수 연구팀이 인공신경망 모델을 활용해, 사람 뇌에서 특별한 학습 없이도 음악 본능이 나타날 수 있는 원리를 규명했다고 16일 밝혔다.
기존 학자들은 다양한 문화권에 존재하는 음악의 보편성과 차별성을 규명하고, 어떻게 이런 공통성이 나타날 수 있는지에 대해 이해하고자 시도해 왔다. 2019년 세계적인 과학 저널 ‘사이언스’에 게재된 연구를 통해 민족지학적으로 구분된 모든 문화에서 음악을 만들어 내고, 유사한 형태의 박자와 멜로디가 사용된다는 것이 발견됐다. 또한, 신경과학자들은 우리 뇌의 청각 피질(Auditory cortex)에 음악 정보처리를 담당하는 특정한 영역이 존재한다는 것을 밝혀냈다.
연구팀은 인공신경망을 사용해, 음악에 대한 학습 없이도 자연에 대한 소리 정보 학습을 통해 음악 인지 기능이 자발적으로 형성됨을 보였다. (그림2) 연구팀은 구글에서 제공하는 대규모 소리 데이터(AudioSet)를 활용해, 인공신경망이 이러한 다양한 소리 데이터를 인식하도록 학습했다. 흥미롭게도, 연구팀은 네트워크 모델 내에 음악에 선택적으로 반응하는 뉴런(신경계의 단위)이 발생함을 발견했다. 즉, 사람의 말(speech), 동물 소리, 환경 소리, 기계 소리 등의 다양한 소리에는 거의 반응을 보이지 않으나 기악이나 성악 등 다양한 음악에 대해서는 높은 반응을 보이는 뉴런들이 자발적으로 형성된 것이다.
이 인공신경망 뉴런들은 실제 뇌의 음악정보처리 영역의 뉴런들과 유사한 반응 성질을 보였다. 예를 들어, 인공 뉴런은 음악을 시간적으로 잘게 나누어 재배열한 소리에 대해 감소된 반응을 보였다. 이는 자발적으로 나타난 음악 선택성 뉴런들이 음악의 시간적 구조를 부호화하고 있음을 의미한다. 이러한 성질은 특정 장르의 음악에만 국한된 것이 아니라, 클래식, 팝, 락, 재즈, 전자음악 등 25개에 달하는 다양한 장르 각각에 대해서도 공통적으로 나타났다.
심지어, 네트워크에서 음악 선택성 뉴런의 활동을 억제하게 되면, 다른 자연 소리에 대한 인식 정확도를 크게 떨어뜨릴 수 있음을 보였다. 즉, 음악 정보처리 기능이 다른 자연 소리 정보처리에 도움을 주며, 따라서 ‘음악성’이란 자연 소리를 처리하기 위한 진화적 적응에 의해 형성되는 본능일 수 있다는 설명이다.
연구를 주도한 정하웅 교수는 “이러한 결과는 다양한 문화권에서 음악 정보처리의 공통된 기저를 형성하는데, 자연 소리 정보처리를 위한 진화적 압력이 기여했을 수 있음을 시사한다”며, “사람과 유사한 음악성을 인공적으로 구현하여, 음악 생성 AI, 음악 치료, 음악 인지 연구 등에 원천 모델로 활용될 수 있을 것으로 기대한다”고 연구의 의의를 설명했다. 그러나 “현 연구는 음악 학습에 의한 발달 과정을 고려하고 있지 않으며, 발달 초기의 기초적인 음악 정보처리에 대한 논의임을 주의해야 한다”고 연구의 한계를 덧붙였다.
우리 대학 물리학과 김광수 박사(現 MIT 뇌인지과학과)가 제1 저자로, 김동겸 박사(現 IBS)와 함께 진행한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 출판됐다. (논문명: ‘Spontaneous emergence of rudimentary music detectors in deep neural networks’, 국문 번역: ‘심층신경망에서 음악 인지기능의 자발적 발생’)
한편 이번 연구는 한국연구재단의 지원을 통해 수행됐다.
2024.01.16
조회수 1662
-
 차미영 교수, 한국인 첫 獨 막스플랑크 연구소 단장 선임
세계적 기초과학 연구기관인 독일 막스플랑크 연구소(Max Planck Institute, MPI)에 첫 한국인 단장이 선임됐다. 우리 대학 전산학부 차미영 교수(기초과학연구원 수리 및 계산 과학 연구단 데이터 사이언스 그룹 CI(Chief Investigator))가 그 주인공이다. 차 교수는 독일 보흠 지역에 있는 막스플랑크 보안 및 정보보호 연구소(MPI for Security and Privacy)에서 6월부터 단장(Scientific Director)직 수행을 시작해 ‘인류를 위한 데이터 과학(Data Science for Humanity)’ 연구그룹을 이끌 예정이다. 현재 본격적인 연구그룹 출범을 준비하고 있다.
막스플랑크 연구소는 기초과학 분야를 아우르며 독일 전역과 해외에 85개 산하 연구소를 운영하고 있다. 연구소를 이끄는 300여 명의 단장 중 한국 국적 과학자가 발탁된 것은 이번이 처음이다. 한국계로는 지난해 8월 울산과학기술원(UNIST) 강사라 교수가 기후과학연구소 단장으로 선임된 바 있다.
차 교수는 구글 스칼라(Google Scholar) 기준 피인용 수 2만 회가 넘는 데이터 과학 분야 전문가로, 우리 대학 전산학부를 졸업하고 동 대학원에서 석·박사 학위를 받은 ‘토종박사’다. 박사 취득 이후 독일 자부르켄에 있는 막스플랑크 연구소에서 박사후연구원으로 근무했으며, 2010년부터 우리 대학 교수로 재직하고 있다. 2019년에는 IBS의 CI로 선정돼 데이터 사이언스 그룹을 이끌며 인공지능(AI) 분야에서 우수 논문을 다수 발표하는 등 국제적 인지도를 높였다.
차 교수가 이끄는 데이터 사이언스 그룹은 2019년 출범해 초대형 데이터를 계산하고 분석하는 방법론을 연구하고 있다. 특히 AI를 이용해 가짜뉴스와 혐오 표현을 탐지하는 등 우리 삶과 밀접한 사회 현상을 분석해 괄목할 만한 연구성과를 창출했다.
코로나19 팬데믹 시절 ‘루머를 앞선 팩트’ 캠페인을 기획해 감염병 관련 잘못된 정보에 대한 팩트체크 결과를 151개국에 전파했다. 최근에는 위성영상을 AI로 분석해 북한을 비롯한 저개발국가의 경제지도를 만들어 무료로 공개했다. 최근 실시한 5년 차 평가에서 AI 기술을 기초과학에 창의적으로 활용해 차별성 있는 연구를 수행했으며, 데이터 과학 연구의 사회적 가치를 제고할 수 있는 핵심 기술을 개발하는 등 국제적 파급력 있는 연구성과를 창출했다는 평가를 받았다.
IBS 노도영 원장은 “IBS는 미래 연구단장을 발굴·육성하기 위해 젊은 연구자를 선정해 독립 연구를 지원하고 있다”라며, “이 제도로 발굴한 연구자가 막스플랑크 연구소 단장으로 초청받은 것에 대해 매우 기쁘게 생각하며 한국과 독일의 국제 연구 교류에도 크게 기여할 것으로 기대한다”라고 전했다.
우리 대학 이광형 총장은 “KAIST가 키워낸 차 교수의 행보는 국제화에 좋은 롤모델이 될 것”이라며, “계속해서 KAIST 학생 및 동료와 협업할 수 있도록 겸직을 비롯한 지원을 아끼지 않겠다”라고 축하의 메시지를 전했다.
차미영 CI는 “KAIST 교수로 쌓아온 경험에 더하여 IBS에서 긴 호흡으로 창의적인 연구를 지속한 덕분에 좋은 결과를 얻은 것 같다”라며, “앞으로 큰 책임감을 가지고 데이터 과학을 통한 사회 공헌을 위해 최선을 다하겠다”라고 포부를 밝혔다.
차미영 교수, 한국인 첫 獨 막스플랑크 연구소 단장 선임
세계적 기초과학 연구기관인 독일 막스플랑크 연구소(Max Planck Institute, MPI)에 첫 한국인 단장이 선임됐다. 우리 대학 전산학부 차미영 교수(기초과학연구원 수리 및 계산 과학 연구단 데이터 사이언스 그룹 CI(Chief Investigator))가 그 주인공이다. 차 교수는 독일 보흠 지역에 있는 막스플랑크 보안 및 정보보호 연구소(MPI for Security and Privacy)에서 6월부터 단장(Scientific Director)직 수행을 시작해 ‘인류를 위한 데이터 과학(Data Science for Humanity)’ 연구그룹을 이끌 예정이다. 현재 본격적인 연구그룹 출범을 준비하고 있다.
막스플랑크 연구소는 기초과학 분야를 아우르며 독일 전역과 해외에 85개 산하 연구소를 운영하고 있다. 연구소를 이끄는 300여 명의 단장 중 한국 국적 과학자가 발탁된 것은 이번이 처음이다. 한국계로는 지난해 8월 울산과학기술원(UNIST) 강사라 교수가 기후과학연구소 단장으로 선임된 바 있다.
차 교수는 구글 스칼라(Google Scholar) 기준 피인용 수 2만 회가 넘는 데이터 과학 분야 전문가로, 우리 대학 전산학부를 졸업하고 동 대학원에서 석·박사 학위를 받은 ‘토종박사’다. 박사 취득 이후 독일 자부르켄에 있는 막스플랑크 연구소에서 박사후연구원으로 근무했으며, 2010년부터 우리 대학 교수로 재직하고 있다. 2019년에는 IBS의 CI로 선정돼 데이터 사이언스 그룹을 이끌며 인공지능(AI) 분야에서 우수 논문을 다수 발표하는 등 국제적 인지도를 높였다.
차 교수가 이끄는 데이터 사이언스 그룹은 2019년 출범해 초대형 데이터를 계산하고 분석하는 방법론을 연구하고 있다. 특히 AI를 이용해 가짜뉴스와 혐오 표현을 탐지하는 등 우리 삶과 밀접한 사회 현상을 분석해 괄목할 만한 연구성과를 창출했다.
코로나19 팬데믹 시절 ‘루머를 앞선 팩트’ 캠페인을 기획해 감염병 관련 잘못된 정보에 대한 팩트체크 결과를 151개국에 전파했다. 최근에는 위성영상을 AI로 분석해 북한을 비롯한 저개발국가의 경제지도를 만들어 무료로 공개했다. 최근 실시한 5년 차 평가에서 AI 기술을 기초과학에 창의적으로 활용해 차별성 있는 연구를 수행했으며, 데이터 과학 연구의 사회적 가치를 제고할 수 있는 핵심 기술을 개발하는 등 국제적 파급력 있는 연구성과를 창출했다는 평가를 받았다.
IBS 노도영 원장은 “IBS는 미래 연구단장을 발굴·육성하기 위해 젊은 연구자를 선정해 독립 연구를 지원하고 있다”라며, “이 제도로 발굴한 연구자가 막스플랑크 연구소 단장으로 초청받은 것에 대해 매우 기쁘게 생각하며 한국과 독일의 국제 연구 교류에도 크게 기여할 것으로 기대한다”라고 전했다.
우리 대학 이광형 총장은 “KAIST가 키워낸 차 교수의 행보는 국제화에 좋은 롤모델이 될 것”이라며, “계속해서 KAIST 학생 및 동료와 협업할 수 있도록 겸직을 비롯한 지원을 아끼지 않겠다”라고 축하의 메시지를 전했다.
차미영 CI는 “KAIST 교수로 쌓아온 경험에 더하여 IBS에서 긴 호흡으로 창의적인 연구를 지속한 덕분에 좋은 결과를 얻은 것 같다”라며, “앞으로 큰 책임감을 가지고 데이터 과학을 통한 사회 공헌을 위해 최선을 다하겠다”라고 포부를 밝혔다.
2024.01.09
조회수 2504
-
 햇빛만으로 결빙 방지되는 필름 개발
열선, 스프레이 및 오일 주기적 도포, 기판 디자인 변경 등 없이도 금나노입자의 광열 효과를 산업현장에 적용할 수 있는 방빙/제빙 필름 코팅 기술이 개발되었다.
우리 대학 기계공학과 김형수 교수 연구팀(유체 및 계면 연구실)과 화학과 윤동기 교수 연구팀(연성 물질 나노조립 연구실)의 공동융합연구를 통해 단순 증발만으로 금 나노막대 입자를 사분면으로 균일하게 패터닝 할 수 있는 원천 기술을 확보하고, 이를 이용해 결빙 방지 및 제빙 표면을 개발했다고 3일 밝혔다.
최근 다양한 코팅 기법을 이용해 목표물 표면의 성질을 제어하려는 연구가 많이 진행되고 있으며, 특히, 기능성 나노 재료 패터닝을 통한 방식이 큰 주목을 받고 있다. 이 중에서도 금 나노 막대(GNR)는 생체 적합성, 화학적 안정성, 비교적 쉬운 합성, 표면 플라즈몬 공명이라는 안정적이면서도 독특한 특성으로 인해 유망한 나노물질 중 하나로 여겨지고 있다. 이때, 금 나노 막대의 성능을 극대화하려면 높은 수준의 증착 필름의 균일도와 금 나노 막대의 정렬도를 획득하는 것이 매우 중요하며, 현재 이를 구현하는 것은 여전히 해결해야 할 큰 문제다.
이를 해결하고자, 공동연구팀은 자연계에서 쉽게 추출이 가능한 차세대 기능성 나노 물질인 셀룰로오스 나노크리스탈(CNC)를 활용했다. 셀룰로오스 나노크리스탈 사분면 템플릿에 금 나노 막대를 공동 자가 조립해 균일하게 건조되면서 코팅 전체 면적에 환형으로 균일하게 정렬된 금 나노막대 필름을 개발하는 데 성공했다. 이번 연구에서 획득한 높은 균일도와 정렬도를 갖는 금 나노막대 필름은 기존 커피링 필름과 비교해 향상된 플라즈모닉 광학/광열 성능을 보였으며, 이는 가시광선 파장 영역대의 빛 조사만으로 방빙/제빙 역할을 해낼 수 있음을 연구팀은 실험적으로 증명했다.
기계공학과 김형수 교수는 “이 기술은 플라스틱 및 유연 표면 위에도 제작이 가능해 이를 외장재 및 필름에 활용하면 자체적으로 열에너지를 발생시킬 수 있어, 겨울철에 큰 문제가 되는 자동차 성에, 항공기 제빙, 주거/상용 공간의 유리창 등 다양한 분야에서 자발적 열에너지 하베스팅 효과를 통해 에너지 절약 효과를 가져다 줄 수 있을 것으로 기대한다”고 언급했다. 한편 화학과 윤동기 교수는 “필름화하기 힘들었던 나노셀룰로오스-금입자 복합체를 대면적에서 자유롭게 패터닝해 결빙 소재로 사용할 수 있고, 금의 플라즈모닉 성질을 이용한다면 마치 유리를 장식하는 스테인드 글래스처럼 사용할 수 있다는 점에서 의미가 있다”고 언급했다.
해당 연구 결과는 기계공학과 편정수 박사과정, 박순모 박사(KAIST졸업, 現 코넬 대학교 박사 후 연구원)가 공동 제1 저자로 참여했으며, 국제학술지 `네이처 커뮤니케이션즈(Nature Communications)' 2023년 12월 8일 字 온라인판에 게재됐다. (논문명 : Plasmonic Metasurfaces of Cellulose Nanocrystal Matrices with Quadrants of Aligned Gold Nanorods for Photothermal Anti-Icing, https://doi.org/10.1038/s41467-023-43511-9) 그리고, 연구의 우수성을 인정받아 국제 저널‘재료과학과 화학(Materials Science and Chemistry)’ 과 ‘무기 물리화학(Inorganic and Physical Chemistry)’ 두 편집자 하이라이트(Editors’ Highlights) 페이지에 선정됐다.
이번 연구는 한국연구재단의 개인기초 중견 연구(MIST: 2021R1A2C2007835)와 멀티스케일 카이랄 구조체 연구센터 (MSIT: 2018R1A5A1025208) 지원을 받아 수행됐다.
햇빛만으로 결빙 방지되는 필름 개발
열선, 스프레이 및 오일 주기적 도포, 기판 디자인 변경 등 없이도 금나노입자의 광열 효과를 산업현장에 적용할 수 있는 방빙/제빙 필름 코팅 기술이 개발되었다.
우리 대학 기계공학과 김형수 교수 연구팀(유체 및 계면 연구실)과 화학과 윤동기 교수 연구팀(연성 물질 나노조립 연구실)의 공동융합연구를 통해 단순 증발만으로 금 나노막대 입자를 사분면으로 균일하게 패터닝 할 수 있는 원천 기술을 확보하고, 이를 이용해 결빙 방지 및 제빙 표면을 개발했다고 3일 밝혔다.
최근 다양한 코팅 기법을 이용해 목표물 표면의 성질을 제어하려는 연구가 많이 진행되고 있으며, 특히, 기능성 나노 재료 패터닝을 통한 방식이 큰 주목을 받고 있다. 이 중에서도 금 나노 막대(GNR)는 생체 적합성, 화학적 안정성, 비교적 쉬운 합성, 표면 플라즈몬 공명이라는 안정적이면서도 독특한 특성으로 인해 유망한 나노물질 중 하나로 여겨지고 있다. 이때, 금 나노 막대의 성능을 극대화하려면 높은 수준의 증착 필름의 균일도와 금 나노 막대의 정렬도를 획득하는 것이 매우 중요하며, 현재 이를 구현하는 것은 여전히 해결해야 할 큰 문제다.
이를 해결하고자, 공동연구팀은 자연계에서 쉽게 추출이 가능한 차세대 기능성 나노 물질인 셀룰로오스 나노크리스탈(CNC)를 활용했다. 셀룰로오스 나노크리스탈 사분면 템플릿에 금 나노 막대를 공동 자가 조립해 균일하게 건조되면서 코팅 전체 면적에 환형으로 균일하게 정렬된 금 나노막대 필름을 개발하는 데 성공했다. 이번 연구에서 획득한 높은 균일도와 정렬도를 갖는 금 나노막대 필름은 기존 커피링 필름과 비교해 향상된 플라즈모닉 광학/광열 성능을 보였으며, 이는 가시광선 파장 영역대의 빛 조사만으로 방빙/제빙 역할을 해낼 수 있음을 연구팀은 실험적으로 증명했다.
기계공학과 김형수 교수는 “이 기술은 플라스틱 및 유연 표면 위에도 제작이 가능해 이를 외장재 및 필름에 활용하면 자체적으로 열에너지를 발생시킬 수 있어, 겨울철에 큰 문제가 되는 자동차 성에, 항공기 제빙, 주거/상용 공간의 유리창 등 다양한 분야에서 자발적 열에너지 하베스팅 효과를 통해 에너지 절약 효과를 가져다 줄 수 있을 것으로 기대한다”고 언급했다. 한편 화학과 윤동기 교수는 “필름화하기 힘들었던 나노셀룰로오스-금입자 복합체를 대면적에서 자유롭게 패터닝해 결빙 소재로 사용할 수 있고, 금의 플라즈모닉 성질을 이용한다면 마치 유리를 장식하는 스테인드 글래스처럼 사용할 수 있다는 점에서 의미가 있다”고 언급했다.
해당 연구 결과는 기계공학과 편정수 박사과정, 박순모 박사(KAIST졸업, 現 코넬 대학교 박사 후 연구원)가 공동 제1 저자로 참여했으며, 국제학술지 `네이처 커뮤니케이션즈(Nature Communications)' 2023년 12월 8일 字 온라인판에 게재됐다. (논문명 : Plasmonic Metasurfaces of Cellulose Nanocrystal Matrices with Quadrants of Aligned Gold Nanorods for Photothermal Anti-Icing, https://doi.org/10.1038/s41467-023-43511-9) 그리고, 연구의 우수성을 인정받아 국제 저널‘재료과학과 화학(Materials Science and Chemistry)’ 과 ‘무기 물리화학(Inorganic and Physical Chemistry)’ 두 편집자 하이라이트(Editors’ Highlights) 페이지에 선정됐다.
이번 연구는 한국연구재단의 개인기초 중견 연구(MIST: 2021R1A2C2007835)와 멀티스케일 카이랄 구조체 연구센터 (MSIT: 2018R1A5A1025208) 지원을 받아 수행됐다.
2024.01.03
조회수 5206
-
 권태형 박사과정, 고지훈 석박사통합과정, IEEE ICDM 2023 최우수논문상 수상
우리 대학 김재철AI대학원 권태형 박사과정, 고지훈 석박사통합과정 (지도교수 신기정)이 지난 12월 중국 상해에서 열린 제23회 IEEE International Conference on Data Mining (IEEE ICDM)에서 최우수 논문상(Best Student Paper Runner-up)을 수상했다.
IEEE ICDM은 매년 개최되는 데이터 마이닝 분야 최고 권위의 국제 학회 중 하나다. 올해는 총 200편의 논문이 발표됐고 그 중 권태형, 고지훈 학생이 참여한 논문을 포함한 4편의 논문이 최우수 논문으로 선정됐다.
논문 제목은 ‘텐서코덱: 데이터에 대한 가정이 필요 없는 간결한 텐서의 손실 압축 기법’(TensorCodec: Compact Lossy Compression of Tensors without Strong Data Assumptions)이다.
이 연구에서는 텐서, 즉 고차원 행렬 데이터를 위한 압축 기술을 제시하였다. 텐서-열차 분해(Tensor-Train Decomposition)와 인공신경망을 결합하여 압축 성능을 향상했으며, 행과 열을 재배치하고 차원을 증가시키는 등 입력 텐서의 형태에 대한 최적화를 통해 압축 성능을 추가로 개선하였다. 또한, 다양한 실세계 데이터를 사용하여 제안된 방법의 우수성과 범용성을 검증하였다.
권태형, 고지훈 학생은 “항상 연구에 대한 열정이 가득하시고, 창의적인 아이디어를 제공하여 연구의 돌파구를 열어 주신 신기정 교수님의 지도 덕분에 수상이 가능했다”며 “해당 아이디어가 더욱 고도화되어, 추천시스템, 이상 탐지, AI 모델 경량화 등 다양한 분야에서 활용될 수 있기를 바란다”고 말했다.
이 연구에는 권태형 박사과정, 고지훈 석박통합과정, 신기정 교수 외에 숭실대학교 정진홍 교수가 참여하였으며, 정보통신기획평가원의 지원을 받은 강건하고 공정하며 확장 가능한 데이터 중심의 연속 학습 과제와 한국연구재단의 지원을 받은 부호화된 그래프 마이닝 과제의 성과다.
권태형 박사과정, 고지훈 석박사통합과정, IEEE ICDM 2023 최우수논문상 수상
우리 대학 김재철AI대학원 권태형 박사과정, 고지훈 석박사통합과정 (지도교수 신기정)이 지난 12월 중국 상해에서 열린 제23회 IEEE International Conference on Data Mining (IEEE ICDM)에서 최우수 논문상(Best Student Paper Runner-up)을 수상했다.
IEEE ICDM은 매년 개최되는 데이터 마이닝 분야 최고 권위의 국제 학회 중 하나다. 올해는 총 200편의 논문이 발표됐고 그 중 권태형, 고지훈 학생이 참여한 논문을 포함한 4편의 논문이 최우수 논문으로 선정됐다.
논문 제목은 ‘텐서코덱: 데이터에 대한 가정이 필요 없는 간결한 텐서의 손실 압축 기법’(TensorCodec: Compact Lossy Compression of Tensors without Strong Data Assumptions)이다.
이 연구에서는 텐서, 즉 고차원 행렬 데이터를 위한 압축 기술을 제시하였다. 텐서-열차 분해(Tensor-Train Decomposition)와 인공신경망을 결합하여 압축 성능을 향상했으며, 행과 열을 재배치하고 차원을 증가시키는 등 입력 텐서의 형태에 대한 최적화를 통해 압축 성능을 추가로 개선하였다. 또한, 다양한 실세계 데이터를 사용하여 제안된 방법의 우수성과 범용성을 검증하였다.
권태형, 고지훈 학생은 “항상 연구에 대한 열정이 가득하시고, 창의적인 아이디어를 제공하여 연구의 돌파구를 열어 주신 신기정 교수님의 지도 덕분에 수상이 가능했다”며 “해당 아이디어가 더욱 고도화되어, 추천시스템, 이상 탐지, AI 모델 경량화 등 다양한 분야에서 활용될 수 있기를 바란다”고 말했다.
이 연구에는 권태형 박사과정, 고지훈 석박통합과정, 신기정 교수 외에 숭실대학교 정진홍 교수가 참여하였으며, 정보통신기획평가원의 지원을 받은 강건하고 공정하며 확장 가능한 데이터 중심의 연속 학습 과제와 한국연구재단의 지원을 받은 부호화된 그래프 마이닝 과제의 성과다.
2024.01.02
조회수 1605
-
 원하는 색깔의 마이크로 LED 전사 기술 개발
기존 OLED 등과 비해 전기적·광학적 특성이 우수한 마이크로 LED는 머리카락 두께인 100마이크로미터(μm) 이하 크기의 무기물 LED 칩을 활용하는 차세대 디스플레이용 광원이다. 마이크로 LED의 상용화를 위해선 성장 기판에 배열된 대량의 마이크로 LED 칩을 최종 기판의 정확한 위치에 원하는 배열로 옮기는 ‘전사 공정’이 가장 중요한 핵심기술이지만, 기존 전사 기술들은 별도의 접착제 사용, 정렬 오차, 낮은 수율, 칩 손상 등으로 마이크로 LED 상용화에 많은 어려움이 존재했다.
우리 대학 신소재공학과 이건재 교수 연구팀이 마이크로진공 흡입력을 조절해 대량의 마이크로 LED 칩을 색깔별 원하는 칩들만 선택적으로 전사하는 기술을 개발했다고 19일 밝혔다.
이 교수팀은 레이저빔 조사시 물질 특성을 조정하여 식각하는 레이저 유도 에칭(Laser-induced etching, LIE) 기술을 활용해 미세 관통홀을 유리 기판에 초당 7,000개 속도로 형성했고, 이를 진공 채널에 연결해 미세진공 흡입력을 발생시켜 마이크로 LED를 전사하는 데 성공했다. 이 기술은 기존 전사 기술 대비 뛰어난 접착력 전환성을 달성하였으며, 다수의 진공 채널별 독립적인 진공 조절을 통해 대량의 마이크로 LED 칩을 선택적으로 전사하였다. 또한 다양한 재료, 크기, 모양, 두께를 지닌 초소형 반도체 칩들을 칩 손상 없이 임의의 기판에 높은 수율로 전사할 수 있었다.
이건재 교수는 “이번에 개발된 마이크로진공 전사 기술은 가파르게 성장하는 마이크로 LED 시장에서 높은 생산 원가를 절감하고 중저가 마이크로 LED 제품 양산화의 핵심 기술로 활용될 것이 기대된다”면서, “현재 얇은 핀으로 칩을 들어 올리는 이젝터 시스템을 적용해 대량의 상용 마이크로 LED를 전사하고, 이를 통해 차세대 디스플레이(대형 TV, 유연․신축성 기기 등) 뿐만 아니라 광-바이오 융합형 미용 면발광 패치 상용화를 진행 중이다”라고 말했다.
한편 이번 연구는 웨어러블플랫폼 소재기술 센터, 중견연구자지원사업, 소부장 전략협력 기술개발사업의 지원을 받아 수행됐으며, 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 11월 26일 자 출판됐다.
원하는 색깔의 마이크로 LED 전사 기술 개발
기존 OLED 등과 비해 전기적·광학적 특성이 우수한 마이크로 LED는 머리카락 두께인 100마이크로미터(μm) 이하 크기의 무기물 LED 칩을 활용하는 차세대 디스플레이용 광원이다. 마이크로 LED의 상용화를 위해선 성장 기판에 배열된 대량의 마이크로 LED 칩을 최종 기판의 정확한 위치에 원하는 배열로 옮기는 ‘전사 공정’이 가장 중요한 핵심기술이지만, 기존 전사 기술들은 별도의 접착제 사용, 정렬 오차, 낮은 수율, 칩 손상 등으로 마이크로 LED 상용화에 많은 어려움이 존재했다.
우리 대학 신소재공학과 이건재 교수 연구팀이 마이크로진공 흡입력을 조절해 대량의 마이크로 LED 칩을 색깔별 원하는 칩들만 선택적으로 전사하는 기술을 개발했다고 19일 밝혔다.
이 교수팀은 레이저빔 조사시 물질 특성을 조정하여 식각하는 레이저 유도 에칭(Laser-induced etching, LIE) 기술을 활용해 미세 관통홀을 유리 기판에 초당 7,000개 속도로 형성했고, 이를 진공 채널에 연결해 미세진공 흡입력을 발생시켜 마이크로 LED를 전사하는 데 성공했다. 이 기술은 기존 전사 기술 대비 뛰어난 접착력 전환성을 달성하였으며, 다수의 진공 채널별 독립적인 진공 조절을 통해 대량의 마이크로 LED 칩을 선택적으로 전사하였다. 또한 다양한 재료, 크기, 모양, 두께를 지닌 초소형 반도체 칩들을 칩 손상 없이 임의의 기판에 높은 수율로 전사할 수 있었다.
이건재 교수는 “이번에 개발된 마이크로진공 전사 기술은 가파르게 성장하는 마이크로 LED 시장에서 높은 생산 원가를 절감하고 중저가 마이크로 LED 제품 양산화의 핵심 기술로 활용될 것이 기대된다”면서, “현재 얇은 핀으로 칩을 들어 올리는 이젝터 시스템을 적용해 대량의 상용 마이크로 LED를 전사하고, 이를 통해 차세대 디스플레이(대형 TV, 유연․신축성 기기 등) 뿐만 아니라 광-바이오 융합형 미용 면발광 패치 상용화를 진행 중이다”라고 말했다.
한편 이번 연구는 웨어러블플랫폼 소재기술 센터, 중견연구자지원사업, 소부장 전략협력 기술개발사업의 지원을 받아 수행됐으며, 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 11월 26일 자 출판됐다.
2023.12.19
조회수 1678
-
 혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14
조회수 1729
 방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
2024.02.15 조회수 998
방사선 유발 DNA 돌연변이 첫 규명
암은 세계적으로 큰 건강 문제로 인식되고 있으며, 암 치료에 대한 지속적인 연구와 기술 발전이 이루어지고 있다. 암치료의 중요한 방법 중 하나인 방사선 치료는 암 조직을 효과적으로 파괴하거나 성장을 억제하는 데 중요한 역할을 하고 있으나 방사선이 실제로 우리의 세포에 유발하는 돌연변이의 종류와 양에 대한 이해는 아직 미흡한 상태였다. 한국의 의과학자들이 이러한 공백을 메울 수 있는 연구 결과를 발표하였다.
우리 대학 의과학대학원 주영석 교수 연구팀이 동남권원자력의학원 손태건 박사, 서울대학교 의과대학 방사선종양학과 김경수, 장지현 교수팀과의 공동 연구로 방사선이 인간 및 생쥐의 정상 세포에서 만들어내는 DNA 돌연변이의 특성을 명확히 규명해 냈다고 15일 밝혔다.
이번 연구는 방사선 연구 분야에서의 중요한 전환점으로 평가되고 있다. 연구진은 실험실에서 방사선을 조사하여 세포에 돌연변이를 유도한 후, 방사선이 만들어낸 돌연변이를 유전체 서열분석 기술을 통해 규명하는 방식으로 방사선이 유발하는 DNA 돌연변이의 양과 패턴을 정밀하게 이해하는 데 성공하였다.
연구팀은 방사선이 인체에 미치는 영향을 종합적으로 이해하기 위하여 생쥐와 사람의 다양한 장기(위, 소장, 대장, 간, 유방, 폐, 췌장, 나팔관 등)에서 얻은 세포를 다양한 선량의 방사선에 노출하였고, 각각의 세포마다 유도된 돌연변이를 정밀하게 검출하기 위해 세포 하나하나를 오가노이드 세포 배양 기술을 응용하여 증폭하였다. 총 200개의 세포 유전체 서열로부터 방사선 피폭 양에 비례하여 증가하는 특정 패턴의 돌연변이들을 규명하는 데 성공하였다 (그림 1).
본 연구에서 1Gy (그레이)의 방사선량은 매 세포마다 약 14개 내외의 돌연변이를 만들어내는 것으로 나타났다 (그림 2). 우리나라 연간 평균 자연방사선 양 (3.08mSV(시버트))을 감안하면 1Gy는 약 320년의 자연방사선 노출에 해당하는 셈이다. 방사선이 만들어내는 변이의 패턴은 다른 원인에 의한 돌연변이와는 달랐는데, 주로 짧은 염기 결손 (short base deletion)과 소수의 염색체의 역위(inversion), 전위 (translocation), 및 다양한 복잡 구조변이(complex genomic rearrangements)들로 구성되어 있었다 (그림 3). 방사선은 서로 다른 세포 종류에도 모두 비슷한 정도의 돌연변이를 만들어 내는 것으로 밝혀졌다.
의과학대학원 주영석 교수는 이번 연구를 통해 "방사선이 분자 수준에서 세포에 미치는 영향을 명확하게 규명했다"며, "방사선이 우리 세포의 DNA를 얼마나, 어떻게 변화시키는지에 대한 첫 규명"이라고 설명했다.
동남권원자력의학원의 손태건 박사는 "이번 연구를 기반으로 앞으로도 초저선량 및 초고선량 방사선이 인체에 미치는 영향을 연구할 것"이라고 밝혔으며, "안전하면서도 효과적인 방사선 치료 기술을 발전시킬 것"이라고 덧붙였다.
서울대학교 의과대학 방사선종양학과 김경수 교수와 장지현 교수는 “이번 연구를 통해 방사선이 인체 DNA 에 미치는 영향에 대해 정확히 알 수 있는 도구를 가지게 된 것으로 생각한다” 면서 “이번 연구에 쓰인 연구 방법론으로 많은 후속 연구가 나올 수 있기를 기대한다” 고 밝혔다.
의과학대학원 육정환 박사 (現 서울대병원 내과 조교수), 임준오 박사 (現 지놈인사이트), 김태우 박사 (現 Weill Cornell 의과대학 박사후연구과정) 및 서울대학교 의과대학 권현우 박사 (現 고려대학교 의과대학 핵의학과 교수), 김은지 박사 (現 서울대학교 의과대학 방사선종양학과 조교수) 등이 공동 제1저자로 참여한 이번 연구 결과는 국제 학술지 '셀 지노믹스(Cell Genomics)'의 온라인판에 14일 발표되었다. (논문명: Quantitative and qualitative mutational impact of ionizing radiation on normal cells).
이번 연구는 한국연구재단, 과학기술정보통신부 국가R&D사업, 서경배과학재단 신진과학자 연구지원 사업, 고려대학교 안암병원 및 국제 연구비 휴먼 프론티어 사이언스 프로그램(HFSP)의 젊은 연구자 지원사업의 도움으로 수행되었으며, 서울대학교 유전공학연구소, 영국 케임브리지 줄기세포 연구소, 오스트리아 분자생명공학연구소(IMBA) 및 KAIST 교원창업기업 지놈 인사이트의 연구자들도 참여하였다.
2024.02.15 조회수 998 100큐비트급 양자컴퓨터 계산데이터 전격 공개
양자컴퓨터는 양자역학의 원리를 활용해 기존의 컴퓨터로는 풀기 어려운 계산을 할 수 있는 컴퓨터다. 양자컴퓨터는 암호 해독, 배터리 소재 개발, 신약 개발 등 다양한 분야에서 그동안 풀지 못한 난제들을 해결할 미래 기술로 주목받고 있다.
우리 대학 물리학과 안재욱 교수 연구팀이 100큐비트급 양자컴퓨터로 조합 최적화 문제를 계산해 계산 결과 데이터베이스와 계산 프로그램을 공개했다고 13일 밝혔다.
조합 최적화 문제 중 하나인 최대 독립집합 문제(Maximum independent set problem)는 SNS상에서 가장 영향력 있는 인물을 찾는 문제, 전력망을 가장 효율적으로 분배하는 법을 찾는 문제 등 다양한 응용이 가능한 문제다. 지난 2023년 KAIST 연구진은 20큐비트급 리드버그 양자컴퓨터를 이용해 최대 독립집합 문제의 풀이를 시연한 바 있다.
일반적으로 100큐비트급 양자컴퓨터의 데이터를 얻기 위해서는 직접 양자컴퓨터를 제작하거나 클라우드 서비스 업체를 이용할 수밖에 없다. 이번에 KAIST 연구진이 공개한 데이터는 관련 분야 연구자뿐 아니라 양자 컴퓨터에 관심 있는 모든 사람이 무료로 데이터에 접근할 수 있게 되었다는 점에서 중요하다고 할 수 있다. 최대 141큐비트를 활용해 70만 종류 이상의 그래프 최적화를 계산했고, 양자컴퓨터의 계산 결과와 데이터분석 프로그램 일체를 공개했다.
연구를 주도한 안재욱 교수는 “이번 연구를 통해 100큐비트급 양자컴퓨터를 활용한 난제 계산 결과 및 계산 프로그램을 모두 공개하여 그동안 양자컴퓨터에 접근이 어려웠던 연구자를 비롯한 많은 사람이 양자 컴퓨팅 연구에 참여할 수 있을 것으로 기대된다. 아울러, 고성능 양자컴퓨터 개발에 필요한 잡음 분석에도 연구팀이 계산한 데이터베이스가 활용될 수 있을 것이라 생각한다”고 말했다.
우리 대학 물리학과 김강흔, 박주영, 변우정 석박사통합과정, 김민혁 박사(現 고려대 물리학과 교수)가 참여한 해당 연구 결과는 국제 학술지 네이처(Nature) 자매지인 ‘사이언티픽 데이터(Scientific data)’1월 11권에 게재됐다. (논문명: Quantum computing dataset of maximum independent set problem on king lattice of over hundred Rydberg atoms).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.02.13 조회수 1442
100큐비트급 양자컴퓨터 계산데이터 전격 공개
양자컴퓨터는 양자역학의 원리를 활용해 기존의 컴퓨터로는 풀기 어려운 계산을 할 수 있는 컴퓨터다. 양자컴퓨터는 암호 해독, 배터리 소재 개발, 신약 개발 등 다양한 분야에서 그동안 풀지 못한 난제들을 해결할 미래 기술로 주목받고 있다.
우리 대학 물리학과 안재욱 교수 연구팀이 100큐비트급 양자컴퓨터로 조합 최적화 문제를 계산해 계산 결과 데이터베이스와 계산 프로그램을 공개했다고 13일 밝혔다.
조합 최적화 문제 중 하나인 최대 독립집합 문제(Maximum independent set problem)는 SNS상에서 가장 영향력 있는 인물을 찾는 문제, 전력망을 가장 효율적으로 분배하는 법을 찾는 문제 등 다양한 응용이 가능한 문제다. 지난 2023년 KAIST 연구진은 20큐비트급 리드버그 양자컴퓨터를 이용해 최대 독립집합 문제의 풀이를 시연한 바 있다.
일반적으로 100큐비트급 양자컴퓨터의 데이터를 얻기 위해서는 직접 양자컴퓨터를 제작하거나 클라우드 서비스 업체를 이용할 수밖에 없다. 이번에 KAIST 연구진이 공개한 데이터는 관련 분야 연구자뿐 아니라 양자 컴퓨터에 관심 있는 모든 사람이 무료로 데이터에 접근할 수 있게 되었다는 점에서 중요하다고 할 수 있다. 최대 141큐비트를 활용해 70만 종류 이상의 그래프 최적화를 계산했고, 양자컴퓨터의 계산 결과와 데이터분석 프로그램 일체를 공개했다.
연구를 주도한 안재욱 교수는 “이번 연구를 통해 100큐비트급 양자컴퓨터를 활용한 난제 계산 결과 및 계산 프로그램을 모두 공개하여 그동안 양자컴퓨터에 접근이 어려웠던 연구자를 비롯한 많은 사람이 양자 컴퓨팅 연구에 참여할 수 있을 것으로 기대된다. 아울러, 고성능 양자컴퓨터 개발에 필요한 잡음 분석에도 연구팀이 계산한 데이터베이스가 활용될 수 있을 것이라 생각한다”고 말했다.
우리 대학 물리학과 김강흔, 박주영, 변우정 석박사통합과정, 김민혁 박사(現 고려대 물리학과 교수)가 참여한 해당 연구 결과는 국제 학술지 네이처(Nature) 자매지인 ‘사이언티픽 데이터(Scientific data)’1월 11권에 게재됐다. (논문명: Quantum computing dataset of maximum independent set problem on king lattice of over hundred Rydberg atoms).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.02.13 조회수 1442 RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07 조회수 1562
RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07 조회수 1562 입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01 조회수 1356
입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01 조회수 1356 지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30 조회수 1665
지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30 조회수 1665 양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29 조회수 1472
양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29 조회수 1472 음악 본능을 인공지능으로 밝혀내다
음악은 세계 공통어로 불릴만큼 문화적 보편 요소로 알려졌다. 그렇다면 어떻게 다양한 문화권의 환경 차이에도 불구하고, ‘음악적 본능’은 어느 정도 공유될 수 있는 것일까?
우리 대학 물리학과 정하웅 교수 연구팀이 인공신경망 모델을 활용해, 사람 뇌에서 특별한 학습 없이도 음악 본능이 나타날 수 있는 원리를 규명했다고 16일 밝혔다.
기존 학자들은 다양한 문화권에 존재하는 음악의 보편성과 차별성을 규명하고, 어떻게 이런 공통성이 나타날 수 있는지에 대해 이해하고자 시도해 왔다. 2019년 세계적인 과학 저널 ‘사이언스’에 게재된 연구를 통해 민족지학적으로 구분된 모든 문화에서 음악을 만들어 내고, 유사한 형태의 박자와 멜로디가 사용된다는 것이 발견됐다. 또한, 신경과학자들은 우리 뇌의 청각 피질(Auditory cortex)에 음악 정보처리를 담당하는 특정한 영역이 존재한다는 것을 밝혀냈다.
연구팀은 인공신경망을 사용해, 음악에 대한 학습 없이도 자연에 대한 소리 정보 학습을 통해 음악 인지 기능이 자발적으로 형성됨을 보였다. (그림2) 연구팀은 구글에서 제공하는 대규모 소리 데이터(AudioSet)를 활용해, 인공신경망이 이러한 다양한 소리 데이터를 인식하도록 학습했다. 흥미롭게도, 연구팀은 네트워크 모델 내에 음악에 선택적으로 반응하는 뉴런(신경계의 단위)이 발생함을 발견했다. 즉, 사람의 말(speech), 동물 소리, 환경 소리, 기계 소리 등의 다양한 소리에는 거의 반응을 보이지 않으나 기악이나 성악 등 다양한 음악에 대해서는 높은 반응을 보이는 뉴런들이 자발적으로 형성된 것이다.
이 인공신경망 뉴런들은 실제 뇌의 음악정보처리 영역의 뉴런들과 유사한 반응 성질을 보였다. 예를 들어, 인공 뉴런은 음악을 시간적으로 잘게 나누어 재배열한 소리에 대해 감소된 반응을 보였다. 이는 자발적으로 나타난 음악 선택성 뉴런들이 음악의 시간적 구조를 부호화하고 있음을 의미한다. 이러한 성질은 특정 장르의 음악에만 국한된 것이 아니라, 클래식, 팝, 락, 재즈, 전자음악 등 25개에 달하는 다양한 장르 각각에 대해서도 공통적으로 나타났다.
심지어, 네트워크에서 음악 선택성 뉴런의 활동을 억제하게 되면, 다른 자연 소리에 대한 인식 정확도를 크게 떨어뜨릴 수 있음을 보였다. 즉, 음악 정보처리 기능이 다른 자연 소리 정보처리에 도움을 주며, 따라서 ‘음악성’이란 자연 소리를 처리하기 위한 진화적 적응에 의해 형성되는 본능일 수 있다는 설명이다.
연구를 주도한 정하웅 교수는 “이러한 결과는 다양한 문화권에서 음악 정보처리의 공통된 기저를 형성하는데, 자연 소리 정보처리를 위한 진화적 압력이 기여했을 수 있음을 시사한다”며, “사람과 유사한 음악성을 인공적으로 구현하여, 음악 생성 AI, 음악 치료, 음악 인지 연구 등에 원천 모델로 활용될 수 있을 것으로 기대한다”고 연구의 의의를 설명했다. 그러나 “현 연구는 음악 학습에 의한 발달 과정을 고려하고 있지 않으며, 발달 초기의 기초적인 음악 정보처리에 대한 논의임을 주의해야 한다”고 연구의 한계를 덧붙였다.
우리 대학 물리학과 김광수 박사(現 MIT 뇌인지과학과)가 제1 저자로, 김동겸 박사(現 IBS)와 함께 진행한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 출판됐다. (논문명: ‘Spontaneous emergence of rudimentary music detectors in deep neural networks’, 국문 번역: ‘심층신경망에서 음악 인지기능의 자발적 발생’)
한편 이번 연구는 한국연구재단의 지원을 통해 수행됐다.
2024.01.16 조회수 1662
음악 본능을 인공지능으로 밝혀내다
음악은 세계 공통어로 불릴만큼 문화적 보편 요소로 알려졌다. 그렇다면 어떻게 다양한 문화권의 환경 차이에도 불구하고, ‘음악적 본능’은 어느 정도 공유될 수 있는 것일까?
우리 대학 물리학과 정하웅 교수 연구팀이 인공신경망 모델을 활용해, 사람 뇌에서 특별한 학습 없이도 음악 본능이 나타날 수 있는 원리를 규명했다고 16일 밝혔다.
기존 학자들은 다양한 문화권에 존재하는 음악의 보편성과 차별성을 규명하고, 어떻게 이런 공통성이 나타날 수 있는지에 대해 이해하고자 시도해 왔다. 2019년 세계적인 과학 저널 ‘사이언스’에 게재된 연구를 통해 민족지학적으로 구분된 모든 문화에서 음악을 만들어 내고, 유사한 형태의 박자와 멜로디가 사용된다는 것이 발견됐다. 또한, 신경과학자들은 우리 뇌의 청각 피질(Auditory cortex)에 음악 정보처리를 담당하는 특정한 영역이 존재한다는 것을 밝혀냈다.
연구팀은 인공신경망을 사용해, 음악에 대한 학습 없이도 자연에 대한 소리 정보 학습을 통해 음악 인지 기능이 자발적으로 형성됨을 보였다. (그림2) 연구팀은 구글에서 제공하는 대규모 소리 데이터(AudioSet)를 활용해, 인공신경망이 이러한 다양한 소리 데이터를 인식하도록 학습했다. 흥미롭게도, 연구팀은 네트워크 모델 내에 음악에 선택적으로 반응하는 뉴런(신경계의 단위)이 발생함을 발견했다. 즉, 사람의 말(speech), 동물 소리, 환경 소리, 기계 소리 등의 다양한 소리에는 거의 반응을 보이지 않으나 기악이나 성악 등 다양한 음악에 대해서는 높은 반응을 보이는 뉴런들이 자발적으로 형성된 것이다.
이 인공신경망 뉴런들은 실제 뇌의 음악정보처리 영역의 뉴런들과 유사한 반응 성질을 보였다. 예를 들어, 인공 뉴런은 음악을 시간적으로 잘게 나누어 재배열한 소리에 대해 감소된 반응을 보였다. 이는 자발적으로 나타난 음악 선택성 뉴런들이 음악의 시간적 구조를 부호화하고 있음을 의미한다. 이러한 성질은 특정 장르의 음악에만 국한된 것이 아니라, 클래식, 팝, 락, 재즈, 전자음악 등 25개에 달하는 다양한 장르 각각에 대해서도 공통적으로 나타났다.
심지어, 네트워크에서 음악 선택성 뉴런의 활동을 억제하게 되면, 다른 자연 소리에 대한 인식 정확도를 크게 떨어뜨릴 수 있음을 보였다. 즉, 음악 정보처리 기능이 다른 자연 소리 정보처리에 도움을 주며, 따라서 ‘음악성’이란 자연 소리를 처리하기 위한 진화적 적응에 의해 형성되는 본능일 수 있다는 설명이다.
연구를 주도한 정하웅 교수는 “이러한 결과는 다양한 문화권에서 음악 정보처리의 공통된 기저를 형성하는데, 자연 소리 정보처리를 위한 진화적 압력이 기여했을 수 있음을 시사한다”며, “사람과 유사한 음악성을 인공적으로 구현하여, 음악 생성 AI, 음악 치료, 음악 인지 연구 등에 원천 모델로 활용될 수 있을 것으로 기대한다”고 연구의 의의를 설명했다. 그러나 “현 연구는 음악 학습에 의한 발달 과정을 고려하고 있지 않으며, 발달 초기의 기초적인 음악 정보처리에 대한 논의임을 주의해야 한다”고 연구의 한계를 덧붙였다.
우리 대학 물리학과 김광수 박사(現 MIT 뇌인지과학과)가 제1 저자로, 김동겸 박사(現 IBS)와 함께 진행한 이번 연구는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 출판됐다. (논문명: ‘Spontaneous emergence of rudimentary music detectors in deep neural networks’, 국문 번역: ‘심층신경망에서 음악 인지기능의 자발적 발생’)
한편 이번 연구는 한국연구재단의 지원을 통해 수행됐다.
2024.01.16 조회수 1662 차미영 교수, 한국인 첫 獨 막스플랑크 연구소 단장 선임
세계적 기초과학 연구기관인 독일 막스플랑크 연구소(Max Planck Institute, MPI)에 첫 한국인 단장이 선임됐다. 우리 대학 전산학부 차미영 교수(기초과학연구원 수리 및 계산 과학 연구단 데이터 사이언스 그룹 CI(Chief Investigator))가 그 주인공이다. 차 교수는 독일 보흠 지역에 있는 막스플랑크 보안 및 정보보호 연구소(MPI for Security and Privacy)에서 6월부터 단장(Scientific Director)직 수행을 시작해 ‘인류를 위한 데이터 과학(Data Science for Humanity)’ 연구그룹을 이끌 예정이다. 현재 본격적인 연구그룹 출범을 준비하고 있다.
막스플랑크 연구소는 기초과학 분야를 아우르며 독일 전역과 해외에 85개 산하 연구소를 운영하고 있다. 연구소를 이끄는 300여 명의 단장 중 한국 국적 과학자가 발탁된 것은 이번이 처음이다. 한국계로는 지난해 8월 울산과학기술원(UNIST) 강사라 교수가 기후과학연구소 단장으로 선임된 바 있다.
차 교수는 구글 스칼라(Google Scholar) 기준 피인용 수 2만 회가 넘는 데이터 과학 분야 전문가로, 우리 대학 전산학부를 졸업하고 동 대학원에서 석·박사 학위를 받은 ‘토종박사’다. 박사 취득 이후 독일 자부르켄에 있는 막스플랑크 연구소에서 박사후연구원으로 근무했으며, 2010년부터 우리 대학 교수로 재직하고 있다. 2019년에는 IBS의 CI로 선정돼 데이터 사이언스 그룹을 이끌며 인공지능(AI) 분야에서 우수 논문을 다수 발표하는 등 국제적 인지도를 높였다.
차 교수가 이끄는 데이터 사이언스 그룹은 2019년 출범해 초대형 데이터를 계산하고 분석하는 방법론을 연구하고 있다. 특히 AI를 이용해 가짜뉴스와 혐오 표현을 탐지하는 등 우리 삶과 밀접한 사회 현상을 분석해 괄목할 만한 연구성과를 창출했다.
코로나19 팬데믹 시절 ‘루머를 앞선 팩트’ 캠페인을 기획해 감염병 관련 잘못된 정보에 대한 팩트체크 결과를 151개국에 전파했다. 최근에는 위성영상을 AI로 분석해 북한을 비롯한 저개발국가의 경제지도를 만들어 무료로 공개했다. 최근 실시한 5년 차 평가에서 AI 기술을 기초과학에 창의적으로 활용해 차별성 있는 연구를 수행했으며, 데이터 과학 연구의 사회적 가치를 제고할 수 있는 핵심 기술을 개발하는 등 국제적 파급력 있는 연구성과를 창출했다는 평가를 받았다.
IBS 노도영 원장은 “IBS는 미래 연구단장을 발굴·육성하기 위해 젊은 연구자를 선정해 독립 연구를 지원하고 있다”라며, “이 제도로 발굴한 연구자가 막스플랑크 연구소 단장으로 초청받은 것에 대해 매우 기쁘게 생각하며 한국과 독일의 국제 연구 교류에도 크게 기여할 것으로 기대한다”라고 전했다.
우리 대학 이광형 총장은 “KAIST가 키워낸 차 교수의 행보는 국제화에 좋은 롤모델이 될 것”이라며, “계속해서 KAIST 학생 및 동료와 협업할 수 있도록 겸직을 비롯한 지원을 아끼지 않겠다”라고 축하의 메시지를 전했다.
차미영 CI는 “KAIST 교수로 쌓아온 경험에 더하여 IBS에서 긴 호흡으로 창의적인 연구를 지속한 덕분에 좋은 결과를 얻은 것 같다”라며, “앞으로 큰 책임감을 가지고 데이터 과학을 통한 사회 공헌을 위해 최선을 다하겠다”라고 포부를 밝혔다.
2024.01.09 조회수 2504
차미영 교수, 한국인 첫 獨 막스플랑크 연구소 단장 선임
세계적 기초과학 연구기관인 독일 막스플랑크 연구소(Max Planck Institute, MPI)에 첫 한국인 단장이 선임됐다. 우리 대학 전산학부 차미영 교수(기초과학연구원 수리 및 계산 과학 연구단 데이터 사이언스 그룹 CI(Chief Investigator))가 그 주인공이다. 차 교수는 독일 보흠 지역에 있는 막스플랑크 보안 및 정보보호 연구소(MPI for Security and Privacy)에서 6월부터 단장(Scientific Director)직 수행을 시작해 ‘인류를 위한 데이터 과학(Data Science for Humanity)’ 연구그룹을 이끌 예정이다. 현재 본격적인 연구그룹 출범을 준비하고 있다.
막스플랑크 연구소는 기초과학 분야를 아우르며 독일 전역과 해외에 85개 산하 연구소를 운영하고 있다. 연구소를 이끄는 300여 명의 단장 중 한국 국적 과학자가 발탁된 것은 이번이 처음이다. 한국계로는 지난해 8월 울산과학기술원(UNIST) 강사라 교수가 기후과학연구소 단장으로 선임된 바 있다.
차 교수는 구글 스칼라(Google Scholar) 기준 피인용 수 2만 회가 넘는 데이터 과학 분야 전문가로, 우리 대학 전산학부를 졸업하고 동 대학원에서 석·박사 학위를 받은 ‘토종박사’다. 박사 취득 이후 독일 자부르켄에 있는 막스플랑크 연구소에서 박사후연구원으로 근무했으며, 2010년부터 우리 대학 교수로 재직하고 있다. 2019년에는 IBS의 CI로 선정돼 데이터 사이언스 그룹을 이끌며 인공지능(AI) 분야에서 우수 논문을 다수 발표하는 등 국제적 인지도를 높였다.
차 교수가 이끄는 데이터 사이언스 그룹은 2019년 출범해 초대형 데이터를 계산하고 분석하는 방법론을 연구하고 있다. 특히 AI를 이용해 가짜뉴스와 혐오 표현을 탐지하는 등 우리 삶과 밀접한 사회 현상을 분석해 괄목할 만한 연구성과를 창출했다.
코로나19 팬데믹 시절 ‘루머를 앞선 팩트’ 캠페인을 기획해 감염병 관련 잘못된 정보에 대한 팩트체크 결과를 151개국에 전파했다. 최근에는 위성영상을 AI로 분석해 북한을 비롯한 저개발국가의 경제지도를 만들어 무료로 공개했다. 최근 실시한 5년 차 평가에서 AI 기술을 기초과학에 창의적으로 활용해 차별성 있는 연구를 수행했으며, 데이터 과학 연구의 사회적 가치를 제고할 수 있는 핵심 기술을 개발하는 등 국제적 파급력 있는 연구성과를 창출했다는 평가를 받았다.
IBS 노도영 원장은 “IBS는 미래 연구단장을 발굴·육성하기 위해 젊은 연구자를 선정해 독립 연구를 지원하고 있다”라며, “이 제도로 발굴한 연구자가 막스플랑크 연구소 단장으로 초청받은 것에 대해 매우 기쁘게 생각하며 한국과 독일의 국제 연구 교류에도 크게 기여할 것으로 기대한다”라고 전했다.
우리 대학 이광형 총장은 “KAIST가 키워낸 차 교수의 행보는 국제화에 좋은 롤모델이 될 것”이라며, “계속해서 KAIST 학생 및 동료와 협업할 수 있도록 겸직을 비롯한 지원을 아끼지 않겠다”라고 축하의 메시지를 전했다.
차미영 CI는 “KAIST 교수로 쌓아온 경험에 더하여 IBS에서 긴 호흡으로 창의적인 연구를 지속한 덕분에 좋은 결과를 얻은 것 같다”라며, “앞으로 큰 책임감을 가지고 데이터 과학을 통한 사회 공헌을 위해 최선을 다하겠다”라고 포부를 밝혔다.
2024.01.09 조회수 2504 햇빛만으로 결빙 방지되는 필름 개발
열선, 스프레이 및 오일 주기적 도포, 기판 디자인 변경 등 없이도 금나노입자의 광열 효과를 산업현장에 적용할 수 있는 방빙/제빙 필름 코팅 기술이 개발되었다.
우리 대학 기계공학과 김형수 교수 연구팀(유체 및 계면 연구실)과 화학과 윤동기 교수 연구팀(연성 물질 나노조립 연구실)의 공동융합연구를 통해 단순 증발만으로 금 나노막대 입자를 사분면으로 균일하게 패터닝 할 수 있는 원천 기술을 확보하고, 이를 이용해 결빙 방지 및 제빙 표면을 개발했다고 3일 밝혔다.
최근 다양한 코팅 기법을 이용해 목표물 표면의 성질을 제어하려는 연구가 많이 진행되고 있으며, 특히, 기능성 나노 재료 패터닝을 통한 방식이 큰 주목을 받고 있다. 이 중에서도 금 나노 막대(GNR)는 생체 적합성, 화학적 안정성, 비교적 쉬운 합성, 표면 플라즈몬 공명이라는 안정적이면서도 독특한 특성으로 인해 유망한 나노물질 중 하나로 여겨지고 있다. 이때, 금 나노 막대의 성능을 극대화하려면 높은 수준의 증착 필름의 균일도와 금 나노 막대의 정렬도를 획득하는 것이 매우 중요하며, 현재 이를 구현하는 것은 여전히 해결해야 할 큰 문제다.
이를 해결하고자, 공동연구팀은 자연계에서 쉽게 추출이 가능한 차세대 기능성 나노 물질인 셀룰로오스 나노크리스탈(CNC)를 활용했다. 셀룰로오스 나노크리스탈 사분면 템플릿에 금 나노 막대를 공동 자가 조립해 균일하게 건조되면서 코팅 전체 면적에 환형으로 균일하게 정렬된 금 나노막대 필름을 개발하는 데 성공했다. 이번 연구에서 획득한 높은 균일도와 정렬도를 갖는 금 나노막대 필름은 기존 커피링 필름과 비교해 향상된 플라즈모닉 광학/광열 성능을 보였으며, 이는 가시광선 파장 영역대의 빛 조사만으로 방빙/제빙 역할을 해낼 수 있음을 연구팀은 실험적으로 증명했다.
기계공학과 김형수 교수는 “이 기술은 플라스틱 및 유연 표면 위에도 제작이 가능해 이를 외장재 및 필름에 활용하면 자체적으로 열에너지를 발생시킬 수 있어, 겨울철에 큰 문제가 되는 자동차 성에, 항공기 제빙, 주거/상용 공간의 유리창 등 다양한 분야에서 자발적 열에너지 하베스팅 효과를 통해 에너지 절약 효과를 가져다 줄 수 있을 것으로 기대한다”고 언급했다. 한편 화학과 윤동기 교수는 “필름화하기 힘들었던 나노셀룰로오스-금입자 복합체를 대면적에서 자유롭게 패터닝해 결빙 소재로 사용할 수 있고, 금의 플라즈모닉 성질을 이용한다면 마치 유리를 장식하는 스테인드 글래스처럼 사용할 수 있다는 점에서 의미가 있다”고 언급했다.
해당 연구 결과는 기계공학과 편정수 박사과정, 박순모 박사(KAIST졸업, 現 코넬 대학교 박사 후 연구원)가 공동 제1 저자로 참여했으며, 국제학술지 `네이처 커뮤니케이션즈(Nature Communications)' 2023년 12월 8일 字 온라인판에 게재됐다. (논문명 : Plasmonic Metasurfaces of Cellulose Nanocrystal Matrices with Quadrants of Aligned Gold Nanorods for Photothermal Anti-Icing, https://doi.org/10.1038/s41467-023-43511-9) 그리고, 연구의 우수성을 인정받아 국제 저널‘재료과학과 화학(Materials Science and Chemistry)’ 과 ‘무기 물리화학(Inorganic and Physical Chemistry)’ 두 편집자 하이라이트(Editors’ Highlights) 페이지에 선정됐다.
이번 연구는 한국연구재단의 개인기초 중견 연구(MIST: 2021R1A2C2007835)와 멀티스케일 카이랄 구조체 연구센터 (MSIT: 2018R1A5A1025208) 지원을 받아 수행됐다.
2024.01.03 조회수 5206
햇빛만으로 결빙 방지되는 필름 개발
열선, 스프레이 및 오일 주기적 도포, 기판 디자인 변경 등 없이도 금나노입자의 광열 효과를 산업현장에 적용할 수 있는 방빙/제빙 필름 코팅 기술이 개발되었다.
우리 대학 기계공학과 김형수 교수 연구팀(유체 및 계면 연구실)과 화학과 윤동기 교수 연구팀(연성 물질 나노조립 연구실)의 공동융합연구를 통해 단순 증발만으로 금 나노막대 입자를 사분면으로 균일하게 패터닝 할 수 있는 원천 기술을 확보하고, 이를 이용해 결빙 방지 및 제빙 표면을 개발했다고 3일 밝혔다.
최근 다양한 코팅 기법을 이용해 목표물 표면의 성질을 제어하려는 연구가 많이 진행되고 있으며, 특히, 기능성 나노 재료 패터닝을 통한 방식이 큰 주목을 받고 있다. 이 중에서도 금 나노 막대(GNR)는 생체 적합성, 화학적 안정성, 비교적 쉬운 합성, 표면 플라즈몬 공명이라는 안정적이면서도 독특한 특성으로 인해 유망한 나노물질 중 하나로 여겨지고 있다. 이때, 금 나노 막대의 성능을 극대화하려면 높은 수준의 증착 필름의 균일도와 금 나노 막대의 정렬도를 획득하는 것이 매우 중요하며, 현재 이를 구현하는 것은 여전히 해결해야 할 큰 문제다.
이를 해결하고자, 공동연구팀은 자연계에서 쉽게 추출이 가능한 차세대 기능성 나노 물질인 셀룰로오스 나노크리스탈(CNC)를 활용했다. 셀룰로오스 나노크리스탈 사분면 템플릿에 금 나노 막대를 공동 자가 조립해 균일하게 건조되면서 코팅 전체 면적에 환형으로 균일하게 정렬된 금 나노막대 필름을 개발하는 데 성공했다. 이번 연구에서 획득한 높은 균일도와 정렬도를 갖는 금 나노막대 필름은 기존 커피링 필름과 비교해 향상된 플라즈모닉 광학/광열 성능을 보였으며, 이는 가시광선 파장 영역대의 빛 조사만으로 방빙/제빙 역할을 해낼 수 있음을 연구팀은 실험적으로 증명했다.
기계공학과 김형수 교수는 “이 기술은 플라스틱 및 유연 표면 위에도 제작이 가능해 이를 외장재 및 필름에 활용하면 자체적으로 열에너지를 발생시킬 수 있어, 겨울철에 큰 문제가 되는 자동차 성에, 항공기 제빙, 주거/상용 공간의 유리창 등 다양한 분야에서 자발적 열에너지 하베스팅 효과를 통해 에너지 절약 효과를 가져다 줄 수 있을 것으로 기대한다”고 언급했다. 한편 화학과 윤동기 교수는 “필름화하기 힘들었던 나노셀룰로오스-금입자 복합체를 대면적에서 자유롭게 패터닝해 결빙 소재로 사용할 수 있고, 금의 플라즈모닉 성질을 이용한다면 마치 유리를 장식하는 스테인드 글래스처럼 사용할 수 있다는 점에서 의미가 있다”고 언급했다.
해당 연구 결과는 기계공학과 편정수 박사과정, 박순모 박사(KAIST졸업, 現 코넬 대학교 박사 후 연구원)가 공동 제1 저자로 참여했으며, 국제학술지 `네이처 커뮤니케이션즈(Nature Communications)' 2023년 12월 8일 字 온라인판에 게재됐다. (논문명 : Plasmonic Metasurfaces of Cellulose Nanocrystal Matrices with Quadrants of Aligned Gold Nanorods for Photothermal Anti-Icing, https://doi.org/10.1038/s41467-023-43511-9) 그리고, 연구의 우수성을 인정받아 국제 저널‘재료과학과 화학(Materials Science and Chemistry)’ 과 ‘무기 물리화학(Inorganic and Physical Chemistry)’ 두 편집자 하이라이트(Editors’ Highlights) 페이지에 선정됐다.
이번 연구는 한국연구재단의 개인기초 중견 연구(MIST: 2021R1A2C2007835)와 멀티스케일 카이랄 구조체 연구센터 (MSIT: 2018R1A5A1025208) 지원을 받아 수행됐다.
2024.01.03 조회수 5206 권태형 박사과정, 고지훈 석박사통합과정, IEEE ICDM 2023 최우수논문상 수상
우리 대학 김재철AI대학원 권태형 박사과정, 고지훈 석박사통합과정 (지도교수 신기정)이 지난 12월 중국 상해에서 열린 제23회 IEEE International Conference on Data Mining (IEEE ICDM)에서 최우수 논문상(Best Student Paper Runner-up)을 수상했다.
IEEE ICDM은 매년 개최되는 데이터 마이닝 분야 최고 권위의 국제 학회 중 하나다. 올해는 총 200편의 논문이 발표됐고 그 중 권태형, 고지훈 학생이 참여한 논문을 포함한 4편의 논문이 최우수 논문으로 선정됐다.
논문 제목은 ‘텐서코덱: 데이터에 대한 가정이 필요 없는 간결한 텐서의 손실 압축 기법’(TensorCodec: Compact Lossy Compression of Tensors without Strong Data Assumptions)이다.
이 연구에서는 텐서, 즉 고차원 행렬 데이터를 위한 압축 기술을 제시하였다. 텐서-열차 분해(Tensor-Train Decomposition)와 인공신경망을 결합하여 압축 성능을 향상했으며, 행과 열을 재배치하고 차원을 증가시키는 등 입력 텐서의 형태에 대한 최적화를 통해 압축 성능을 추가로 개선하였다. 또한, 다양한 실세계 데이터를 사용하여 제안된 방법의 우수성과 범용성을 검증하였다.
권태형, 고지훈 학생은 “항상 연구에 대한 열정이 가득하시고, 창의적인 아이디어를 제공하여 연구의 돌파구를 열어 주신 신기정 교수님의 지도 덕분에 수상이 가능했다”며 “해당 아이디어가 더욱 고도화되어, 추천시스템, 이상 탐지, AI 모델 경량화 등 다양한 분야에서 활용될 수 있기를 바란다”고 말했다.
이 연구에는 권태형 박사과정, 고지훈 석박통합과정, 신기정 교수 외에 숭실대학교 정진홍 교수가 참여하였으며, 정보통신기획평가원의 지원을 받은 강건하고 공정하며 확장 가능한 데이터 중심의 연속 학습 과제와 한국연구재단의 지원을 받은 부호화된 그래프 마이닝 과제의 성과다.
2024.01.02 조회수 1605
권태형 박사과정, 고지훈 석박사통합과정, IEEE ICDM 2023 최우수논문상 수상
우리 대학 김재철AI대학원 권태형 박사과정, 고지훈 석박사통합과정 (지도교수 신기정)이 지난 12월 중국 상해에서 열린 제23회 IEEE International Conference on Data Mining (IEEE ICDM)에서 최우수 논문상(Best Student Paper Runner-up)을 수상했다.
IEEE ICDM은 매년 개최되는 데이터 마이닝 분야 최고 권위의 국제 학회 중 하나다. 올해는 총 200편의 논문이 발표됐고 그 중 권태형, 고지훈 학생이 참여한 논문을 포함한 4편의 논문이 최우수 논문으로 선정됐다.
논문 제목은 ‘텐서코덱: 데이터에 대한 가정이 필요 없는 간결한 텐서의 손실 압축 기법’(TensorCodec: Compact Lossy Compression of Tensors without Strong Data Assumptions)이다.
이 연구에서는 텐서, 즉 고차원 행렬 데이터를 위한 압축 기술을 제시하였다. 텐서-열차 분해(Tensor-Train Decomposition)와 인공신경망을 결합하여 압축 성능을 향상했으며, 행과 열을 재배치하고 차원을 증가시키는 등 입력 텐서의 형태에 대한 최적화를 통해 압축 성능을 추가로 개선하였다. 또한, 다양한 실세계 데이터를 사용하여 제안된 방법의 우수성과 범용성을 검증하였다.
권태형, 고지훈 학생은 “항상 연구에 대한 열정이 가득하시고, 창의적인 아이디어를 제공하여 연구의 돌파구를 열어 주신 신기정 교수님의 지도 덕분에 수상이 가능했다”며 “해당 아이디어가 더욱 고도화되어, 추천시스템, 이상 탐지, AI 모델 경량화 등 다양한 분야에서 활용될 수 있기를 바란다”고 말했다.
이 연구에는 권태형 박사과정, 고지훈 석박통합과정, 신기정 교수 외에 숭실대학교 정진홍 교수가 참여하였으며, 정보통신기획평가원의 지원을 받은 강건하고 공정하며 확장 가능한 데이터 중심의 연속 학습 과제와 한국연구재단의 지원을 받은 부호화된 그래프 마이닝 과제의 성과다.
2024.01.02 조회수 1605 원하는 색깔의 마이크로 LED 전사 기술 개발
기존 OLED 등과 비해 전기적·광학적 특성이 우수한 마이크로 LED는 머리카락 두께인 100마이크로미터(μm) 이하 크기의 무기물 LED 칩을 활용하는 차세대 디스플레이용 광원이다. 마이크로 LED의 상용화를 위해선 성장 기판에 배열된 대량의 마이크로 LED 칩을 최종 기판의 정확한 위치에 원하는 배열로 옮기는 ‘전사 공정’이 가장 중요한 핵심기술이지만, 기존 전사 기술들은 별도의 접착제 사용, 정렬 오차, 낮은 수율, 칩 손상 등으로 마이크로 LED 상용화에 많은 어려움이 존재했다.
우리 대학 신소재공학과 이건재 교수 연구팀이 마이크로진공 흡입력을 조절해 대량의 마이크로 LED 칩을 색깔별 원하는 칩들만 선택적으로 전사하는 기술을 개발했다고 19일 밝혔다.
이 교수팀은 레이저빔 조사시 물질 특성을 조정하여 식각하는 레이저 유도 에칭(Laser-induced etching, LIE) 기술을 활용해 미세 관통홀을 유리 기판에 초당 7,000개 속도로 형성했고, 이를 진공 채널에 연결해 미세진공 흡입력을 발생시켜 마이크로 LED를 전사하는 데 성공했다. 이 기술은 기존 전사 기술 대비 뛰어난 접착력 전환성을 달성하였으며, 다수의 진공 채널별 독립적인 진공 조절을 통해 대량의 마이크로 LED 칩을 선택적으로 전사하였다. 또한 다양한 재료, 크기, 모양, 두께를 지닌 초소형 반도체 칩들을 칩 손상 없이 임의의 기판에 높은 수율로 전사할 수 있었다.
이건재 교수는 “이번에 개발된 마이크로진공 전사 기술은 가파르게 성장하는 마이크로 LED 시장에서 높은 생산 원가를 절감하고 중저가 마이크로 LED 제품 양산화의 핵심 기술로 활용될 것이 기대된다”면서, “현재 얇은 핀으로 칩을 들어 올리는 이젝터 시스템을 적용해 대량의 상용 마이크로 LED를 전사하고, 이를 통해 차세대 디스플레이(대형 TV, 유연․신축성 기기 등) 뿐만 아니라 광-바이오 융합형 미용 면발광 패치 상용화를 진행 중이다”라고 말했다.
한편 이번 연구는 웨어러블플랫폼 소재기술 센터, 중견연구자지원사업, 소부장 전략협력 기술개발사업의 지원을 받아 수행됐으며, 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 11월 26일 자 출판됐다.
2023.12.19 조회수 1678
원하는 색깔의 마이크로 LED 전사 기술 개발
기존 OLED 등과 비해 전기적·광학적 특성이 우수한 마이크로 LED는 머리카락 두께인 100마이크로미터(μm) 이하 크기의 무기물 LED 칩을 활용하는 차세대 디스플레이용 광원이다. 마이크로 LED의 상용화를 위해선 성장 기판에 배열된 대량의 마이크로 LED 칩을 최종 기판의 정확한 위치에 원하는 배열로 옮기는 ‘전사 공정’이 가장 중요한 핵심기술이지만, 기존 전사 기술들은 별도의 접착제 사용, 정렬 오차, 낮은 수율, 칩 손상 등으로 마이크로 LED 상용화에 많은 어려움이 존재했다.
우리 대학 신소재공학과 이건재 교수 연구팀이 마이크로진공 흡입력을 조절해 대량의 마이크로 LED 칩을 색깔별 원하는 칩들만 선택적으로 전사하는 기술을 개발했다고 19일 밝혔다.
이 교수팀은 레이저빔 조사시 물질 특성을 조정하여 식각하는 레이저 유도 에칭(Laser-induced etching, LIE) 기술을 활용해 미세 관통홀을 유리 기판에 초당 7,000개 속도로 형성했고, 이를 진공 채널에 연결해 미세진공 흡입력을 발생시켜 마이크로 LED를 전사하는 데 성공했다. 이 기술은 기존 전사 기술 대비 뛰어난 접착력 전환성을 달성하였으며, 다수의 진공 채널별 독립적인 진공 조절을 통해 대량의 마이크로 LED 칩을 선택적으로 전사하였다. 또한 다양한 재료, 크기, 모양, 두께를 지닌 초소형 반도체 칩들을 칩 손상 없이 임의의 기판에 높은 수율로 전사할 수 있었다.
이건재 교수는 “이번에 개발된 마이크로진공 전사 기술은 가파르게 성장하는 마이크로 LED 시장에서 높은 생산 원가를 절감하고 중저가 마이크로 LED 제품 양산화의 핵심 기술로 활용될 것이 기대된다”면서, “현재 얇은 핀으로 칩을 들어 올리는 이젝터 시스템을 적용해 대량의 상용 마이크로 LED를 전사하고, 이를 통해 차세대 디스플레이(대형 TV, 유연․신축성 기기 등) 뿐만 아니라 광-바이오 융합형 미용 면발광 패치 상용화를 진행 중이다”라고 말했다.
한편 이번 연구는 웨어러블플랫폼 소재기술 센터, 중견연구자지원사업, 소부장 전략협력 기술개발사업의 지원을 받아 수행됐으며, 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 11월 26일 자 출판됐다.
2023.12.19 조회수 1678 혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14 조회수 1729
혹시 나도 수면 질환? AI로 간단히 검사해 보세요
각종 장비를 몸에 부착한 채 병원에서 하룻밤을 보내야 하는 번거로운 검사 없이 웹사이트를 통해 간단히 수면 질환 위험도를 파악할 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀이 삼성서울병원 주은연‧최수정 교수팀, 이화여대 서울병원 김지현 교수팀과 공동 연구를 통해 개발한 세 가지 수면 질환을 예측할 수 있는 알고리즘 ‘슬립스(SLEEPS‧SimpLe quEstionnairE Predicting Sleep disorders)’를 12일 공개했다.
‘잠이 보약’이라는 말처럼 수면은 정신적‧신체적 건강에 주요한 영향을 미친다. 성인의 60%가량이 수면 질환을 앓고 있지만, 관련하여 전문 의료진에게 문의한 비율은 6% 수준에 불과하다. 병원 방문을 꺼리는 원인 중 하나로는 수면 질환 진단을 받기 위해 시행하는 수면다원검사가 번거롭다는 이유가 있다.
공동연구진은 약 5,000명의 수면다원검사 결과를 기계 학습을 통해 학습시켜 수면 질환 위험도를 예측하는 알고리즘 ‘슬립스’를 개발했다. 슬립스에서 나이, 성별, 키, 체중, 최근 2주간의 수면 시 어려움, 수면 유지 어려움, 기상 시 어려움, 수면 패턴에 대한 만족도, 수면이 일상 기능에 미치는 영향 등 간단한 9개의 질문에 답하는 것만으로 만성불면증, 수면호흡장애, 수면호흡장애를 동반한 불면증의 위험도를 90%의 정확도로 예측할 수 있다. 가령, 슬립스 검사 결과 수면호흡장애 위험도가 50%라는 결과가 나왔다면, 실제 수면다원검사를 시행했을 때 수면호흡장애가 발견될 확률이 50%임을 의미한다.
제1 저자인 하석민 미국 MIT 박사과정생(前 IBS 의생명 수학 그룹 연구원)은 “미국 하버드대 연구팀도 AI 기반 수면 질환 검사 알고리즘을 개발한 바 있으나, 이 시스템은 목둘레, 혈압 등 쉽게 답하기 어려운 문항이 포함되어 있어 사용이 까다로웠다”며 “또한, 하버드대 연구팀의 시스템은 예측 정확도도 70% 정도에 그쳤다”고 말했다.
슬립스 사이트(www.sleep-math.com)를 통해 누구나 수면 질환 여부를 예측해볼 수 있다. 현재 본인의 상태를 기준으로 몸무게 변화나 나이가 듦에 따른 수면 질환 위험도 변화도 살펴볼 수 있다.
김재경 교수는 “이번 연구는 수학으로 우리가 직면한 건강 문제를 해결해보고자 하는 시도에서 시작됐고, 중요하지만 쉽게 간과할 수 있는 수면 질환에 기계 학습을 접목했다”며 “수면 질환 진단의 복잡한 과정을 줄인 만큼, 많은 사람이 슬립스를 통해 자신의 수면 건강을 알 수 있는 계기가 되길 바란다”고 말했다.
주은연 삼성서울병원 교수는 “슬립스는 간편한 수면 질환 자가 검진 시스템”이라며 “향후 건강검진 항목에 AI 기반 자가 검진 시스템을 포함한다면 잠재적인 수면 질환 환자들을 스크리닝하여 수면 질환으로 인해 발생하는 수많은 질병을 선제적으로 예방할 수 있을 것”이라고 말했다.
슬립스 개발 성과는 지난 9월 의료 건강 분야 국제학술지 ‘Journal of Medical Internet Research’에 실린 바 있다.
2023.12.14 조회수 1729