-
 신소재공학과 염지현, 기계공학과 심기동 교수, 포스코사이언스펠로우 선정
우리 대학 신소재공학과 염지현, 기계공학과 심기동 교수가 포스코청암재단에서 선정하는 제12기 '포스코사이언스펠로우'로 선발됐다고 2020년 9월 7일 발표됐다.
포스코사이언스펠로우십은 2009년에 시작해 대한민국의 미래를 이끌어 갈 과학기술 인재양성을 목표로 매년 기초과학 및 응용과학을 연구하는 유능한 신진교수를 선발하고 있다. 이는 독자적인 연구와 실험을 시작하는 신진교수에게 2년간 총 1억원을 지원하는 명예로운 사업이다. 올해 신진교수 166명이 지원해 8:1이 넘는 치열한 경쟁률 속에서 수상한 만큼 그 의미가 더 깊다.
염지현 교수는 우리 대학 신소재공학과 학사과정을 졸업한 후 미시간대학교에서 박사학위를, MIT에서 포스닥을 하는 동안 Overberger Research Award 등 20개 가까이되는 명예로운 상들을 수상한 실적을 보유하고 있다. 더불어 조교수로 신소재공학과에 부임한지 불과 6개월만에 포스코사이언스펠로쉽을 수상하는 쾌거도 이루었다.
심기동 교수는 우리 대학 기계공학과에서 2012년도 박사 학위를 받고, 하버드 대학교 포스닥 펠로우, 존스홉킨스 대학교 Research Scientist를 거쳐 2018년 2월에 KAIST 조교수로 부임하였다. 현재 iCaRE(in-situ Characterization and Reliability Evaluation) 연구실 학생들과 재료의 기계적 거동을 다양한 length-scale 및 환경 조건에서 이해하기 위한 연구를 진행하고 있다.
염지현, 심기동 교수는 내년 1월부터 2년간 지원을 받을 예정이다.
신소재공학과 염지현, 기계공학과 심기동 교수, 포스코사이언스펠로우 선정
우리 대학 신소재공학과 염지현, 기계공학과 심기동 교수가 포스코청암재단에서 선정하는 제12기 '포스코사이언스펠로우'로 선발됐다고 2020년 9월 7일 발표됐다.
포스코사이언스펠로우십은 2009년에 시작해 대한민국의 미래를 이끌어 갈 과학기술 인재양성을 목표로 매년 기초과학 및 응용과학을 연구하는 유능한 신진교수를 선발하고 있다. 이는 독자적인 연구와 실험을 시작하는 신진교수에게 2년간 총 1억원을 지원하는 명예로운 사업이다. 올해 신진교수 166명이 지원해 8:1이 넘는 치열한 경쟁률 속에서 수상한 만큼 그 의미가 더 깊다.
염지현 교수는 우리 대학 신소재공학과 학사과정을 졸업한 후 미시간대학교에서 박사학위를, MIT에서 포스닥을 하는 동안 Overberger Research Award 등 20개 가까이되는 명예로운 상들을 수상한 실적을 보유하고 있다. 더불어 조교수로 신소재공학과에 부임한지 불과 6개월만에 포스코사이언스펠로쉽을 수상하는 쾌거도 이루었다.
심기동 교수는 우리 대학 기계공학과에서 2012년도 박사 학위를 받고, 하버드 대학교 포스닥 펠로우, 존스홉킨스 대학교 Research Scientist를 거쳐 2018년 2월에 KAIST 조교수로 부임하였다. 현재 iCaRE(in-situ Characterization and Reliability Evaluation) 연구실 학생들과 재료의 기계적 거동을 다양한 length-scale 및 환경 조건에서 이해하기 위한 연구를 진행하고 있다.
염지현, 심기동 교수는 내년 1월부터 2년간 지원을 받을 예정이다.
2020.09.16
조회수 22682
-
 에티오피아 장관, KAIST서 4년 연구 끝에 박사학위 취득
올해 지천명(知天命·50세)의 나이를 맞은 에티오피아의 현직 장관이 우리 대학에서 박사학위를 취득해 화제가 되고 있다. 기술경영학부 글로벌IT기술대학원에서 지난 8월 박사학위를 취득한 메쿠리아 테클레마리암(Mekuria Teklemariam) 에티오피아 국무총리자문 장관이 그 주인공이다.
메쿠리아 장관은 2016년 9월 KAIST에서 박사과정 첫 학기를 시작한 지 4년만인 지난 8월 경영학박사 학위를 취득했다.
메쿠리아 장관은 "한국은 지난 수십 년간 정치·경제를 포함한 모든 분야에서 눈부신 발전을 이뤄낸 나라ˮ라면서 "에티오피아의 발전을 위해 성공사례를 보유한 국가의 성장 원동력을 학문적으로 연구해보고 싶었다ˮ라고 유학 배경을 밝혔다.
40세에 도시개발주택부 장관으로 취임해 에티오피아 역사상 최연소 장관이라는 기록을 세운 메쿠리아 장관은 6년의 재임 기간에 신도시·스마트시티 개발, 토지관리, 주택개발 등의 정책을 수립하고 집행하며 에티오피아의 경제 개발을 이끌어왔다.
그러나 그는 자신의 행보에 만족하지 못했다. 외적으로는 여러 가지 성취를 거뒀지만 비슷한 일들을 거듭하다 보니 행정가가 지녀야 할 능력이 정체된다는 고민이 커졌기 때문이다.
학업에 대한 결심을 굳힌 뒤 정부에 사임 의사를 밝혔지만, 국무총리는 현직에 남아 달라고 당부하며 한 가지를 물어왔다. '유학 가려는 이유가 개인의 이력을 위한 것인지 나라를 위한 것인지'를 확인하는 질문이었다.
국무총리의 말은 메쿠리아 장관의 한국행을 결심하는 계기가 됐다. 영국의 개방대학이나 미국 MIT의 최고위 과정을 선택하면 비교적 짧은 시간을 투자해 수월하게 공부할 수 있다는 장점이 있었다. 그러나 최빈국에서 강대국으로 성장한 한국의 사례를 연구하는 것이야말로 자국 발전에 기여하고 싶다는 목적에 가장 부합하는 선택이라고 결론 내린 것이다.
이후, 메쿠리아 장관은 KAIST에 지원했다. 과학기술 분야의 전문성, 탁월한 연구성과, 국제화에 특화된 대학원 과정 등 모든 면에서 학업을 이어가기 가장 좋은 환경이 마련돼 있었기 때문이다.
6개월여의 준비 끝에 2015년 KAIST 대학원에 합격했지만 메쿠리아 장관은 한국 땅을 밟지 못했다. 사임 의사가 또다시 반려된 탓이었다. 그러나 그는 포기하지 않았다. 일단 휴학을 신청한 뒤 지도교수인 기술경영학부 권영선 교수와 함께 계속해서 정부를 설득해나갔다.
메쿠리아 장관의 의지를 확인한 에티오피아 정부는 9인으로 구성된 위원회를 열어 그의 유학에 관한 투표를 진행했다. 다수의 위원이 국가 발전을 위해 학업을 선택한 그의 결정에 지지를 보냈고 도시개발주택부 장관에서 국무총리자문 장관으로 직위를 변경한 끝에 유학길에 오를 수 있었다.
2016년 가을부터 한국 생활을 시작한 메쿠리아 장관은 지난 4년간 학업에 매진했다. 정보격차 해소가 경제성장과 부패통제에 미치는 영향·개발도상국의 초고속인터넷 보급 및 확산정책 등의 주제를 연구해 국내외 학회에서 발표했다.
특히, 정보통신산업진흥원(NIPA)·과학기술정책연구원(STEPI) 등과의 협업 연구를 진행해 글로벌IT기술대학원에서 수여하는 우수 협력연구상을 2018년에 두 차례 수상했다. 또한, 졸업논문 연구로 수행한 '단계별 맞춤형 모바일 초고속인터넷 확산 정책'에 관한 논문은 정보통신 분야의 최우수 국제학술지에 속하는 SSCI 저널인 텔레커뮤니케이션즈 폴리시(Telecommunications Policy)에 지난 8월 졸업에 앞서 게재됐다.
광대역 통신망을 갖춘 국가들의 효과적인 정보통신 정책을 분석해 개발도상국에 맞춤형 정책을 제안하는 계량적 정책 연구를 성공적으로 완수한 결과다.
이런 성과들을 바탕으로 메쿠리아 장관은 글로벌IT기술대학원의 최우수 졸업생이란 영예와 함께 지난달 13일 박사학위를 취득했다.
"내 결정이 옳았다. 기대한 것보다 더 많이 배우고 간다ˮ고 소감을 밝힌 메쿠리아 장관은 "학업은 물론 주변 사람들과의 관계 속에서 얻는 가치들로 인해 더없이 즐겁고 행복한 시간이었다ˮ라고 말했다.
지난달 18일 신성철 총장을 접견한 메쿠리아 장관은 "지난 4년간 직접 경험한 KAIST의 연구·행정·산학협력 등을 벤치마킹해 에티오피아 과학기술대학의 경쟁력 향상에 일조하고 싶다ˮ는 뜻을 전달했다. 신 총장은 "국가 발전에 기여한 KAIST의 지식과 경험이 에티오피아 과학기술원 혁신과 양국의 교류 확대를 위해 유용하게 활용될 수 있는 협력 방안을 모색하자ˮ고 화답했다.
에티오피아에 적용해보고 싶은 한국의 정책 사례로 새마을 운동, 누구나 손쉽게 인터넷에 접근할 수 있는 인프라 구축, 장년층을 대상으로 하는 IT 활용기술 교육프로그램 등을 꼽은 메쿠리아 장관은 오는 12일 본국으로 돌아간다.
그는 "어느 자리에 있든 자신의 몫을 다 하기 위해 노력하는 것은 물론 말에서 그치는 것이 아니라 행동으로 실천하고 한국인들의 모습을 인상 깊게 지켜봤다ˮ라고 전하며 "한국과 KAIST에서 배운 것들을 에티오피아에 적용하고 실천하겠다ˮ라고 밝혔다.
에티오피아 장관, KAIST서 4년 연구 끝에 박사학위 취득
올해 지천명(知天命·50세)의 나이를 맞은 에티오피아의 현직 장관이 우리 대학에서 박사학위를 취득해 화제가 되고 있다. 기술경영학부 글로벌IT기술대학원에서 지난 8월 박사학위를 취득한 메쿠리아 테클레마리암(Mekuria Teklemariam) 에티오피아 국무총리자문 장관이 그 주인공이다.
메쿠리아 장관은 2016년 9월 KAIST에서 박사과정 첫 학기를 시작한 지 4년만인 지난 8월 경영학박사 학위를 취득했다.
메쿠리아 장관은 "한국은 지난 수십 년간 정치·경제를 포함한 모든 분야에서 눈부신 발전을 이뤄낸 나라ˮ라면서 "에티오피아의 발전을 위해 성공사례를 보유한 국가의 성장 원동력을 학문적으로 연구해보고 싶었다ˮ라고 유학 배경을 밝혔다.
40세에 도시개발주택부 장관으로 취임해 에티오피아 역사상 최연소 장관이라는 기록을 세운 메쿠리아 장관은 6년의 재임 기간에 신도시·스마트시티 개발, 토지관리, 주택개발 등의 정책을 수립하고 집행하며 에티오피아의 경제 개발을 이끌어왔다.
그러나 그는 자신의 행보에 만족하지 못했다. 외적으로는 여러 가지 성취를 거뒀지만 비슷한 일들을 거듭하다 보니 행정가가 지녀야 할 능력이 정체된다는 고민이 커졌기 때문이다.
학업에 대한 결심을 굳힌 뒤 정부에 사임 의사를 밝혔지만, 국무총리는 현직에 남아 달라고 당부하며 한 가지를 물어왔다. '유학 가려는 이유가 개인의 이력을 위한 것인지 나라를 위한 것인지'를 확인하는 질문이었다.
국무총리의 말은 메쿠리아 장관의 한국행을 결심하는 계기가 됐다. 영국의 개방대학이나 미국 MIT의 최고위 과정을 선택하면 비교적 짧은 시간을 투자해 수월하게 공부할 수 있다는 장점이 있었다. 그러나 최빈국에서 강대국으로 성장한 한국의 사례를 연구하는 것이야말로 자국 발전에 기여하고 싶다는 목적에 가장 부합하는 선택이라고 결론 내린 것이다.
이후, 메쿠리아 장관은 KAIST에 지원했다. 과학기술 분야의 전문성, 탁월한 연구성과, 국제화에 특화된 대학원 과정 등 모든 면에서 학업을 이어가기 가장 좋은 환경이 마련돼 있었기 때문이다.
6개월여의 준비 끝에 2015년 KAIST 대학원에 합격했지만 메쿠리아 장관은 한국 땅을 밟지 못했다. 사임 의사가 또다시 반려된 탓이었다. 그러나 그는 포기하지 않았다. 일단 휴학을 신청한 뒤 지도교수인 기술경영학부 권영선 교수와 함께 계속해서 정부를 설득해나갔다.
메쿠리아 장관의 의지를 확인한 에티오피아 정부는 9인으로 구성된 위원회를 열어 그의 유학에 관한 투표를 진행했다. 다수의 위원이 국가 발전을 위해 학업을 선택한 그의 결정에 지지를 보냈고 도시개발주택부 장관에서 국무총리자문 장관으로 직위를 변경한 끝에 유학길에 오를 수 있었다.
2016년 가을부터 한국 생활을 시작한 메쿠리아 장관은 지난 4년간 학업에 매진했다. 정보격차 해소가 경제성장과 부패통제에 미치는 영향·개발도상국의 초고속인터넷 보급 및 확산정책 등의 주제를 연구해 국내외 학회에서 발표했다.
특히, 정보통신산업진흥원(NIPA)·과학기술정책연구원(STEPI) 등과의 협업 연구를 진행해 글로벌IT기술대학원에서 수여하는 우수 협력연구상을 2018년에 두 차례 수상했다. 또한, 졸업논문 연구로 수행한 '단계별 맞춤형 모바일 초고속인터넷 확산 정책'에 관한 논문은 정보통신 분야의 최우수 국제학술지에 속하는 SSCI 저널인 텔레커뮤니케이션즈 폴리시(Telecommunications Policy)에 지난 8월 졸업에 앞서 게재됐다.
광대역 통신망을 갖춘 국가들의 효과적인 정보통신 정책을 분석해 개발도상국에 맞춤형 정책을 제안하는 계량적 정책 연구를 성공적으로 완수한 결과다.
이런 성과들을 바탕으로 메쿠리아 장관은 글로벌IT기술대학원의 최우수 졸업생이란 영예와 함께 지난달 13일 박사학위를 취득했다.
"내 결정이 옳았다. 기대한 것보다 더 많이 배우고 간다ˮ고 소감을 밝힌 메쿠리아 장관은 "학업은 물론 주변 사람들과의 관계 속에서 얻는 가치들로 인해 더없이 즐겁고 행복한 시간이었다ˮ라고 말했다.
지난달 18일 신성철 총장을 접견한 메쿠리아 장관은 "지난 4년간 직접 경험한 KAIST의 연구·행정·산학협력 등을 벤치마킹해 에티오피아 과학기술대학의 경쟁력 향상에 일조하고 싶다ˮ는 뜻을 전달했다. 신 총장은 "국가 발전에 기여한 KAIST의 지식과 경험이 에티오피아 과학기술원 혁신과 양국의 교류 확대를 위해 유용하게 활용될 수 있는 협력 방안을 모색하자ˮ고 화답했다.
에티오피아에 적용해보고 싶은 한국의 정책 사례로 새마을 운동, 누구나 손쉽게 인터넷에 접근할 수 있는 인프라 구축, 장년층을 대상으로 하는 IT 활용기술 교육프로그램 등을 꼽은 메쿠리아 장관은 오는 12일 본국으로 돌아간다.
그는 "어느 자리에 있든 자신의 몫을 다 하기 위해 노력하는 것은 물론 말에서 그치는 것이 아니라 행동으로 실천하고 한국인들의 모습을 인상 깊게 지켜봤다ˮ라고 전하며 "한국과 KAIST에서 배운 것들을 에티오피아에 적용하고 실천하겠다ˮ라고 밝혔다.
2020.09.08
조회수 21206
-
 항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25
조회수 26128
-
 제49주년 개교기념식에서 ‘2019년 올해의 KAIST인 상’ 등 총 45명 교원 시상
지난 7월 30일 열린 개교 49주년 기념식 행사에서 우리 대학은 물리학과 심흥선 교수를 '2019년 올해의 KAIST인'으로 선정해 시상했다.
'올해의 KAIST인 상'은 한 해 동안 국내·외에서 KAIST 발전을 위해 노력하고 학술 및 연구 실적이 탁월한 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
19번째 수상의 영예를 거머쥔 심흥선 교수는 2019년 한 해 동안 네이처(Nature)지에 물리학 난제인 콘도 스핀 구름의 존재를 세계 최초로 입증하는 연구성과를, 네이처 나노테크놀로지(Nature Nanotechnology)지에는 양자 기술의 핵심문제인 전자의 파동성 제어·관측을 위해 전자 파동의 피코초 진동 관측법을 발견하는 연구성과를 게재하는 등 KAIST의 위상을 크게 높였다는 평가를 받았다.
심흥선 교수는 "올해의 KAIST인 상을 수상하게 되어 영광이며, 이는 함께 연구하고 있는 학생들 덕분이며, 그들에게 고마움을 전한다. 자연에 대한 더 깊이 있는 이해를 얻기 위해 노력하겠다.”라고 소감을 밝혔다.
이 외에도 우리 대학은 교육, 학술, 연구, 국제협력 성과가 탁월하거나 KAIST의 위상에 크게 공헌한 총 32명의 교원에게 ‘개교기념 우수교원 포상 및 특별포상’을, 12명의 교원에게 '송암 미래 석학 우수연구상', '2019년 대표 연구성과 10선' 상 등을 수여했다.
주요 수상자는 다음과 같다.
학술대상을 수상한 기계공학과 김승우 교수는 현대 첨단 산업이 요구하는 초정밀 광학계측 기술의 선도적 개발을 주도했으며, 특히 첨단 광계측 기술 분야의 세계적 연구 결과를 창출하여 KAIST를 대표할 만한 탁월한 학술 연구업적을 낸 점을 높이 평가받았다.
창의강의대상을 수상한 전산학부 김주호 교수는 전산학에 인문학 지식을 결합한 CS+X 형태의 융합형 교과목을 개설해 사람을 위한 기술을 강조하는 등 학생 교육의 질적 향상에 크게 기여한 공로를 인정받았다.
우수강의대상을 수상한 경영공학부 윤여선 교수는 최근 5년간 강의평가 결과 상위 20위 내 진입 횟수가 10회에 이르는 등 탁월한 강의로 KAIST 학생 교육의 질적 향상 및 인재 양성에 기여한 점을 높이 평가받았다.
공적대상을 수상한 전기및전자공학부 김종환 교수는 세계 최초대회인 AI World Cup의 창시자로 2017년부터 매년 대회를 개최해 세계 각국의 연구자들에게 AI 기술력의 경쟁 무대를 제공하고, AI 기술을 대중화시키는 등 KAIST의 위상을 크게 제고한 것으로 평가받았다.
연구대상을 수상한 전기및전자공학부 심현철 교수는 최근 5년간 연구계약과 O/H 흡수실적, 지식재산권실적, Royalty 수입실적을 평가하는 연구상 부문에서 가장 높은 역량을 인정받았다.
사회봉사부문 우수교원 특별포상 대상을 수상한 전기및전자공학부 최성율 교수는 KAIST 소재·부품·장비 기술자문단 단장으로서 30여개 기업에 대한 자문을 통해 현장의 문제를 해결하는 등 국가의 위기극복과 미래혁신에 대한 성과를 인정받았다.
임형규 LINKGENESIS-Best Teacher Award 대상을 수상한 기계공학과 김성진 교수는 2012년부터 ‘연성 박막 초열전도체 개발’이라는 주제로 창의과제를 수행하는 등 창의적인 인재 양성에 크게 기여한 점을 높이 평가받았다.
이수영 교수학습혁신상 대상을 수상한 신소재공학과 홍승범 교수는 2017년부터 Flipped Learning 교과목의 설계 및 운영을 통해 창의적 수업방식을 실천하는 등의 탁월한 성과를 인정받았다.
제49주년 개교기념식에서 ‘2019년 올해의 KAIST인 상’ 등 총 45명 교원 시상
지난 7월 30일 열린 개교 49주년 기념식 행사에서 우리 대학은 물리학과 심흥선 교수를 '2019년 올해의 KAIST인'으로 선정해 시상했다.
'올해의 KAIST인 상'은 한 해 동안 국내·외에서 KAIST 발전을 위해 노력하고 학술 및 연구 실적이 탁월한 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
19번째 수상의 영예를 거머쥔 심흥선 교수는 2019년 한 해 동안 네이처(Nature)지에 물리학 난제인 콘도 스핀 구름의 존재를 세계 최초로 입증하는 연구성과를, 네이처 나노테크놀로지(Nature Nanotechnology)지에는 양자 기술의 핵심문제인 전자의 파동성 제어·관측을 위해 전자 파동의 피코초 진동 관측법을 발견하는 연구성과를 게재하는 등 KAIST의 위상을 크게 높였다는 평가를 받았다.
심흥선 교수는 "올해의 KAIST인 상을 수상하게 되어 영광이며, 이는 함께 연구하고 있는 학생들 덕분이며, 그들에게 고마움을 전한다. 자연에 대한 더 깊이 있는 이해를 얻기 위해 노력하겠다.”라고 소감을 밝혔다.
이 외에도 우리 대학은 교육, 학술, 연구, 국제협력 성과가 탁월하거나 KAIST의 위상에 크게 공헌한 총 32명의 교원에게 ‘개교기념 우수교원 포상 및 특별포상’을, 12명의 교원에게 '송암 미래 석학 우수연구상', '2019년 대표 연구성과 10선' 상 등을 수여했다.
주요 수상자는 다음과 같다.
학술대상을 수상한 기계공학과 김승우 교수는 현대 첨단 산업이 요구하는 초정밀 광학계측 기술의 선도적 개발을 주도했으며, 특히 첨단 광계측 기술 분야의 세계적 연구 결과를 창출하여 KAIST를 대표할 만한 탁월한 학술 연구업적을 낸 점을 높이 평가받았다.
창의강의대상을 수상한 전산학부 김주호 교수는 전산학에 인문학 지식을 결합한 CS+X 형태의 융합형 교과목을 개설해 사람을 위한 기술을 강조하는 등 학생 교육의 질적 향상에 크게 기여한 공로를 인정받았다.
우수강의대상을 수상한 경영공학부 윤여선 교수는 최근 5년간 강의평가 결과 상위 20위 내 진입 횟수가 10회에 이르는 등 탁월한 강의로 KAIST 학생 교육의 질적 향상 및 인재 양성에 기여한 점을 높이 평가받았다.
공적대상을 수상한 전기및전자공학부 김종환 교수는 세계 최초대회인 AI World Cup의 창시자로 2017년부터 매년 대회를 개최해 세계 각국의 연구자들에게 AI 기술력의 경쟁 무대를 제공하고, AI 기술을 대중화시키는 등 KAIST의 위상을 크게 제고한 것으로 평가받았다.
연구대상을 수상한 전기및전자공학부 심현철 교수는 최근 5년간 연구계약과 O/H 흡수실적, 지식재산권실적, Royalty 수입실적을 평가하는 연구상 부문에서 가장 높은 역량을 인정받았다.
사회봉사부문 우수교원 특별포상 대상을 수상한 전기및전자공학부 최성율 교수는 KAIST 소재·부품·장비 기술자문단 단장으로서 30여개 기업에 대한 자문을 통해 현장의 문제를 해결하는 등 국가의 위기극복과 미래혁신에 대한 성과를 인정받았다.
임형규 LINKGENESIS-Best Teacher Award 대상을 수상한 기계공학과 김성진 교수는 2012년부터 ‘연성 박막 초열전도체 개발’이라는 주제로 창의과제를 수행하는 등 창의적인 인재 양성에 크게 기여한 점을 높이 평가받았다.
이수영 교수학습혁신상 대상을 수상한 신소재공학과 홍승범 교수는 2017년부터 Flipped Learning 교과목의 설계 및 운영을 통해 창의적 수업방식을 실천하는 등의 탁월한 성과를 인정받았다.
2020.07.30
조회수 24776
-
 항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
2020.06.16
조회수 18413
-
 실시간 영상 전송 보안 기술 개발
전산학부 김명철 교수 연구팀이 웹캠, 영상 드론, CCTV, 증강현실(AR), 가상현실(VR) 등에 사용하는 영상 전송 장비용 실시간 영상 암호화 및 전산 자원(CPU, 배터리 등) 소모 저감 기술을 개발했다.
연구팀의 실시간 영상 전송 보안기술은 비디오 코덱 종류에 상관없이 적용될 수 있는 범용성을 가질 뿐 아니라 영상전송기기의 CPU나 배터리를 최대 50%까지 절약하면서도 최고 수준의 보안성능을 제공하는 결과를 보였다.
고경민 박사 주도로 개발된 이번 연구결과는 보안 분야의 국제 학술지 IEEE TDSC(Transactions on Dependable and Secure Computing) 3월 13일 자 온라인판에 게재됐다. (논문명: Secure video transmission framework for battery-powered video devices) 또한, 국내 특허로 등록, 미국특허로 출원돼 2차 심사가 진행 중이다. (국내특허명: 통신 시스템의 암호화 패킷 전송 방법)
기존 실시간 영상 전송 보안기술은 촬영한 모든 영상을 암호화해 전송하거나 비디오 데이터 식별 없이 무작위로 암호화하기 때문에 전산 자원이 제한된 상황에서 적용하기에는 한계가 있다. 문제 해결을 위해 연구팀은 새로운 실시간 영상 암호화 및 배터리 소모 저감 기술을 개발했다. 이 기술은 영상전송 장비에서 동작하는 자원 모니터링 결과에 따라 카메라로 촬영한 영상을 구성하는 비디오 데이터를 데이터중요도 관점에서 선별적으로 암호화 전송을 수행한다.
암호화 전송 시에는 영상 송신 장비의 가용자원량에 따라 실시간으로 암호화 정도를 조정하며, 다중 전송경로 지원을 통해 보안성을 높인다. 수신된 영상 데이터는 실시간 영상 재생이 가능한 단위로 그 순서를 복원한 후 화면에 표시된다. 이 기술은 가용 전산 자원의 모니터링 결과에 따라 촬영된 영상을 구성하는 비디오 데이터 단위로 암호화가 가능해 전산 자원 가용량에 따른 선별적 적용이 가능하다.
연구팀은 카메라 장비를 상용 영상 드론에 탑재해 무선을 통한 영상전송 시 전산 자원 소모를 낮추면서 보안성을 높일 수 있음을 증명했다. 최근 코로나로 인해 널리 활용되는 비대면 강의 및 미팅의 보안성 강화에 기여할 수 있을 것으로 기대된다.
김명철 교수는 “영상전송 보안이 중요한 온라인 교육/회의, 스마트시티의 CCTV, 민군 드론 영상 송수신, 증강현실(AR), 가상현실(VR) 등에서 특허화된 개발기술이 원천기술로 활용될 수 있도록 산학협력을 활발히 추진하고 있다”라고 말했다.
실시간 영상 전송 보안 기술 개발
전산학부 김명철 교수 연구팀이 웹캠, 영상 드론, CCTV, 증강현실(AR), 가상현실(VR) 등에 사용하는 영상 전송 장비용 실시간 영상 암호화 및 전산 자원(CPU, 배터리 등) 소모 저감 기술을 개발했다.
연구팀의 실시간 영상 전송 보안기술은 비디오 코덱 종류에 상관없이 적용될 수 있는 범용성을 가질 뿐 아니라 영상전송기기의 CPU나 배터리를 최대 50%까지 절약하면서도 최고 수준의 보안성능을 제공하는 결과를 보였다.
고경민 박사 주도로 개발된 이번 연구결과는 보안 분야의 국제 학술지 IEEE TDSC(Transactions on Dependable and Secure Computing) 3월 13일 자 온라인판에 게재됐다. (논문명: Secure video transmission framework for battery-powered video devices) 또한, 국내 특허로 등록, 미국특허로 출원돼 2차 심사가 진행 중이다. (국내특허명: 통신 시스템의 암호화 패킷 전송 방법)
기존 실시간 영상 전송 보안기술은 촬영한 모든 영상을 암호화해 전송하거나 비디오 데이터 식별 없이 무작위로 암호화하기 때문에 전산 자원이 제한된 상황에서 적용하기에는 한계가 있다. 문제 해결을 위해 연구팀은 새로운 실시간 영상 암호화 및 배터리 소모 저감 기술을 개발했다. 이 기술은 영상전송 장비에서 동작하는 자원 모니터링 결과에 따라 카메라로 촬영한 영상을 구성하는 비디오 데이터를 데이터중요도 관점에서 선별적으로 암호화 전송을 수행한다.
암호화 전송 시에는 영상 송신 장비의 가용자원량에 따라 실시간으로 암호화 정도를 조정하며, 다중 전송경로 지원을 통해 보안성을 높인다. 수신된 영상 데이터는 실시간 영상 재생이 가능한 단위로 그 순서를 복원한 후 화면에 표시된다. 이 기술은 가용 전산 자원의 모니터링 결과에 따라 촬영된 영상을 구성하는 비디오 데이터 단위로 암호화가 가능해 전산 자원 가용량에 따른 선별적 적용이 가능하다.
연구팀은 카메라 장비를 상용 영상 드론에 탑재해 무선을 통한 영상전송 시 전산 자원 소모를 낮추면서 보안성을 높일 수 있음을 증명했다. 최근 코로나로 인해 널리 활용되는 비대면 강의 및 미팅의 보안성 강화에 기여할 수 있을 것으로 기대된다.
김명철 교수는 “영상전송 보안이 중요한 온라인 교육/회의, 스마트시티의 CCTV, 민군 드론 영상 송수신, 증강현실(AR), 가상현실(VR) 등에서 특허화된 개발기술이 원천기술로 활용될 수 있도록 산학협력을 활발히 추진하고 있다”라고 말했다.
2020.04.16
조회수 8310
-
 배상민 교수, 독일 iF 어워드 패키지부문 본상 수상
우리 대학 산업디자인학과 배상민 교수 연구팀(ID+IM 디자인 연구소)이 ‘제주용암수’ 생수병 디자인으로 세계 최고권위 디자인 대회인 2020 독일 iF 디자인 어워드 패키지 디자인 부문 본상을 받았다.
독일 하노버전시센터(Hannover Exhibition Center)에서 주관하는 iF 디자인 어워드는 세계 3대 디자인 대회 중 하나로, 60개국 7천 점 이상의 작품이 출품된다. 수상한 ‘제주용암수 디자인’은 ㈜오리온 제주 용암수와 KAIST와의 산학 협력으로 이루어진 프리미엄 미네랄 생수 디자인 프로젝트이다. 배상민 교수팀이 디자인한 생수병은 제주도의 아름다운 자연을 모티브로 주상절리와 바다의 수평선을 형상화한 세로 선과 가로섬을 활용해 단순하면서도 감각적인 디자인을 완성했다.
나아가 이러한 병의 형태는 획기적으로 적은 양의 재료를 사용함에도, 일반적인 형태의 플라스틱병에 비해 약 4배 정도의 고압 하중을 견뎌낼 수 있는 효율적인 구조이기 때문에 심미적 영역뿐 아니라 기능적 영역에서도 뛰어난 우수성을 보인다. 병 라벨에는 물을 통해 투과돼 보이는 신비로운 한라산과 밤하늘에 빛나는 오리온 별자리를 담아 제주 한라산의 낮과 밤을 감성적으로 그려냄과 동시에 ㈜오리온의 브랜드를 상징화했다.
배상민 교수는 “ 먼저 학생들과 산학 프로젝트로 연구한 결과물을 상품화해 대량생산되고 그 결과가 국제적 디자인 대회에서 인정받아 기쁘다”라며 제조 및 유통 공정상 디자인에 제약이 많은 상황이었지만 구조 및 기능적인 부분에 대한 고안과 외형의 아름다움까지 표현하려 노력을 기울였다”라고 말했다.
배상민 교수, 독일 iF 어워드 패키지부문 본상 수상
우리 대학 산업디자인학과 배상민 교수 연구팀(ID+IM 디자인 연구소)이 ‘제주용암수’ 생수병 디자인으로 세계 최고권위 디자인 대회인 2020 독일 iF 디자인 어워드 패키지 디자인 부문 본상을 받았다.
독일 하노버전시센터(Hannover Exhibition Center)에서 주관하는 iF 디자인 어워드는 세계 3대 디자인 대회 중 하나로, 60개국 7천 점 이상의 작품이 출품된다. 수상한 ‘제주용암수 디자인’은 ㈜오리온 제주 용암수와 KAIST와의 산학 협력으로 이루어진 프리미엄 미네랄 생수 디자인 프로젝트이다. 배상민 교수팀이 디자인한 생수병은 제주도의 아름다운 자연을 모티브로 주상절리와 바다의 수평선을 형상화한 세로 선과 가로섬을 활용해 단순하면서도 감각적인 디자인을 완성했다.
나아가 이러한 병의 형태는 획기적으로 적은 양의 재료를 사용함에도, 일반적인 형태의 플라스틱병에 비해 약 4배 정도의 고압 하중을 견뎌낼 수 있는 효율적인 구조이기 때문에 심미적 영역뿐 아니라 기능적 영역에서도 뛰어난 우수성을 보인다. 병 라벨에는 물을 통해 투과돼 보이는 신비로운 한라산과 밤하늘에 빛나는 오리온 별자리를 담아 제주 한라산의 낮과 밤을 감성적으로 그려냄과 동시에 ㈜오리온의 브랜드를 상징화했다.
배상민 교수는 “ 먼저 학생들과 산학 프로젝트로 연구한 결과물을 상품화해 대량생산되고 그 결과가 국제적 디자인 대회에서 인정받아 기쁘다”라며 제조 및 유통 공정상 디자인에 제약이 많은 상황이었지만 구조 및 기능적인 부분에 대한 고안과 외형의 아름다움까지 표현하려 노력을 기울였다”라고 말했다.
2020.02.18
조회수 6665
-
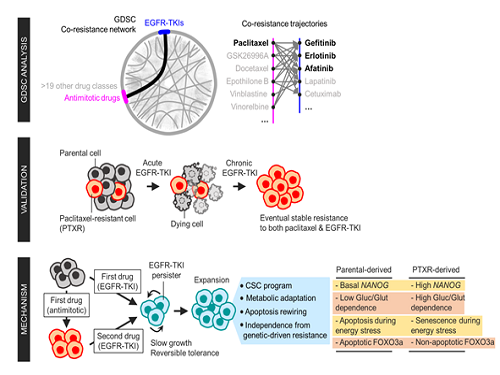 암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17
조회수 9068
-
 조광현 교수, 암세포를 정상세포로 되돌리는 초기 원천기술 개발
우리대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 대장암세포를 일반적인 정상 세포로 되돌리는 초기 원천기술을 개발하는 데 성공했다.
연구팀은 대장암세포와 정상 대장 세포의 유전자 조절 네트워크를 분석해 대장암세포를 정상 대장 세포로 변환하는데 필요한 핵심 인자를 규명하고, 이를 통해 암세포의 정상 세포화라는 새로운 치료 원리를 개발했다.
KAIST 이수범 연구원, 황채영, 김동산 박사, 한영현 박사과정, 서울삼성병원의 이찬수 박사, 홍성노 교수, 김석형 교수 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 ‘분자암연구(Molecular Cancer Research)’ 1월 2일 자 표지논문으로 게재됐으며, 하이라이트 특집 기사도 함께 출판됐다. (논문명: Network inference analysis identifies SETDB1 as a key regulator for reverting colorectal cancer cells into differentiated normal-like cells).
현재 항암치료로 가장 널리 사용되는 항암 화학요법은 빠르게 분열하는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 이 기술은 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 부작용을 일으킨다.
게다가 암세포들은 항암제에 본질적인 내성을 갖거나 새로운 내성을 갖게 돼 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 현재의 항암치료는 내성을 보이는 암세포를 없애기 위해 더 많은 정상 세포의 사멸을 감수해야만 하는 문제를 갖는다.
이를 극복하기 위해 암세포만을 특이적으로 없애는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽여야 하는 공통적인 조건 때문에 근본적인 한계를 가진다.
문제 해결을 위해 연구팀은 암세포를 정상 세포로 변환하는 새로운 방식의의 치료전략을 제안했다. 암세포가 정상 세포로 변환되는 현상은 20세기 초부터 간혹 관찰됐지만, 그 원리가 연구되지 않았으며 또한 이를 인위적으로 제어하는 기술도 연구된 바 없었다.
1907년 스위스 병리학자 막스 아스카나지(Max Askanazy)가 난소의 기형종(테라토마)이 정상 세포로 분화되는 현상을 발견한 이래로 다양한 암종에서 정상 세포로 변화되는 현상들이 산발적으로 보고됐고, 이러한 보고에서는 암세포가 돌연변이를 지닌 상태에서 주변 미세환경의 변화나 특정 자극 때문에 정상 세포의 상태로 되돌아가는 현상만이 관찰됐다.
조 교수 연구팀은 시스템생물학 연구방법을 통해 대장암세포를 정상 대장 세포로 변환할 수 있는 핵심조절인자를 탐구했고, 그 결과 다섯 개의 핵심전사인자(CDX2, ELF3, HNF4G, PPARG, VDR)와 이들의 전사 활성도를 억제하고 있는 후성유전학적 조절인자인 SETDB1을 발견했다.
연구팀은 이번 연구를 통해 SETDB1을 억제함으로써 암세포를 효과적으로 정상 세포로 변환할 수 있음을 분자세포실험을 통해 증명했다. 대장암세포에서 SETDB1을 억제했을 때 세포가 분열을 중지하고 정상 대장 세포의 유전자 발현패턴을 회복하는 것을 확인했다.
이번 연구에 따르면 암세포에서는 암 특이적으로 활성화된 후성유전학적 조절인자 SETDB1이 정상 세포의 핵심전사인자를 억제해 암세포가 정상 세포로 변환하는 것을 차단하고 있는 것으로 밝혀졌다. 즉, SETDB1을 조절함으로써 다시 원래의 정상 세포 상태로 되돌릴 수 있음을 증명한 것이다.
조 교수 연구팀은 서울삼성병원과의 협동 연구를 통해 SETDB1이 높게 발현되는 대장암세포를 가진 환자들에게서 더 안 좋은 예후가 나타남을 확인했으며, 환자 유래 대장암 오가노이드(3차원으로 배양한 장기유사체)에서 SETDB1의 발현을 억제했을 때 다시 정상 세포와 같은 형태로 변화함을 관찰했다.
이번 연구에서 찾아낸 타겟 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 전임상실험을 통해 암세포의 정상 세포화라는 새로운 치료 기술이 본격적으로 실현될 수 있을 것으로 보인다.
이러한 새로운 개념의 치료전략이 적용된다면 현재 항암치료의 많은 부작용과 내성 발생을 모두 최소화함으로써 환자의 고통을 완화해 삶의 질을 크게 높일 수 있을 것으로 기대된다.
조 교수는 “그동안 암은 유전자 변이 축적에 의한 현상이므로 되돌릴 수 없다고 여겨졌으나 이를 되돌릴 가능성을 보여줬다”라며 “이번 연구는 암을 당뇨나 고혈압과 같은 만성질환으로서 잘 관리하면서 삶의 질을 유지할 수 있도록 하는 새로운 항암치료의 서막을 열었다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, KAIST Grand Challenge 30 사업의 지원으로 수행됐다.
□ 그림 설명
조광현 교수 연구팀은 SETDB1 단백질이 대장암세포가 정상대장세포로 분화하는 것을 차단하는 후성유전학적 장애물을 형성하고 있다는 사실을 밝히고 이를 억제함으로써 대장암세포를 정상대장세포로 효과적으로 분화시킬 수 있음을 증명하였다.
□ 분자암연구 표지 이미지
조광현 교수, 암세포를 정상세포로 되돌리는 초기 원천기술 개발
우리대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 대장암세포를 일반적인 정상 세포로 되돌리는 초기 원천기술을 개발하는 데 성공했다.
연구팀은 대장암세포와 정상 대장 세포의 유전자 조절 네트워크를 분석해 대장암세포를 정상 대장 세포로 변환하는데 필요한 핵심 인자를 규명하고, 이를 통해 암세포의 정상 세포화라는 새로운 치료 원리를 개발했다.
KAIST 이수범 연구원, 황채영, 김동산 박사, 한영현 박사과정, 서울삼성병원의 이찬수 박사, 홍성노 교수, 김석형 교수 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 ‘분자암연구(Molecular Cancer Research)’ 1월 2일 자 표지논문으로 게재됐으며, 하이라이트 특집 기사도 함께 출판됐다. (논문명: Network inference analysis identifies SETDB1 as a key regulator for reverting colorectal cancer cells into differentiated normal-like cells).
현재 항암치료로 가장 널리 사용되는 항암 화학요법은 빠르게 분열하는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 이 기술은 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 부작용을 일으킨다.
게다가 암세포들은 항암제에 본질적인 내성을 갖거나 새로운 내성을 갖게 돼 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 현재의 항암치료는 내성을 보이는 암세포를 없애기 위해 더 많은 정상 세포의 사멸을 감수해야만 하는 문제를 갖는다.
이를 극복하기 위해 암세포만을 특이적으로 없애는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽여야 하는 공통적인 조건 때문에 근본적인 한계를 가진다.
문제 해결을 위해 연구팀은 암세포를 정상 세포로 변환하는 새로운 방식의의 치료전략을 제안했다. 암세포가 정상 세포로 변환되는 현상은 20세기 초부터 간혹 관찰됐지만, 그 원리가 연구되지 않았으며 또한 이를 인위적으로 제어하는 기술도 연구된 바 없었다.
1907년 스위스 병리학자 막스 아스카나지(Max Askanazy)가 난소의 기형종(테라토마)이 정상 세포로 분화되는 현상을 발견한 이래로 다양한 암종에서 정상 세포로 변화되는 현상들이 산발적으로 보고됐고, 이러한 보고에서는 암세포가 돌연변이를 지닌 상태에서 주변 미세환경의 변화나 특정 자극 때문에 정상 세포의 상태로 되돌아가는 현상만이 관찰됐다.
조 교수 연구팀은 시스템생물학 연구방법을 통해 대장암세포를 정상 대장 세포로 변환할 수 있는 핵심조절인자를 탐구했고, 그 결과 다섯 개의 핵심전사인자(CDX2, ELF3, HNF4G, PPARG, VDR)와 이들의 전사 활성도를 억제하고 있는 후성유전학적 조절인자인 SETDB1을 발견했다.
연구팀은 이번 연구를 통해 SETDB1을 억제함으로써 암세포를 효과적으로 정상 세포로 변환할 수 있음을 분자세포실험을 통해 증명했다. 대장암세포에서 SETDB1을 억제했을 때 세포가 분열을 중지하고 정상 대장 세포의 유전자 발현패턴을 회복하는 것을 확인했다.
이번 연구에 따르면 암세포에서는 암 특이적으로 활성화된 후성유전학적 조절인자 SETDB1이 정상 세포의 핵심전사인자를 억제해 암세포가 정상 세포로 변환하는 것을 차단하고 있는 것으로 밝혀졌다. 즉, SETDB1을 조절함으로써 다시 원래의 정상 세포 상태로 되돌릴 수 있음을 증명한 것이다.
조 교수 연구팀은 서울삼성병원과의 협동 연구를 통해 SETDB1이 높게 발현되는 대장암세포를 가진 환자들에게서 더 안 좋은 예후가 나타남을 확인했으며, 환자 유래 대장암 오가노이드(3차원으로 배양한 장기유사체)에서 SETDB1의 발현을 억제했을 때 다시 정상 세포와 같은 형태로 변화함을 관찰했다.
이번 연구에서 찾아낸 타겟 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 전임상실험을 통해 암세포의 정상 세포화라는 새로운 치료 기술이 본격적으로 실현될 수 있을 것으로 보인다.
이러한 새로운 개념의 치료전략이 적용된다면 현재 항암치료의 많은 부작용과 내성 발생을 모두 최소화함으로써 환자의 고통을 완화해 삶의 질을 크게 높일 수 있을 것으로 기대된다.
조 교수는 “그동안 암은 유전자 변이 축적에 의한 현상이므로 되돌릴 수 없다고 여겨졌으나 이를 되돌릴 가능성을 보여줬다”라며 “이번 연구는 암을 당뇨나 고혈압과 같은 만성질환으로서 잘 관리하면서 삶의 질을 유지할 수 있도록 하는 새로운 항암치료의 서막을 열었다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, KAIST Grand Challenge 30 사업의 지원으로 수행됐다.
□ 그림 설명
조광현 교수 연구팀은 SETDB1 단백질이 대장암세포가 정상대장세포로 분화하는 것을 차단하는 후성유전학적 장애물을 형성하고 있다는 사실을 밝히고 이를 억제함으로써 대장암세포를 정상대장세포로 효과적으로 분화시킬 수 있음을 증명하였다.
□ 분자암연구 표지 이미지
2020.01.09
조회수 14843
-
 정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
2019.09.24
조회수 8347
-
 정보보호대학원, 독일 정보보안센터(CISPA)와 MOU 체결
우리 대학 정보보호대학원(책임교수 신인식)이 지난 8월 28일 독일 자르브뤼켄에서 독일 정보보안센터(CISPA(Helmholtz Center for Information Security)) 및 KIST 유럽연구소와 함께 정보보호 관련 협력과 공동 목표에 관한 MOU를 체결했다.
KAIST는 국내 대학 최초로 체결한 이번 협약을 통해 CISPA와 KIST 유럽과 함께 ▲ 공동 프로젝트 추진 ▲ 시스템 보안, 웹 보안, 암호학 등 분야 관련 협력 ▲ KIST 유럽의 테스트베드 플랫폼 공동사용 등 다양한 분야에서 협력할 예정이다.
KAIST와 협력하게 될 독일의 CISPA는 연간 5300만 유로의 예산이 투입되는 독일 최대 연구기관인 헬름홀츠(Helmholtz) 연구협회 연구센터로 지난 2018년 선정됐다. CISPA는 협회 최초로 IT분야를 수행하는 대형연구센터로 출범했으며 2026년까지 최소 500명~800명의 연구 인력을 보유한 대형 연구센터로 발돋움할 계획이다.
CISPA는 최근 4년 동안 정보보호 분야의 TOP 4 국제학회에서 세계 최고의 연구 실적을 올렸으며(csrankings.org 기준 세계 1위), 매년 500억 원(원화 기준)이 넘는 연구비를 헬름홀츠 연구협회에서 지원을 받고 있다.
28일(현지시각)에는 MOU 행사와 더불어 독일 대사관에서 한독 사이버 보안 세미나가 개최되어 세계 최고 수준의 보안 분야 기술을 소개하는 시간이 마련됐다. 특히, `데이터 보호, 웹 보안, 시스템 보안을 위한 연구자들 워크숍'에서는 신인식, 강병훈, 손수엘 교수 등이 KAIST를 대표해 각각 시스템 보안 및 웹 보안 내용을 발표했으며, CISPA와 공동 협업 주제를 구체화했다.
신인식 정보보호 대학원 책임 교수는 "이번 MOU 참여 기관들과 공동 프로젝트, 세미나 및 인턴십 등을 추진해 공동 기술개발, 인력양성 및 산학협력 등에 이바지해 세계 최고 수준의 대학원으로 거듭 발전할 계획ˮ이라고 밝혔다.
이날 행사에는 KAIST 정보보호대학원 신인식 책임교수, CISPA 마이클 벡키스 소장, 김준경 KIST 유럽연구소장 등이 참석해서 MOU에 서명했다.
정보보호대학원, 독일 정보보안센터(CISPA)와 MOU 체결
우리 대학 정보보호대학원(책임교수 신인식)이 지난 8월 28일 독일 자르브뤼켄에서 독일 정보보안센터(CISPA(Helmholtz Center for Information Security)) 및 KIST 유럽연구소와 함께 정보보호 관련 협력과 공동 목표에 관한 MOU를 체결했다.
KAIST는 국내 대학 최초로 체결한 이번 협약을 통해 CISPA와 KIST 유럽과 함께 ▲ 공동 프로젝트 추진 ▲ 시스템 보안, 웹 보안, 암호학 등 분야 관련 협력 ▲ KIST 유럽의 테스트베드 플랫폼 공동사용 등 다양한 분야에서 협력할 예정이다.
KAIST와 협력하게 될 독일의 CISPA는 연간 5300만 유로의 예산이 투입되는 독일 최대 연구기관인 헬름홀츠(Helmholtz) 연구협회 연구센터로 지난 2018년 선정됐다. CISPA는 협회 최초로 IT분야를 수행하는 대형연구센터로 출범했으며 2026년까지 최소 500명~800명의 연구 인력을 보유한 대형 연구센터로 발돋움할 계획이다.
CISPA는 최근 4년 동안 정보보호 분야의 TOP 4 국제학회에서 세계 최고의 연구 실적을 올렸으며(csrankings.org 기준 세계 1위), 매년 500억 원(원화 기준)이 넘는 연구비를 헬름홀츠 연구협회에서 지원을 받고 있다.
28일(현지시각)에는 MOU 행사와 더불어 독일 대사관에서 한독 사이버 보안 세미나가 개최되어 세계 최고 수준의 보안 분야 기술을 소개하는 시간이 마련됐다. 특히, `데이터 보호, 웹 보안, 시스템 보안을 위한 연구자들 워크숍'에서는 신인식, 강병훈, 손수엘 교수 등이 KAIST를 대표해 각각 시스템 보안 및 웹 보안 내용을 발표했으며, CISPA와 공동 협업 주제를 구체화했다.
신인식 정보보호 대학원 책임 교수는 "이번 MOU 참여 기관들과 공동 프로젝트, 세미나 및 인턴십 등을 추진해 공동 기술개발, 인력양성 및 산학협력 등에 이바지해 세계 최고 수준의 대학원으로 거듭 발전할 계획ˮ이라고 밝혔다.
이날 행사에는 KAIST 정보보호대학원 신인식 책임교수, CISPA 마이클 벡키스 소장, 김준경 KIST 유럽연구소장 등이 참석해서 MOU에 서명했다.
2019.09.09
조회수 7984
-
 김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
2019.08.01
조회수 11528
 신소재공학과 염지현, 기계공학과 심기동 교수, 포스코사이언스펠로우 선정
우리 대학 신소재공학과 염지현, 기계공학과 심기동 교수가 포스코청암재단에서 선정하는 제12기 '포스코사이언스펠로우'로 선발됐다고 2020년 9월 7일 발표됐다.
포스코사이언스펠로우십은 2009년에 시작해 대한민국의 미래를 이끌어 갈 과학기술 인재양성을 목표로 매년 기초과학 및 응용과학을 연구하는 유능한 신진교수를 선발하고 있다. 이는 독자적인 연구와 실험을 시작하는 신진교수에게 2년간 총 1억원을 지원하는 명예로운 사업이다. 올해 신진교수 166명이 지원해 8:1이 넘는 치열한 경쟁률 속에서 수상한 만큼 그 의미가 더 깊다.
염지현 교수는 우리 대학 신소재공학과 학사과정을 졸업한 후 미시간대학교에서 박사학위를, MIT에서 포스닥을 하는 동안 Overberger Research Award 등 20개 가까이되는 명예로운 상들을 수상한 실적을 보유하고 있다. 더불어 조교수로 신소재공학과에 부임한지 불과 6개월만에 포스코사이언스펠로쉽을 수상하는 쾌거도 이루었다.
심기동 교수는 우리 대학 기계공학과에서 2012년도 박사 학위를 받고, 하버드 대학교 포스닥 펠로우, 존스홉킨스 대학교 Research Scientist를 거쳐 2018년 2월에 KAIST 조교수로 부임하였다. 현재 iCaRE(in-situ Characterization and Reliability Evaluation) 연구실 학생들과 재료의 기계적 거동을 다양한 length-scale 및 환경 조건에서 이해하기 위한 연구를 진행하고 있다.
염지현, 심기동 교수는 내년 1월부터 2년간 지원을 받을 예정이다.
2020.09.16 조회수 22682
신소재공학과 염지현, 기계공학과 심기동 교수, 포스코사이언스펠로우 선정
우리 대학 신소재공학과 염지현, 기계공학과 심기동 교수가 포스코청암재단에서 선정하는 제12기 '포스코사이언스펠로우'로 선발됐다고 2020년 9월 7일 발표됐다.
포스코사이언스펠로우십은 2009년에 시작해 대한민국의 미래를 이끌어 갈 과학기술 인재양성을 목표로 매년 기초과학 및 응용과학을 연구하는 유능한 신진교수를 선발하고 있다. 이는 독자적인 연구와 실험을 시작하는 신진교수에게 2년간 총 1억원을 지원하는 명예로운 사업이다. 올해 신진교수 166명이 지원해 8:1이 넘는 치열한 경쟁률 속에서 수상한 만큼 그 의미가 더 깊다.
염지현 교수는 우리 대학 신소재공학과 학사과정을 졸업한 후 미시간대학교에서 박사학위를, MIT에서 포스닥을 하는 동안 Overberger Research Award 등 20개 가까이되는 명예로운 상들을 수상한 실적을 보유하고 있다. 더불어 조교수로 신소재공학과에 부임한지 불과 6개월만에 포스코사이언스펠로쉽을 수상하는 쾌거도 이루었다.
심기동 교수는 우리 대학 기계공학과에서 2012년도 박사 학위를 받고, 하버드 대학교 포스닥 펠로우, 존스홉킨스 대학교 Research Scientist를 거쳐 2018년 2월에 KAIST 조교수로 부임하였다. 현재 iCaRE(in-situ Characterization and Reliability Evaluation) 연구실 학생들과 재료의 기계적 거동을 다양한 length-scale 및 환경 조건에서 이해하기 위한 연구를 진행하고 있다.
염지현, 심기동 교수는 내년 1월부터 2년간 지원을 받을 예정이다.
2020.09.16 조회수 22682 에티오피아 장관, KAIST서 4년 연구 끝에 박사학위 취득
올해 지천명(知天命·50세)의 나이를 맞은 에티오피아의 현직 장관이 우리 대학에서 박사학위를 취득해 화제가 되고 있다. 기술경영학부 글로벌IT기술대학원에서 지난 8월 박사학위를 취득한 메쿠리아 테클레마리암(Mekuria Teklemariam) 에티오피아 국무총리자문 장관이 그 주인공이다.
메쿠리아 장관은 2016년 9월 KAIST에서 박사과정 첫 학기를 시작한 지 4년만인 지난 8월 경영학박사 학위를 취득했다.
메쿠리아 장관은 "한국은 지난 수십 년간 정치·경제를 포함한 모든 분야에서 눈부신 발전을 이뤄낸 나라ˮ라면서 "에티오피아의 발전을 위해 성공사례를 보유한 국가의 성장 원동력을 학문적으로 연구해보고 싶었다ˮ라고 유학 배경을 밝혔다.
40세에 도시개발주택부 장관으로 취임해 에티오피아 역사상 최연소 장관이라는 기록을 세운 메쿠리아 장관은 6년의 재임 기간에 신도시·스마트시티 개발, 토지관리, 주택개발 등의 정책을 수립하고 집행하며 에티오피아의 경제 개발을 이끌어왔다.
그러나 그는 자신의 행보에 만족하지 못했다. 외적으로는 여러 가지 성취를 거뒀지만 비슷한 일들을 거듭하다 보니 행정가가 지녀야 할 능력이 정체된다는 고민이 커졌기 때문이다.
학업에 대한 결심을 굳힌 뒤 정부에 사임 의사를 밝혔지만, 국무총리는 현직에 남아 달라고 당부하며 한 가지를 물어왔다. '유학 가려는 이유가 개인의 이력을 위한 것인지 나라를 위한 것인지'를 확인하는 질문이었다.
국무총리의 말은 메쿠리아 장관의 한국행을 결심하는 계기가 됐다. 영국의 개방대학이나 미국 MIT의 최고위 과정을 선택하면 비교적 짧은 시간을 투자해 수월하게 공부할 수 있다는 장점이 있었다. 그러나 최빈국에서 강대국으로 성장한 한국의 사례를 연구하는 것이야말로 자국 발전에 기여하고 싶다는 목적에 가장 부합하는 선택이라고 결론 내린 것이다.
이후, 메쿠리아 장관은 KAIST에 지원했다. 과학기술 분야의 전문성, 탁월한 연구성과, 국제화에 특화된 대학원 과정 등 모든 면에서 학업을 이어가기 가장 좋은 환경이 마련돼 있었기 때문이다.
6개월여의 준비 끝에 2015년 KAIST 대학원에 합격했지만 메쿠리아 장관은 한국 땅을 밟지 못했다. 사임 의사가 또다시 반려된 탓이었다. 그러나 그는 포기하지 않았다. 일단 휴학을 신청한 뒤 지도교수인 기술경영학부 권영선 교수와 함께 계속해서 정부를 설득해나갔다.
메쿠리아 장관의 의지를 확인한 에티오피아 정부는 9인으로 구성된 위원회를 열어 그의 유학에 관한 투표를 진행했다. 다수의 위원이 국가 발전을 위해 학업을 선택한 그의 결정에 지지를 보냈고 도시개발주택부 장관에서 국무총리자문 장관으로 직위를 변경한 끝에 유학길에 오를 수 있었다.
2016년 가을부터 한국 생활을 시작한 메쿠리아 장관은 지난 4년간 학업에 매진했다. 정보격차 해소가 경제성장과 부패통제에 미치는 영향·개발도상국의 초고속인터넷 보급 및 확산정책 등의 주제를 연구해 국내외 학회에서 발표했다.
특히, 정보통신산업진흥원(NIPA)·과학기술정책연구원(STEPI) 등과의 협업 연구를 진행해 글로벌IT기술대학원에서 수여하는 우수 협력연구상을 2018년에 두 차례 수상했다. 또한, 졸업논문 연구로 수행한 '단계별 맞춤형 모바일 초고속인터넷 확산 정책'에 관한 논문은 정보통신 분야의 최우수 국제학술지에 속하는 SSCI 저널인 텔레커뮤니케이션즈 폴리시(Telecommunications Policy)에 지난 8월 졸업에 앞서 게재됐다.
광대역 통신망을 갖춘 국가들의 효과적인 정보통신 정책을 분석해 개발도상국에 맞춤형 정책을 제안하는 계량적 정책 연구를 성공적으로 완수한 결과다.
이런 성과들을 바탕으로 메쿠리아 장관은 글로벌IT기술대학원의 최우수 졸업생이란 영예와 함께 지난달 13일 박사학위를 취득했다.
"내 결정이 옳았다. 기대한 것보다 더 많이 배우고 간다ˮ고 소감을 밝힌 메쿠리아 장관은 "학업은 물론 주변 사람들과의 관계 속에서 얻는 가치들로 인해 더없이 즐겁고 행복한 시간이었다ˮ라고 말했다.
지난달 18일 신성철 총장을 접견한 메쿠리아 장관은 "지난 4년간 직접 경험한 KAIST의 연구·행정·산학협력 등을 벤치마킹해 에티오피아 과학기술대학의 경쟁력 향상에 일조하고 싶다ˮ는 뜻을 전달했다. 신 총장은 "국가 발전에 기여한 KAIST의 지식과 경험이 에티오피아 과학기술원 혁신과 양국의 교류 확대를 위해 유용하게 활용될 수 있는 협력 방안을 모색하자ˮ고 화답했다.
에티오피아에 적용해보고 싶은 한국의 정책 사례로 새마을 운동, 누구나 손쉽게 인터넷에 접근할 수 있는 인프라 구축, 장년층을 대상으로 하는 IT 활용기술 교육프로그램 등을 꼽은 메쿠리아 장관은 오는 12일 본국으로 돌아간다.
그는 "어느 자리에 있든 자신의 몫을 다 하기 위해 노력하는 것은 물론 말에서 그치는 것이 아니라 행동으로 실천하고 한국인들의 모습을 인상 깊게 지켜봤다ˮ라고 전하며 "한국과 KAIST에서 배운 것들을 에티오피아에 적용하고 실천하겠다ˮ라고 밝혔다.
2020.09.08 조회수 21206
에티오피아 장관, KAIST서 4년 연구 끝에 박사학위 취득
올해 지천명(知天命·50세)의 나이를 맞은 에티오피아의 현직 장관이 우리 대학에서 박사학위를 취득해 화제가 되고 있다. 기술경영학부 글로벌IT기술대학원에서 지난 8월 박사학위를 취득한 메쿠리아 테클레마리암(Mekuria Teklemariam) 에티오피아 국무총리자문 장관이 그 주인공이다.
메쿠리아 장관은 2016년 9월 KAIST에서 박사과정 첫 학기를 시작한 지 4년만인 지난 8월 경영학박사 학위를 취득했다.
메쿠리아 장관은 "한국은 지난 수십 년간 정치·경제를 포함한 모든 분야에서 눈부신 발전을 이뤄낸 나라ˮ라면서 "에티오피아의 발전을 위해 성공사례를 보유한 국가의 성장 원동력을 학문적으로 연구해보고 싶었다ˮ라고 유학 배경을 밝혔다.
40세에 도시개발주택부 장관으로 취임해 에티오피아 역사상 최연소 장관이라는 기록을 세운 메쿠리아 장관은 6년의 재임 기간에 신도시·스마트시티 개발, 토지관리, 주택개발 등의 정책을 수립하고 집행하며 에티오피아의 경제 개발을 이끌어왔다.
그러나 그는 자신의 행보에 만족하지 못했다. 외적으로는 여러 가지 성취를 거뒀지만 비슷한 일들을 거듭하다 보니 행정가가 지녀야 할 능력이 정체된다는 고민이 커졌기 때문이다.
학업에 대한 결심을 굳힌 뒤 정부에 사임 의사를 밝혔지만, 국무총리는 현직에 남아 달라고 당부하며 한 가지를 물어왔다. '유학 가려는 이유가 개인의 이력을 위한 것인지 나라를 위한 것인지'를 확인하는 질문이었다.
국무총리의 말은 메쿠리아 장관의 한국행을 결심하는 계기가 됐다. 영국의 개방대학이나 미국 MIT의 최고위 과정을 선택하면 비교적 짧은 시간을 투자해 수월하게 공부할 수 있다는 장점이 있었다. 그러나 최빈국에서 강대국으로 성장한 한국의 사례를 연구하는 것이야말로 자국 발전에 기여하고 싶다는 목적에 가장 부합하는 선택이라고 결론 내린 것이다.
이후, 메쿠리아 장관은 KAIST에 지원했다. 과학기술 분야의 전문성, 탁월한 연구성과, 국제화에 특화된 대학원 과정 등 모든 면에서 학업을 이어가기 가장 좋은 환경이 마련돼 있었기 때문이다.
6개월여의 준비 끝에 2015년 KAIST 대학원에 합격했지만 메쿠리아 장관은 한국 땅을 밟지 못했다. 사임 의사가 또다시 반려된 탓이었다. 그러나 그는 포기하지 않았다. 일단 휴학을 신청한 뒤 지도교수인 기술경영학부 권영선 교수와 함께 계속해서 정부를 설득해나갔다.
메쿠리아 장관의 의지를 확인한 에티오피아 정부는 9인으로 구성된 위원회를 열어 그의 유학에 관한 투표를 진행했다. 다수의 위원이 국가 발전을 위해 학업을 선택한 그의 결정에 지지를 보냈고 도시개발주택부 장관에서 국무총리자문 장관으로 직위를 변경한 끝에 유학길에 오를 수 있었다.
2016년 가을부터 한국 생활을 시작한 메쿠리아 장관은 지난 4년간 학업에 매진했다. 정보격차 해소가 경제성장과 부패통제에 미치는 영향·개발도상국의 초고속인터넷 보급 및 확산정책 등의 주제를 연구해 국내외 학회에서 발표했다.
특히, 정보통신산업진흥원(NIPA)·과학기술정책연구원(STEPI) 등과의 협업 연구를 진행해 글로벌IT기술대학원에서 수여하는 우수 협력연구상을 2018년에 두 차례 수상했다. 또한, 졸업논문 연구로 수행한 '단계별 맞춤형 모바일 초고속인터넷 확산 정책'에 관한 논문은 정보통신 분야의 최우수 국제학술지에 속하는 SSCI 저널인 텔레커뮤니케이션즈 폴리시(Telecommunications Policy)에 지난 8월 졸업에 앞서 게재됐다.
광대역 통신망을 갖춘 국가들의 효과적인 정보통신 정책을 분석해 개발도상국에 맞춤형 정책을 제안하는 계량적 정책 연구를 성공적으로 완수한 결과다.
이런 성과들을 바탕으로 메쿠리아 장관은 글로벌IT기술대학원의 최우수 졸업생이란 영예와 함께 지난달 13일 박사학위를 취득했다.
"내 결정이 옳았다. 기대한 것보다 더 많이 배우고 간다ˮ고 소감을 밝힌 메쿠리아 장관은 "학업은 물론 주변 사람들과의 관계 속에서 얻는 가치들로 인해 더없이 즐겁고 행복한 시간이었다ˮ라고 말했다.
지난달 18일 신성철 총장을 접견한 메쿠리아 장관은 "지난 4년간 직접 경험한 KAIST의 연구·행정·산학협력 등을 벤치마킹해 에티오피아 과학기술대학의 경쟁력 향상에 일조하고 싶다ˮ는 뜻을 전달했다. 신 총장은 "국가 발전에 기여한 KAIST의 지식과 경험이 에티오피아 과학기술원 혁신과 양국의 교류 확대를 위해 유용하게 활용될 수 있는 협력 방안을 모색하자ˮ고 화답했다.
에티오피아에 적용해보고 싶은 한국의 정책 사례로 새마을 운동, 누구나 손쉽게 인터넷에 접근할 수 있는 인프라 구축, 장년층을 대상으로 하는 IT 활용기술 교육프로그램 등을 꼽은 메쿠리아 장관은 오는 12일 본국으로 돌아간다.
그는 "어느 자리에 있든 자신의 몫을 다 하기 위해 노력하는 것은 물론 말에서 그치는 것이 아니라 행동으로 실천하고 한국인들의 모습을 인상 깊게 지켜봤다ˮ라고 전하며 "한국과 KAIST에서 배운 것들을 에티오피아에 적용하고 실천하겠다ˮ라고 밝혔다.
2020.09.08 조회수 21206 항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25 조회수 26128
항암제 표적 단백질을 약물 전달체로 쓴다?
우리 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 항암제를 이용한 암 치료에 새로운 가능성이 열릴 전망이다.
우리 대학 생명과학과 김진주 박사·바이오및뇌공학과 이준철 박사과정 학생이 공동 제1 저자로 그리고 생명과학과 전상용·바이오및뇌공학과 최명철 교수가 공동 교신저자로 참여한 이번 연구결과는 국제학술지 ‘어드밴스드 머티리얼스(Advanced Materials, IF=27.4)’ 8월 20일 字 표지논문으로 게재됐다. (논문명: Tubulin-based Nanotubes as Delivery Platform for Microtubule-Targeting Agents)
우리 몸속 세포가 분열할 때 염색체*들은 세포 한가운데에 정렬해 두 개의 딸세포로 나눠지는데 이 염색체들을 끌어당기는 끈이 바로 `미세소관(microtubule)'이다. 미세소관은 `튜불린(tubulin)' 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
☞ 염색체(Chromosome): DNA와 단백질이 응축하여 만드는 막대 형태의 구조체로 생명체의 모든 유전 정보를 지니고 있다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제(microtubule-targeting agents)’는 임상에서 다양한 암의 치료에 활용되고 있다. 이들은 암세포 미세소관에 결합해 앞서 언급한 끈 역할을 방해함으로써, 암세포의 분열을 억제, 결국 사멸을 유도한다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리(binding site)가 여럿 존재한다. 연구진은 이 점에 착안해 표적 물질인 튜불린 단백질을 약물 전달체로 사용한다는 획기적인 아이디어를 세계 최초로 구현했다. 공동연구팀은 튜불린 나노 튜브(Tubulin-based NanoTube), 약자로 TNT로 명명한 전달체를 개발하고 항암 효능을 실험으로 확인한 것이다. TNT라는 이름에는 암 치료를 위한 폭발물이라는 의미도 담고 있다.
미세소관 표적 치료제는 TNT에 자발적으로 탑재된다. 약물 입장에서는 세포 내 미세소관에 결합하는 것과 다를 바가 없기 때문이다. 이는 항암제마다 적합한 전달체를 찾아야 했던 기존의 어려움을 해소해준다. 즉 TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 잠재력을 가진‘만능 전달체’인 셈이다.
연구진은 먼저 튜불린 단백질에 블록 혼성 중합체*인 PEG-PLL(pegylated poly-L-lysine)을 섞어 기본적인 TNT 구조를 만들었다. 여기서 튜불린은 빌딩 블록, PEG-PLL은 이들을 붙여주는 접착제이다. 그 다음, 도세탁셀(docetaxel), 라우리말라이드(laulimalide), 그리고 모노메틸아우리스타틴 E(monomethyl auristatin E) 3종의 약물이 TNT에 탑재됨을 보였다. 이 약물들은 실제 유방암, 두경부암, 위암, 방광암 등의 화학요법에 활용되고 있는 항암제들이다.
☞ 블록 혼성 중합체(Block copolymer): 두 종류 이상의 단위체로 이루어진 고분자 화합물로, 각 단위체들이 길게 반복되는 특징이 있다.
연구팀은 또 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 사실을 밝혀냈다. 이는 TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는‘적응형 전달체’임을 보여주고 있다.
연구팀은 특히 항암제가 탑재된 TNT가 엔도좀-리소좀 경로(endo-lysosomal pathway)로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보인다는 점을 세포 및 동물을 대상으로 한 실험을 통해 확인했다.
적응형 만능 약물 전달체가 성공적으로 구현이 가능했던 배경에는 연구진이 보유한 튜불린 분자 제어 기술력 때문이다. 연구진은 튜불린 단백질을 일종의 레고 블록으로 보았다. 블록의 형태를 변형하고 쌓아 올리는 방식을 제어하여, 튜브 형태의 구조체를 조립하는 노하우를 축적해왔다. 연구팀은 이번 연구에서 포항 방사광 가속기의 소각 X-선 산란 장치를 이용해 TNT 구조를 나노미터(nm, 10억 분의 1미터) 이하의 정확도로 분석했다.
공동연구팀은 "이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다ˮ고 밝혔다. 연구팀은 이어 "TNT는 현재까지 개발된, 또 향후 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며, 다양한 항암제들의 시너지 효과(synergy effect)를 기대할 수 있는 `플랫폼 전달체'가 될 것ˮ이라고 강조했다.
이번 연구는 한국연구재단 (중견연구, 리더연구, 방사선기술, 바이오의료기술개발사업) 한국원자력연구원, KUSTAR-KAIST의 지원으로 수행됐다.
2020.08.25 조회수 26128 제49주년 개교기념식에서 ‘2019년 올해의 KAIST인 상’ 등 총 45명 교원 시상
지난 7월 30일 열린 개교 49주년 기념식 행사에서 우리 대학은 물리학과 심흥선 교수를 '2019년 올해의 KAIST인'으로 선정해 시상했다.
'올해의 KAIST인 상'은 한 해 동안 국내·외에서 KAIST 발전을 위해 노력하고 학술 및 연구 실적이 탁월한 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
19번째 수상의 영예를 거머쥔 심흥선 교수는 2019년 한 해 동안 네이처(Nature)지에 물리학 난제인 콘도 스핀 구름의 존재를 세계 최초로 입증하는 연구성과를, 네이처 나노테크놀로지(Nature Nanotechnology)지에는 양자 기술의 핵심문제인 전자의 파동성 제어·관측을 위해 전자 파동의 피코초 진동 관측법을 발견하는 연구성과를 게재하는 등 KAIST의 위상을 크게 높였다는 평가를 받았다.
심흥선 교수는 "올해의 KAIST인 상을 수상하게 되어 영광이며, 이는 함께 연구하고 있는 학생들 덕분이며, 그들에게 고마움을 전한다. 자연에 대한 더 깊이 있는 이해를 얻기 위해 노력하겠다.”라고 소감을 밝혔다.
이 외에도 우리 대학은 교육, 학술, 연구, 국제협력 성과가 탁월하거나 KAIST의 위상에 크게 공헌한 총 32명의 교원에게 ‘개교기념 우수교원 포상 및 특별포상’을, 12명의 교원에게 '송암 미래 석학 우수연구상', '2019년 대표 연구성과 10선' 상 등을 수여했다.
주요 수상자는 다음과 같다.
학술대상을 수상한 기계공학과 김승우 교수는 현대 첨단 산업이 요구하는 초정밀 광학계측 기술의 선도적 개발을 주도했으며, 특히 첨단 광계측 기술 분야의 세계적 연구 결과를 창출하여 KAIST를 대표할 만한 탁월한 학술 연구업적을 낸 점을 높이 평가받았다.
창의강의대상을 수상한 전산학부 김주호 교수는 전산학에 인문학 지식을 결합한 CS+X 형태의 융합형 교과목을 개설해 사람을 위한 기술을 강조하는 등 학생 교육의 질적 향상에 크게 기여한 공로를 인정받았다.
우수강의대상을 수상한 경영공학부 윤여선 교수는 최근 5년간 강의평가 결과 상위 20위 내 진입 횟수가 10회에 이르는 등 탁월한 강의로 KAIST 학생 교육의 질적 향상 및 인재 양성에 기여한 점을 높이 평가받았다.
공적대상을 수상한 전기및전자공학부 김종환 교수는 세계 최초대회인 AI World Cup의 창시자로 2017년부터 매년 대회를 개최해 세계 각국의 연구자들에게 AI 기술력의 경쟁 무대를 제공하고, AI 기술을 대중화시키는 등 KAIST의 위상을 크게 제고한 것으로 평가받았다.
연구대상을 수상한 전기및전자공학부 심현철 교수는 최근 5년간 연구계약과 O/H 흡수실적, 지식재산권실적, Royalty 수입실적을 평가하는 연구상 부문에서 가장 높은 역량을 인정받았다.
사회봉사부문 우수교원 특별포상 대상을 수상한 전기및전자공학부 최성율 교수는 KAIST 소재·부품·장비 기술자문단 단장으로서 30여개 기업에 대한 자문을 통해 현장의 문제를 해결하는 등 국가의 위기극복과 미래혁신에 대한 성과를 인정받았다.
임형규 LINKGENESIS-Best Teacher Award 대상을 수상한 기계공학과 김성진 교수는 2012년부터 ‘연성 박막 초열전도체 개발’이라는 주제로 창의과제를 수행하는 등 창의적인 인재 양성에 크게 기여한 점을 높이 평가받았다.
이수영 교수학습혁신상 대상을 수상한 신소재공학과 홍승범 교수는 2017년부터 Flipped Learning 교과목의 설계 및 운영을 통해 창의적 수업방식을 실천하는 등의 탁월한 성과를 인정받았다.
2020.07.30 조회수 24776
제49주년 개교기념식에서 ‘2019년 올해의 KAIST인 상’ 등 총 45명 교원 시상
지난 7월 30일 열린 개교 49주년 기념식 행사에서 우리 대학은 물리학과 심흥선 교수를 '2019년 올해의 KAIST인'으로 선정해 시상했다.
'올해의 KAIST인 상'은 한 해 동안 국내·외에서 KAIST 발전을 위해 노력하고 학술 및 연구 실적이 탁월한 인물에게 수여하는 상으로 지난 2001년에 처음 제정됐다.
19번째 수상의 영예를 거머쥔 심흥선 교수는 2019년 한 해 동안 네이처(Nature)지에 물리학 난제인 콘도 스핀 구름의 존재를 세계 최초로 입증하는 연구성과를, 네이처 나노테크놀로지(Nature Nanotechnology)지에는 양자 기술의 핵심문제인 전자의 파동성 제어·관측을 위해 전자 파동의 피코초 진동 관측법을 발견하는 연구성과를 게재하는 등 KAIST의 위상을 크게 높였다는 평가를 받았다.
심흥선 교수는 "올해의 KAIST인 상을 수상하게 되어 영광이며, 이는 함께 연구하고 있는 학생들 덕분이며, 그들에게 고마움을 전한다. 자연에 대한 더 깊이 있는 이해를 얻기 위해 노력하겠다.”라고 소감을 밝혔다.
이 외에도 우리 대학은 교육, 학술, 연구, 국제협력 성과가 탁월하거나 KAIST의 위상에 크게 공헌한 총 32명의 교원에게 ‘개교기념 우수교원 포상 및 특별포상’을, 12명의 교원에게 '송암 미래 석학 우수연구상', '2019년 대표 연구성과 10선' 상 등을 수여했다.
주요 수상자는 다음과 같다.
학술대상을 수상한 기계공학과 김승우 교수는 현대 첨단 산업이 요구하는 초정밀 광학계측 기술의 선도적 개발을 주도했으며, 특히 첨단 광계측 기술 분야의 세계적 연구 결과를 창출하여 KAIST를 대표할 만한 탁월한 학술 연구업적을 낸 점을 높이 평가받았다.
창의강의대상을 수상한 전산학부 김주호 교수는 전산학에 인문학 지식을 결합한 CS+X 형태의 융합형 교과목을 개설해 사람을 위한 기술을 강조하는 등 학생 교육의 질적 향상에 크게 기여한 공로를 인정받았다.
우수강의대상을 수상한 경영공학부 윤여선 교수는 최근 5년간 강의평가 결과 상위 20위 내 진입 횟수가 10회에 이르는 등 탁월한 강의로 KAIST 학생 교육의 질적 향상 및 인재 양성에 기여한 점을 높이 평가받았다.
공적대상을 수상한 전기및전자공학부 김종환 교수는 세계 최초대회인 AI World Cup의 창시자로 2017년부터 매년 대회를 개최해 세계 각국의 연구자들에게 AI 기술력의 경쟁 무대를 제공하고, AI 기술을 대중화시키는 등 KAIST의 위상을 크게 제고한 것으로 평가받았다.
연구대상을 수상한 전기및전자공학부 심현철 교수는 최근 5년간 연구계약과 O/H 흡수실적, 지식재산권실적, Royalty 수입실적을 평가하는 연구상 부문에서 가장 높은 역량을 인정받았다.
사회봉사부문 우수교원 특별포상 대상을 수상한 전기및전자공학부 최성율 교수는 KAIST 소재·부품·장비 기술자문단 단장으로서 30여개 기업에 대한 자문을 통해 현장의 문제를 해결하는 등 국가의 위기극복과 미래혁신에 대한 성과를 인정받았다.
임형규 LINKGENESIS-Best Teacher Award 대상을 수상한 기계공학과 김성진 교수는 2012년부터 ‘연성 박막 초열전도체 개발’이라는 주제로 창의과제를 수행하는 등 창의적인 인재 양성에 크게 기여한 점을 높이 평가받았다.
이수영 교수학습혁신상 대상을 수상한 신소재공학과 홍승범 교수는 2017년부터 Flipped Learning 교과목의 설계 및 운영을 통해 창의적 수업방식을 실천하는 등의 탁월한 성과를 인정받았다.
2020.07.30 조회수 24776 항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
2020.06.16 조회수 18413
항암 백신 및 면역치료를 최적화한 신기술 개발
우리 연구진이 새로운 항암 나노 백신을 개발하고 또 이를 이용해 면역치료를 최적화한 기술 개발을 통해 효과적인 암 예방 및 암 치료가 가능케 함으로써 암 정복에 한 걸음 더 다가서는 계기를 마련했다.
우리 대학 생명과학과 전상용 교수 연구팀이 효과적인 항암 면역치료를 위한 나노입자 백신 개발에 성공했다고 16일 밝혔다.
전 교수 연구팀은 면역 반응을 유도하는 아미노산 중합체인 종양 펩타이드 항원과 면역보조제의 동시전달이 가능한 나노입자 기반 항암 백신을 개발했다. 전 교수 연구팀은 또 세포성 면역을 담당하는 림프구의 일종인 T 세포(면역 세포) 기반 `특이적 면역(specific immunity, 선천 면역과는 다른 고도로 발전된 방어체계)' 반응을 얻는 성과를 거뒀다. 결과적으로 전 교수팀은 특히 새로 개발한 나노입자 기반 항암 백신을 기존 항암 면역 치료제로 주목받고 있는 면역 관용 억제제를 병용하여 투여 순서와 시기를 적절히 조절, 사용하면 효능은 물론 치료 효과를 크게 증대시킬 수 있음을 확인했다.
생명과학과 김유진 박사과정, 강석모 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 `앙게반테 케미(Angewandte chemie, 독일화학회지)' 5월 19일 字 온라인판에 게재됐다. (논문명 : Sequential and timely combination of cancer nanovaccine with immune checkpoint blockade effectively inhibits tumor growth and relapse)
항암 백신은 종양 항원 특이적 면역 반응을 유도할 수 있다는 장점에도 불구하고, 면역 회피가 유도돼 우리 몸에서 백신에 대한 저항성이 발생할 수 있다는 한계가 있다. 최근 항암 치료제로 주목받고 있는 면역 관용 억제제의 경우 면역 억제를 되돌려 항암 효과를 유도할 수는 있으나, 적절한 면역 반응이 존재하지 않는 경우 효과가 극히 제한적인 것으로 알려져 있다.
연구팀은 이 같은 한계를 극복하기 위해 항암 백신과 면역 관용 억제제의 병용요법 진행을 통해 병용요법의 치료 효능을 증대시킬 수 있는 전략을 활용했다. 특히 항암 백신의 효능 증가를 위해 나노입자 전달 플랫폼을 새롭게 개발했다. 결과적으로 새로 개발한 나노입자 백신이 기존 대비 항원과 T 세포 기반 특이적 면역 반응을 더욱 증가시킬 뿐만 아니라 종양 동물모델에서 효과적인 암 예방 및 치료 효과를 거두는 성과를 확인했다.
연구팀은 또 항암 나노 백신의 치료 효과를 더욱 증대시키기 위해 면역 관용 억제제인 `PD-1 항체(활성화된 T 세포의 표면에 있는 단백질)'와 병용해 진행했는데 병용 순서에 따라 치료 효능이 달라질 수 있음을 발견했다. 이 밖에 나노 백신과 PD-1 항체의 병용 치료를 순차적으로 시기를 조절하면 종양 성장과 종양 재발을 효과적으로 억제한다는 사실도 함께 입증했다.
전상용 교수는 "효과적인 항암 면역치료를 목적으로 나노입자 백신을 개발했다ˮ면서 "이와 함께 기존 항암 백신 및 면역 관용 억제제가 가지는 한계를 극복할 수 있는 새로운 병용요법 전략을 개발했는데 이를 통해 향후 다양한 항암 면역치료법에 적용해 치료 효능을 더욱 증대시킬 수 있을 것으로 기대한다ˮ고 말했다. 한편, 이번 연구는 한국연구재단의 리더연구사업 및 바이오 의료기술 개발사업의 지원을 받아 수행됐다.
2020.06.16 조회수 18413 실시간 영상 전송 보안 기술 개발
전산학부 김명철 교수 연구팀이 웹캠, 영상 드론, CCTV, 증강현실(AR), 가상현실(VR) 등에 사용하는 영상 전송 장비용 실시간 영상 암호화 및 전산 자원(CPU, 배터리 등) 소모 저감 기술을 개발했다.
연구팀의 실시간 영상 전송 보안기술은 비디오 코덱 종류에 상관없이 적용될 수 있는 범용성을 가질 뿐 아니라 영상전송기기의 CPU나 배터리를 최대 50%까지 절약하면서도 최고 수준의 보안성능을 제공하는 결과를 보였다.
고경민 박사 주도로 개발된 이번 연구결과는 보안 분야의 국제 학술지 IEEE TDSC(Transactions on Dependable and Secure Computing) 3월 13일 자 온라인판에 게재됐다. (논문명: Secure video transmission framework for battery-powered video devices) 또한, 국내 특허로 등록, 미국특허로 출원돼 2차 심사가 진행 중이다. (국내특허명: 통신 시스템의 암호화 패킷 전송 방법)
기존 실시간 영상 전송 보안기술은 촬영한 모든 영상을 암호화해 전송하거나 비디오 데이터 식별 없이 무작위로 암호화하기 때문에 전산 자원이 제한된 상황에서 적용하기에는 한계가 있다. 문제 해결을 위해 연구팀은 새로운 실시간 영상 암호화 및 배터리 소모 저감 기술을 개발했다. 이 기술은 영상전송 장비에서 동작하는 자원 모니터링 결과에 따라 카메라로 촬영한 영상을 구성하는 비디오 데이터를 데이터중요도 관점에서 선별적으로 암호화 전송을 수행한다.
암호화 전송 시에는 영상 송신 장비의 가용자원량에 따라 실시간으로 암호화 정도를 조정하며, 다중 전송경로 지원을 통해 보안성을 높인다. 수신된 영상 데이터는 실시간 영상 재생이 가능한 단위로 그 순서를 복원한 후 화면에 표시된다. 이 기술은 가용 전산 자원의 모니터링 결과에 따라 촬영된 영상을 구성하는 비디오 데이터 단위로 암호화가 가능해 전산 자원 가용량에 따른 선별적 적용이 가능하다.
연구팀은 카메라 장비를 상용 영상 드론에 탑재해 무선을 통한 영상전송 시 전산 자원 소모를 낮추면서 보안성을 높일 수 있음을 증명했다. 최근 코로나로 인해 널리 활용되는 비대면 강의 및 미팅의 보안성 강화에 기여할 수 있을 것으로 기대된다.
김명철 교수는 “영상전송 보안이 중요한 온라인 교육/회의, 스마트시티의 CCTV, 민군 드론 영상 송수신, 증강현실(AR), 가상현실(VR) 등에서 특허화된 개발기술이 원천기술로 활용될 수 있도록 산학협력을 활발히 추진하고 있다”라고 말했다.
2020.04.16 조회수 8310
실시간 영상 전송 보안 기술 개발
전산학부 김명철 교수 연구팀이 웹캠, 영상 드론, CCTV, 증강현실(AR), 가상현실(VR) 등에 사용하는 영상 전송 장비용 실시간 영상 암호화 및 전산 자원(CPU, 배터리 등) 소모 저감 기술을 개발했다.
연구팀의 실시간 영상 전송 보안기술은 비디오 코덱 종류에 상관없이 적용될 수 있는 범용성을 가질 뿐 아니라 영상전송기기의 CPU나 배터리를 최대 50%까지 절약하면서도 최고 수준의 보안성능을 제공하는 결과를 보였다.
고경민 박사 주도로 개발된 이번 연구결과는 보안 분야의 국제 학술지 IEEE TDSC(Transactions on Dependable and Secure Computing) 3월 13일 자 온라인판에 게재됐다. (논문명: Secure video transmission framework for battery-powered video devices) 또한, 국내 특허로 등록, 미국특허로 출원돼 2차 심사가 진행 중이다. (국내특허명: 통신 시스템의 암호화 패킷 전송 방법)
기존 실시간 영상 전송 보안기술은 촬영한 모든 영상을 암호화해 전송하거나 비디오 데이터 식별 없이 무작위로 암호화하기 때문에 전산 자원이 제한된 상황에서 적용하기에는 한계가 있다. 문제 해결을 위해 연구팀은 새로운 실시간 영상 암호화 및 배터리 소모 저감 기술을 개발했다. 이 기술은 영상전송 장비에서 동작하는 자원 모니터링 결과에 따라 카메라로 촬영한 영상을 구성하는 비디오 데이터를 데이터중요도 관점에서 선별적으로 암호화 전송을 수행한다.
암호화 전송 시에는 영상 송신 장비의 가용자원량에 따라 실시간으로 암호화 정도를 조정하며, 다중 전송경로 지원을 통해 보안성을 높인다. 수신된 영상 데이터는 실시간 영상 재생이 가능한 단위로 그 순서를 복원한 후 화면에 표시된다. 이 기술은 가용 전산 자원의 모니터링 결과에 따라 촬영된 영상을 구성하는 비디오 데이터 단위로 암호화가 가능해 전산 자원 가용량에 따른 선별적 적용이 가능하다.
연구팀은 카메라 장비를 상용 영상 드론에 탑재해 무선을 통한 영상전송 시 전산 자원 소모를 낮추면서 보안성을 높일 수 있음을 증명했다. 최근 코로나로 인해 널리 활용되는 비대면 강의 및 미팅의 보안성 강화에 기여할 수 있을 것으로 기대된다.
김명철 교수는 “영상전송 보안이 중요한 온라인 교육/회의, 스마트시티의 CCTV, 민군 드론 영상 송수신, 증강현실(AR), 가상현실(VR) 등에서 특허화된 개발기술이 원천기술로 활용될 수 있도록 산학협력을 활발히 추진하고 있다”라고 말했다.
2020.04.16 조회수 8310 배상민 교수, 독일 iF 어워드 패키지부문 본상 수상
우리 대학 산업디자인학과 배상민 교수 연구팀(ID+IM 디자인 연구소)이 ‘제주용암수’ 생수병 디자인으로 세계 최고권위 디자인 대회인 2020 독일 iF 디자인 어워드 패키지 디자인 부문 본상을 받았다.
독일 하노버전시센터(Hannover Exhibition Center)에서 주관하는 iF 디자인 어워드는 세계 3대 디자인 대회 중 하나로, 60개국 7천 점 이상의 작품이 출품된다. 수상한 ‘제주용암수 디자인’은 ㈜오리온 제주 용암수와 KAIST와의 산학 협력으로 이루어진 프리미엄 미네랄 생수 디자인 프로젝트이다. 배상민 교수팀이 디자인한 생수병은 제주도의 아름다운 자연을 모티브로 주상절리와 바다의 수평선을 형상화한 세로 선과 가로섬을 활용해 단순하면서도 감각적인 디자인을 완성했다.
나아가 이러한 병의 형태는 획기적으로 적은 양의 재료를 사용함에도, 일반적인 형태의 플라스틱병에 비해 약 4배 정도의 고압 하중을 견뎌낼 수 있는 효율적인 구조이기 때문에 심미적 영역뿐 아니라 기능적 영역에서도 뛰어난 우수성을 보인다. 병 라벨에는 물을 통해 투과돼 보이는 신비로운 한라산과 밤하늘에 빛나는 오리온 별자리를 담아 제주 한라산의 낮과 밤을 감성적으로 그려냄과 동시에 ㈜오리온의 브랜드를 상징화했다.
배상민 교수는 “ 먼저 학생들과 산학 프로젝트로 연구한 결과물을 상품화해 대량생산되고 그 결과가 국제적 디자인 대회에서 인정받아 기쁘다”라며 제조 및 유통 공정상 디자인에 제약이 많은 상황이었지만 구조 및 기능적인 부분에 대한 고안과 외형의 아름다움까지 표현하려 노력을 기울였다”라고 말했다.
2020.02.18 조회수 6665
배상민 교수, 독일 iF 어워드 패키지부문 본상 수상
우리 대학 산업디자인학과 배상민 교수 연구팀(ID+IM 디자인 연구소)이 ‘제주용암수’ 생수병 디자인으로 세계 최고권위 디자인 대회인 2020 독일 iF 디자인 어워드 패키지 디자인 부문 본상을 받았다.
독일 하노버전시센터(Hannover Exhibition Center)에서 주관하는 iF 디자인 어워드는 세계 3대 디자인 대회 중 하나로, 60개국 7천 점 이상의 작품이 출품된다. 수상한 ‘제주용암수 디자인’은 ㈜오리온 제주 용암수와 KAIST와의 산학 협력으로 이루어진 프리미엄 미네랄 생수 디자인 프로젝트이다. 배상민 교수팀이 디자인한 생수병은 제주도의 아름다운 자연을 모티브로 주상절리와 바다의 수평선을 형상화한 세로 선과 가로섬을 활용해 단순하면서도 감각적인 디자인을 완성했다.
나아가 이러한 병의 형태는 획기적으로 적은 양의 재료를 사용함에도, 일반적인 형태의 플라스틱병에 비해 약 4배 정도의 고압 하중을 견뎌낼 수 있는 효율적인 구조이기 때문에 심미적 영역뿐 아니라 기능적 영역에서도 뛰어난 우수성을 보인다. 병 라벨에는 물을 통해 투과돼 보이는 신비로운 한라산과 밤하늘에 빛나는 오리온 별자리를 담아 제주 한라산의 낮과 밤을 감성적으로 그려냄과 동시에 ㈜오리온의 브랜드를 상징화했다.
배상민 교수는 “ 먼저 학생들과 산학 프로젝트로 연구한 결과물을 상품화해 대량생산되고 그 결과가 국제적 디자인 대회에서 인정받아 기쁘다”라며 제조 및 유통 공정상 디자인에 제약이 많은 상황이었지만 구조 및 기능적인 부분에 대한 고안과 외형의 아름다움까지 표현하려 노력을 기울였다”라고 말했다.
2020.02.18 조회수 6665 암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 9068
암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 9068 조광현 교수, 암세포를 정상세포로 되돌리는 초기 원천기술 개발
우리대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 대장암세포를 일반적인 정상 세포로 되돌리는 초기 원천기술을 개발하는 데 성공했다.
연구팀은 대장암세포와 정상 대장 세포의 유전자 조절 네트워크를 분석해 대장암세포를 정상 대장 세포로 변환하는데 필요한 핵심 인자를 규명하고, 이를 통해 암세포의 정상 세포화라는 새로운 치료 원리를 개발했다.
KAIST 이수범 연구원, 황채영, 김동산 박사, 한영현 박사과정, 서울삼성병원의 이찬수 박사, 홍성노 교수, 김석형 교수 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 ‘분자암연구(Molecular Cancer Research)’ 1월 2일 자 표지논문으로 게재됐으며, 하이라이트 특집 기사도 함께 출판됐다. (논문명: Network inference analysis identifies SETDB1 as a key regulator for reverting colorectal cancer cells into differentiated normal-like cells).
현재 항암치료로 가장 널리 사용되는 항암 화학요법은 빠르게 분열하는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 이 기술은 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 부작용을 일으킨다.
게다가 암세포들은 항암제에 본질적인 내성을 갖거나 새로운 내성을 갖게 돼 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 현재의 항암치료는 내성을 보이는 암세포를 없애기 위해 더 많은 정상 세포의 사멸을 감수해야만 하는 문제를 갖는다.
이를 극복하기 위해 암세포만을 특이적으로 없애는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽여야 하는 공통적인 조건 때문에 근본적인 한계를 가진다.
문제 해결을 위해 연구팀은 암세포를 정상 세포로 변환하는 새로운 방식의의 치료전략을 제안했다. 암세포가 정상 세포로 변환되는 현상은 20세기 초부터 간혹 관찰됐지만, 그 원리가 연구되지 않았으며 또한 이를 인위적으로 제어하는 기술도 연구된 바 없었다.
1907년 스위스 병리학자 막스 아스카나지(Max Askanazy)가 난소의 기형종(테라토마)이 정상 세포로 분화되는 현상을 발견한 이래로 다양한 암종에서 정상 세포로 변화되는 현상들이 산발적으로 보고됐고, 이러한 보고에서는 암세포가 돌연변이를 지닌 상태에서 주변 미세환경의 변화나 특정 자극 때문에 정상 세포의 상태로 되돌아가는 현상만이 관찰됐다.
조 교수 연구팀은 시스템생물학 연구방법을 통해 대장암세포를 정상 대장 세포로 변환할 수 있는 핵심조절인자를 탐구했고, 그 결과 다섯 개의 핵심전사인자(CDX2, ELF3, HNF4G, PPARG, VDR)와 이들의 전사 활성도를 억제하고 있는 후성유전학적 조절인자인 SETDB1을 발견했다.
연구팀은 이번 연구를 통해 SETDB1을 억제함으로써 암세포를 효과적으로 정상 세포로 변환할 수 있음을 분자세포실험을 통해 증명했다. 대장암세포에서 SETDB1을 억제했을 때 세포가 분열을 중지하고 정상 대장 세포의 유전자 발현패턴을 회복하는 것을 확인했다.
이번 연구에 따르면 암세포에서는 암 특이적으로 활성화된 후성유전학적 조절인자 SETDB1이 정상 세포의 핵심전사인자를 억제해 암세포가 정상 세포로 변환하는 것을 차단하고 있는 것으로 밝혀졌다. 즉, SETDB1을 조절함으로써 다시 원래의 정상 세포 상태로 되돌릴 수 있음을 증명한 것이다.
조 교수 연구팀은 서울삼성병원과의 협동 연구를 통해 SETDB1이 높게 발현되는 대장암세포를 가진 환자들에게서 더 안 좋은 예후가 나타남을 확인했으며, 환자 유래 대장암 오가노이드(3차원으로 배양한 장기유사체)에서 SETDB1의 발현을 억제했을 때 다시 정상 세포와 같은 형태로 변화함을 관찰했다.
이번 연구에서 찾아낸 타겟 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 전임상실험을 통해 암세포의 정상 세포화라는 새로운 치료 기술이 본격적으로 실현될 수 있을 것으로 보인다.
이러한 새로운 개념의 치료전략이 적용된다면 현재 항암치료의 많은 부작용과 내성 발생을 모두 최소화함으로써 환자의 고통을 완화해 삶의 질을 크게 높일 수 있을 것으로 기대된다.
조 교수는 “그동안 암은 유전자 변이 축적에 의한 현상이므로 되돌릴 수 없다고 여겨졌으나 이를 되돌릴 가능성을 보여줬다”라며 “이번 연구는 암을 당뇨나 고혈압과 같은 만성질환으로서 잘 관리하면서 삶의 질을 유지할 수 있도록 하는 새로운 항암치료의 서막을 열었다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, KAIST Grand Challenge 30 사업의 지원으로 수행됐다.
□ 그림 설명
조광현 교수 연구팀은 SETDB1 단백질이 대장암세포가 정상대장세포로 분화하는 것을 차단하는 후성유전학적 장애물을 형성하고 있다는 사실을 밝히고 이를 억제함으로써 대장암세포를 정상대장세포로 효과적으로 분화시킬 수 있음을 증명하였다.
□ 분자암연구 표지 이미지
2020.01.09 조회수 14843
조광현 교수, 암세포를 정상세포로 되돌리는 초기 원천기술 개발
우리대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 대장암세포를 일반적인 정상 세포로 되돌리는 초기 원천기술을 개발하는 데 성공했다.
연구팀은 대장암세포와 정상 대장 세포의 유전자 조절 네트워크를 분석해 대장암세포를 정상 대장 세포로 변환하는데 필요한 핵심 인자를 규명하고, 이를 통해 암세포의 정상 세포화라는 새로운 치료 원리를 개발했다.
KAIST 이수범 연구원, 황채영, 김동산 박사, 한영현 박사과정, 서울삼성병원의 이찬수 박사, 홍성노 교수, 김석형 교수 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 ‘분자암연구(Molecular Cancer Research)’ 1월 2일 자 표지논문으로 게재됐으며, 하이라이트 특집 기사도 함께 출판됐다. (논문명: Network inference analysis identifies SETDB1 as a key regulator for reverting colorectal cancer cells into differentiated normal-like cells).
현재 항암치료로 가장 널리 사용되는 항암 화학요법은 빠르게 분열하는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 이 기술은 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 부작용을 일으킨다.
게다가 암세포들은 항암제에 본질적인 내성을 갖거나 새로운 내성을 갖게 돼 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 현재의 항암치료는 내성을 보이는 암세포를 없애기 위해 더 많은 정상 세포의 사멸을 감수해야만 하는 문제를 갖는다.
이를 극복하기 위해 암세포만을 특이적으로 없애는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽여야 하는 공통적인 조건 때문에 근본적인 한계를 가진다.
문제 해결을 위해 연구팀은 암세포를 정상 세포로 변환하는 새로운 방식의의 치료전략을 제안했다. 암세포가 정상 세포로 변환되는 현상은 20세기 초부터 간혹 관찰됐지만, 그 원리가 연구되지 않았으며 또한 이를 인위적으로 제어하는 기술도 연구된 바 없었다.
1907년 스위스 병리학자 막스 아스카나지(Max Askanazy)가 난소의 기형종(테라토마)이 정상 세포로 분화되는 현상을 발견한 이래로 다양한 암종에서 정상 세포로 변화되는 현상들이 산발적으로 보고됐고, 이러한 보고에서는 암세포가 돌연변이를 지닌 상태에서 주변 미세환경의 변화나 특정 자극 때문에 정상 세포의 상태로 되돌아가는 현상만이 관찰됐다.
조 교수 연구팀은 시스템생물학 연구방법을 통해 대장암세포를 정상 대장 세포로 변환할 수 있는 핵심조절인자를 탐구했고, 그 결과 다섯 개의 핵심전사인자(CDX2, ELF3, HNF4G, PPARG, VDR)와 이들의 전사 활성도를 억제하고 있는 후성유전학적 조절인자인 SETDB1을 발견했다.
연구팀은 이번 연구를 통해 SETDB1을 억제함으로써 암세포를 효과적으로 정상 세포로 변환할 수 있음을 분자세포실험을 통해 증명했다. 대장암세포에서 SETDB1을 억제했을 때 세포가 분열을 중지하고 정상 대장 세포의 유전자 발현패턴을 회복하는 것을 확인했다.
이번 연구에 따르면 암세포에서는 암 특이적으로 활성화된 후성유전학적 조절인자 SETDB1이 정상 세포의 핵심전사인자를 억제해 암세포가 정상 세포로 변환하는 것을 차단하고 있는 것으로 밝혀졌다. 즉, SETDB1을 조절함으로써 다시 원래의 정상 세포 상태로 되돌릴 수 있음을 증명한 것이다.
조 교수 연구팀은 서울삼성병원과의 협동 연구를 통해 SETDB1이 높게 발현되는 대장암세포를 가진 환자들에게서 더 안 좋은 예후가 나타남을 확인했으며, 환자 유래 대장암 오가노이드(3차원으로 배양한 장기유사체)에서 SETDB1의 발현을 억제했을 때 다시 정상 세포와 같은 형태로 변화함을 관찰했다.
이번 연구에서 찾아낸 타겟 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 전임상실험을 통해 암세포의 정상 세포화라는 새로운 치료 기술이 본격적으로 실현될 수 있을 것으로 보인다.
이러한 새로운 개념의 치료전략이 적용된다면 현재 항암치료의 많은 부작용과 내성 발생을 모두 최소화함으로써 환자의 고통을 완화해 삶의 질을 크게 높일 수 있을 것으로 기대된다.
조 교수는 “그동안 암은 유전자 변이 축적에 의한 현상이므로 되돌릴 수 없다고 여겨졌으나 이를 되돌릴 가능성을 보여줬다”라며 “이번 연구는 암을 당뇨나 고혈압과 같은 만성질환으로서 잘 관리하면서 삶의 질을 유지할 수 있도록 하는 새로운 항암치료의 서막을 열었다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, KAIST Grand Challenge 30 사업의 지원으로 수행됐다.
□ 그림 설명
조광현 교수 연구팀은 SETDB1 단백질이 대장암세포가 정상대장세포로 분화하는 것을 차단하는 후성유전학적 장애물을 형성하고 있다는 사실을 밝히고 이를 억제함으로써 대장암세포를 정상대장세포로 효과적으로 분화시킬 수 있음을 증명하였다.
□ 분자암연구 표지 이미지
2020.01.09 조회수 14843 정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
2019.09.24 조회수 8347
정인경 교수, 인체 조직의 3차원 게놈지도 해독
〈 정인경 교수, 이정운 박사과정 〉
우리 대학 생명과학과 정인경 교수와 美 루드윅 암 연구소(Ludwig Institute of Cancer Research) 빙 렌 (Bing Ren) 교수 공동 연구팀이 인체 조직의 3차원 게놈 지도를 해독하는 데 성공했다.
연구팀은 인체의 27개 부위 조직의 3차원 게놈 지도를 분석해 치매, 심혈관계 질환 등을 포함한 2만 7천여 개 이상의 복합 질환 관련 유전 변이 기능을 예측했다.
정인경 교수, 빙 렌 교수가 공동 교신 저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 제네틱스(Nature Genetics) 9월 10일 자 온라인판에 게재됐다. (논문명 : A compendium of promoter-centered long-range chromatin interactions in the human genome)
현재까지 수많은 연구를 통해 알츠하이머병, 파킨슨병, 자가면역질환 등 다양한 복합 질환의 원인을 규명하려는 시도가 이뤄지면서 실제 다수의 질환과 관련한 중요 유전변이가 발견됐다.
하지만 이들 대부분의 유전변이는 DNA가 단백질을 생성하지 않는 비전사 지역에 존재하기 때문에 1차원적 DNA 서열 분석에 기반한 유전체 연구로는 모든 기능을 규명하는 데 한계가 있다.
이에 지난 10년간 비약적으로 발전한 3차원 게놈 구조 연구는 비전사 지역에 존재하는 유전변이도 3차원 게놈 구조에 의해 형성되는 염색질 고리 구조(chromatin loop)를 통해 멀리 떨어진 유전자를 조절할 수 있다는 모델을 제시했다.
그러나 이러한 3차원 게놈 구조 연구는 몇 가지 세포주를 대상으로만 국한돼 있고, 질환과 직접 연관이 있는 각 인체 조직을 표적으로 한 게놈 3차 구조는 규명되지 않았다.
연구팀은 인체 내의 27개 조직을 대상으로 이들 게놈의 3차원 구조를 규명하기 위해 전사촉진 부위만 선택적으로 분석하는 ‘표적 염색질 3차 구조 포착법(promoter-capture Hi-C)’이라 불리는 신규 실험 기법을 활용해 고해상도의 3차원 게놈 참조 지도를 작성했다.
그 결과 인간 게놈에 존재하는 약 90만 개의 게놈 3차원 염색질 고리 구조를 발굴하고, 이들 중 상당수가 각 인체 조직 특이적으로 존재한다는 사실도 규명했다.
연구팀은 3차원 게놈 구조를 기반으로 지금까지 기능이 명확하게 정의되지 않은 2만 7천여 개 이상의 질환 연관 유전 변이의 표적 유전자를 정의해 이들 변이의 기능을 예측했다. 나아가 각 질환의 표적 유전자 유사도에 기반해 질환과 질환 사이의 신규 관계를 규명했고, 이를 바탕으로 여러 질환에 공통으로 관여하는 신규 분자 기전을 제시했다.
정 교수는 “복합 질환 기전 규명을 위해 비전사 게놈의 중요성을 강조하고 존재하는 다수의 중요 유전변이를 3차원 게놈 구조 해독을 통해 규명 가능함을 보였다”라며 “이번 결과는 퇴행성 뇌 질환을 포함 다양한 복합 질환의 신규 기전 규명 및 표적 발굴에 활용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업, 보건복지부 질환극복기술개발사업, 서경배 과학재단의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 3차원 게놈 구조 모식도 (modified from Stefano et al., 2016)
2019.09.24 조회수 8347 정보보호대학원, 독일 정보보안센터(CISPA)와 MOU 체결
우리 대학 정보보호대학원(책임교수 신인식)이 지난 8월 28일 독일 자르브뤼켄에서 독일 정보보안센터(CISPA(Helmholtz Center for Information Security)) 및 KIST 유럽연구소와 함께 정보보호 관련 협력과 공동 목표에 관한 MOU를 체결했다.
KAIST는 국내 대학 최초로 체결한 이번 협약을 통해 CISPA와 KIST 유럽과 함께 ▲ 공동 프로젝트 추진 ▲ 시스템 보안, 웹 보안, 암호학 등 분야 관련 협력 ▲ KIST 유럽의 테스트베드 플랫폼 공동사용 등 다양한 분야에서 협력할 예정이다.
KAIST와 협력하게 될 독일의 CISPA는 연간 5300만 유로의 예산이 투입되는 독일 최대 연구기관인 헬름홀츠(Helmholtz) 연구협회 연구센터로 지난 2018년 선정됐다. CISPA는 협회 최초로 IT분야를 수행하는 대형연구센터로 출범했으며 2026년까지 최소 500명~800명의 연구 인력을 보유한 대형 연구센터로 발돋움할 계획이다.
CISPA는 최근 4년 동안 정보보호 분야의 TOP 4 국제학회에서 세계 최고의 연구 실적을 올렸으며(csrankings.org 기준 세계 1위), 매년 500억 원(원화 기준)이 넘는 연구비를 헬름홀츠 연구협회에서 지원을 받고 있다.
28일(현지시각)에는 MOU 행사와 더불어 독일 대사관에서 한독 사이버 보안 세미나가 개최되어 세계 최고 수준의 보안 분야 기술을 소개하는 시간이 마련됐다. 특히, `데이터 보호, 웹 보안, 시스템 보안을 위한 연구자들 워크숍'에서는 신인식, 강병훈, 손수엘 교수 등이 KAIST를 대표해 각각 시스템 보안 및 웹 보안 내용을 발표했으며, CISPA와 공동 협업 주제를 구체화했다.
신인식 정보보호 대학원 책임 교수는 "이번 MOU 참여 기관들과 공동 프로젝트, 세미나 및 인턴십 등을 추진해 공동 기술개발, 인력양성 및 산학협력 등에 이바지해 세계 최고 수준의 대학원으로 거듭 발전할 계획ˮ이라고 밝혔다.
이날 행사에는 KAIST 정보보호대학원 신인식 책임교수, CISPA 마이클 벡키스 소장, 김준경 KIST 유럽연구소장 등이 참석해서 MOU에 서명했다.
2019.09.09 조회수 7984
정보보호대학원, 독일 정보보안센터(CISPA)와 MOU 체결
우리 대학 정보보호대학원(책임교수 신인식)이 지난 8월 28일 독일 자르브뤼켄에서 독일 정보보안센터(CISPA(Helmholtz Center for Information Security)) 및 KIST 유럽연구소와 함께 정보보호 관련 협력과 공동 목표에 관한 MOU를 체결했다.
KAIST는 국내 대학 최초로 체결한 이번 협약을 통해 CISPA와 KIST 유럽과 함께 ▲ 공동 프로젝트 추진 ▲ 시스템 보안, 웹 보안, 암호학 등 분야 관련 협력 ▲ KIST 유럽의 테스트베드 플랫폼 공동사용 등 다양한 분야에서 협력할 예정이다.
KAIST와 협력하게 될 독일의 CISPA는 연간 5300만 유로의 예산이 투입되는 독일 최대 연구기관인 헬름홀츠(Helmholtz) 연구협회 연구센터로 지난 2018년 선정됐다. CISPA는 협회 최초로 IT분야를 수행하는 대형연구센터로 출범했으며 2026년까지 최소 500명~800명의 연구 인력을 보유한 대형 연구센터로 발돋움할 계획이다.
CISPA는 최근 4년 동안 정보보호 분야의 TOP 4 국제학회에서 세계 최고의 연구 실적을 올렸으며(csrankings.org 기준 세계 1위), 매년 500억 원(원화 기준)이 넘는 연구비를 헬름홀츠 연구협회에서 지원을 받고 있다.
28일(현지시각)에는 MOU 행사와 더불어 독일 대사관에서 한독 사이버 보안 세미나가 개최되어 세계 최고 수준의 보안 분야 기술을 소개하는 시간이 마련됐다. 특히, `데이터 보호, 웹 보안, 시스템 보안을 위한 연구자들 워크숍'에서는 신인식, 강병훈, 손수엘 교수 등이 KAIST를 대표해 각각 시스템 보안 및 웹 보안 내용을 발표했으며, CISPA와 공동 협업 주제를 구체화했다.
신인식 정보보호 대학원 책임 교수는 "이번 MOU 참여 기관들과 공동 프로젝트, 세미나 및 인턴십 등을 추진해 공동 기술개발, 인력양성 및 산학협력 등에 이바지해 세계 최고 수준의 대학원으로 거듭 발전할 계획ˮ이라고 밝혔다.
이날 행사에는 KAIST 정보보호대학원 신인식 책임교수, CISPA 마이클 벡키스 소장, 김준경 KIST 유럽연구소장 등이 참석해서 MOU에 서명했다.
2019.09.09 조회수 7984 김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
2019.08.01 조회수 11528
김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
2019.08.01 조회수 11528