연구

< 사진 1. 수리과학과 김재경 교수 >
효과가 높은 신약 및 치료법 개발을 위한 단서가 제시됐다. 우리 대학 수리과학과 김재경 교수(기초과학연구원(IBS) 수리 및 계산 과학 연구단 의생명 수학 그룹 CI(Chief Investigator)) 연구팀은 인공지능(AI)을 이용해 동일 외부 자극에 개별 세포마다 반응하는 정도가 다른 ‘세포 간 이질성’의 근본적인 원인을 찾아내고, 이질성을 최소화할 수 있는 전략을 제시했다.
우리 몸속 세포는 약물, 삼투압 변화 등 다양한 외부 자극에 반응하는 신호 전달 체계(signaling pathway)가 있다. 신호 전달 체계는 세포가 외부 환경과 상호작용하며 생존하는 데 핵심적인 역할을 한다. 세포의 신호 전달 체계는 노벨생리의학상의 단골 주제일 정도로 중요하지만, 규명을 위해서는 수십 년에 걸친 연구가 필요하다.
신호 전달 체계는 세포 간 이질성에도 영향을 미친다. 세포 간 이질성은 똑같은 유전자를 가진 세포들이 동일 외부 자극에 다르게 반응하는 정도를 뜻한다. 하지만 복잡한 신호 전달 체계의 전 과정을 직접 관측하는 일이 현재 기술로는 어렵기 때문에 지금까지는 신호 전달 체계와 세포 간 이질성의 명확한 연결고리를 알지 못했다.
세포 간 이질성은 질병 치료에 있어 더욱 중요한 고려 요소다. 가령, 항암제를 투여했을 때 세포 간 이질성으로 인해 일부 암세포만 사멸되고, 일부는 살아남는다면 완치가 되지 않는다. 세포 간 이질성의 근본적인 원인을 찾고, 이질성을 최소화할 수 있는 전략을 도출해야 치료 효과를 높인 신약 설계가 가능해진다.
제1 저자인 홍혁표 IBS 전(前) 학생연수원(現 미국 위스콘신 메디슨대 방문조교수)은 “우리 연구진은 선행 연구(Science Advances, 2022)에서 세포 내 신호 전달 체계를 묘사한 수리 모델을 개발한 바 있다”며 “당시엔 신호 전달 체계의 중간 과정이 한 개의 경로만 있다고 가정해 얻을 수 있는 정보도 한계가 있었지만, 이번 연구에서는 AI를 활용해 중간 과정의 비밀까지 풀어냈다”고 말했다.
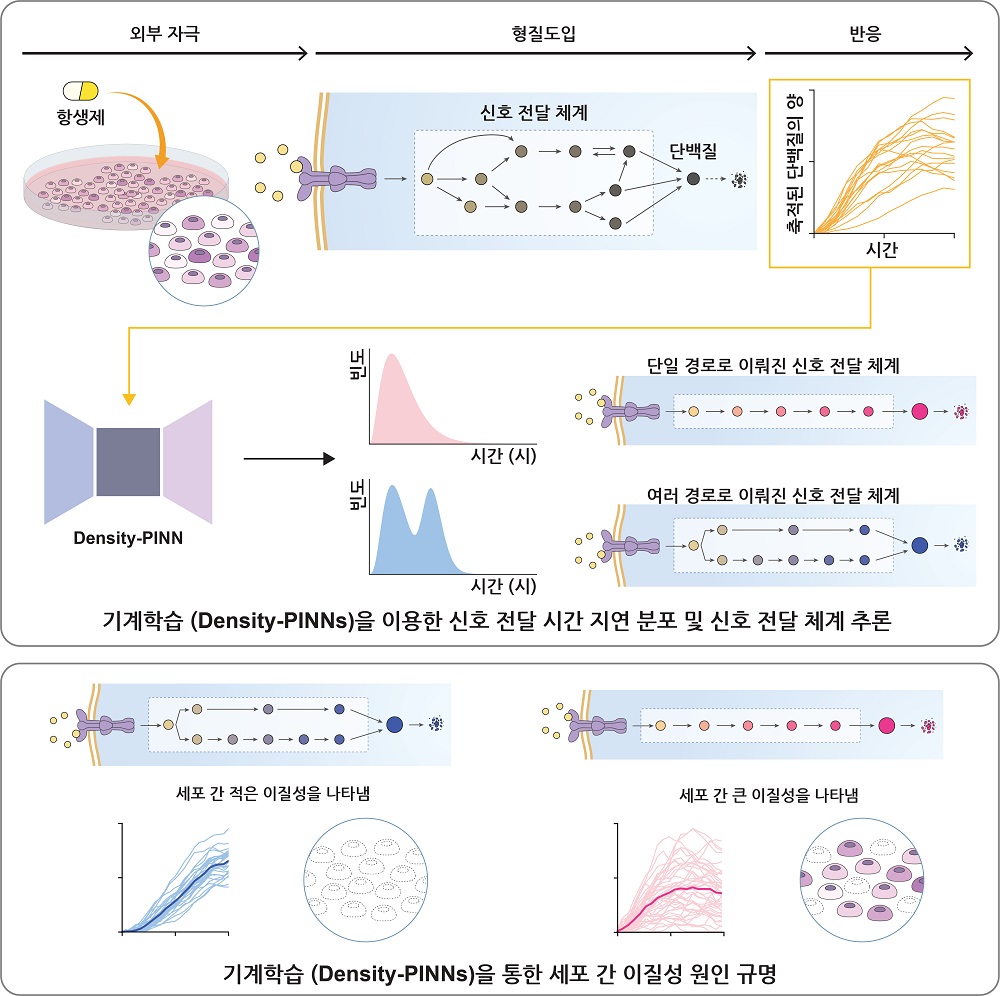
< 그림 1. 기계학습방법론(Density-PINNs)을 통한 세포 간 이질성 원인 규명 >
연구진은 기계 학습 방법론인 ‘Density-PINNs(Density Physics-Informed Neural Networks)’를 개발해 신호 전달 체계와 세포 간 이질성의 연결고리를 찾았다. 세포가 외부 자극에 노출되면 신호 전달 체계를 거쳐 반응 단백질이 생성된다. 시간에 따라 축적된 반응 단백질의 양을 이용하면 신호 전달 소요 시간의 분포를 추론할 수 있다. 이 분포는 신호 전달 체계가 몇 개의 경로로 구성됐는지를 알려준다. 즉, Density-PINNs를 이용하면 쉽게 관측할 수 있는 반응 단백질의 시계열 데이터로부터 직접 관찰하기 어려운 신호 전달 체계에 대한 정보를 추정할 수 있다는 의미다.
이어 연구진은 실제 대장균의 항생제에 대한 반응 실험 데이터에 Density-PINNs를 적용하여 세포 간 이질성의 원인도 찾았다. 신호 전달 체계가 단일 경로로 이뤄진 때(직렬)에 비해 여러 경로로 이뤄졌을 때(병렬)가 세포 간 이질성이 적다는 것을 알아냈다.
제1 저자인 조현태 연구원은 “추가 연구가 필요하지만, 신호 전달 체계가 병렬 구조일 경우 극단적인 신호가 서로 상쇄되어서 세포 간 이질성이 적어지는 것으로 보인다”며 “신호 전달 체계가 병렬 구조를 보이도록 약물이나 화학 요법 치료 전략을 세우면 치료 효과를 높일 수 있다는 의미”라고 설명했다.
연구를 이끈 김재경 교수는 “복잡한 세포 신호 전달 체계의 전 과정을 파악하려면 수십 년의 연구가 필요하지만, 우리 연구진이 제시한 방법론은 수 시간 내에 치료에 필요한 핵심 정보만 알아내 치료에 활용할 수 있다”며 “이번 연구를 실제 현장에서 사용되는 약물에 적용하여 치료 효과를 개선할 수 있기를 기대한다”고 말했다.
연구 결과는 지난해 12월 26일 국제학술지 셀(Cell)의 자매지인 ‘패턴스(Patterns)’에 실렸다.
※ 논문명: Density physics-informed neural networks reveal sources of cell heterogeneity in signal transduction
-
연구 지질 뗏목의 원리 밝혀 질병 치료에 희소식
지질 뗏목은 세포막 간 융합, 신호 전달, 바이러스 침투 등 세포 기능과 질병 발병의 핵심 과정에 중요한 역할을 한다. 한국 연구진이 지금까지 알려지지 않았던 지질 뗏목의 정렬 원인과 그 조절 메커니즘을 밝혀내어 세포막 간 상호작용을 조절하여 질병 치료에 새로운 접근법을 제공할 수 있을 것으로 기대된다. 우리 대학 바이오및뇌공학과 최명철 교수팀이 고등과학원(원장 최재경) 현창봉 교수팀, 포항가속기연구소(소장 강흥식) 이현휘 박사와 공동으로 세포막 간의 상호작용을 매개하는 지질 뗏목(Lipid Raft)의 정렬 현상의 원리를 최초로 규명했다고 5일 밝혔다. 세포 융합, 바이러스 침투, 세포 간 신호 전달 등 다양한 세포막 간의 상호작용을 조절할 수 있는 핵심 기전을 밝힌 것이다. 세포막(Cell membrane)은 세포의 내부와 외부를 구분하는 얇고 유연한 막으로, 지질 이중층(lipid bilayer)으로 구성돼 있다. 세포막에는 수많은 막단백질(membrane prote
2024-06-05 -
연구 암세포 약물반응 예측 ‘그레이박스’ 개발
지난 수십 년간 많은 의생명과학자의 집중적인 연구에도 불구하고 여전히 국내 사망원인 1위는 암이다. 이처럼 암 치료가 난해한 이유는 환자마다 암 발생의 원인이 되는 유전자 돌연변이와 그로 인한 유전자 네트워크 변형이 서로 달라서 전통적인 실험생물학 접근만으로 표적치료를 적용하는 데에는 본질적인 한계가 있기 때문이다. 한편 딥러닝과 같은 소위 블랙박스(black-box) 방식의 인공지능 기술을 활용해 실험을 대체하고 데이터 학습을 통해 약물 반응을 예측할 수 있으나 이에 대한 생물학적 근거를 설명할 수 없어 결과를 신뢰하기 어려웠다. 우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 인공지능과 시스템생물학을 융합해 암세포의 약물 반응 예측 및 메커니즘 분석을 동시에 이룰 수 있는 새로운 개념의 ‘그레이박스’ 기술을 개발했다고 3일 밝혔다. 조광현 교수 연구팀은 높은 예측 성능을 보이지만 그 근거를 알 수 없어 블랙박스로 불리는 딥러닝과 복잡한 대규모 모델
2024-06-03 -
연구 세계 최대 규모 암 데이터베이스 구축하다
디지털 암 정보 축적의 시대에는 데이터 생산을 넘어서, 데이터의 수집 및 관리 방법을 정립하고 거대 규모의 빅 데이터를 운용하는 것이 가장 큰 경쟁력이 될 수 있다. 전략적으로는 정밀 임상 정보와 연계할 수 있는 국내 생산 데이터와 다양성에 대한 이해를 도모할 수 있는 대규모 국제 데이터를 모두 수집해 통합하는 것은 매우 중요한 과제다. 우리 대학 의과학대학원 박종은 교수, 바이오및뇌공학과 최정균 교수 공동 연구팀(제1 저자: 강준호 박사, 이준형 박사)이 세계 최대 규모의 암 조직 단일세포 및 공간전사체* 데이터베이스를 구성하고, 이를 바탕으로 삼성서울병원 이세훈 교수 연구팀과 함께 면역 치료의 예후 예측에 중요한 세포 생태계 타입을 보고했다고 22일 밝혔다. *단일세포 및 공간전사체: 모든 유전자의 발현 양상을 개별 세포 단위에서 혹은 3차원 조직 구조상에서 분석한 데이터 암은 우리 몸 안에서 스스로 진화하는 특성을 가지고 있어 암 조직 내의 세포 생태계를 구성하는
2024-05-22 -
연구 개인 맞춤형 정밀 의학 정확도 높일 ‘렌즈’ 개발
평균이 아닌 개인차를 고려하는 정밀 의학 시대가 열렸다. 사람마다 다른 유전적 특징을 알아내는 기술이 비약적으로 발전한 덕분이다. 더 빠르고, 정확하게 전사체를 해독할 수 있는 새로운 도구가 개발됐다. 우리 대학 수리과학과 김재경 교수(IBS 수리 및 계산 과학 연구단 의생명 수학 그룹 CI) 연구팀은 전사체 분석 빅데이터에서 유용한 생물학적 정보만 골라내는 새로운 도구인 ‘scLENS(single-cell Low-dimension Embedding using Effective Noise Subtraction)’를 개발했다. 단일세포 전사체 분석은 최근 생물학, 신약 개발, 임상 연구 등 여러 분야에서 주목받는 도구다. 개별 세포 단위에서 유전적 변화를 확인할 수 있기 때문이다. 가령, 단일세포 전사체 분석을 이용하면 암 조직 내 수십 가지 종류의 세포를 구분하고, 유전적 변이가 발생한 세포만 표적하는 정밀 치료가 가능해진다. 단일세포 전사체 분석 기술이
2024-05-09 -
연구 소금 결핍 시 장에서 섭취 욕구 조절하다
나트륨은 생물이 살아가는 데 필요한 중요한 미량영양소 중 하나로, 수분 균형과 혈압을 조절하며 근육 수축 및 신경세포의 작용전위 생성에 필수적이다. 한국 연구진은 소금 섭취 욕구가 짠맛에만 의존하는 것이 아니라, 체내 나트륨 수준에 따라 결정된다는 새로운 시각을 제시했고 미각 감지 기작과는 다르게 장 감지 기작은 소금 결핍에 의해 활성화된다는 놀라운 사실을 발견했다. 우리 대학 생명과학과 서성배 교수 연구팀이 나트륨이라는 미량영양소에 대한 우리 몸의 새로운 감지 기작과 그 욕구를 조절하는 새로운 메커니즘을 발견했다고 2일 밝혔다. 연구팀은 소금에 대한 미각 감지 기작을 넘어 장내 신경세포가 나트륨에 직접적으로 반응하고 이 반응이 동물의 소금에 대한 섭취 욕구를 조절하는 새로운 감지 기작으로 작용한다는 연구 결과를 밝혔다. 해당 연구에서는 초파리를 이용해 나트륨 결핍 상태에 따른 소금에 대한 선호도가 증가함을 확인했다. 더욱 흥미로운 점은 나트륨에 대한 선호도가 소금에
2024-05-02